文档内容
2025 届高三年级期初阳光调研试卷
化学
注意事项:
1.本试卷分为单项选择题和非选择题两部分,试卷满分 100分。考试时间75分钟。
2.将选择题答案填涂在答题卡的对应位置上,非选择題的答案写在答题卡的指定栏目内。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Fe 56 Mo 96
一、单项选择题:共 13题,每题 3分,共39分。每题只有一个选项最符合题意。
1.第19届杭州亚运会采用石墨烯纳米防滑涂层以增加地面防滑性。石墨烯属于( )
A.有机材料 B.无机非金属材料 C.金属材料 D.复合材料
2.草酸易被NaClO氧化:H C O +NaClO=NaCl+2CO +H O,下列说法不
.
正确的是( )
2 2 4 2 2
A.CO 的空间构型为直线形 B.NaClO属于离子化合物
2
C.H O的电子式为H+[∶O∶]2-H+ D.Cl的结构示意图为
2
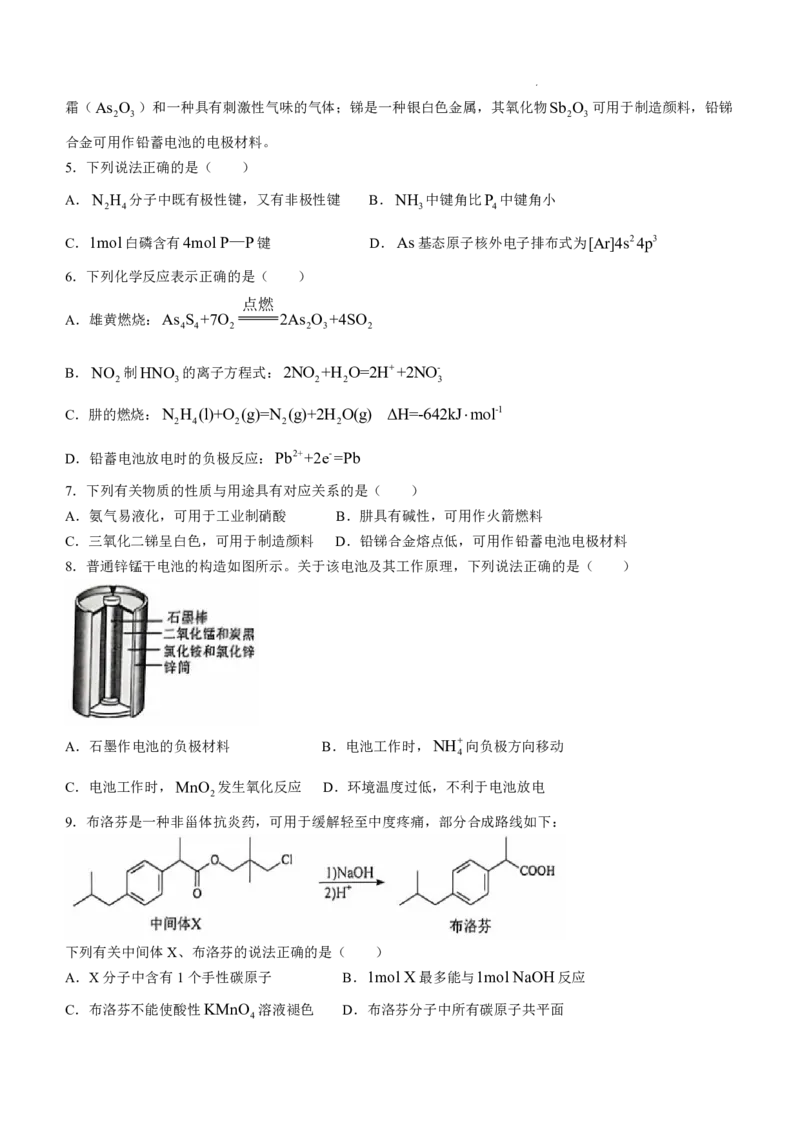
3.实验室模拟侯氏制碱法制备Na CO ,下列装置与原理均正确的是( )
2 3
A.制取CO B.制取NH C.制取NaHCO D.制取Na CO
2 3 3 2 3
4.
Cu NH
SO 常用作杀虫剂、媒染剂。下列说法正确的是( )
3 4 4
A.原子半径:r(N)>r(O)>r(S) B.沸点:H S>H O>NH
2 2 3
C.第一电离能:I (N)>I (O)>I (S) D.电负性:χ(N)>χ(O)>χ(Cu)
1 1 1
阅读下列材料,完成5~7题:
VA族元素及其化合物应用广泛。NH 催化氧化生成NO,NO继续被氧化为NO ,将NO 通入水中
3 2 2
可制得HNO ;肼(N H )常温下为液态,燃烧热大(642kJmol-1),产物无污染,常用作火箭燃料:白
3 2 4
磷(P )为正四面体结构,常用来制烟雾弹、燃烧弹;雄黄(As S )具有解毒、杀虫功效,燃烧后生成砒
4 4 4
学科网(北京)股份有限公司霜(As O )和一种具有刺激性气味的气体;锑是一种银白色金属,其氧化物Sb O 可用于制造颜料,铅锑
2 3 2 3
合金可用作铅蓄电池的电极材料。
5.下列说法正确的是( )
A.N H 分子中既有极性键,又有非极性键 B.NH 中键角比P 中键角小
2 4 3 4
C.1mol白磷含有4mol P—P键 D.As基态原子核外电子排布式为[Ar]4s24p3
6.下列化学反应表示正确的是( )
点燃
A.雄黄燃烧:As S +7O 2As O +4SO
4 4 2 2 3 2
B.NO 制HNO 的离子方程式:2NO +H O=2H++2NO-
2 3 2 2 3
C.肼的燃烧:N H (l)+O (g)=N (g)+2H O(g) ΔH=-642kJmol-1
2 4 2 2 2
D.铅蓄电池放电时的负极反应:Pb2++2e-=Pb
7.下列有关物质的性质与用途具有对应关系的是( )
A.氨气易液化,可用于工业制硝酸 B.肼具有碱性,可用作火箭燃料
C.三氧化二锑呈白色,可用于制造颜料 D.铅锑合金熔点低,可用作铅蓄电池电极材料
8.普通锌锰干电池的构造如图所示。关于该电池及其工作原理,下列说法正确的是( )
A.石墨作电池的负极材料 B.电池工作时,NH+向负极方向移动
4
C.电池工作时,MnO 发生氧化反应 D.环境温度过低,不利于电池放电
2
9.布洛芬是一种非甾体抗炎药,可用于缓解轻至中度疼痛,部分合成路线如下:
下列有关中间体X、布洛芬的说法正确的是( )
A.X分子中含有1个手性碳原子 B.1mol X最多能与1mol NaOH反应
C.布洛芬不能使酸性KMnO 溶液褪色 D.布洛芬分子中所有碳原子共平面
4
学科网(北京)股份有限公司10.以Cu-ZnO-Al O 作催化剂发生如下反应:
2 3
2CH CHO(g)+H O(g)C H OH(g)+CH COOH(g) ΔH<0,下列说法正确的是( )
3 2 2 5 3
A.该反应的ΔS>0
c
C H OH
c
CH COOH
B.该反应的平衡常数K= 2 5 3
c2
CH CHO
3
C.催化剂Cu-ZnO-Al O 能降低该反应的活化能
2 3
D.该反应中每消耗1mol CH CHO,转移电子数约为26.021023
3
11.下列实验探究方案能达到探究目的的是( )
选项 探究方案 探究目的
向淀粉溶液中加适量20% H SO 溶液,加热,冷却后加新制
2 4
A 淀粉发生水解
Cu(OH) 悬浊液,加热,观察溶液变化
2
向NaCl、NaI的混合稀溶液中滴入少量稀AgNO 溶液,观察
B 3 K (AgCl)>K (AgI)
sp sp
产生沉淀颜色
C 用pH计测定等浓度盐酸和HI溶液的pH Cl的非金属性比I强
向含有FeSO 溶液的试管中滴加几滴KSCN溶液,振荡,再滴
D 4 Fe2+具有还原性
加几滴新制氯水,观察溶液颜色变化
A.A B.B C.C D.D
12.工程师研究利用Na S和FeS处理水样中的Cd2+。已知25C时,K H S =10-6.97,K H S =10-12.90,
2 al 2 a2 2
K (FeS)=10-17.20,K (CdS)=10-26.10。下列说法正确的是( )
sp sp
A.0.01molL-1 Na S溶液中:c OH- =c H+ +c HS- +c H S
2 2
B.0.01molL-1 Na S溶液中:c Na+ >c S2- >c OH- >c HS-
2
c
Fe2+
C.反应FeS+Cd2+ Fe2++CdS正向进行,需满足 >108.9
c
Cd2+
K (CdS)
D.向含Cd2+水样中加入足量FeS浸泡一段时间后,上层清液中存在c Cd2+ = sp
c S2-
13.CH 和CO 联合重整能减少温室气体的排放。重整时发生如下反应:
4 2
学科网(北京)股份有限公司反应I:CH (g)+CO (g)=2H (g)+2CO(g) ΔH =247.1kJmol-1
4 2 2 1
反应Ⅱ:CO (g)+H (g)=CO(g)+H O(g) ΔH =41.2kJmol-1
2 2 2 2
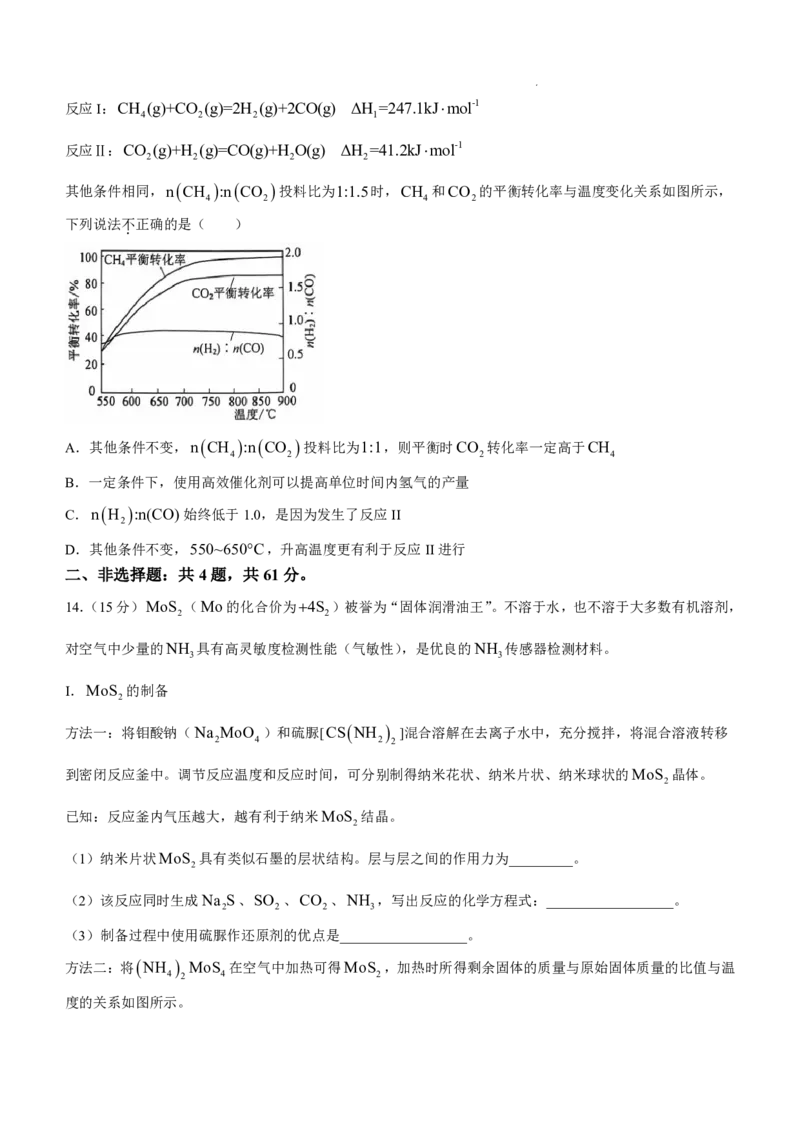
其他条件相同,n CH :n CO 投料比为1:1.5时,CH 和CO 的平衡转化率与温度变化关系如图所示,
4 2 4 2
下列说法不正确的是( )
.
A.其他条件不变,n CH :n CO 投料比为1:1,则平衡时CO 转化率一定高于CH
4 2 2 4
B.一定条件下,使用高效催化剂可以提高单位时间内氢气的产量
C.n H :n(CO)始终低于1.0,是因为发生了反应II
2
D.其他条件不变,550~650C,升高温度更有利于反应II进行
二、非选择题:共 4题,共 61分。
14.(15分)MoS (Mo的化合价为4S )被誉为“固体润滑油王”。不溶于水,也不溶于大多数有机溶剂,
2 2
对空气中少量的NH 具有高灵敏度检测性能(气敏性),是优良的NH 传感器检测材料。
3 3
I.MoS 的制备
2
方法一:将钼酸钠(Na MoO )和硫脲[CS NH ]混合溶解在去离子水中,充分搅拌,将混合溶液转移
2 4 2 2
到密闭反应釜中。调节反应温度和反应时间,可分别制得纳米花状、纳米片状、纳米球状的MoS 晶体。
2
已知:反应釜内气压越大,越有利于纳米MoS 结晶。
2
(1)纳米片状MoS 具有类似石墨的层状结构。层与层之间的作用力为_________。
2
(2)该反应同时生成Na S、SO 、CO 、NH ,写出反应的化学方程式:__________________。
2 2 2 3
(3)制备过程中使用硫脲作还原剂的优点是__________________。
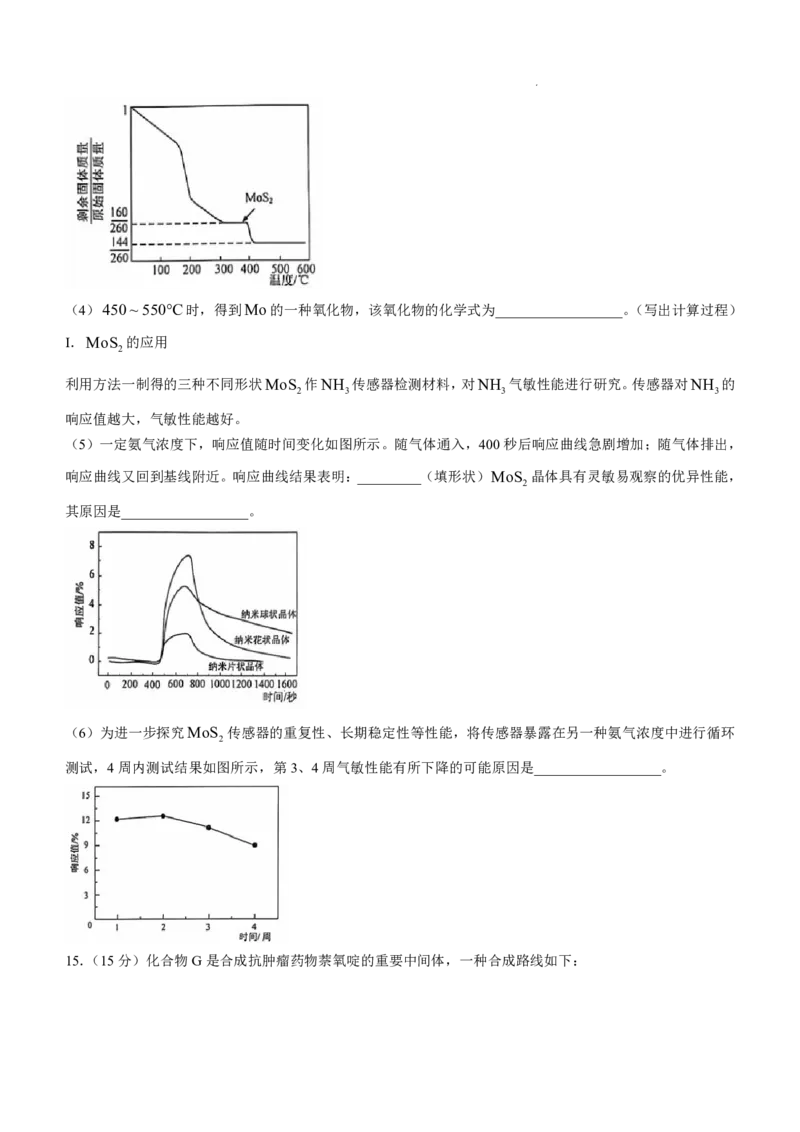
方法二:将 NH MoS 在空气中加热可得MoS ,加热时所得剩余固体的质量与原始固体质量的比值与温
4 2 4 2
度的关系如图所示。
学科网(北京)股份有限公司(4)450~550C时,得到Mo的一种氧化物,该氧化物的化学式为__________________。(写出计算过程)
I.MoS 的应用
2
利用方法一制得的三种不同形状MoS 作NH 传感器检测材料,对NH 气敏性能进行研究。传感器对NH 的
2 3 3 3
响应值越大,气敏性能越好。
(5)一定氨气浓度下,响应值随时间变化如图所示。随气体通入,400秒后响应曲线急剧增加;随气体排出,
响应曲线又回到基线附近。响应曲线结果表明:_________(填形状)MoS 晶体具有灵敏易观察的优异性能,
2
其原因是__________________。
(6)为进一步探究MoS 传感器的重复性、长期稳定性等性能,将传感器暴露在另一种氨气浓度中进行循环
2
测试,4周内测试结果如图所示,第3、4周气敏性能有所下降的可能原因是__________________。
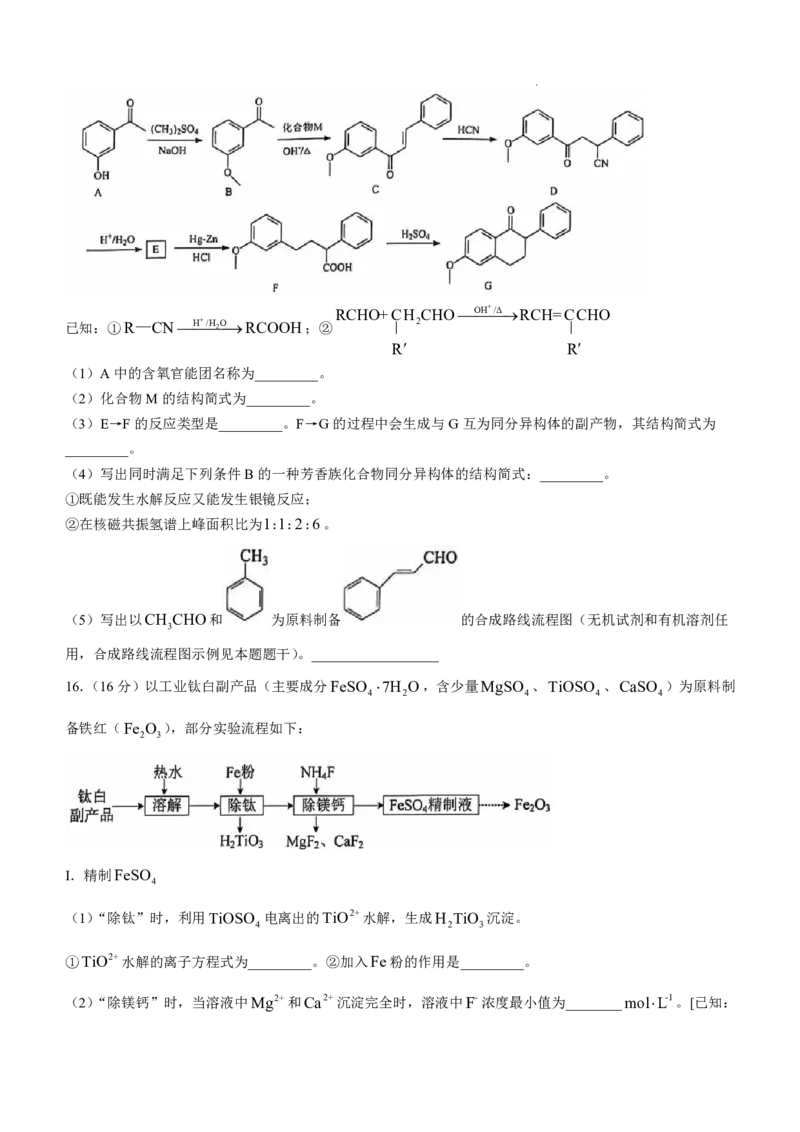
15.(15分)化合物G是合成抗肿瘤药物萘氧啶的重要中间体,一种合成路线如下:
学科网(北京)股份有限公司RCHO+CH CHO
OH+/ΔRCH=CCHO
已知:①R—CNH+/H2 ORCOOH;② | 2 |
R R
(1)A中的含氧官能团名称为_________。
(2)化合物M的结构简式为_________。
(3)E→F的反应类型是_________。F→G的过程中会生成与G互为同分异构体的副产物,其结构简式为
_________。
(4)写出同时满足下列条件B的一种芳香族化合物同分异构体的结构简式:_________。
①既能发生水解反应又能发生银镜反应;
②在核磁共振氢谱上峰面积比为1:1:2:6。
(5)写出以CH CHO和 为原料制备 的合成路线流程图(无机试剂和有机溶剂任
3
用,合成路线流程图示例见本题题干)。__________________
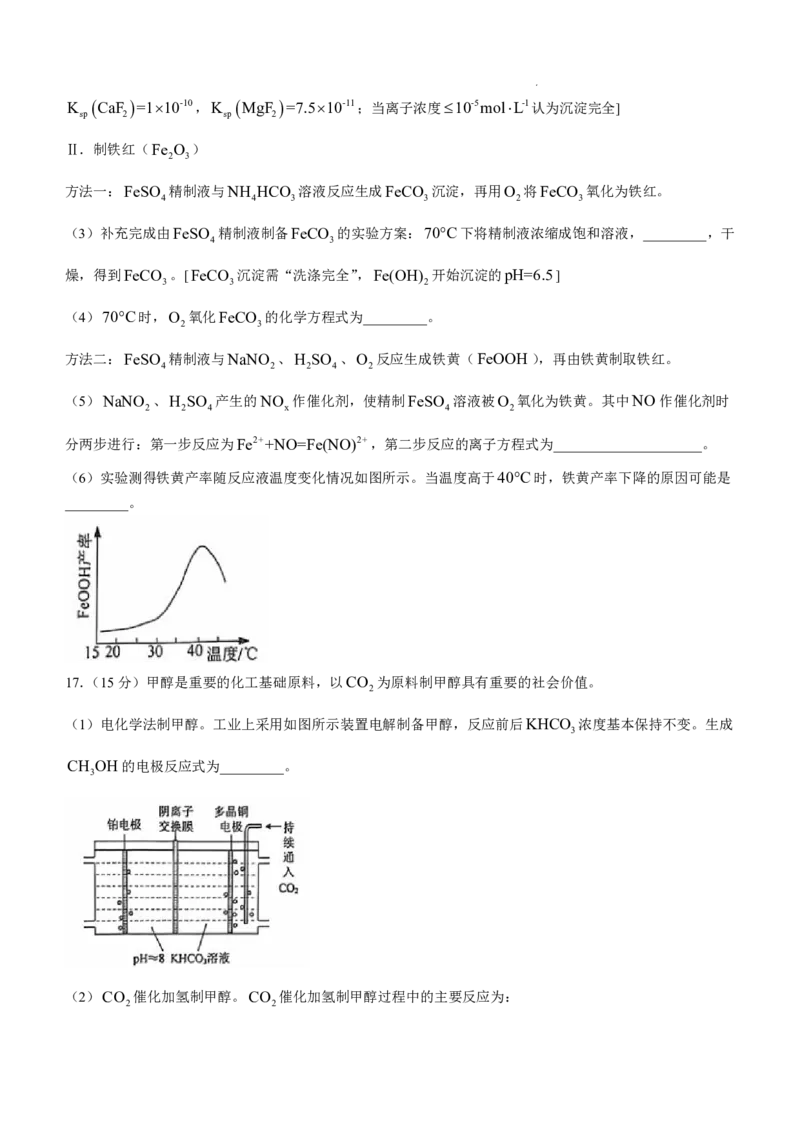
16.(16分)以工业钛白副产品(主要成分FeSO 7H O,含少量MgSO 、TiOSO 、CaSO )为原料制
4 2 4 4 4
备铁红(Fe O ),部分实验流程如下:
2 3
I.精制FeSO
4
(1)“除钛”时,利用TiOSO 电离出的TiO2+水解,生成H TiO 沉淀。
4 2 3
①TiO2+水解的离子方程式为_________。②加入Fe粉的作用是_________。
(2)“除镁钙”时,当溶液中Mg2+和Ca2+沉淀完全时,溶液中F-浓度最小值为________molL-1。[已知:
学科网(北京)股份有限公司K CaF =110-10,K MgF =7.510-11;当离子浓度10-5molL-1认为沉淀完全]
sp 2 sp 2
Ⅱ.制铁红(Fe O )
2 3
方法一:FeSO 精制液与NH HCO 溶液反应生成FeCO 沉淀,再用O 将FeCO 氧化为铁红。
4 4 3 3 2 3
(3)补充完成由FeSO 精制液制备FeCO 的实验方案:70C下将精制液浓缩成饱和溶液,_________,干
4 3
燥,得到FeCO 。[FeCO 沉淀需“洗涤完全”,Fe(OH) 开始沉淀的pH=6.5]
3 3 2
(4)70C时,O 氧化FeCO 的化学方程式为_________。
2 3
方法二:FeSO 精制液与NaNO 、H SO 、O 反应生成铁黄(FeOOH),再由铁黄制取铁红。
4 2 2 4 2
(5)NaNO 、H SO 产生的NO 作催化剂,使精制FeSO 溶液被O 氧化为铁黄。其中NO作催化剂时
2 2 4 x 4 2
分两步进行:第一步反应为Fe2++NO=Fe(NO)2+,第二步反应的离子方程式为_____________________。
(6)实验测得铁黄产率随反应液温度变化情况如图所示。当温度高于40C时,铁黄产率下降的原因可能是
_________。
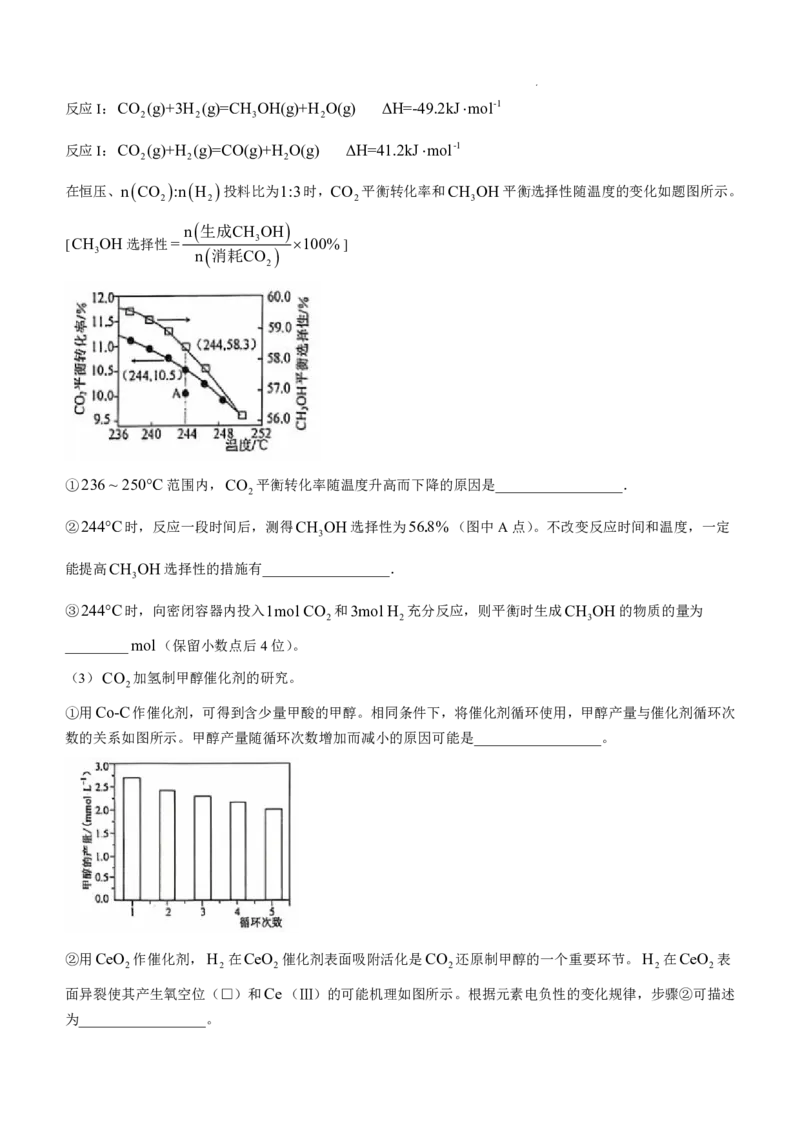
17.(15分)甲醇是重要的化工基础原料,以CO 为原料制甲醇具有重要的社会价值。
2
(1)电化学法制甲醇。工业上采用如图所示装置电解制备甲醇,反应前后KHCO 浓度基本保持不变。生成
3
CH OH的电极反应式为_________。
3
(2)CO 催化加氢制甲醇。CO 催化加氢制甲醇过程中的主要反应为:
2 2
学科网(北京)股份有限公司反应I:CO (g)+3H (g)=CH OH(g)+H O(g) ΔH=-49.2kJmol-1
2 2 3 2
反应I:CO (g)+H (g)=CO(g)+H O(g) ΔH=41.2kJmol-1
2 2 2
在恒压、n CO :n H 投料比为1:3时,CO 平衡转化率和CH OH平衡选择性随温度的变化如题图所示。
2 2 2 3
n
生成CH
OH
[CH OH选择性= 3 100%]
3 n 消耗CO
2
①236~ 250C范围内,CO 平衡转化率随温度升高而下降的原因是__________________.
2
②244C时,反应一段时间后,测得CH OH选择性为56.8%(图中A点)。不改变反应时间和温度,一定
3
能提高CH OH选择性的措施有__________________.
3
③244C时,向密闭容器内投入1mol CO 和3mol H 充分反应,则平衡时生成CH OH的物质的量为
2 2 3
_________mol(保留小数点后4位)。
(3)CO 加氢制甲醇催化剂的研究。
2
①用Co-C作催化剂,可得到含少量甲酸的甲醇。相同条件下,将催化剂循环使用,甲醇产量与催化剂循环次
数的关系如图所示。甲醇产量随循环次数增加而减小的原因可能是__________________。
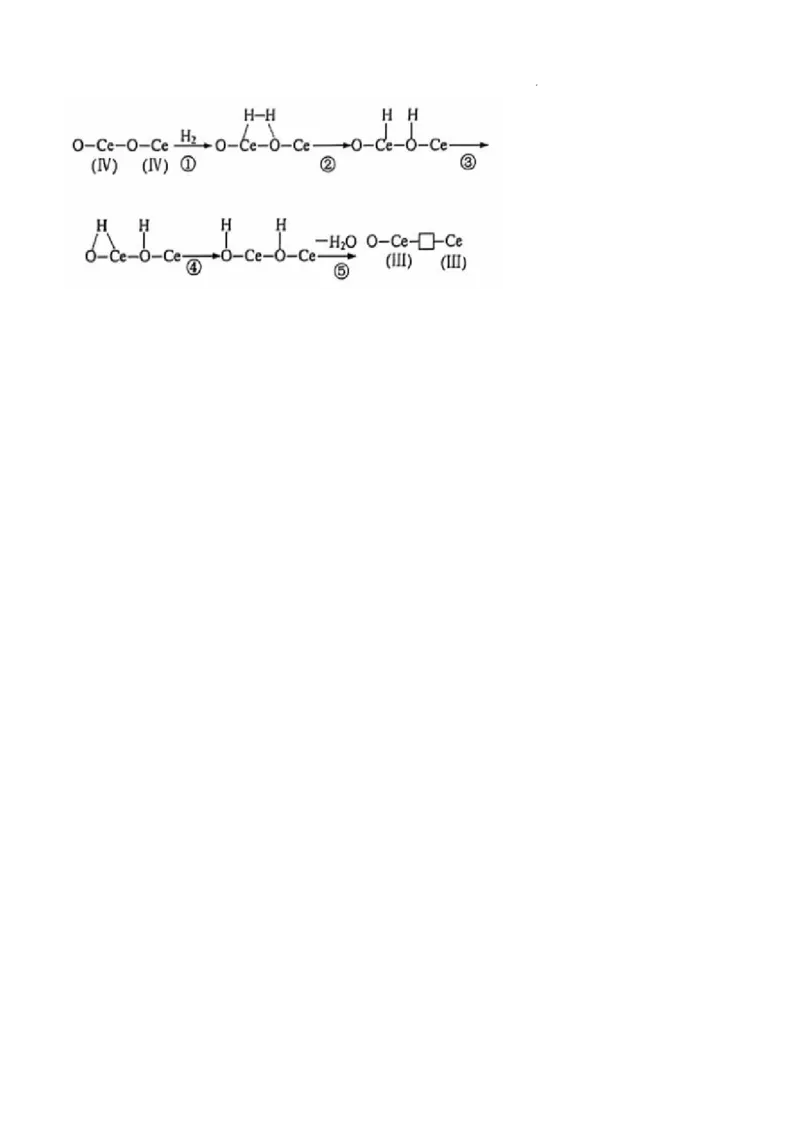
②用CeO 作催化剂,H 在CeO 催化剂表面吸附活化是CO 还原制甲醇的一个重要环节。H 在CeO 表
2 2 2 2 2 2
面异裂使其产生氧空位(□)和Ce(Ⅲ)的可能机理如图所示。根据元素电负性的变化规律,步骤②可描述
为__________________。
学科网(北京)股份有限公司学科网(北京)股份有限公司