文档内容
南漳一中
高二年级 12 月教学交流考试化学学科试题
河口一中
宜城一中 出题人: 学校 宜城一中 审题人: 学校 宜城一中
考试时间:75分钟 分值:100分
第Ⅰ卷
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.化学与社会、科学、技术、环境密切相关,下列说法错误的是
A.人体中 缓冲体系起到稳定血液pH的作用
B.中国古代利用明矾溶液的酸性清除铜镜表面的铜锈
C.天宫课堂“五环实验”,向碳酸钠溶液中滴加甲基橙溶液后变成红色
D.古代中国人发明的酒曲酿酒利用了催化剂加快反应速率的原理
2.下列有关化学用语表示正确的是
A. 的电子式:
B.S的原子结构示意图:
C. Cr的原子核外电子排布式:[Ar]3d 4s
24 4 2
D.电子排布图 违背了洪特规则
3.下列实验事实不能用勒夏特列原理来解释的是
A.用 与稀硫酸制氢气时,为加快反应速率,将锌片换成锌粉
B.向 溶液中加入铁粉,溶液颜色变浅
C.配制 溶液时将 晶体溶在浓盐酸中再加水稀释到所需浓度
D.向2mL0.1mol/LK Cr O 溶液中滴加10滴6mol/LNaOH溶液,溶液变为黄色
2 2 7
4.常温下,下列各组离子在相应的条件下一定能大量共存的是
A.0.2mol/L的 溶液中: 、 、 、
B. 的溶液中: 、 、 、
C. 的溶液中: 、 、 、
D.由水电离产生的 的溶液中: 、 、 、
5.劳动创造美好生活。下列劳动项目与所述的化学知识没有关联的是
选 劳动项目 化学知识
项
升高温度,能促进纯碱的水解,溶液碱性增强,更有利于酯的水解
A 用热的纯碱溶液洗涤餐具上的油污
B 用 Fe (SO ) 可作净水剂 Fe3+有氧化性
2 4 3C 灰混粪,粪混灰,灰粪相混损肥分 草木灰与铵态氮肥混合发生双水解
D 用冰箱保存疫苗 温度越低,反应速率越慢
6.近期发现,H S是继NO、CO之后的第三个生命体系气体信号分子,它具有参与调节神经信
2
号传递、舒张血管减轻高血压的功能。下列事实中,不能比较氢硫酸与亚硫酸的酸性强弱的
是
A.氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸可以
B.氢硫酸的导电能力低于相同浓度的亚硫酸
C.0.10mol/L的氢硫酸和亚硫酸的pH分别为4.5和2.1
D.氢硫酸的还原性强于亚硫酸
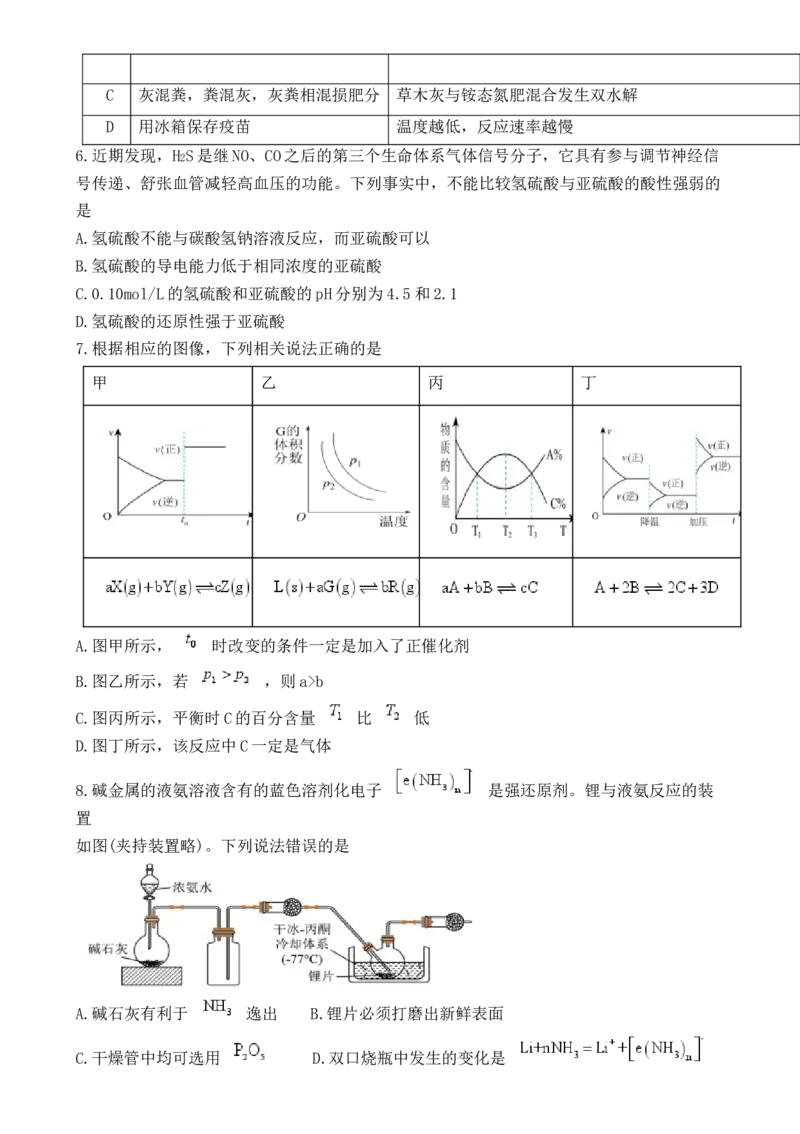
7.根据相应的图像,下列相关说法正确的是
甲 乙 丙 丁
A.图甲所示, 时改变的条件一定是加入了正催化剂
B.图乙所示,若 ,则a>b
C.图丙所示,平衡时C的百分含量 比 低
D.图丁所示,该反应中C一定是气体
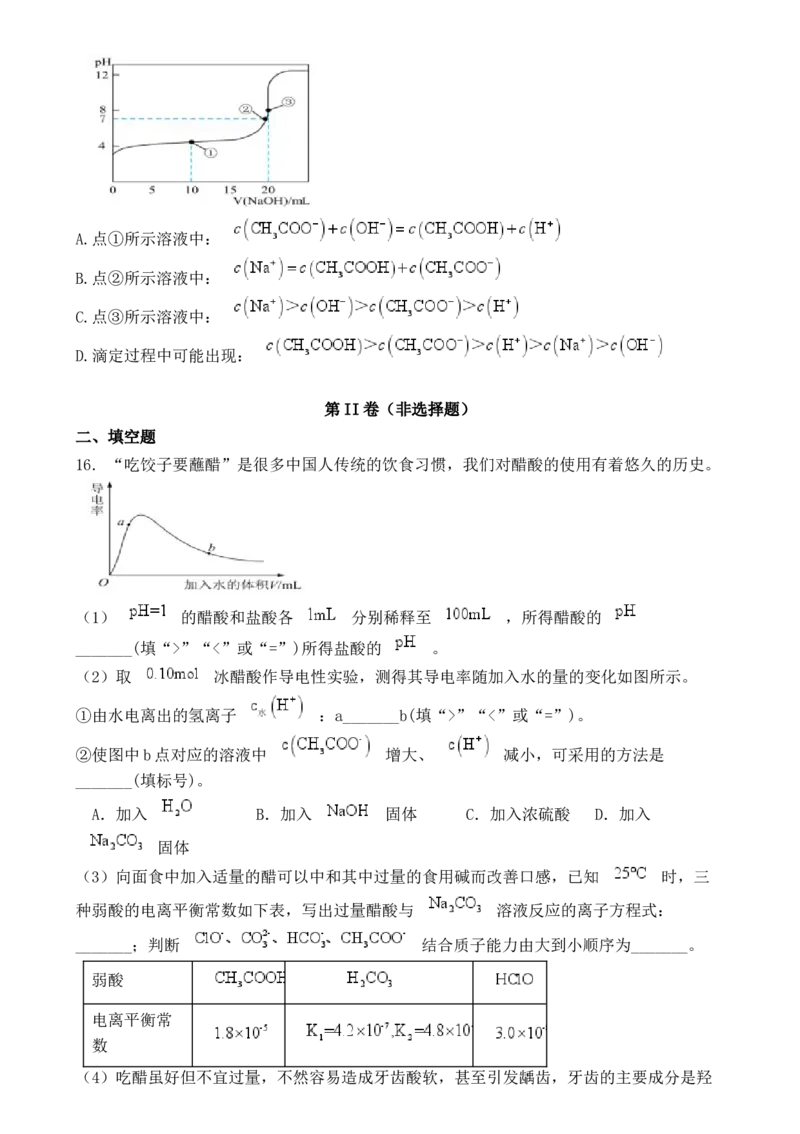
8.碱金属的液氨溶液含有的蓝色溶剂化电子 是强还原剂。锂与液氨反应的装
置
如图(夹持装置略)。下列说法错误的是
A.碱石灰有利于 逸出 B.锂片必须打磨出新鲜表面
C.干燥管中均可选用 D.双口烧瓶中发生的变化是9.液氨与纯水类似,也存在微弱的电离: ,T℃时,液氨的离子积常
数 ,若用定义 的方式来规定 ,则下列叙
述正确的是
A.其他条件不变,增加液氨的量,电离平衡正向移动
B.液氨达到电离平衡时
C.T℃时的液氨中,
D.一定温度下,向液氨中加入氯化铵固体,电离平衡逆向移动,K值减小
10.哈伯在1908年申请循环法合成氨的专利,合成氨实验所用装置如下。下列说法不正确的
是
A.进口a通入的是经过压缩的N 和H
2 2
B.出口b的气体可以直接通入饿催化剂反应器
C.出口c是液态NH 出口,可用于冷却离开催化剂的气体
3
D.冷却水从A口进,B口出,用来给合成氨反应降温防止温度过热
11.下列判断正确的有几项:
①中和等体积、等pH的盐酸和醋酸,中和盐酸所需氢氧化钠的物质的量小于醋酸
②配置 溶液要加入铁粉,配置 溶液要加入盐酸,二者原理相同
③电解精炼铜,阳极为纯铜、阴极为粗铜,电解质溶液可以是硫酸铜或氯化铜溶液
④用 固体作为沉淀剂除去工业废水中的 :
,反
应达平衡后,继续加入 , 的去除率增大
⑤镀锌或镀锡的钢管在镀层破损后仍能对钢管起保护作用
⑥水电离出的 为 的溶液一定呈中性
A.0项 B.1项 C.2项 D.3项
12.某温度下,在密闭容器中充入一定量的X(g),发生下列反应:X(g) Y(g)(ΔH <0),
1
Y(g) Z(g)(ΔH <0),测得各气体浓度与反应时间的关系如图所示。下列反应进程示意图符
2 ⇌
合题意的是
⇌A. B. C. D.
13.恒容高压氢气氛围中,CO在铑基催化剂表面主要发生的反应为
,该反应的速率方程为v=kc (CO) ,其中k
2
为速率常数。下列说法中错误的是
A.在该体系中加入适量生石灰,可提高反应物的平衡转化率
B.充入CO的量越多,平衡体系中 的浓度越大
C.在该体系中继续充入 ,可提高反应速率
D.对铑基催化剂进行改良,可能会进一步提高催化效率
14. 我国科学家设计如图所示的电解池,实现了海水直接制备氢气技术的绿色化。该装置工
作时阳极无 生成且KOH溶液的浓度不变,电解生成氢气的速率为 。下列
说法错误的是
A.b电极反应式为
B.海水为电解池补水的速率为
C.离子交换膜为阴离子交换膜
D.电解时海水中动能高的水分子可穿过PTFE膜
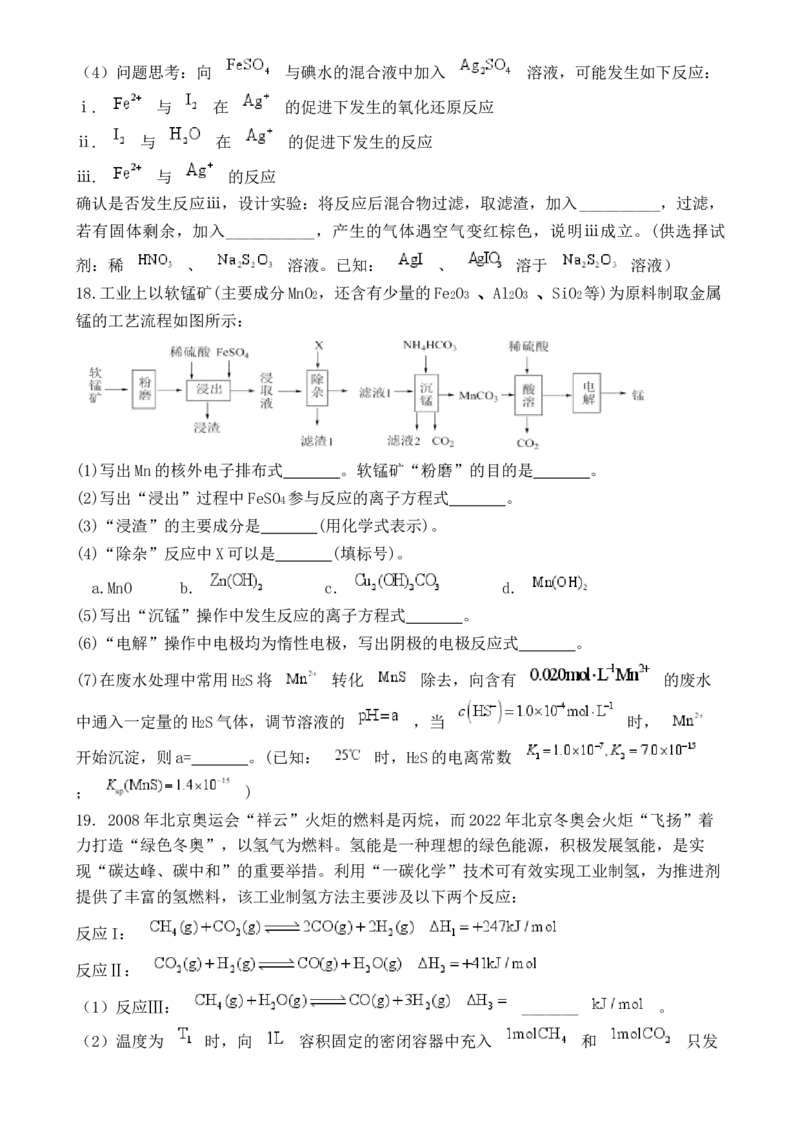
15.常温下,用 0.1000 mol·L NaOH溶液滴定 20.00mL0.1000 mol·L
溶液所得滴定曲线如图。下列说法正确的是A.点①所示溶液中:
B.点②所示溶液中:
C.点③所示溶液中:
D.滴定过程中可能出现:
第II卷(非选择题)
二、填空题
16. “吃饺子要蘸醋”是很多中国人传统的饮食习惯,我们对醋酸的使用有着悠久的历史。
(1) 的醋酸和盐酸各 分别稀释至 ,所得醋酸的
_______(填“>”“<”或“=”)所得盐酸的 。
(2)取 冰醋酸作导电性实验,测得其导电率随加入水的量的变化如图所示。
①由水电离出的氢离子 :a_______b(填“>”“<”或“=”)。
②使图中b点对应的溶液中 增大、 减小,可采用的方法是
_______(填标号)。
A.加入 B.加入 固体 C.加入浓硫酸 D.加入
固体
(3)向面食中加入适量的醋可以中和其中过量的食用碱而改善口感,已知 时,三
种弱酸的电离平衡常数如下表,写出过量醋酸与 溶液反应的离子方程式:
_______;判断 结合质子能力由大到小顺序为_______。
弱酸
电离平衡常
数
(4)吃醋虽好但不宜过量,不然容易造成牙齿酸软,甚至引发龋齿,牙齿的主要成分是羟基磷灰石 ,市面上含氟牙膏常添加了 来预防龋齿,请结合化学
用语解释含氟牙膏预防龋齿的原因:__________________________[已知 难
溶于酸]。
(5)常温下,某同学取 物质的量浓度为 的醋酸,向其中滴入
溶液,当滴入的 溶液的体积为 ,溶液呈中性,
则醋酸的电离平衡常数 _______(用含x的代数式表示)。
17. 小组验证“ ”(反应A)存在限度,并探究外加试剂对该平衡
的影响。
(1)从正反应方向探究实验。取 溶液,加入 溶
液 ,溶液呈棕黄色,不再发生变化。(已知I 易溶于 )
2
①通过检测出___________,证实反应A存在限度。化学实验中常用___________(填化学
式)检验 ,现象是出现蓝色沉淀。
②加入 ,振荡,平衡向___________反应移动(填“正”或“逆”)。
(2)从逆反应方向探究实验:向碘水(含淀粉)中加入酸性 溶液,无明显变化,未
检出 。
①甲同学认为加入 溶液可增大 与 的反应程度。甲同学依据的原理是
________。
②验证:加入 溶液,产生沉淀a,溶液蓝色褪去,能检出 。
(3)乙同学认为碘水中含有 ,加入 溶液也可能产生沉淀。做对照实验:直
接向碘水(含淀粉)中加入 溶液。产生沉淀,溶液蓝色褪去。
查阅资料:
实验验证:
已知: 、 (微溶)
①Ⅲ中KI溶液的作用是___________(用离子方程式表示)。
②Ⅳ中KI溶液的作用是___________(用离子方程式表示)。(4)问题思考:向 与碘水的混合液中加入 溶液,可能发生如下反应:
ⅰ. 与 在 的促进下发生的氧化还原反应
ⅱ. 与 在 的促进下发生的反应
ⅲ. 与 的反应
确认是否发生反应ⅲ,设计实验:将反应后混合物过滤,取滤渣,加入__________,过滤,
若有固体剩余,加入___________,产生的气体遇空气变红棕色,说明ⅲ成立。(供选择试
剂:稀 、 溶液。已知: 、 溶于 溶液)
18.工业上以软锰矿(主要成分MnO ,还含有少量的Fe O 、Al O 、SiO 等)为原料制取金属
2 2 3 2 3 2
锰的工艺流程如图所示:
(1)写出Mn的核外电子排布式 。软锰矿“粉磨”的目的是 。
(2)写出“浸出”过程中FeSO 参与反应的离子方程式 。
4
(3)“浸渣”的主要成分是 (用化学式表示)。
(4)“除杂”反应中X可以是 (填标号)。
a.MnO b. c. d.
(5)写出“沉锰”操作中发生反应的离子方程式 。
(6)“电解”操作中电极均为惰性电极,写出阴极的电极反应式 。
(7)在废水处理中常用H S将 转化 除去,向含有 的废水
2
中通入一定量的H S气体,调节溶液的 ,当 时,
2
开始沉淀,则a= 。(已知: 时,H S的电离常数
2
; )
19. 2008年北京奥运会“祥云”火炬的燃料是丙烷,而2022年北京冬奥会火炬“飞扬”着
力打造“绿色冬奥”,以氢气为燃料。氢能是一种理想的绿色能源,积极发展氢能,是实
现“碳达峰、碳中和”的重要举措。利用“一碳化学”技术可有效实现工业制氢,为推进剂
提供了丰富的氢燃料,该工业制氢方法主要涉及以下两个反应:
反应I:
反应Ⅱ:
(1)反应Ⅲ: _______ 。
(2)温度为 时,向 容积固定的密闭容器中充入 和 只发生反应I,初始压强为 后达到平衡,平衡时体系压强为初始压强的 。
①该条件下,该时段内 _______,反应I的压强平衡常数 _______
(已知分压=总压×物质的量分数)。
②反应I在_______(填“高温”或“低温”)下可自发进行。达上述平衡后,向容器中充入
和 ,此时反应I的 _______
(填“>”“<”或“=”)。
(3)研究表明,反应Ⅱ的逆反应在 催化下进
行,反应历程如图所示,写出该反应历程中速率控制
步骤(即速率最慢步骤)对应的反应方程式:_______。
(4)氢能的高效利用途径之一是在燃料电池中产生电能。某研究小组的自制熔融碳酸盐燃
料电池工作原理如图2所示,正极上的电极反应式是_________。该电池以 恒定电
流工作14分钟,消耗 体积为 ,故可测得该电池将化学能转化为电能的转化
率为_______。[已知:该条件下 的摩尔体积为 ;电荷量 电流
时间 ; ;
。]