文档内容
哈师大附中 2023 级高二上期中考试化学试题
可能用到的相对原子质量:H1 C12 N14 O16 Cl35.5 Fe56
一、单选题(共22小题,每小题2分,共44分)
1.下列有关水蒸汽变成雨的过程中焓变和熵变的判断正确的是( )
A.H 0,S 0 B.H 0,S 0
C.H 0,S 0 D.H 0,S 0
2.下列描述原子结构的化学用语错误的是( )
A.基态Br原子的价层电子排布式:3d104s24p5
B.Mn2的价电子轨道表示式:
C.钛原子结构示意图:
D.氧原子核外能量最高能级的电子云轮廓图:
3.反应A g 3B g 2C g 2D g 在四种不同情况下的反应速率分别为:
①v A 0.6molL1min1 ②v B 0.45molL1s1③v C 0.4molL1s1④v D 0.45molL1s1
该反应进行的快慢顺序为( )
A.①>③>④>② B.④>③>②>① C.①>④>②>③ D.①>④>③>②
4.下列不属于水解反应或水解方程式书写不正确的个数有( )
①F H O HFOH
2
②AlCl 3H OAl OH 3HCl
3 2 3
③Na CO 2H O H CO 2NaOH
2 3 2 2 3
④NH Cl溶于D O中:NH D O NH D OH
4 2 4 2 3 2
A.1个 B.2个 C.3个 D.4个
5.设N 为阿伏加德罗常数的值,下列说法不正确的是( )
A
A.常温常压下,0.1molNH 与0.1molHCl 充分反应后所得产物含有的分子数为0.1N
3 A
B.20gNO 和26gN O 的混合气体中氧原子总数为2N
2 2 4 A
C.100g质量分数为46%的乙醇溶液中,含OH键的数目为7N
A
D.在25℃时,1LpH2的H SO 溶液中含有H数目为0.01N
2 4 A
学科网(北京)股份有限公司 16.下列关于盐类水解的说法中正确的是( )
A.加热蒸干Na CO 溶液,最后得到NaOH固体
2 3
B.可以加入NaOH固体来除去MgCl 溶液中的Fe3
2
C.泡沫灭火器的原理可表示为Al3 3HCO Al OH 3CO
3 3 2
D.配制FeCl 溶液时,加入铁粉的目的是防止Fe2水解
2
7.下列事实能用勒夏特列原理来解释的是( )
A.工业制硫酸中常采用常压来合成SO
3
B.实验室中用饱和的NaHSO 溶液除掉SO 气体中少量氯化氢
3 2
C.500℃左右比室温更有利于合成氨反应[已知N g 3H g 2NH g H 0
2 2 3
D.对于反应2HI g H g I g 达平衡后,缩小容器体积可使体系颜色变深
2 2
8.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.pH7的溶液中:K、ClO、CO2、Cl
3
B.在0.1molL1氯化钠溶液中:Fe3、SO2、Ca2、HCO
4 3
C.无色溶液中:H、Na、Cl、NO
3
D.由水电离的c H 1012molL1的溶液中:Na、NH、Cl、K
4
9.下列实验能达到相应目的的是( )
A.测中和热 B. 排 出 盛 有
C.制备无水 MgCl D.研究H浓度对平衡移动的
2
KMnO 溶液滴
4 固体 影响
定管尖嘴内的气
泡
学科网(北京)股份有限公司 210.已知N g 3H g 2NH g H 92kJmol1 S 198Jmol1。工业合成氨的流程如图所
2 2 3
示。下列说法正确的是( )
A.步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率,所以生产中压强越大越好
B.高温可以加快反应速率,所以生产中温度越高越好
C.步骤②④⑤⑥均有利于提高原料的平衡转化率
D.步骤③中热交换的目的是为原料气提供热量,提高经济效益
11.常温下,下列叙述正确的是( )
A.pH2的盐酸与pH12的氨水等体积混合后pH7
B.pH4的醋酸溶液,稀释至原体积的10倍后pH5
C.pH10的醋酸钠溶液与等体积水混合后pH9
D.将水加热至100℃,其pH6,所以水在100℃时呈酸性
12.常温下,pH13的强碱溶液与pH2的强酸溶液混合,所得混合液的pH11,则强碱与强酸的体积比是( )
A.11:1 B.9:1 C.1:11 D.1:9
13.短周期主族元素X、Y、Z、W的原子序数依次增大,Z可与X形成淡黄色化合物Z X ,Y、W最外层电子数相
2 2
同。下列说法正确的是( )
A.第一电离能:W>X>Y>Z B.简单离子的还原性:Y>X>W
C.简单离子的半径:W>X>Y>Z D.氢化物水溶液的酸性:Y>W
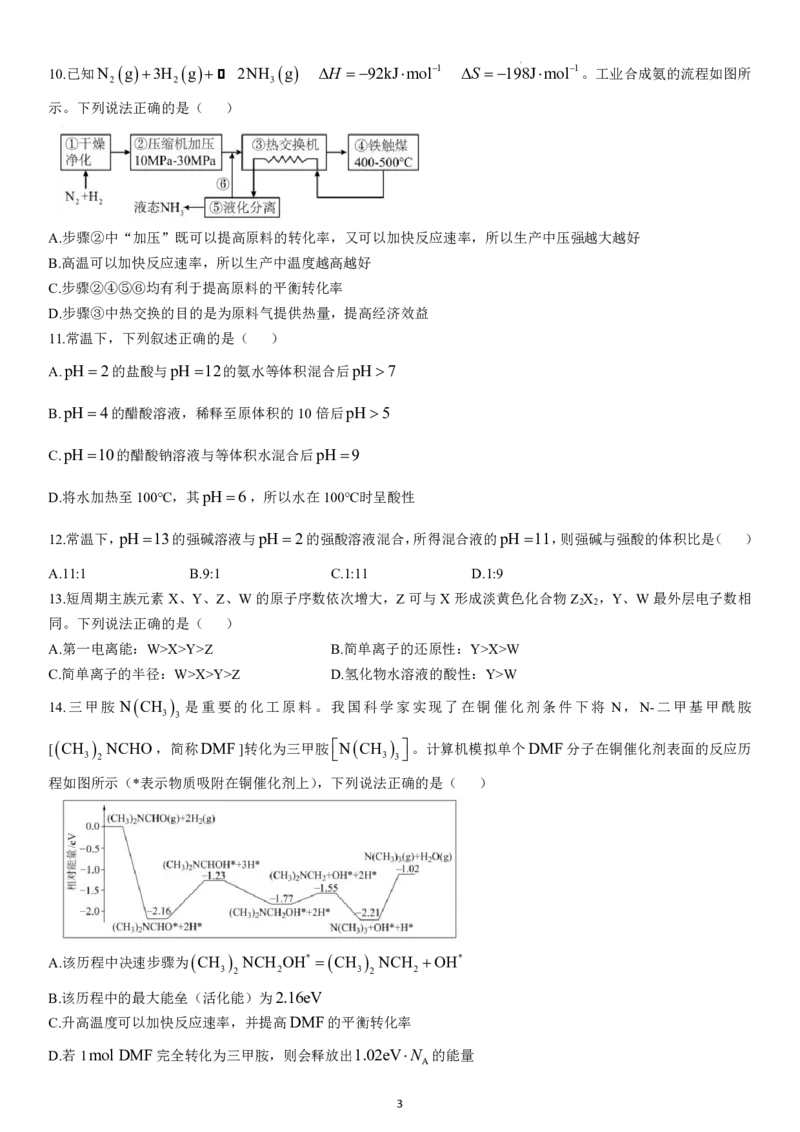
14.三甲胺 N CH 是重要的化工原料。我国科学家实现了在铜催化剂条件下将 N,N-二甲基甲酰胺
3 3
[ CH 3 2 NCHO,简称DMF]转化为三甲胺 N CH 3 3 。计算机模拟单个DMF分子在铜催化剂表面的反应历
程如图所示(*表示物质吸附在铜催化剂上),下列说法正确的是( )
A.该历程中决速步骤为 CH NCH OH* CH NCH OH*
3 2 2 3 2 2
B.该历程中的最大能垒(活化能)为2.16eV
C.升高温度可以加快反应速率,并提高DMF的平衡转化率
D.若1mol DMF完全转化为三甲胺,则会释放出1.02eVN 的能量
A
学科网(北京)股份有限公司 315.现有HX、H Y和H Z三种酸,各酸及其盐之间不发生氧化还原反应,它们的电离常数如下表所示。下列说法
2 2
正确的是( )
酸 HX
H Y H Z
2 2
电离常数(25℃)
K 109.2 K 106.4 , K 101.9 ,
a a1 a1
K 1010.3 K 107.2
a2 a2
A.三种酸的强弱关系:H ZH YHX
2 2
B.在水溶液中结合H的能力:Y2 Z2
C.Na Y溶液与过量HX溶液混合:HXY2 HY X
2
D.NaHY溶液与NaHZ溶液混合:HY HZ H YZ2
2
16.常温下,下列有关电解质溶液的说法正确的是( )
c
H
A.向0.1molL1CH COOH 溶液中加入少量水,溶液 减小
3 c CH COOH
3
c
CH
COO
B.将CH COONa溶液从20℃温至30℃,溶液中 3 增大
3
c
CH COOH
c OH
3
C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液中:c
Na
c
CH
COO
c
H
c
OH
3
D.H S溶液与NaOH溶液混合,所得混合溶液中:c
Na
c
H
c
OH
2c
S2
c
HS
2
17.吡啶 C H N 是一种有机弱碱,可与盐酸反应生成盐酸盐(C H NHCl)。下列关于0.01molL1C H NHCl 水
5 5 5 5 5 5
溶液的叙述正确的是( )
A.水溶液的pH2
B.加水稀释,pH降低
C.水溶液中:c
H
c
C H
NH
c
OH
5 5
D.水溶液中:c
Cl
c
C H
NH
c
H
5 5
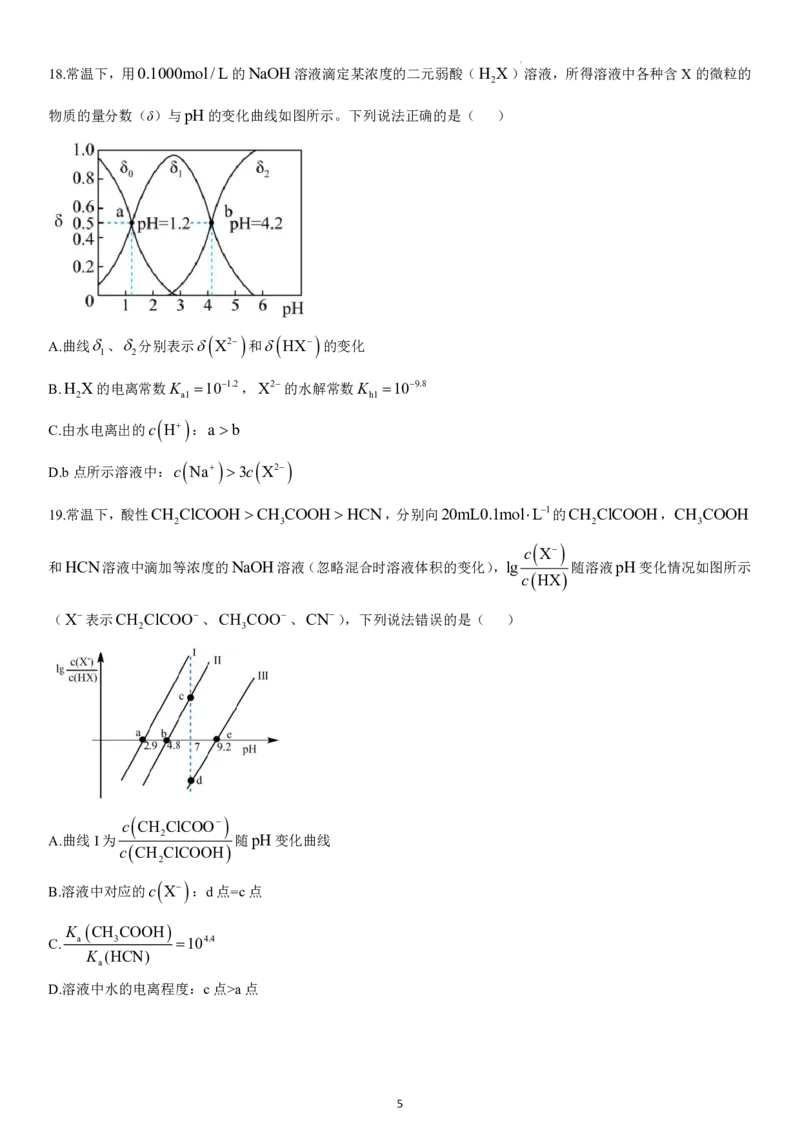
学科网(北京)股份有限公司 418.常温下,用0.1000mol/L的NaOH溶液滴定某浓度的二元弱酸(H X)溶液,所得溶液中各种含X的微粒的
2
物质的量分数(δ)与pH的变化曲线如图所示。下列说法正确的是( )
A.曲线、分别表示
X2
和
HX
的变化
1 2
B.H X的电离常数K 101.2,X2的水解常数K 109.8
2 a1 h1
C.由水电离出的c
H
:a b
D.b点所示溶液中:c
Na
3c
X2
19.常温下,酸性CH ClCOOHCH COOHHCN,分别向20mL0.1molL1的CH ClCOOH,CH COOH
2 3 2 3
c
X
和HCN溶液中滴加等浓度的NaOH溶液(忽略混合时溶液体积的变化),lg 随溶液pH变化情况如图所示
c HX
(X表示CH ClCOO、CH COO、CN),下列说法错误的是( )
2 3
c
CH
ClCOO
A.曲线I为 2 随pH变化曲线
c CH ClCOOH
2
B.溶液中对应的c
X
:d点=c点
K CH COOH
C. a 3 104.4
K (HCN)
a
D.溶液中水的电离程度:c点>a点
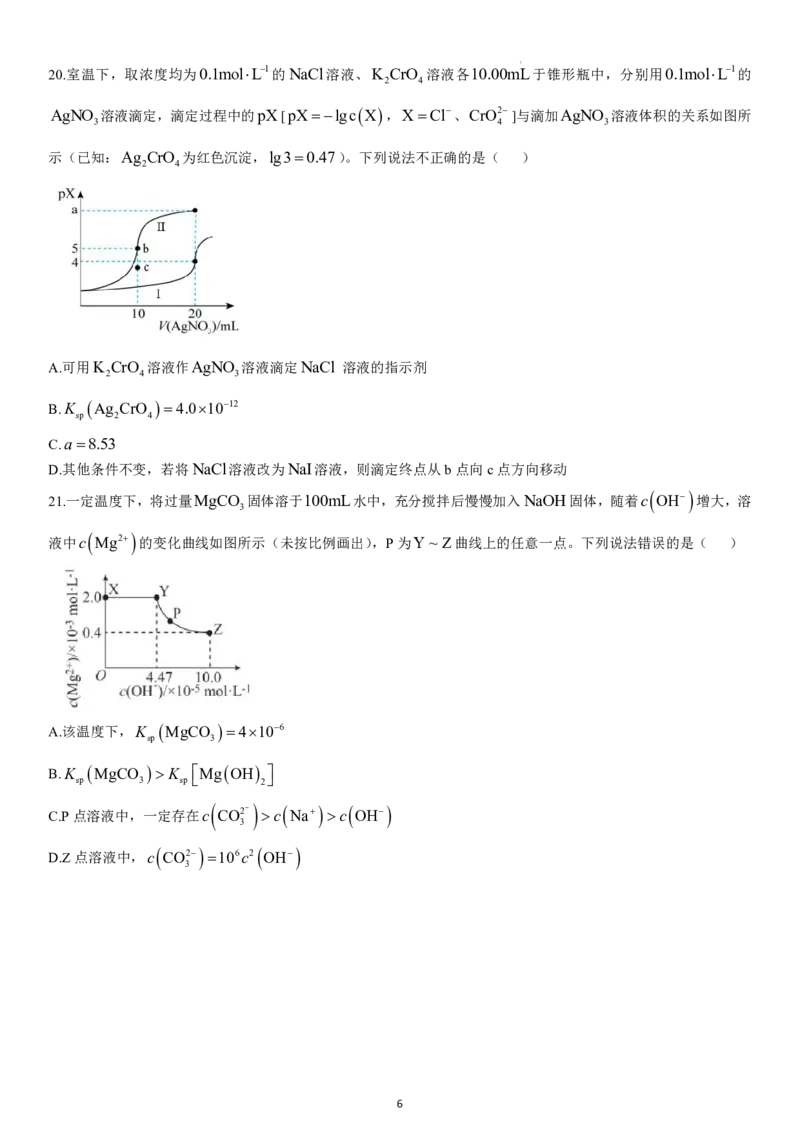
学科网(北京)股份有限公司 520.室温下,取浓度均为0.1molL1的NaCl溶液、K CrO 溶液各10.00mL于锥形瓶中,分别用0.1molL1的
2 4
AgNO 溶液滴定,滴定过程中的pX[pXlgc X ,XCl、CrO2 ]与滴加AgNO 溶液体积的关系如图所
3 4 3
示(已知:Ag CrO 为红色沉淀,lg30.47)。下列说法不正确的是( )
2 4
A.可用K CrO 溶液作AgNO 溶液滴定NaCl 溶液的指示剂
2 4 3
B.K
Ag CrO
4.01012
sp 2 4
C.a8.53
D.其他条件不变,若将NaCl溶液改为NaI溶液,则滴定终点从b点向c点方向移动
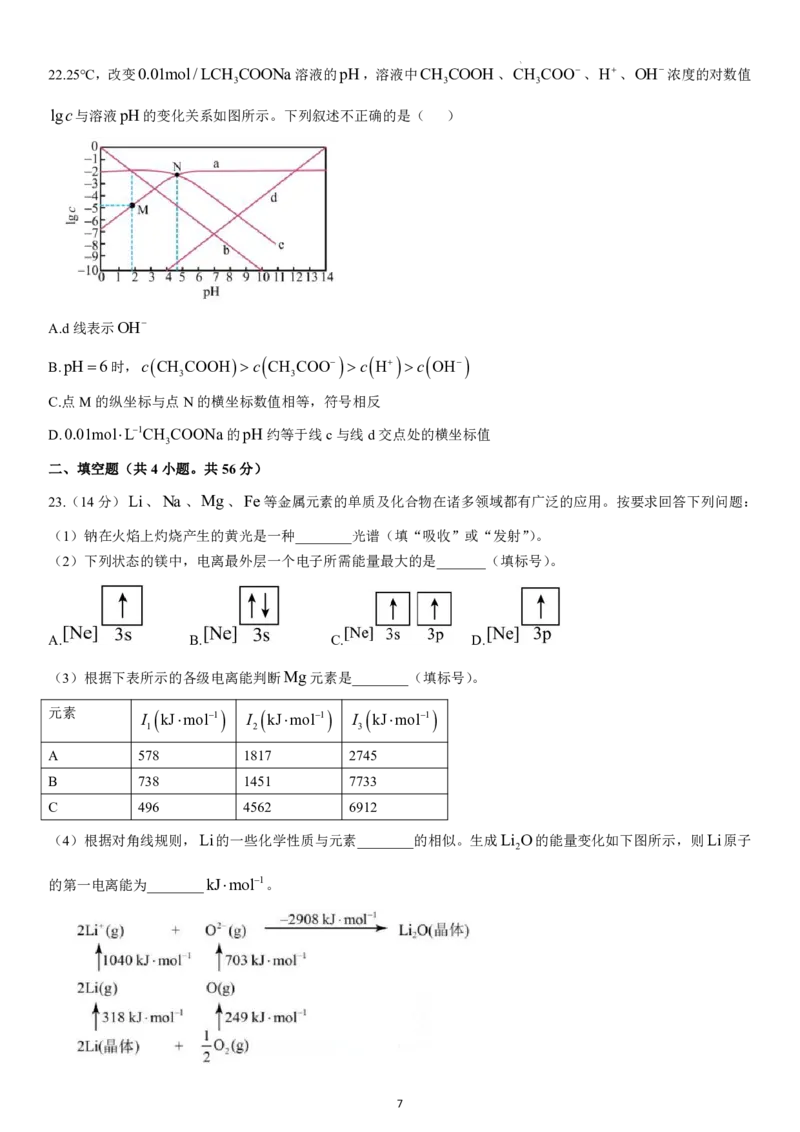
21.一定温度下,将过量MgCO 固体溶于100mL水中,充分搅拌后慢慢加入NaOH固体,随着c
OH
增大,溶
3
液中c
Mg2
的变化曲线如图所示(未按比例画出),P为Y~ Z曲线上的任意一点。下列说法错误的是( )
A.该温度下,K MgCO 4106
sp 3
B.K MgCO K
Mg OH
sp 3 sp 2
C.P点溶液中,一定存在c
CO2
c
Na
c
OH
3
D.Z点溶液中,c
CO2
106c2
OH
3
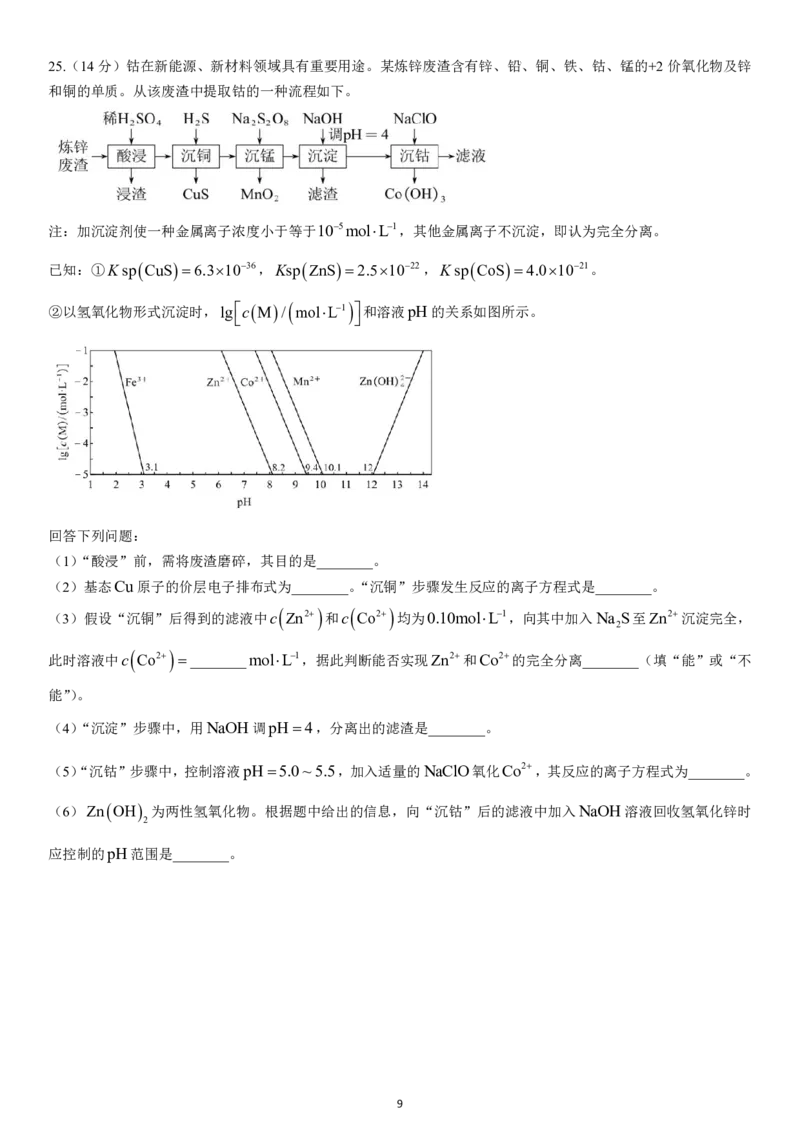
学科网(北京)股份有限公司 622.25℃,改变0.01mol/LCH COONa溶液的pH,溶液中CH COOH、CH COO、H、OH浓度的对数值
3 3 3
lgc与溶液pH的变化关系如图所示。下列叙述不正确的是( )
A.d线表示OH
B.pH6时,c CH COOH c CH COO c H c OH
3 3
C.点M的纵坐标与点N的横坐标数值相等,符号相反
D.0.01molL1CH COONa的pH约等于线c与线d交点处的横坐标值
3
二、填空题(共4小题。共56分)
23.(14分)Li、Na、Mg、Fe等金属元素的单质及化合物在诸多领域都有广泛的应用。按要求回答下列问题:
(1)钠在火焰上灼烧产生的黄光是一种________光谱(填“吸收”或“发射”)。
(2)下列状态的镁中,电离最外层一个电子所需能量最大的是_______(填标号)。
A. B. C. D.
(3)根据下表所示的各级电离能判断Mg元素是________(填标号)。
元素 I kJmol1 I kJmol1 I kJmol1
1 2 3
A 578 1817 2745
B 738 1451 7733
C 496 4562 6912
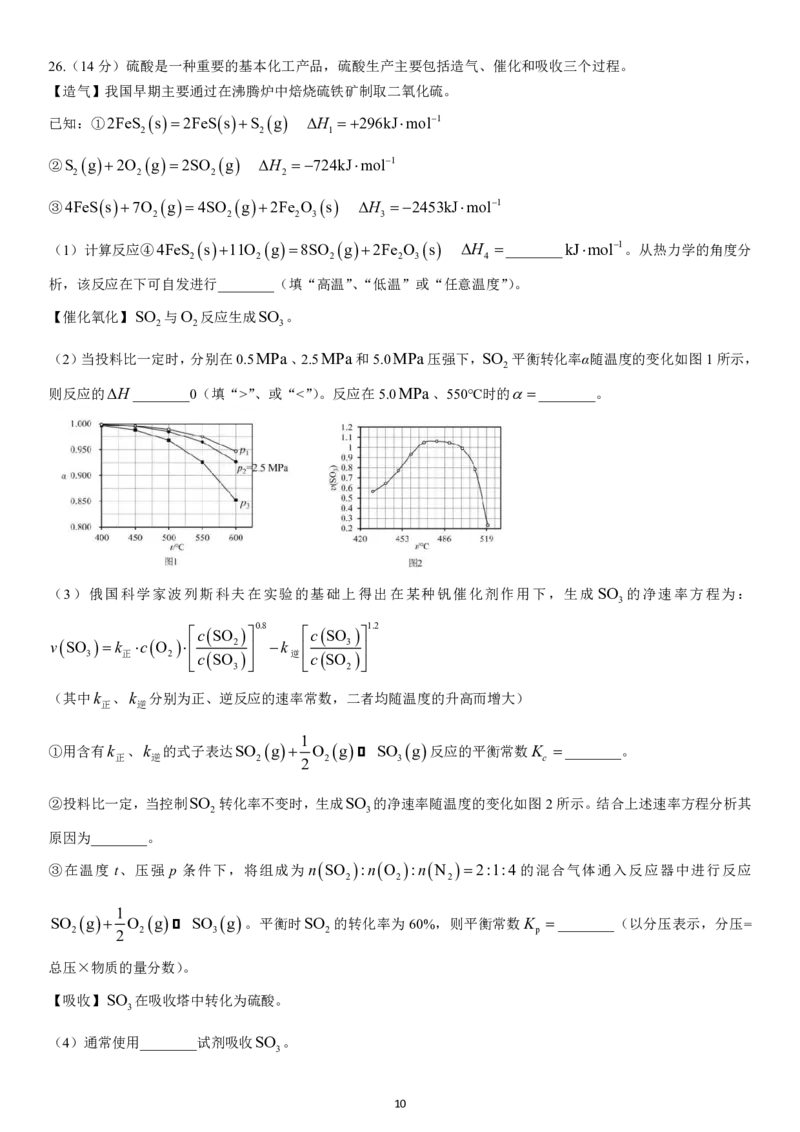
(4)根据对角线规则,Li的一些化学性质与元素________的相似。生成Li O的能量变化如下图所示,则Li原子
2
的第一电离能为________kJmol1。
学科网(北京)股份有限公司 7(5)富马酸亚铁(FeC H O )是一种补铁剂。
4 2 4
①富马酸亚铁中各元素的电负性由大到小的顺序为________。基态O原子的价电子中,两种自旋状态的电子数之比
为________。
②基态Fe原子中,电子占据的最高能层的符号为________,该能层具有的原子轨道数为________。
③建议补铁剂与维生素C同时服用以促进“亚铁”的吸收,避免生成Fe3。从结构角度看,Fe2易被氧化成Fe3
的原因是________。
24.(14分)氯化铁是一种重要的铁盐,广泛应用于金属刻蚀、污水处理等领域。现测定某FeCl 6H O样品的纯
3 2
度,回答下列问题:
Ⅰ.采用氧化还原滴定法定量。
主要实验原理:利用SnCl 溶液还原Fe3生成Fe2,再用K Cr O 标准溶液继续滴定Fe2至终点(滴定过程中
2 2 2 7
Cr O2转化为Cr3,Cl不反应)。
2 7
(1)应将K Cr O 溶液加入________(填“酸式”或“碱式”)滴定管中。
2 2 7
(2)写出酸性条件下K Cr O 溶液滴定Fe2的离子方程式________。
2 2 7
(3)若其他操作均正确,滴定过程中起始时仰视读数,终点时俯视读数,则测得结果________(填“偏高”、“偏
低”或“无影响”)。
(4)由FeCl 溶液结晶获得FeCl 6H O晶体的操作为________、________、过滤。
3 3 2
Ⅱ.采用络合滴定法定量。
文献资料:溶液中Fe3与EDTA以物质的量之比1:1形成稳定的络合物,其溶液颜色为亮黄色。磺基水杨酸溶于
水得到无色溶液,在pH1.5~2.5时与Fe3 形成红色络合物,可用作滴定Fe3 的指示剂。实验操作:称取
2.50gFeCl 样品溶于盐酸中,稀释成250mL溶液。取25.00mL于锥形瓶中,滴几滴磺基水杨酸溶液,滴加稀硫酸
3
至pH2左右,用0.0500molL1EDTA溶液滴定至终点,平均消耗EDTA溶液26.50mL(杂质不参与反应)。
(5)配制FeCl 溶液时,先取一定量FeCl 6H O溶于浓盐酸中,再加水稀释。盐酸的作用是________。
3 3 2
(6)部分滴定有关操作如下,正确的先后排序为________(填字母)。
A.润洗滴定管 B.检查滴定管是否漏水
C.装液、调零并排气泡D.记录标准液用量
(7)达到滴定终点的现象是________。
(8)该样品含FeCl 的质量分数为________%(保留2位小数)。
3
学科网(北京)股份有限公司 825.(14分)钴在新能源、新材料领域具有重要用途。某炼锌废渣含有锌、铅、铜、铁、钴、锰的+2价氧化物及锌
和铜的单质。从该废渣中提取钴的一种流程如下。
注:加沉淀剂使一种金属离子浓度小于等于105molL1,其他金属离子不沉淀,即认为完全分离。
已知:①Ksp CuS 6.31036,Ksp ZnS 2.51022,Ksp CoS 4.01021。
②以氢氧化物形式沉淀时,lgc M / molL1 和溶液pH的关系如图所示。
回答下列问题:
(1)“酸浸”前,需将废渣磨碎,其目的是________。
(2)基态Cu原子的价层电子排布式为________。“沉铜”步骤发生反应的离子方程式是________。
(3)假设“沉铜”后得到的滤液中c Zn2 和c Co2 均为0.10molL1,向其中加入Na S至Zn2沉淀完全,
2
此时溶液中c Co2 ________molL1,据此判断能否实现Zn2和Co2的完全分离________(填“能”或“不
能”)。
(4)“沉淀”步骤中,用NaOH调pH4,分离出的滤渣是________。
(5)“沉钴”步骤中,控制溶液pH5.0~5.5,加入适量的NaClO氧化Co2,其反应的离子方程式为________。
(6)Zn OH 为两性氢氧化物。根据题中给出的信息,向“沉钴”后的滤液中加入NaOH溶液回收氢氧化锌时
2
应控制的pH范围是________。
学科网(北京)股份有限公司 926.(14分)硫酸是一种重要的基本化工产品,硫酸生产主要包括造气、催化和吸收三个过程。
【造气】我国早期主要通过在沸腾炉中焙烧硫铁矿制取二氧化硫。
已知:①2FeS s 2FeS s S g H 296kJmol1
2 2 1
②S g 2O g 2SO g H 724kJmol1
2 2 2 2
③4FeS s 7O g 4SO g 2Fe O s H 2453kJmol1
2 2 2 3 3
(1)计算反应④4FeS s 11O g 8SO g 2Fe O s H ________kJmol1。从热力学的角度分
2 2 2 2 3 4
析,该反应在下可自发进行________(填“高温”、“低温”或“任意温度”)。
【催化氧化】SO 与O 反应生成SO 。
2 2 3
(2)当投料比一定时,分别在0.5MPa、2.5MPa和5.0MPa压强下,SO 平衡转化率α随温度的变化如图1所示,
2
则反应的H ________0(填“>”、或“<”)。反应在5.0MPa、550℃时的________。
(3)俄国科学家波列斯科夫在实验的基础上得出在某种钒催化剂作用下,生成SO 的净速率方程为:
3
c SO 0.8 c SO 1.2
v SO k c O 2 k 3
3 正 2 c SO 逆 c SO
3 2
(其中k 、k 分别为正、逆反应的速率常数,二者均随温度的升高而增大)
正 逆
1
①用含有k 、k 的式子表达SO g O g SO g 反应的平衡常数K ________。
正 逆 2 2 2 3 c
②投料比一定,当控制SO 转化率不变时,生成SO 的净速率随温度的变化如图2所示。结合上述速率方程分析其
2 3
原因为________。
③在温度 t、压强 p 条件下,将组成为 n SO :n O :n N 2:1:4的混合气体通入反应器中进行反应
2 2 2
1
SO g O g SO g 。平衡时SO 的转化率为60%,则平衡常数K ________(以分压表示,分压=
2 2 2 3 2 p
总压×物质的量分数)。
【吸收】SO 在吸收塔中转化为硫酸。
3
(4)通常使用________试剂吸收SO 。
3
学科网(北京)股份有限公司 10哈师大附中 2023 级高二上期中考试化学答案
1 2 3 4 5 6 7 8 9 10 11
D A B C A C B C D D A
12 13 14 15 16 17 18 19 20 21 22
D C D C D D B B D C B
23.除标记外,每空1分
(1)发射 (2)A(2分) (3)B (4)Mg 520(2分)
(5)①OCHFe(2分) 1:2(或2:1) ②N 16
③Fe2价层电子排布式为3d6,Fe3价层电子排布式为3d5,为半充满状态,更稳定(2分)
24.除标记外,每空2分
(1)酸式(1分)
(2)Cr O2 6Fe2 14H 2Cr3 6Fe3 7H O
2 7 2
(3)偏低(1分)
(4)蒸发浓缩(1分) 冷却结晶(1分)
(5)抑制Fe3水解
(6)BACD
(7)因最后半滴标准液的滴入,溶液恰好由红色变为亮黄色,且半分钟内不复原
(8)86.13
25除标记外,每空2分
(1)增大固体与酸的接触面积,加快反应速率,提高浸出率
(2)3d104s1(1分) Cu2 H SCuS2H ;
2
(3)1.6104 不能(1分)
(4)Fe OH
3
(5)2Co2 ClO 5H O2Co OH Cl 4H
2 3
(6)8.2~12
学科网(北京)股份有限公司 1126除标记外,每空2分
k
(1)-3309低温(1分) (2)<0.975 (3)① 正
k
逆
②(温度升高,k 、k 均增大,)其它条件相同时,较低温范围内v SO 的大小由k 决定,较高温范围内v SO
正 逆 3 正 3
的大小由k 决定(或其它合理答案)
逆
6
③ (4)98.3%的浓硫酸(1分)
p
学科网(北京)股份有限公司 12