文档内容
配套《高中必刷题 化学 必修第一册 LK》使用
第3章 物质的性质与转化
第3节 氮的循环
课时2氨的转化与生成
一、氨的转化
1.氨气的物理性质
颜色状态 气味 密度 溶解性
极易溶于水,常温、常压下 1
无色气体 刺激性气味 小于空气
体积水能溶解约700 体积氨气
2.氨气的化学性质
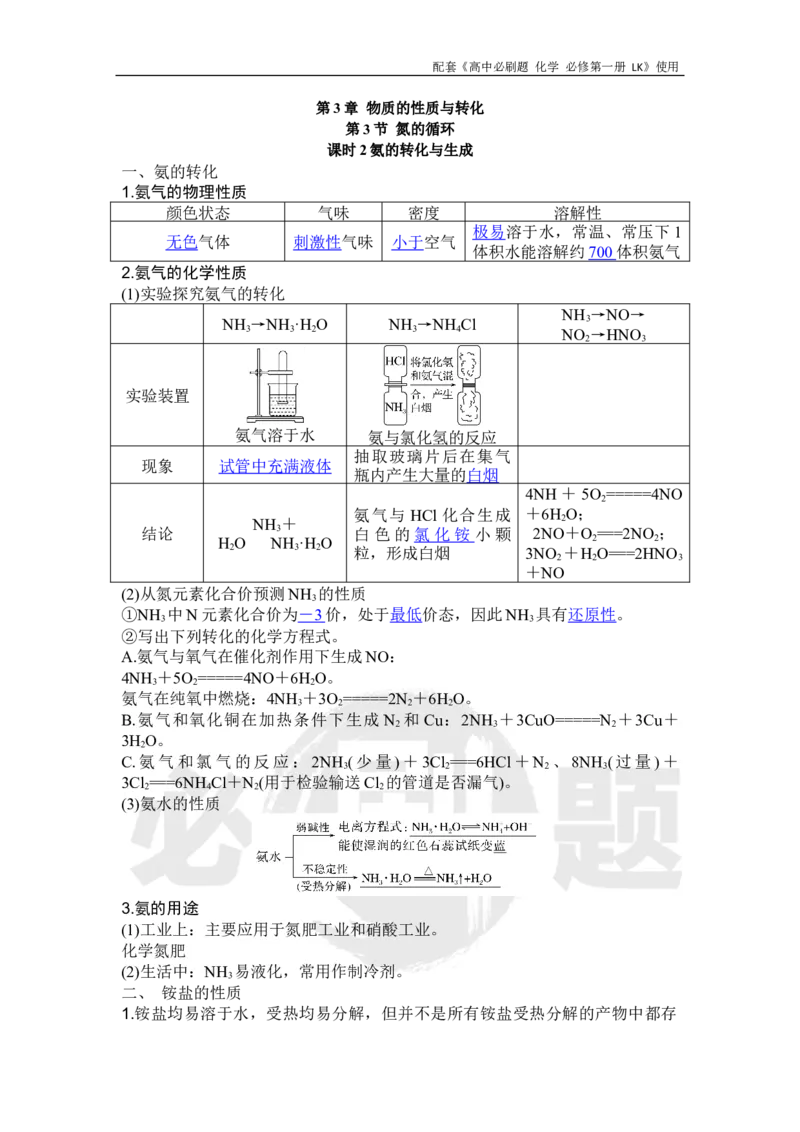
(1)实验探究氨气的转化
NH →NO→
NH →NH ·H O NH →NH Cl 3
3 3 2 3 4 NO →HNO
2 3
实验装置
氨气溶于水 氨与氯化氢的反应
抽取玻璃片后在集气
现象 试管中充满液体
瓶内产生大量的白烟
4NH + 5O =====4NO
2
氨气与 HCl 化合生成 +6H O;
NH + 2
结论 3 白色的 氯化铵 小颗 2NO+O ===2NO ;
H ONH ·H O 2 2
2 3 2 粒,形成白烟 3NO +H O===2HNO
2 2 3
+NO
(2)从氮元素化合价预测NH 的性质
3
①NH 中N元素化合价为 - 3 价,处于最低价态,因此NH 具有还原性。
3 3
②写出下列转化的化学方程式。
A.氨气与氧气在催化剂作用下生成NO:
4NH +5O =====4NO+6H O。
3 2 2
氨气在纯氧中燃烧:4NH +3O =====2N +6H O。
3 2 2 2
B.氨气和氧化铜在加热条件下生成 N 和 Cu:2NH +3CuO=====N +3Cu+
2 3 2
3H O。
2
C.氨气和氯气的反应:2NH (少量)+3Cl ===6HCl+N 、8NH (过量)+
3 2 2 3
3Cl ===6NH Cl+N (用于检验输送Cl 的管道是否漏气)。
2 4 2 2
(3)氨水的性质
3.氨的用途
(1)工业上:主要应用于氮肥工业和硝酸工业。
化学氮肥
(2)生活中:NH 易液化,常用作制冷剂。
3
二、 铵盐的性质
1.铵盐均易溶于水,受热均易分解,但并不是所有铵盐受热分解的产物中都存配套《高中必刷题 化学 必修第一册 LK》使用
在NH 。如NH NO 在不同温度分解时的产物不同,在某温度时其分解的方程
3 4 3
式为5NH NO =====4N ↑+2HNO +9H O。
4 3 2 3 2
2.与碱反应规律
氯化铵固体与 NaOH 固体反应的化学方程式:NaOH+NH Cl=====NaCl+
4
NH ↑+H O。
3 2
氯化铵固体与NaOH溶液反应的离子方程式:
加热: NH + OH - ===== NH ↑ + H O;
3 2
不加热: NH + OH - == =NH ·H O。
3 2
3.NH的检验
(1)实验操作步骤:取样品少许→溶解或加入试剂→必要的操作→描述现象→得
出结论。
(2)检验方法