文档内容
2008年天津市高考化学试卷
一、选择题(共7小题,每小题6分,满分42分)
1.(6分)二十世纪化学合成技术的发展对人类健康水平和生活质量的提高做出了巨大贡
献.下列各组物质全部由化学合成得到的是( )
A.玻璃 纤维素 青霉素
B.尿素 食盐 聚乙烯
C.涤纶 洗衣粉 阿司匹林
D.石英 橡胶 磷化铟
2.(6分)对平衡体系CO (g) CO (aq)△H=﹣19.75kJ•mol﹣1,为了减小温室效应
2 2
的产生,增大二氧化碳气体在水⇌中的溶解度,应采取的方法是( )
A.升温增压 B.降温减压 C.升温减压 D.降温增压
3.(6分)醋酸溶液中存在电离平衡:CH COOH→H++CH COO﹣,下列叙述不正确的
3 3
是( )
A.CH COOH 溶液中离子浓度的关系满足:c(H+)═c(OH﹣)+c(CH COO﹣)
3 3
B.0.1 mol•L﹣1的CH COOH 溶液加水稀释,溶液中c(OH﹣)减小
3
C.CH COOH 溶液中加入少量CH COONa固体,平衡逆向移动
3 3
D.常温下,pH=2的CH COOH 溶液与pH=12的NaOH 溶液等体积混合后,溶液的
3
pH<7
4.(6分)下列叙述正确的是( )
A.1个甘氨酸分子中存在9对共用电子对(甘氨酸的结构简式为NH ﹣CH ﹣COOH)
2 2
B.PCl 和BCl 分子中所有原子的最外层都达到8电子稳定结构
3 3
C.H S和CS 分子都是含极性键的极性分子
2 2
D.熔点由高到低的顺序是:金刚石>碳化硅>晶体硅
5.(6分)下列离子方程式书写正确的是( )
A.石灰乳与Na CO 溶液混合:Ca2++CO 2﹣=CaCO
2 3 3 3
B.NH HSO 溶液与足量的NaOH溶液混合加热:NH ++HSO ﹣+2OH﹣ NH ↑+SO 2
4 3 4 3 3 3
﹣+2H O
2C.酸性条件下KIO 溶液与KI溶液发生反应生成I :IO ﹣+5I﹣+3H O=3I +6OH﹣
3 2 3 2 2
D.AgNO 溶液中加入过量的氨水:Ag++NH •H O=AgOH+NH +
3 3 2 4
6.(6分)下列叙述正确的是( )
A.在原电池的负极和电解池的阴极上都是发生失电子的氧化反应
B.用惰性电极电解Na SO 溶液,阴阳两极产物的物质的量之比为1:2
2 4
C.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1mol NaOH
D.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀
7.(6分)下列实验方法合理的是( )
A.可用水鉴别己烷、四氯化碳、乙醇三种无色液体
B.油脂皂化后可用渗析的方法使高级脂肪酸钠和甘油充分分离
C.可用澄清石灰水鉴别Na CO 溶液和NaHCO 溶液
2 3 3
D.为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量应相等
二、解答题(共4小题,满分66分)
8.(14分)(2008•天津理综,26)W、X、Y、Z是原子序数依次增大的同一短周期元素,
W、X是金属元素,Y、Z是非金属元素.
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方
程式为 .
(2)W与Y可形成化合物W Y,该化合物的电子式为 .
2
(3)X的硝酸盐水溶液显 性,用离子方程式解释原因: .
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为 .
(5)比较Y、Z气态氢化物的稳定性: > (用分子式表示).
(6)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是 >
> > .
(7)Z的最高价氧化物为无色液体,0.25mol该物质与一定量水混合得到一种稀溶液,
并放出Q kJ的热量.写出该反应的热化学方程式: .
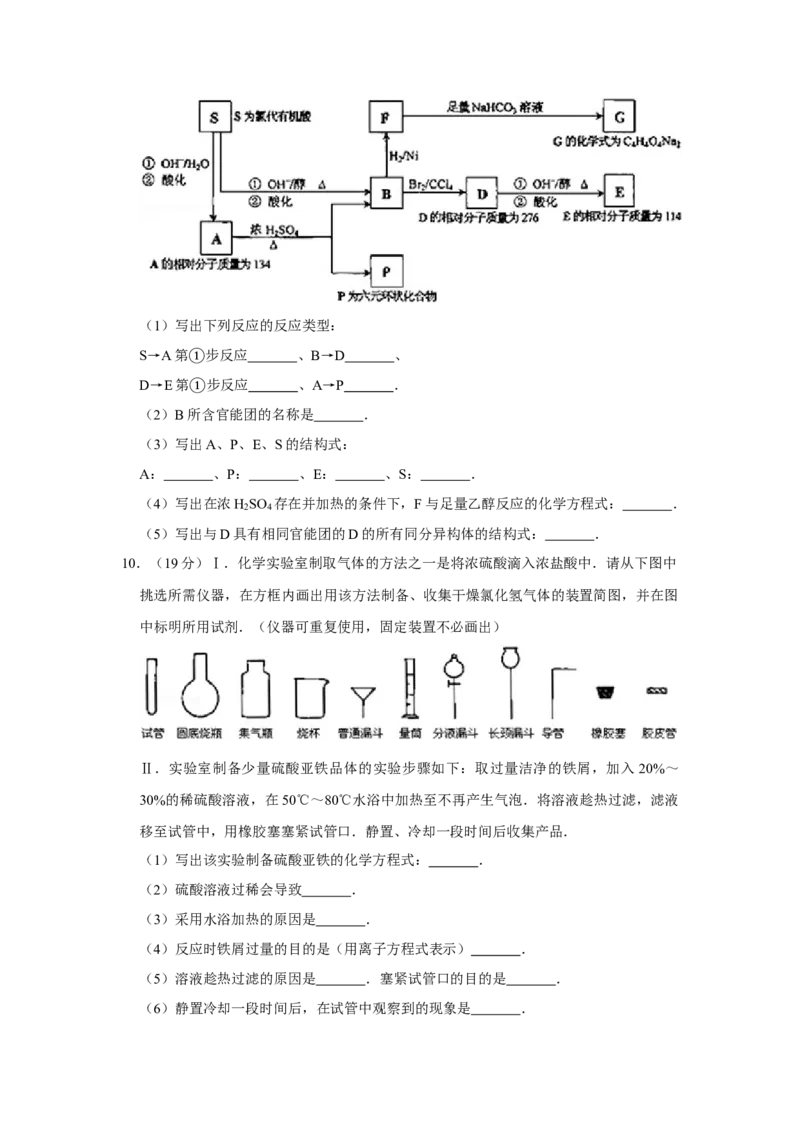
9.(19分)某天然有机化合物A仅含C、H、O元素,与A相关的反应框图如下:(1)写出下列反应的反应类型:
S→A第 步反应 、B→D 、
D→E第①步反应 、A→P .
(2)B所①含官能团的名称是 .
(3)写出A、P、E、S的结构式:
A: 、P: 、E: 、S: .
(4)写出在浓H SO 存在并加热的条件下,F与足量乙醇反应的化学方程式: .
2 4
(5)写出与D具有相同官能团的D的所有同分异构体的结构式: .
10.(19分)Ⅰ.化学实验室制取气体的方法之一是将浓硫酸滴入浓盐酸中.请从下图中
挑选所需仪器,在方框内画出用该方法制备、收集干燥氯化氢气体的装置简图,并在图
中标明所用试剂.(仪器可重复使用,固定装置不必画出)
Ⅱ.实验室制备少量硫酸亚铁品体的实验步骤如下:取过量洁净的铁屑,加入 20%~
30%的稀硫酸溶液,在50℃~80℃水浴中加热至不再产生气泡.将溶液趁热过滤,滤液
移至试管中,用橡胶塞塞紧试管口.静置、冷却一段时间后收集产品.
(1)写出该实验制备硫酸亚铁的化学方程式: .
(2)硫酸溶液过稀会导致 .
(3)采用水浴加热的原因是 .
(4)反应时铁屑过量的目的是(用离子方程式表示) .
(5)溶液趁热过滤的原因是 .塞紧试管口的目的是 .
(6)静置冷却一段时间后,在试管中观察到的现象是 .11.(14分)(1)配平氧化还原反应方程式:
C O 2﹣+ MnO ﹣+ H+═ CO ↑+ Mn2++ H O
2 4 4 2 2
(2)称取6.0g含H C O •2H O、KHC O 和K SO 的试样,加水溶解,配成250mL 溶
2 2 4 2 2 4 2 4
液.量取两份此溶液各25mL,分别置于两个锥形瓶中.
第一份溶液中加入2滴酚酞试液,滴加0.25mol/L NaOH 溶液至20mL时,溶液由无
①色变为浅红色.该溶液被中和的H+的物质的量为 mol.
第二份溶液滴加0.10mol/L 酸性KMnO 溶液至16mL时反应完全,此时溶液颜色,
4
②由 变为 .该溶液中还原剂的物质的量 mol.
原试样中H C O •2H O的质量分数为 ,KHC O 的质量分数为 .
2 2 4 2 2 4
③