文档内容
B.电池工作一段时间后,甲池的c(SO 2﹣)减小
2015年天津市高考化学试卷 4
C.电池工作一段时间后,乙池溶液的总质量增加
一、选择题:
D.阴阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
1.(6分)下列有关“化学与生活”的叙述不正确的是( )
5.(6分)室温下,将0.20mol Na CO 固体溶于水配成100mL溶液,向溶液中加入下列物质,有关结论正确
2 3
A.点燃爆竹后,硫燃烧生成SO
3 的是( )
B.中国古代利用明矾溶液的酸性清除铜镜表面的铜锈
加入的物质 结论
C.服用阿司匹林出现水杨酸反应时,用NaHCO 溶液解毒
3 A 100mL 2mol•L﹣1H SO 反应结束后,c(Na+)=c
2 4
D.使用含钙离子浓度较大的地下水洗衣服,肥皂去污能力减弱 (SO
4
2﹣)
2.(6分)下列关于物质或离子检验的叙述正确的是( ) B 0.20molCaO
溶液中 增大
A.在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+
B.气体通过无水CuSO 4 ,粉末变蓝,证明原气体中含有水蒸气 C 200mL H 2 O 由水电离出的c(H+)•c(OH
﹣)不变
C.灼烧白色粉末,火焰呈黄色,证明原粉末中有Na+,无K+
D 0.4molNaHSO 固体 反应完全后,溶液pH减小,c
4
D.将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO
2
(Na+)不变
3.(6分)下列说法不正确的是( ) A.A B.B C.C D.D
A.Na与H 2 O的反应是熵增的放热反应,该反应能自发进行 6.(6分)某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+mY(g) 3Z
B.饱和Na 2 SO 4 溶液或浓硝酸均可使蛋白质溶液产生沉淀,但原理不同 (g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%,在此平衡体系中加入1molZ(g),再将⇌达
C.FeCl 和MnO 均可加快H O 分解,同等条件下二者对H O 分解速率的改变相同
3 2 2 2 2 2 到平衡后,X、Y、Z的体积分数不变.下列叙述不正确的是( )
D.Mg(OH) 2 固体在溶液存在平衡:Mg(OH) 2 (s) Mg2+(aq)+2OH﹣(aq),该固体可溶于NH 4 Cl A.m=2
溶液 ⇌ B.两次平衡的平衡常数相同
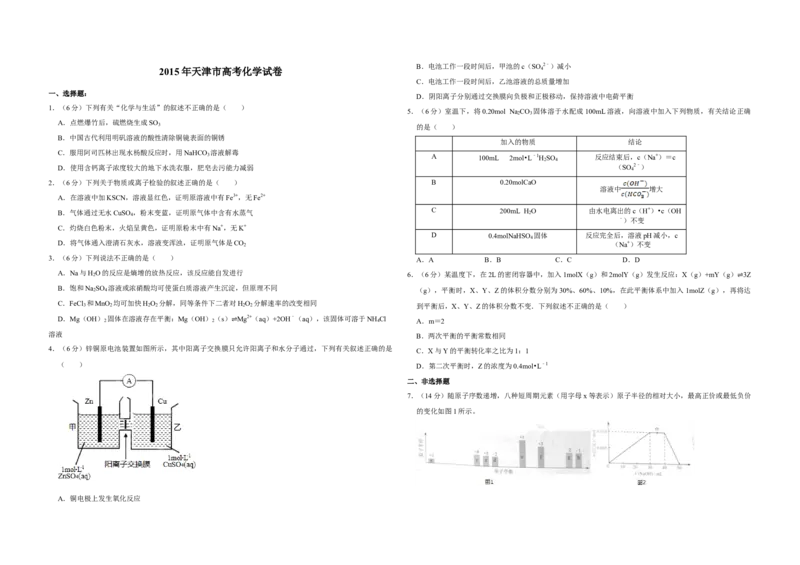
4.(6分)锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是
C.X与Y的平衡转化率之比为1:1
( ) D.第二次平衡时,Z的浓度为0.4mol•L﹣1
二、非选择题
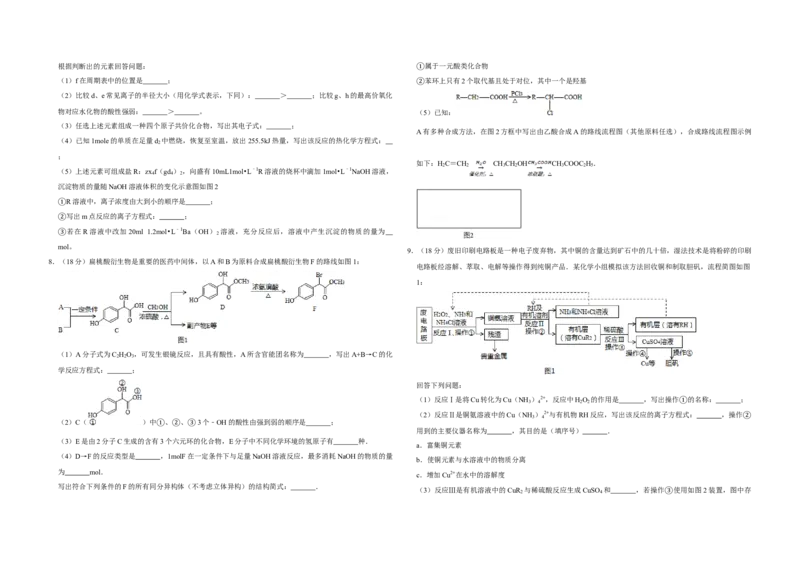
7.(14分)随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小,最高正价或最低负价
的变化如图1所示。
A.铜电极上发生氧化反应根据判断出的元素回答问题: 属于一元酸类化合物
(1)f在周期表中的位置是 ; ①苯环上只有2个取代基且处于对位,其中一个是羟基
(2)比较d、e常见离子的半径大小(用化学式表示,下同): > ;比较g、h的最高价氧化 ②
物对应水化物的酸性强弱: > 。 (5)已知:
(3)任选上述元素组成一种四个原子共价化合物,写出其电子式: ;
A有多种合成方法,在图2方框中写出由乙酸合成A的路线流程图(其他原料任选),合成路线流程图示例
(4)已知1mole的单质在足量d 中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式:
2
;
如下:H C=CH CH CH OH CH COOC H .
2 2 3 2 3 2 5
(5)上述元素可组成盐R:zx f(gd ) ,向盛有10mL1mol•L﹣1R溶液的烧杯中滴加1mol•L﹣1NaOH溶液,
4 4 2
沉淀物质的量随NaOH溶液体积的变化示意图如图2
R溶液中,离子浓度由大到小的顺序是 ;
①写出m点反应的离子方程式: ;
②若在R溶液中改加20ml 1.2mol•L﹣1Ba(OH)
2
溶液,充分反应后,溶液中产生沉淀的物质的量为
③mol。
9.(18分)废旧印刷电路板是一种电子废弃物,其中铜的含量达到矿石中的几十倍,湿法技术是将粉碎的印刷
8.(18分)扁桃酸衍生物是重要的医药中间体,以A和B为原料合成扁桃酸衍生物F的路线如图1:
电路板经溶解、萃取、电解等操作得到纯铜产品.某化学小组模拟该方法回收铜和制取胆矾,流程简图如图
1:
(1)A分子式为C H O ,可发生银镜反应,且具有酸性,A所含官能团名称为 ,写出A+B→C的化
2 2 3
学反应方程式: ;
回答下列问题:
(1)反应Ⅰ是将Cu转化为Cu(NH ) 2+,反应中H O 的作用是 ,写出操作 的名称: ;
3 4 2 2
(2)反应Ⅱ是铜氨溶液中的Cu(NH
3
)
4
2+与有机物RH反应,写出该反应的离子方程①式: ,操作
(2)C( )中 、 、 3个﹣OH的酸性由强到弱的顺序是 ;
用到的主要仪器名称为 ,其目的是(填序号) . ②
① ② ③
(3)E是由2分子C生成的含有3个六元环的化合物,E分子中不同化学环境的氢原子有 种.
a.富集铜元素
(4)D→F的反应类型是 ,1molF在一定条件下与足量NaOH溶液反应,最多消耗NaOH的物质的量
b.使铜元素与水溶液中的物质分离
为 mol.
c.增加Cu2+在水中的溶解度
写出符合下列条件的F的所有同分异构体(不考虑立体异构)的结构简式: .
(3)反应Ⅲ是有机溶液中的CuR 与稀硫酸反应生成CuSO 和 ,若操作 使用如图2装置,图中存
2 4
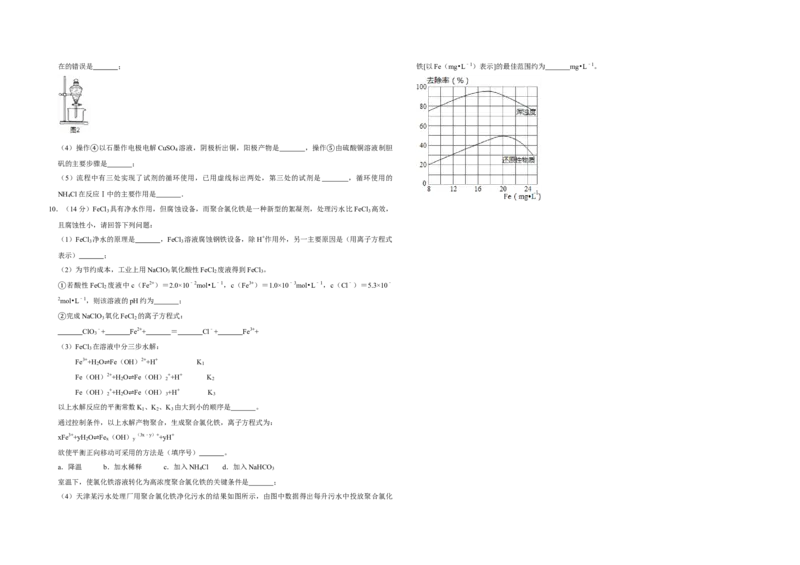
③在的错误是 ; 铁[以Fe(mg•L﹣1)表示]的最佳范围约为 mg•L﹣1。
(4)操作 以石墨作电极电解CuSO 溶液,阴极析出铜,阳极产物是 ,操作 由硫酸铜溶液制胆
4
矾的主要步④骤是 ; ⑤
(5)流程中有三处实现了试剂的循环使用,已用虚线标出两处,第三处的试剂是 ,循环使用的
NH Cl在反应Ⅰ中的主要作用是 .
4
10.(14分)FeCl 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl 高效,
3 3
且腐蚀性小,请回答下列问题:
(1)FeCl 净水的原理是 ,FeCl 溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式
3 3
表示) ;
(2)为节约成本,工业上用NaClO 氧化酸性FeCl 废液得到FeCl 。
3 2 3
若酸性FeCl 废液中c(Fe2+)=2.0×10﹣2mol•L﹣1,c(Fe3+)=1.0×10﹣3mol•L﹣1,c(Cl﹣)=5.3×10﹣
2
①2mol•L﹣1,则该溶液的pH约为 ;
完成NaClO 氧化FeCl 的离子方程式:
3 2
② ClO ﹣+ Fe2++ = Cl﹣+ Fe3++
3
(3)FeCl 在溶液中分三步水解:
3
Fe3++H O Fe(OH)2++H+ K
2 1
Fe(OH)⇌ 2++H
2
O Fe(OH)
2
++H+ K
2
Fe(OH)
2
++H
2
O⇌Fe(OH)
3
+H+ K
3
以上水解反应的平衡常⇌数K
1
、K
2
、K
3
由大到小的顺序是 。
通过控制条件,以上水解产物聚合,生成聚合氯化铁,离子方程式为:
xFe3++yH O Fe (OH) (3x﹣y)++yH+
2 x y
欲使平衡正向⇌移动可采用的方法是(填序号) 。
a.降温 b.加水稀释 c.加入NH Cl d.加入NaHCO
4 3
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是 ;
(4)天津某污水处理厂用聚合氯化铁净化污水的结果如图所示,由图中数据得出每升污水中投放聚合氯化