文档内容
2024-2025学年度第一学期12份月考考试
高三化学试题
分值:100分 考试时间:75分钟
可能用到的相对原子质量:
H-1,C-12,O-16,S-32,Na-23,Mg-24,Al-27,Cu-64,si-28,N-14,Cl-35.5
一、单选题(每小题3分,共60分)
1.下列关于氯及其化合物的叙述中错误的是
A.常温常压下, 是黄绿色气体 B.氯水和液氯的成分完全相同
C. 在光照条件下易发生分解 D.含氯漂白液的有效成分为
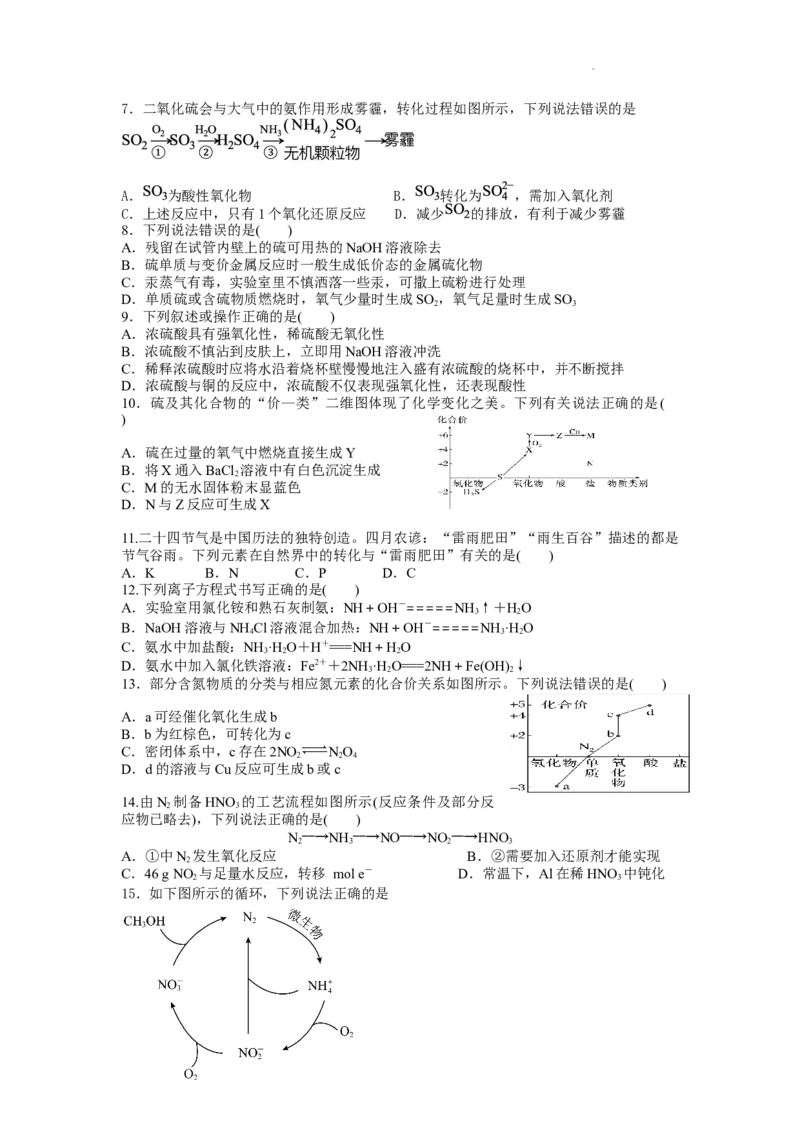
2.氯元素可形成多种物质,为了研究方便,绘制氯及其化合物的价类二维图如下图所示。
下列说法不正确的
A.a溶液与e溶液混合在一定条件下可发生氧化还原反应
B.可用pH试纸测定b的水溶液的pH值
C.c溶液中通入二氧化碳可增强其漂白、杀菌消毒的能力
D.d在化学反应中既能做氧化剂,也能做还原剂
3.下列说法正确的是
A.向久置的氯水中滴入紫色石蕊试液,溶液将先变红后褪色
B.新制氯水的颜色为浅黄绿色,光照新制氯水有气体逸出,该气体为HCl
C.漂白粉的有效成分是Ca(ClO),应密封保存
2
D.氯气有漂白性,所以氯气能使湿润的有色布条褪色
4.许多物质性质上都存在着递变规律,下列有关说法正确的是( )
A.卤化银的颜色按AgCl、AgBr、AgI的顺序依次变浅
B.卤化氢的键长按H—F、H—Cl、H—Br、H—I的顺序依次增大
C.卤化氢的沸点按HF、HCl、HBr、HI的顺序依次升高
D.卤素单质与氢气化合按F、Cl、Br 、I 的顺序由难变易
2 2 2 2
5.向下列溶液中通入氯气,现象和结论描述正确的是( )
A.品红溶液:红色褪去,加热该褪色溶液,溶液又恢复红色;次氯酸具有漂白性
B.紫色石蕊溶液:先变红,后褪色;氯气与水反应生成盐酸和次氯酸
C.含酚酞的氢氧化钠溶液:红色褪去;氯气只作氧化剂
D.硫化钠溶液:溶液变浑浊;氯气作还原剂
6.下列有关二氧化硫的说法中,错误的是
A.实验室可用氢氧化钠溶液吸收二氧化硫
B.二氧化硫水溶液能使紫色石蕊试液变红,说明二氧化硫与水发生了反应
C.二氧化硫能使酸性高锰酸钾溶液褪色,说明二氧化硫具有还原性
D.二氧化硫能使品红溶液褪色,说明它具有氧化性
学科网(北京)股份有限公司7.二氧化硫会与大气中的氨作用形成雾霾,转化过程如图所示,下列说法错误的是
A. 为酸性氧化物 B. 转化为 ,需加入氧化剂
C.上述反应中,只有1个氧化还原反应 D.减少 的排放,有利于减少雾霾
8.下列说法错误的是( )
A.残留在试管内壁上的硫可用热的NaOH溶液除去
B.硫单质与变价金属反应时一般生成低价态的金属硫化物
C.汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理
D.单质硫或含硫物质燃烧时,氧气少量时生成SO ,氧气足量时生成SO
2 3
9.下列叙述或操作正确的是( )
A.浓硫酸具有强氧化性,稀硫酸无氧化性
B.浓硫酸不慎沾到皮肤上,立即用NaOH溶液冲洗
C.稀释浓硫酸时应将水沿着烧杯壁慢慢地注入盛有浓硫酸的烧杯中,并不断搅拌
D.浓硫酸与铜的反应中,浓硫酸不仅表现强氧化性,还表现酸性
10.硫及其化合物的“价—类”二维图体现了化学变化之美。下列有关说法正确的是(
)
A.硫在过量的氧气中燃烧直接生成Y
B.将X通入BaCl 溶液中有白色沉淀生成
2
C.M的无水固体粉末显蓝色
D.N与Z反应可生成X
11.二十四节气是中国历法的独特创造。四月农谚:“雷雨肥田”“雨生百谷”描述的都是
节气谷雨。下列元素在自然界中的转化与“雷雨肥田”有关的是( )
A.K B.N C.P D.C
12.下列离子方程式书写正确的是( )
A.实验室用氯化铵和熟石灰制氨:NH+OH-=====NH ↑+HO
3 2
B.NaOH溶液与NH Cl溶液混合加热:NH+OH-=====NH ·H O
4 3 2
C.氨水中加盐酸:NH ·H O+H+===NH+HO
3 2 2
D.氨水中加入氯化铁溶液:Fe2++2NH ·H O===2NH+Fe(OH) ↓
3 2 2
13.部分含氮物质的分类与相应氮元素的化合价关系如图所示。下列说法错误的是( )
A.a可经催化氧化生成b
B.b为红棕色,可转化为c
C.密闭体系中,c存在2NO NO
2 2 4
D.d的溶液与Cu反应可生成b或c
14.由N 制备HNO 的工艺流程如图所示(反应条件及部分反
2 3
应物已略去),下列说法正确的是( )
N――→NH ――→NO――→NO ――→HNO
2 3 2 3
A.①中N 发生氧化反应 B.②需要加入还原剂才能实现
2
C.46 g NO 与足量水反应,转移 mol e- D.常温下,Al在稀HNO 中钝化
2 3
15.如下图所示的循环,下列说法正确的是
学科网(北京)股份有限公司A.该循环为碳循环 B.该循环为氮循环
C. 转化成 属于氮的固定 D.图中氮的化合价仅有0、+3、+5
16.中国力争在2030年前实现碳达峰、2060年前实现碳中和,关于碳及其化合物,下列
说法不正确的是( )
A.金刚石和石墨是碳元素的两种不同单质,二者互称为同素异形体
B.在100 kPa时,1 mol石墨转变为金刚石要吸收1.895 kJ的热量,故金刚石比石墨稳定
C.考古时常用于测定文物年代的是碳元素的一种核素C,该核素的中子数为8
D.引起温室效应的气体之一CO 中含极性共价键
2
17.下列关于二氧化硅的说法正确的是( )
A.二氧化硅是酸性氧化物,因此能与水反应生成硅酸
B.二氧化硅制成的光导纤维,由于导电能力强而被用于制造光缆
C.二氧化硅能与碳酸钠固体在高温时发生反应
D.用二氧化硅制取单质硅时,当生成2.24 L气体(标准状况)时,得到2.8 g硅
18.二氧化硅广泛存在于自然界中,在日常生活、生产、科研及新型材料等方面有着重要的
用途。a~e是对①~⑤反应中SiO 所表现的化学性质或作用进行的判断,其中正确的是
2
①SiO+2NaOH===NaSiO+HO ②SiO+2C=====Si+2CO↑
2 2 3 2 2
③SiO+4HF===SiF↑+2HO ④NaCO+SiO=====NaSiO+CO↑
2 4 2 2 3 2 2 3 2
⑤SiO+3C=====SiC+2CO↑
2
a.反应①中SiO 作为玻璃的成分被消耗,用于刻蚀玻璃
2
b.反应②中SiO 表现出氧化性
2
c.反应③中SiO 表现了酸性氧化物的通性
2
d.反应④符合用难挥发性的酸酐制取易挥发性的酸酐的原理
e.反应⑤中SiO 未参加氧化还原反应
2
A.ace B.bde C.cde D.ab
19.“九秋风露越窑开,夺得千峰翠色来”是赞誉越窑秘色青瓷的诗句,描绘了我国古代精
美的青瓷工艺品。玻璃、水泥和陶瓷均为硅酸盐制品,下列有关说法正确的是( )
A.玻璃是人类最早使用的硅酸盐制品 B.制水泥的原料为纯碱、石灰石和石英
C.硅酸盐制品的性质稳定、熔点较高 D.陶瓷的烧制过程为物理变化
20.物质的性质决定用途。下列说法正确的是
A. 具有漂白性,葡萄酒中添加 起到漂白作用
B. 溶液具有酸性,可用于腐蚀覆铜板制作印刷电路板
C. 具有强氧化性,可清洗附在试管内壁的银镜
D.维生素C具有氧化性,可用于水果罐头的抗还原剂
第II卷(非选择题)
二、填空题(共40分)
21.已知FeCl 呈棕红色、易潮解,100 ℃左右时升华。某化学实验小组利用氯气与金属铁
3
反应制备无水三氯化铁,并设计(Ⅰ)和(Ⅱ)两套不同的收集方案。
(1)B中反应的化学方程式为_____________________________________。
(2)D中反应的化学方程式为_____________________________________。
学科网(北京)股份有限公司(3)(Ⅰ)和(Ⅱ)中装置F的作用分别是_______________________________________________、
______________________________________________________________________________
。
(4)如果选用(Ⅱ)来完成实验,则必须采取的改进措施是_____________________________。
22.铜与浓硫酸在加热条件下可发生化学反应,为检验部分产物的性质,某研究小组设计了
如图所示的实验。请据此回答下列问题。
(1)铜与浓硫酸反应的化学方程式为___________。
(2)反应过程中观察到品红溶液___________,说明产物二氧化硫具有漂白性。
(3)浸A溶液的棉团的作用是吸收多余的尾气,防止污染空气,A是___________。
(4)工业生产中二氧化硫的大量排放使雨水的pH___________5.6(选填“>”或“<”),会
形成酸雨,使土壤、湖泊酸化,还能加速建筑物的腐蚀。
(5)实验室中 的检验方法:向溶液中加入稀盐酸,然后加入___________溶液,观察是
否有白色沉淀生成。
23.某小组同学欲探究NH 的催化氧化反应,按下图装置进行实验(夹持装置已略去)。
3
已知A、B装置可选药品:浓氨水、HO、蒸馏水、生石灰、MnO 。
2 2 2
(1)仪器a的名称为____________;仪器b的名称为_______________。
(2)装置A烧瓶中固体的作用为________(填字母,下同)。
A.催化剂 B.氧化剂 C.还原剂 D.反应物
学科网(北京)股份有限公司(3)仪器b中盛放的试剂是__________。
A.浓硫酸 B.碱石灰 C.五氧化二磷 D.硫酸铜
(4) 装 置 E 中 发 生 反 应 的 化 学 方 程 式 为
_______________________________________________。
24.硅的提纯是电子工业一项十分重要的工作,可用粗硅与干燥的 HCl 气体反应制
SiHCl (其中含有BCl 、SiCl ),SiHCl 与过量H 在1 000~1 100 ℃反应制得纯硅。有关物
3 3 4 3 2
质的物理性质见下表:
物质 SiCl BCl SiHCl
4 3 3
沸点/℃ 57.6 12.5 33.0
熔点/℃ -70.0 -107 -127
室可以采用如图装置(夹持、尾气处理装置及部分加热装置均略去)用SiHCl 与过量干燥H
3 2
反应制取纯硅。
(1)基态Si原子的价层电子排布式________;
(2)装置B中的试剂为________。
(3) 将 装 置 C 水 浴 加 热 , 该 加 热 方 式 的 优 点 是
_________________________________________。
(4)为保证实验安全,加热装置 D 前必须完成的操作是:ⅰ.检验装置的气密性;ⅱ.
_____________________________________________________________________,
(5)该装置中发生反应的化学方程式为_____________________________________________。
学科网(北京)股份有限公司