文档内容
化学参考答案
1.A
解析 酸是电离时生成的阳离子全部是H+的化合物,CO 为酸性氧化物,NaCl属于盐,NaOH
2
属于碱。
2.B
解析 A为烧杯,C为容量瓶,D为烧瓶。
3.C
解析 酒精、蔗糖属于非电解质,铜丝属于单质,既不是电解质,也不是非电解质。
4.A
解析 B项,H 还原CuO,H 作还原剂,H O是氧化产物;C项,Cl 和H O反应,Cl 既
2 2 2 2 2 2
是氧化剂又是还原剂;D项,SO 和H O反应不是氧化还原反应。
3 2
5.B
解析 A项,NaOH水溶液显碱性是因为NaOH的电离;C项,Na 2 CO 3 的水溶液因为CO2 3 -
的水解呈碱性;D项,NaCl的水溶液呈中性。
6.C
解析 配制生理盐水用的是食盐;工业上利用SiO 、Na CO 、CaCO 在高温下制造普通玻
2 2 3 3
璃;MgO的熔点很高,所以可用作耐高温材料;在海水中钠元素是以Na+形式存在。
7.D
解析 A项,NaCl的电子式应为Na+[· ·Cl · ·]-;B项,二氧化碳的结构式应为OCO;C项,
S2-的结构示意图: 。
8.A
解析 SO 和品红发生化合反应而使品红溶液褪色,但褪色不稳定,加热会恢复红色。
2
9.A
解析 石油、煤、天然气属于传统能源,均不能再生。
10.A
解析 B项,烧瓶不能用酒精灯直接加热,应垫石棉网;C项,氯化氢在水中才能发生电离,
所以氯化氢气体不能使干燥的蓝色石蕊试纸变红;D项,由于玻璃中的SiO 能和NaOH反
2
应,所以盛放NaOH的试剂瓶不能用玻璃塞,应用橡胶塞。
11.B
解析 A项,146C中质子数为6,中子数为8;B项,CH OH是一元醇,而甘油是三元醇,
3
第1页 | 共8页所以它们不是同系物;C项,C H 的同分异构体有正戊烷、异戊烷和新戊烷,它们的沸点
5 12
各不相同;D项, ,其名称为2甲基戊烷。
12.C
解析 A项,由于该反应为可逆反应,且没给出反应物物质的量,所以反应放出热量不确定;
B项,达到平衡时,X、Y的物质的量之比不一定为1∶2,它和起始量、转化率均有关系;
D项,达到平衡时,X的正反应速率与Z的逆反应速率应符合其化学计量数之比。
13.B
解析 A项,不符合电子守恒,应为2Na+2H
2
O===2Na++2OH-+H
2
↑;C项,应为2NH+
4
+SO2 4 -+Ba2++2OH-===BaSO 4 ↓+2NH 3 ·H 2 O;D项,应为HCO- 3 +Ca2++OH-===CaCO 3 ↓
+H O。
2
14.D
解析 根据元素在周期表中的位置,可以推断,X为O,Y为S,Z为Cl,W为Si。A项,
同周期原子半径逐渐减小,同族元素从上到下,随电子层数增多,原子半径增大;B项,稳
定性HCl>H S;C项,由于C可形成C H ,Si和C是同主族元素,所以Si也可能形成
2 2 6
Si H ;D项,Cl +Na S===S↓+2NaCl,反过来不能进行。
2 6 2 2
15.C
解析 A项,由于甲烷是正四面体结构,所以它的二氯代物只有一种;B项,苯使溴水褪色
因为萃取,而乙烯使溴水褪色是因为发生加成反应;C项,由于乙炔和苯的最简式相同,所
以当质量相同时,其耗氧量也相同;D项,苯与氯气反应生成氯苯,发生取代反应。
16.B
解析 A项,油脂、糖类中的单糖、二糖均不是高分子化合物;C项,在加银氨溶液之前,
应加入NaOH溶液中和硫酸;D项,甲醛能使蛋白质变性。
17.D
解析 A项,在铁的吸氧腐蚀过程中,铁片发生氧化反应而被腐蚀;B项,铁片负极腐蚀最严
重,由于离子的移动,在正极区域生成铁锈最多;C项,铁片负极反应式应为Fe-2e-===Fe2
+。
18.D
解析 A项,若0.1 mol·L-1醋酸溶液的pH>1,则证明醋酸是弱电解质;B项,若0.1 mol·L
-1 CH COONa溶液呈碱性,则证明CH COO-发生水解,从而证明CH COOH是弱电解质;
3 3 3
C项,比较浓度均为0.1 mol·L-1的盐酸和醋酸溶液的导电能力,若前者强,则证明醋酸是
弱电解质;D项,当NaOH溶液和醋酸溶液的物质的量浓度相同时,恰好完全反应时,消
耗两溶液的体积也相同,无法证明醋酸是弱电解质。
19.D
第2页 | 共8页解析 根据图示,N (g)+3H (g) 2NH (g) ΔH=-2(b-a) kJ·mol-1,所以,A、B两
2 2 3
项错误,根据图示:2NH (l)===N (g)+3H (g) ΔH=2(b+c-a) kJ·mol-1,所以C项错误,
3 2 2
D项正确。
20.A
解析 A项,对于组成结构相似的物质,相对分子质量越大,分子间作用力越大,错误;B
项,由于石英(SiO )是原子晶体,所以加热熔化时需破坏共价键;C项,NaOH加热熔化时,
2
电离成自由移动的OH-和Na+,所以具有导电性,正确;D项,水分解破坏氢氧键,生成
H 和O ,形成共价键,正确。
2 2
21.D
1.4-0.8mol·L-1
解析 A项,v(R)= =0.030 mol·L-1·min-1,正确;B项,在50 min时,
20 min
两个温度下R全部分解,分解率均为100%,正确;C项,在50 min时,30 ℃时,R分解
了1.6 mol·L-1,而在25 ℃时,R分解了1.3 mol·L-1,所以在0~50 min内,R的平均分解
速率随温度升高而增大,正确;D项,对比30 ℃和10 ℃的曲线,不能在同一时刻,应指明
在同一段时间内R的分解速率随温度升高而增大,错误。
22.C
解析 A项,铁与盐酸反应生成Fe2+,所以转移电子数应为0.1N ,错误;B项,在pH=
A
13的NaOH溶液中,c(H+) =10-13mol·L-1,所以1 L pH=13 NaOH溶液中,n(H+) =10-
水 水
13mol,错误;C项,根据2H +O ===2H O、2CO+O ===2CO ,标准状况,8.96 L(即0.4 mol)
2 2 2 2 2
该混合气体完全燃烧,消耗氧分子数目为0.2N ,正确;D项,1.2 g金刚石中含有碳碳单键
A
的数目为0.2N ,而1.2 g的石墨中含有碳碳单键的数目为0.15N ,所以1.2 g的该混合物中,
A A
含有碳碳单键的数目应在0.15N ~0.2N 之间,错误。
A A
23.B
解析 根据加入的NaOH溶液体积和混合溶液pH变化曲线可知,HY为强酸,HX为弱酸。
A项,由于HY为强酸,所以c(X-)<c(Y-),错误;B项,当V(NaOH)=10.00 mL时,HX、
HY均反应一半,根据pH,此时溶液呈酸性,说明HX的电离大于X-的水解,所以c(X-)>
c(Na+)>c(HX)>c(H+)>c(OH-),正确;C项,当V(NaOH)=20.00 mL时,正好完全反应生
成NaX,溶液呈碱性,此时c(Na+)>c(X-)>c(OH-)>c(H+),错误;D项,当pH=7时,
c(Na+)=c(Y-)>c(X-),错误。
24.C
解析 由于还原性SO2
3
->I-,所以通入Cl
2
发生的反应依次为
SO2
3
-+Cl
2
+H
2
O===SO2
4
-+2H++2Cl-①
2I-+Cl ===I +2Cl-②
2 2
第3页 | 共8页b 5
A项,当a≥b时,Cl 不足,只发生反应①,正确;B项,当5a=4b时,即 = 时,既发
2
a 4
生反应①,又发生反应②,正确;C项,当b=a时,只发生反应①,转移电子数为2a,当b
3 3
= a 时,转移电子数为 2a+a=3a mol,所以当 a≤b≤ a 时,转移电子数为 2a≤n(e
2 2
3
-)≤3a,错误;D项,当a<b< a时,此时,n(SO2
4
-)=a mol,I-为[a-2(b-a)]=(3a-2b)
2
mol,Cl-为2b mol,正确。
25.B
解析 根据向溶液X中加入过量稀盐酸有气体放出,可以推断X中含有CO2
3
-,根据离子共
存原则,没有Ca2+、Fe2+,根据电荷守恒,一定有Na+;根据沉淀,X中一定有SiO2
3
-,根
据向溶液1中加入过量AgNO 溶液产生的现象,一定没有Br-,因为没有产生黄色沉淀,
3
可能有SO2 4 -、Cl-,综上所述,A错误,B正确;C项,应加入Ba(NO 3 ) 2 ,不能加入BaCl 2 ,
因为Ag+干扰SO2
4
-的检验,错误;D项,溶液中不含Fe2+,所以不会发生该现象,错误。
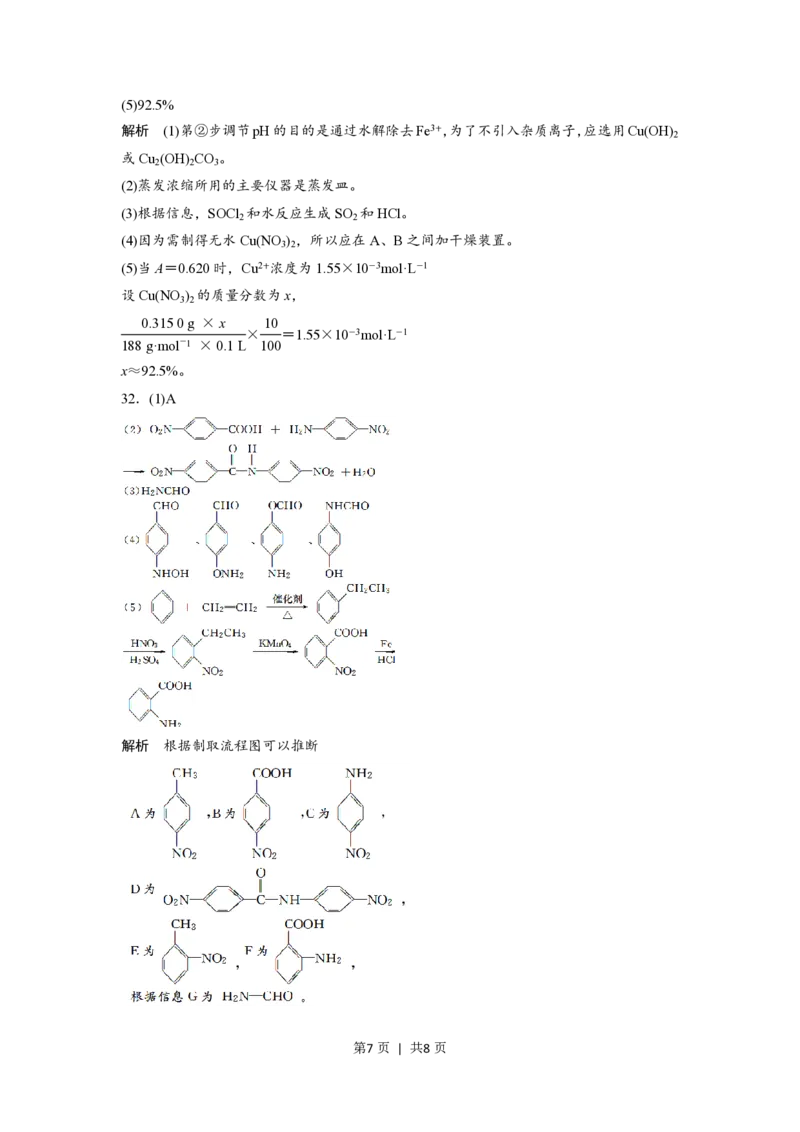
26.(1)醛基
催化剂
(2)CH CH +CH COOH ― ― →CH COOCH CH
2 2 3 3 2 3
(3)CH CH ONa+H O―→CH CH OH+NaOH
3 2 2 3 2
(4)AD
解析 A的摩尔质量为1.25 g·L-1×22.4 L·mol-1=28 g·mol-1,应为C H ,根据转化关系,
2 4
B为CH CHO,C为CH COOH,D为C H OH。(3)Na与C H OH反应生成C H ONa,C H ONa
3 3 2 5 2 5 2 5 2 5
强烈水解生成C H OH和NaOH,所以滴入酚酞溶液呈红色。(4)A项,CH CH +HOC H
2 5 2 2 2 5
一定条件
― ― →C H OC H ,正确;B项,CH CHO与Cu(OH) 反应生成砖红色沉淀,CH COOH
2 5 2 5 3 2 3
能使Cu(OH) 溶解,而C H OH和Cu(OH) 不反应,所以用新制Cu(OH) 悬浊液能区分B、
2 2 5 2 2
C、D,错误;C项,分离乙酸乙酯和乙酸的混合液,应加入饱和Na CO 溶液,再分液,错
2 3
误;D项,CH COOC H +H O CH COOH+C H OH,当加入NaOH时,由于CH COOH
3 2 5 2 3 2 5 3
和NaOH反应,平衡右移,所以乙酸乙酯在NaOH溶液中水解较在稀硫酸中更完全。
27.(1)S、Cu
Cu (OH) SO 或者2Cu(OH) ·CuSO
3 4 4 2 4
(2)4NaOH+3CuSO ===Cu (OH) SO ↓+2Na SO
4 3 4 4 2 4
解析 (1)根据反应流程,白色沉淀为BaSO ,其物质的量为0.01 mol,黑色固体为CuO,
4
其物质的量为0.01 mol,所以X中除H、O外,还有S、Cu。固体中有CuSO ,其物质的量
4
为0.01 mol,其质量为1.60 g,1.60 g的黑色固体应为CuO,其物质的量为0.02 mol,所以Cu2
+共有 0.03 mol, OH-共有 0.04 mol,SO2 4 -共有 0.01 mol,X 的化学式为 Cu 3 (OH) 4 SO 4 或
2Cu(OH) ·CuSO 。(2)若用非氧化还原反应制取X,可用NaOH溶液与CuSO 溶液反应制取。
2 4 4
第4页 | 共8页28.(1)B
(2)用胶头滴管滴加蒸馏水至溶液凹面正好与刻度线相切
(3)AC
解析 (1)在配制一定物质的量浓度溶液时,量筒可用也可不用。
(3)A项,若称取相同质量的Na CO ·10H O,造成Na CO 的质量偏小,所配溶液浓度偏低;
2 3 2 2 3
B项,定容时俯视刻度线,溶液体积偏小,所配溶液浓度偏高;C项,摇匀后,发现液面低
于刻度线,若此时再加水,造成溶液体积偏大,所配溶液浓度偏低;D项,未清洗容量瓶,
造成溶液有残留,所配溶液浓度偏高。
29.(1)2∶1(或2)
(2)2.50 mol·L-1
解析 (1)根据表中数据分析,第Ⅰ组实验,Na CO 、NaHCO 完全反应,设Na CO 、NaHCO
2 3 3 2 3 3
的物质的量分别为x、y,
{84 g·mol-1 ×y+106 g·mol-1 ×x=2.96 g
x+y=0.03 mol
{x=0.02 mol
解得
y=0.01 mol
Na CO 、NaHCO 的物质的量之比为2∶1。
2 3 3
(2)设NaHCO 的物质的量为x,则Na CO 的物质的量为2x,
3 2 3
实验Ⅱ:106 g·mol-1×2x+84 g·mol-1×x=3.70 g
x=0.012 5 mol,
实验Ⅲ:106 g·mol-1×2x+84 g·mol-1×x=5.18 g
x=0.017 5 mol,
实验Ⅳ:106 g·mol-1×2x+84 g·mol-1×x=6.66 g
x=0.022 5 mol
实验Ⅳ中,Na CO 为0.045 mol,NaHCO 为0.022 5 mol,Na CO 完全反应生成NaHCO ,
2 3 3 2 3 3
而NaHCO 反应了0.03 mol,所以消耗HCl的物质的量为0.045 mol+0.03 mol=0.075 mol,
3
0.075 mol
c(HCl)= =2.5 mol·L-1。
0.03 L
(注:用实验Ⅲ数据也可以计算)
30.(1)①放热反应,ΔS<0且反应自发
②
第5页 | 共8页(2)①3NaClO(aq)===2NaCl(aq)+NaClO (aq) ΔH=-116 kJ·mol-1(其他合理答案均可)
3
2c 0 -c 1 5c 0 -2c 1
②c + 或
0
3 3
③反应Ⅰ的活化能高,活化分子百分数低,不利于ClO-向ClO-
2
转化
通电
(3)2NaClO +O ===== 2NaClO (其他合理答案均可)
3 2 4
解析 (1)该反应为放热反应,反应自发进行即ΔG=ΔH-TΔS<0,又因ΔS<0,所以ΔH<
0为放热反应。
(2)①NaClO分解生成NaClO 的化学方程式为
3
3NaClO===2NaCl+NaClO
3
3NaClO(aq)+3NaCl(aq)+3H O(l)===3Cl (g)+6NaOH(aq) ΔH=306 kJ·mol-1
2 2
3Cl (g)+6NaOH(aq)===5NaCl(aq)+NaClO (aq)+3H O(l) ΔH =-422 kJ·mol-1
2 3 2 2
上述两式相加得
3NaClO(aq)===2NaCl(aq)+NaClO (aq) ΔH=-116 kJ·mol-1
3
②Cl +2NaOH===NaCl+NaClO+H O
2 2
c c
0 0
3NaClO===2NaCl+NaClO
3
2c 0 -c 1
c -c
0 1
3
2c 0 -c 1
所以c(Cl-)=c + 。
0
3
(3)电极反应式为
阳极:ClO-
3
-2e-+H
2
O===ClO-
4
+2H+
阴极:2H++2e-===H
2
利用O 把生成H 除去,2H +O ===2H O,
2 2 2 2 2
通电
总反应式为2NaClO +O ===== 2NaClO 。
3 2 4
31.(1)Cu(OH) 或Cu (OH) CO
2 2 2 3
(2)将溶液转移到蒸发皿中,控制温度加热至溶液表面形成一层晶膜 减慢冷却结晶的速度
(3)Cu(NO ) ·3H O+3SOCl ===Cu(NO ) +3SO ↑+6HCl↑
3 2 2 2 3 2 2
(4)在A、B之间增加干燥装置,防止B中水蒸气进入反应器A b
第6页 | 共8页(5)92.5%
解析 (1)第②步调节pH的目的是通过水解除去Fe3+,为了不引入杂质离子,应选用Cu(OH)
2
或Cu (OH) CO 。
2 2 3
(2)蒸发浓缩所用的主要仪器是蒸发皿。
(3)根据信息,SOCl 和水反应生成SO 和HCl。
2 2
(4)因为需制得无水Cu(NO ) ,所以应在A、B之间加干燥装置。
3 2
(5)当A=0.620时,Cu2+浓度为1.55×10-3mol·L-1
设Cu(NO ) 的质量分数为x,
3 2
0.315 0 g ×x 10
× =1.55×10-3mol·L-1
188 g·mol-1 ×0.1 L 100
x≈92.5%。
32.(1)A
解析 根据制取流程图可以推断
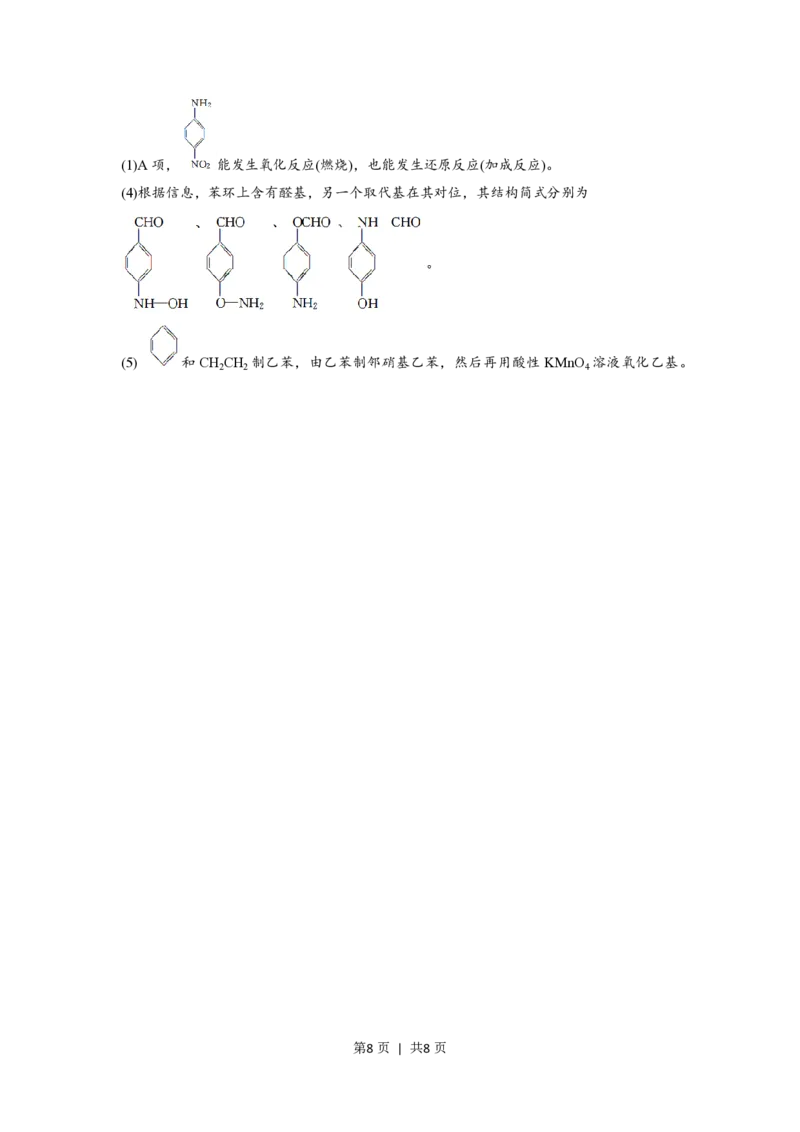
第7页 | 共8页(1)A项, 能发生氧化反应(燃烧),也能发生还原反应(加成反应)。
(4)根据信息,苯环上含有醛基,另一个取代基在其对位,其结构简式分别为
(5) 和CH CH 制乙苯,由乙苯制邻硝基乙苯,然后再用酸性KMnO 溶液氧化乙基。
2 2 4
第8页 | 共8页