文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
题型 04 化学计算题
►类型1 有关化学式的计算与推断........................................................................................................................1
►类型2 技巧性计算................................................................................................................................................6
►类型3 利用化学方程式进行计算的选择题......................................................................................................10
►类型4 纯净物的化学方程式计算......................................................................................................................18
►类型5 含有杂质的化学方程式计算问题..........................................................................................................23
►类型6 溶液溶质质量分数的计算......................................................................................................................31
►类型7 关于溶液配制的计算问题......................................................................................................................40
►类型1 有关化学式的计算与推断
角度1 计算原子个数(比)/元素种类
1.(2024·四川内江节选)内江人喜食羊肉汤,羊肉富含蛋白质,能产生有利于增鲜的氨基酸——谷氨酸
(C H NO )。请回答下列问题:
5 9 4
(1)谷氨酸由 种元素组成。一个谷氨酸分子由 个原子构成。
2.(2024·天津节选)蛋白质由甘氨酸(C H O N)等多种氨基酸构成。计算:
2 5 2
(1)甘氨酸由 种元素组成(写数值)。(2)一个甘氨酸分子中含有 个原子。
3.(2024·黑龙江节选)奥司他韦(化学式为 )是目前治疗和预防流感的药物之一。请回答:
(2)奥司他韦分子中碳、氧原子个数比为 (最简整数比)。
4.(2024·山东济宁节选)菠萝具有特殊的果香,是由于菠萝中含有的丁酸乙酯[化学式为 ,结构
简式为 发出的芳香气味。请回答:
(1)丁酸乙酯分子中,C、H、O三种原子的个数比为 .
5.(2024·海南节选)某品牌矿泉水瓶底标有如图所示标志。回答下列问题:
(3)合成PET的原料之一为乙二醇(C H O ),乙二醇分子中碳、氢原子个数比为 (最简整数比)。
2 6 2
角度2 计算相对分子质量
1.(2024·黑龙江节选)奥司他韦(化学式为 )是目前治疗和预防流感的药物之一。请回答:
(1)奥司他韦的相对分子质量是 。
2.(2024·黑龙江齐齐哈尔节选)蔗糖(化学式为 )是红糖、白糖和冰糖的主要成分,是生活中
常用的甜味剂。请根据蔗糖的化学式进行计算:
(1)蔗糖的相对分子质量是 。
角度3 计算元素质量比
1.(2024·山西)早在距今约六千年的半坡文化时期,陶制品上便出现了最早的彩绘。彩绘颜料种类多样,
有红彩、黑彩和白彩(主要成分是硫酸钙等),硫酸钙(CaSO )中,氧元素与钙元素的质量比为
4
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.5:8 B.8:5 C.5:6 D.6:5
2.(2024·四川内江节选)
(2)味精的主要成分为谷氨酸钠(C H NO Na)谷氨酸钠中氢、氧元素的质量比为 。
5 8 4
3.(2024·吉林节选)(1)CaO中钙元素和氧元素质量的最简整数比为 。
4.(2024·湖北节选)(1) 中钛、氯元素的质量比为 。
5.(2024·四川遂宁节选)(1)CaH 中钙元素和氢元素的质量比为 (化为最简整数比)。
2
6.(2024·重庆节选)(1) 中钠元素与氧元素的质量比为 。
7.(2024·四川南充节选)北京时间2024年4月25日,搭载神舟十八号载人飞船的长征二号F遥十八运载
火箭在酒泉卫星发射中心成功发射。该火箭的推进剂是偏二甲肼(化学式为C H N )。
2 8 2
(1)偏二甲肼中碳、氢、氮三种元素的质量比为 (填最简整数比)。
8.(2024·江西节选)(4)陶艺空间:硫酸锶( )常用于制陶器,其中硫元素为 价,则锶元素
(Sr)的化合价为 价。 中硫元素、氧元素的质量比为 。
9.(2024·内蒙古兴安盟)有机玻璃透光性能好,耐热、耐寒、耐腐蚀,并具有极强的耐冲击性,常用作
飞机、汽车挡风玻璃。工业上用甲基丙烯酸甲酯(C H O )来合成有机玻璃。请回答下列问题。
5 8 2
(2)甲基丙烯酸甲酯中碳、氢元素的质量比为 (填最简整数比)。
10.(2024·山东济宁节选)菠萝具有特殊的果香,是由于菠萝中含有的丁酸乙酯[化学式为 ,结构
简式为 发出的芳香气味。请回答:
(2)丁酸乙酯中,C、H、O三种元素的质量比为 。
角度4 计算元素的质量分数
1.(2024·山东菏泽节选)牡丹以其花大色艳、寓意吉祥而深受人们喜爱。
(3) 亚麻酸( )是人体脑细胞和组织细胞的重要组成成分,在牡丹籽油中含量较高, 亚麻酸中
质量分数最大的元素是 。
2.(2024·山东威海)如图是某葡萄糖酸锌口服液的标签,下列说法正确的是
A.锌是人体必需的常量元素 ××牌补锌口服液
B.葡萄糖酸锌中碳元素质量分数最大 主要成分:葡萄糖酸锌
C.每支口服液含葡萄糖酸锌45.5mg
化学式:CHOZn
122214
D.葡萄糖酸锌中碳、氢、氧、锌元素质量比为12:22:14:1
含锌量:每支口服液含锌6.5mg
3.(2024·山东东营)蔬菜和水果中都含有食物纤维,食物纤维的主要成分是纤维素[化学式为 ],
下列关于纤维素的说法正确的是
A.纤维素属于有机高分子化合物 B.纤维素中氢元素的质量分数最大
C.纤维素的相对分子质量为162 D.纤维素不能被人体吸收,对人体健康无益
4.(2024·广东深圳)梓醇( )是中药材地黄的主要成分,下列关于梓醇的说法正确的是
A.由三个元素组成 B.碳元素和氧元素的质量比
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.其中氢元素的质量分数最小 D.由碳元素、氢元素和氧元素构成
易错提醒 6
物质和元素都是宏观概念,用“组成”来描述;而分子、原子和离子等是微观粒子,用“构成”来 .
描述。 (
20
24·甘肃临夏)大河家鸡蛋皮核桃是临夏州特产之一,富含叶酸和维生素 等营养物质。下列有关叶酸
的说法正确的是
A.叶酸属于氧化物 B.叶酸由19个碳元素、19个氢元素、7个氮元素和6个氧元素组成
C.叶酸中碳、氢、氮、氧四种元素质量比为 D.叶酸中氢元素的质量分数最小
6.(2024·广东广州)蔗糖是食品中常用的甜味剂,其化学式为C H O 。下列关于蔗糖的说法正确的是
12 22 11
A.属于无机化合物 B.C、H、O三种元素的质量比为12:22:11
C.1个蔗糖分子中含有11个水分子 D.氧元素的质量分数为
7.(2024·江苏常州)《本草纲目》记载食肉桂能“面生光华”。肉桂酸( )是肉桂的主要有效成分,
下列说法正确的是
A.肉桂酸由碳、氢、氧三种原子构成 B.肉桂酸中碳与氢元素质量比为9∶8
C.肉桂酸中氧元素的质量分数为21.6% D.一个肉桂酸分子中含有一个氧分子
角度5 计算物质中元素的质量
易错提醒 1
化合物中某元素的质量=该化合物的质量×该化合物中该元素的质量分数。 .
(
2024·黑龙江齐齐哈尔节选)蔗糖(化学式为 )是红糖、白糖和冰糖的主要成分,是生活中常用
的甜味剂。请根据蔗糖的化学式进行计算:
(3)34.2g蔗糖中含有 碳元素。
2.(2024·黑龙江节选)奥司他韦(化学式为 )是目前治疗和预防流感的药物之一。请回答:
(3)15.6g奥司他韦中氮元素的质量为 g。
3.(2024·四川南充节选)北京时间2024年4月25日,搭载神舟十八号载人飞船的长征二号F遥十八运载
火箭在酒泉卫星发射中心成功发射。该火箭的推进剂是偏二甲肼(化学式为C H N )。
2 8 2
(2) g偏二甲肼中含氮元素的质量是42g。
4.(2024·天津节选)蛋白质由甘氨酸(C H O N)等多种氨基酸构成。计算:
2 5 2
(3)75g甘氨酸中含有氮元素的质量为 g。
5.(2024·黑龙江牡丹江节选)(2)含有相同质量氧元素的 和 的质量最简比为 。
►类型2 技巧性计算
1.(2024·四川达州)实验室有部分被氧化的镁条8.0g与300.0g溶质质量分数为7.3%的稀盐酸恰好完全反
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
应,该镁条中镁元素的质量为
A.7.8g B.7.2g C.6.0g D.2.4g
8.(2024·四川广元)乙醇(C H OH)是常用的燃料。现有4.6g乙醇与一定量氧气混合于密闭容器内,在一
2 5
定条件下反应物全部转化为一氧化碳、二氧化碳和水,恢复到室温,测得所得气体中氧元素质量分数为
70%,则参加反应的氧气质量为
A.6.4g B.8.0g C.8.8g D.9.6g
1.(24-25九年级上·江苏扬州·阶段练习)将 缓慢通入盛有20gCuO的试管中,加热使其反应,过一会
儿停止加热,冷却至室温后,称得剩余固体质量为19.2g。则生成铜的质量为
A.16g B.19.2g C.2.8g D.3.2g
2.(24-25九年级上·河南·阶段练习)若某同学取CuO和Cu的混合物10克,用足量CO还原,充分反应并
冷却后称得剩余固体的质量为8.4克,则原混合物中Cu的质量分数为
A.20% B.64% C.80% D.95%
3.(24-25九年级上·四川遂宁·期中)已知由NaHS、MgSO 、NaHSO 组成的混合物,硫元素的质量分数为
4 4
a%,则混合物中氧元素的质量分数为
A.a% B.2a% C.1-1.75a% D.1-0.75a%
4.(24-25九年级上·河南周口·期中)某技术人员对甲醛(HCHO)、乙酸 和乳酸 的混
合水溶液进行测定,其中氧元素的质量分数为64%,则该溶液中碳元素的质量分数为
A.28% B.30% C.32% D.36%
5.(24-25九年级上·重庆长寿·阶段练习)某密闭容器中有CO和 的混合气体,已知C元素的质量分数
为24%,则混合气体中S元素的质量分数为
A.6% B.18% C.22% D.28%
6.(24-25九年级上·广西柳州·阶段练习)有 、 、 组成的混合物,经测定含氧元素的
质量分数为 ,则氢元素的质量分数为
A. B. C. D.
7.(24-25九年级上·黑龙江大庆·阶段练习)在稀硫酸和硫酸铜的混合液中,加入适量铁粉,使其恰好反
应。反应后得到的固体质量与所加铁粉质量相等。则原混合液中硫酸和硫酸铜的质量比为
A.7∶8 B.8∶7 C.7∶80 D.80∶7
8.(2024·河南驻马店·模拟预测)将 的碳酸钙和铜粉的混合物在空气中煅烧使其完全反应,若反应
前后固体的质量保持不变,则原混合物中碳酸钙的质量为
A. B. C. D.
9.(2024·河南·一模)12.8 g MgO和CuO的混合物与足量的稀盐酸充分反应,所得溶液蒸发结晶并充分干
燥后称量固体的质量为23.8 g,则原混合物中金属元素的质量分数为
A.25% B.75% C.78% D.80%
►类型3 利用化学方程式进行计算的选择题
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
1.(2024·四川绵阳)将一定质量的水煤气(CO和 的混合物)在氧气中充分燃烧,燃烧产物依次通过
足量的浓硫酸和NaOH溶液,浓硫酸增重0.9g,NaOH溶液增重2.2g。该水煤气中CO和 的质量比为
A.7:1 B.14:1 C.28:1 D.56:1
2.(2024·江苏镇江)已知:2NaHCO Na CO +CO ↑+H O,将16.8gNaHCO 固体加热一段时间后,剩余固
3 2 3 2 2 3
体质量为13.7g。下列说法正确的是
A.原固体加热生成3.1gCO
2
B.加热后,固体中钠元素的质量分数减小
C.剩余固体中NaHCO 和Na CO 的质量比为42:53
3 2 3
D.将13.7g剩余固体溶于足量盐酸后,蒸发结晶,得11.7gNaCl
3.(2024·江苏南通)学习小组为探究氢气还原氧化铜所得固体产物X的组成,设计如下实验:
步骤1 观察产物X的颜色为红色。
步骤2 向产物X中加入过量的盐酸充分反应,过滤得到9.6g红色固体和蓝色溶液。
步骤3 向步骤2所得蓝色溶液中加入过量的Na H Y溶液,测得与CuCl 反应的Na H Y的质量为33.6g。
2 2 2 2 2
已知:①Na H Y的相对分子质量为336 ②Cu O为红色固体
2 2 2
③Cu O+2HCl=Cu+CuCl +H O CuCl +Na H Y=CuH Y+2NaCl
2 2 2 2 2 2 2
下列说法正确的是
A.产物X为Cu单质 B.步骤2所得蓝色溶液中仅含有Cu2+、Cl﹣两种离子
C.步骤3中参加反应的CuCl 的质量为27gD.产物X中Cu元素的质量分数为90.9%
2
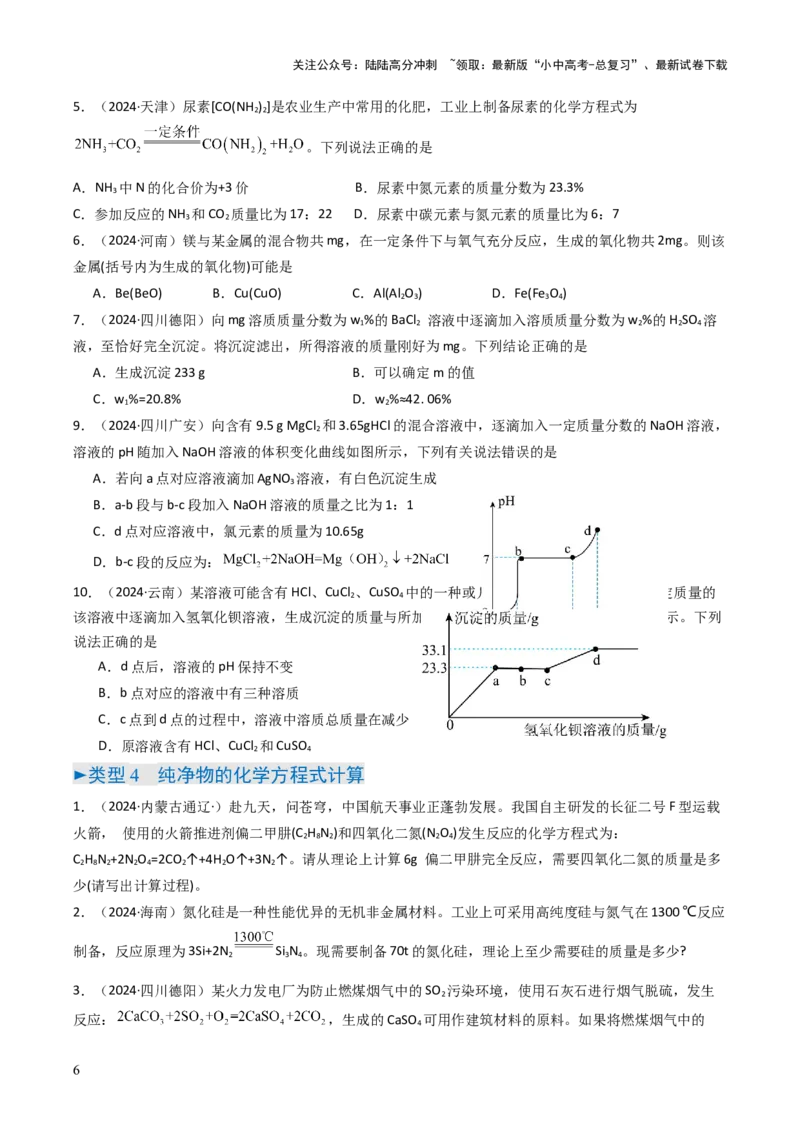
4.(2024·湖北武汉)化学项目小组为探究久置后自制干燥剂的组成,取一定质量的样品,加入足量水,
充分溶解,静置,再逐滴加入质量分数为 的稀盐酸,生成二氧化碳的质量与加入稀盐酸的质量变化关
系如图所示。(忽略二氧化碳的溶解)已知:①向碳酸钠溶液中滴加稀盐酸依次发生反应:
, ;②碳酸氢钠能与氢氧化钠反应生成
碳酸钠和水。
下列说法错误的是
A.该久置后自制干燥剂样品中一定含
B.该久置后自制干燥剂样品中一定含 和
C.图中 ,且M点溶液中一定只含一种溶质
D.变质前自制干燥剂中 与 的质量比为
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
5.(2024·天津)尿素[CO(NH ) ]是农业生产中常用的化肥,工业上制备尿素的化学方程式为
2 2
。下列说法正确的是
A.NH 中N的化合价为+3价 B.尿素中氮元素的质量分数为23.3%
3
C.参加反应的NH 和CO 质量比为17:22 D.尿素中碳元素与氮元素的质量比为6:7
3 2
6.(2024·河南)镁与某金属的混合物共mg,在一定条件下与氧气充分反应,生成的氧化物共2mg。则该
金属(括号内为生成的氧化物)可能是
A.Be(BeO) B.Cu(CuO) C.Al(Al O ) D.Fe(Fe O )
2 3 3 4
7.(2024·四川德阳)向mg溶质质量分数为w %的BaCl 溶液中逐滴加入溶质质量分数为w %的H SO 溶
1 2 2 2 4
液,至恰好完全沉淀。将沉淀滤出,所得溶液的质量刚好为mg。下列结论正确的是
A.生成沉淀233 g B.可以确定m的值
C.w %=20.8% D.w %≈42. 06%
1 2
9.(2024·四川广安)向含有9.5 g MgCl 和3.65gHCl的混合溶液中,逐滴加入一定质量分数的NaOH溶液,
2
溶液的pH随加入NaOH溶液的体积变化曲线如图所示,下列有关说法错误的是
A.若向a点对应溶液滴加AgNO 溶液,有白色沉淀生成
3
B.a-b段与b-c段加入NaOH溶液的质量之比为1:1
C.d点对应溶液中,氯元素的质量为10.65g
D.b-c段的反应为:
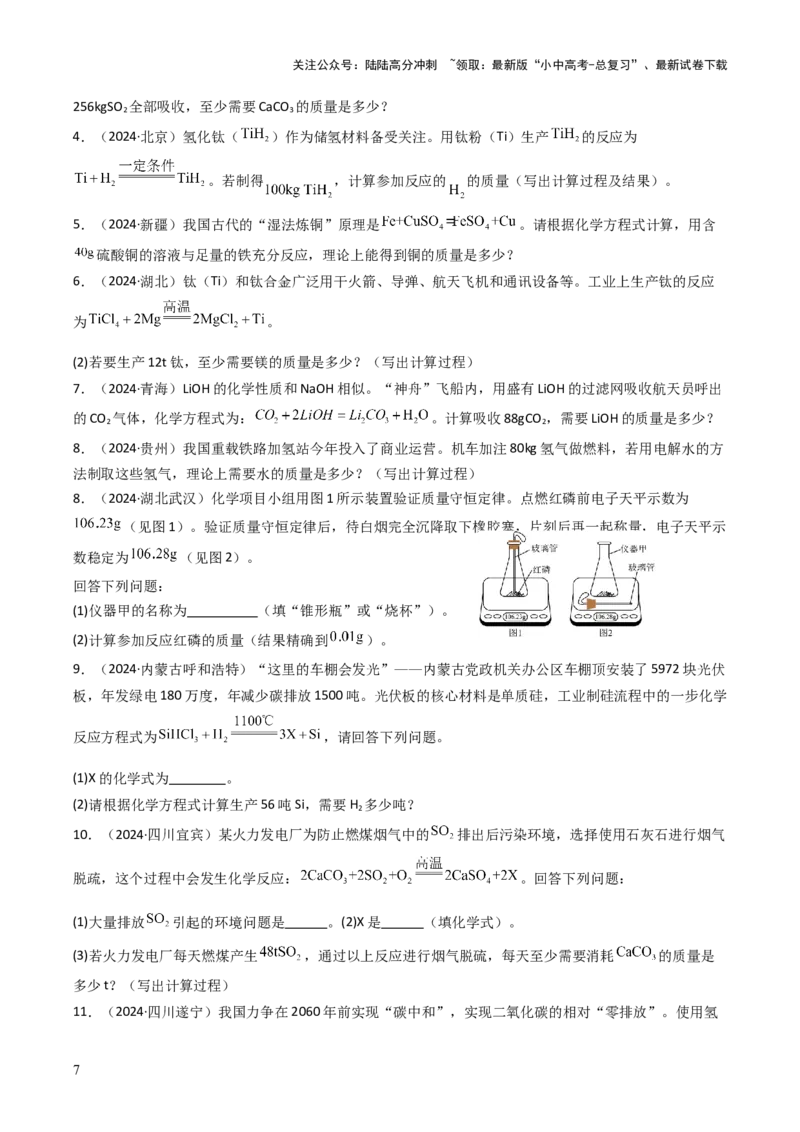
10.(2024·云南)某溶液可能含有HCl、CuCl 、CuSO 中的一种或几种,为了探究其组成,向一定质量的
2 4
该溶液中逐滴加入氢氧化钡溶液,生成沉淀的质量与所加氢氧化钡溶液的质量之间的关系如图所示。下列
说法正确的是
A.d点后,溶液的pH保持不变
B.b点对应的溶液中有三种溶质
C.c点到d点的过程中,溶液中溶质总质量在减少
D.原溶液含有HCl、CuCl 和CuSO
2 4
►类型4 纯净物的化学方程式计算
1.(2024·内蒙古通辽·)赴九天,问苍穹,中国航天事业正蓬勃发展。我国自主研发的长征二号F型运载
火箭, 使用的火箭推进剂偏二甲肼(C H N )和四氧化二氮(N O )发生反应的化学方程式为:
2 8 2 2 4
C H N +2N O =2CO ↑+4H O↑+3N ↑。请从理论上计算6g 偏二甲肼完全反应,需要四氧化二氮的质量是多
2 8 2 2 4 2 2 2
少(请写出计算过程)。
2.(2024·海南)氮化硅是一种性能优异的无机非金属材料。工业上可采用高纯度硅与氮气在1300 ℃反应
制备,反应原理为3Si+2N Si N 。现需要制备70t的氮化硅,理论上至少需要硅的质量是多少?
2 3 4
3.(2024·四川德阳)某火力发电厂为防止燃煤烟气中的SO 污染环境,使用石灰石进行烟气脱硫,发生
2
反应: ,生成的CaSO 可用作建筑材料的原料。如果将燃煤烟气中的
4
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
256kgSO 全部吸收,至少需要CaCO 的质量是多少?
2 3
4.(2024·北京)氢化钛( )作为储氢材料备受关注。用钛粉(Ti)生产 的反应为
。若制得 ,计算参加反应的 的质量(写出计算过程及结果)。
5.(2024·新疆)我国古代的“湿法炼铜”原理是 。请根据化学方程式计算,用含
硫酸铜的溶液与足量的铁充分反应,理论上能得到铜的质量是多少?
6.(2024·湖北)钛(Ti)和钛合金广泛用干火箭、导弹、航天飞机和通讯设备等。工业上生产钛的反应
为 。
(2)若要生产12t钛,至少需要镁的质量是多少?(写出计算过程)
7.(2024·青海)LiOH的化学性质和NaOH相似。“神舟”飞船内,用盛有LiOH的过滤网吸收航天员呼出
的CO 气体,化学方程式为: 。计算吸收88gCO ,需要LiOH的质量是多少?
2 2
8.(2024·贵州)我国重载铁路加氢站今年投入了商业运营。机车加注80kg氢气做燃料,若用电解水的方
法制取这些氢气,理论上需要水的质量是多少?(写出计算过程)
8.(2024·湖北武汉)化学项目小组用图1所示装置验证质量守恒定律。点燃红磷前电子天平示数为
(见图1)。验证质量守恒定律后,待白烟完全沉降取下橡胶塞,片刻后再一起称量,电子天平示
数稳定为 (见图2)。
回答下列问题:
(1)仪器甲的名称为 (填“锥形瓶”或“烧杯”)。
(2)计算参加反应红磷的质量(结果精确到 )。
9.(2024·内蒙古呼和浩特)“这里的车棚会发光”——内蒙古党政机关办公区车棚顶安装了5972块光伏
板,年发绿电180万度,年减少碳排放1500吨。光伏板的核心材料是单质硅,工业制硅流程中的一步化学
反应方程式为 ,请回答下列问题。
(1)X的化学式为 。
(2)请根据化学方程式计算生产56吨Si,需要H 多少吨?
2
10.(2024·四川宜宾)某火力发电厂为防止燃煤烟气中的 排出后污染环境,选择使用石灰石进行烟气
脱疏,这个过程中会发生化学反应: 。回答下列问题:
(1)大量排放 引起的环境问题是 。(2)X是 (填化学式)。
(3)若火力发电厂每天燃煤产生 ,通过以上反应进行烟气脱硫,每天至少需要消耗 的质量是
多少t?(写出计算过程)
11.(2024·四川遂宁)我国力争在2060年前实现“碳中和”,实现二氧化碳的相对“零排放”。使用氢
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
能源汽车可以有效减少二氧化碳的排放。氢化钙(CaH )是一种重要的制氢剂,氢化钙可与物质M反应生
2
成氢气,反应的化学方程式为: ,请完成下列各题:
(1)CaH 中钙元素和氢元素的质量比为 (化为最简整数比)。(2)M的化学式为 。
2
(3)若制取8kg氢气,计算理论上需要CaH 的质量(写出计算过程)。
2
►类型5 含有杂质的化学方程式计算问题
1.(2024·山东淄博)硅化镁 在能源器件、激光和半导体制造等领域具有重要应用价值,可通过
石英砂(主要成分为 ,杂质不含硅元素)和金属镁反应制得,反应的化学方程式为
。
(1)上述化学方程式中X为 (填化学式)。
(2)用 石英砂与足量镁充分反应得到 硅化镁,计算石英砂中 的质量分数(写出计算过程)。
2.(2024·四川广安)碱石灰(CaO、NaOH)常用作气体的干燥剂。化学兴趣小组为测定某种碱石灰中
CaO的质量分数,将10g碱石灰加入到80gNa CO 溶液中,发生反应: 。
2 3
待碱石灰中CaO完全反应后,测得生成CaCO 固体的质量为10g。
3
回答下列问题:
(1)除去CaCO 固体后,所得溶液的质量为 g。
3
(2)求该碱石灰中CaO的质量分数。(写出计算过程)
3.(2024·山东威海)某品牌“发热鞋垫”中发热剂的主要成分为铁粉、活性炭和氯化钠等。为测定其中
铁粉的含量,小明同学进行如下实验:取5g发热剂样品于烧杯中,逐滴加入稀硫酸至不再产生气泡,测得
加入稀硫酸的质量为23.4g,反应后烧杯内剩余物的总质量为28.3g,计算发热剂中铁粉的质量分数(假设其
他成分不与酸反应)。
4.(2024·云南)为测定某过氧化氢溶液的溶质质量分数,实验中记录的相关数据如表。
反应前物质的质量 完全反应后物质的质量
过氧化氢溶液质 固体与液体混合物质
二氧化锰质量 氧气质量
量 量
34.0g 0.1g 33.3g _______g
请计算:
(1)表中氧气的质量为 g。
(2)该过氧化氢溶液的溶质质量分数。(温馨提示: )
5.(2024·山东菏泽)超市卖的纯碱产品中,往往含有少量的 。化学兴趣小组的同学要通过实验来测
定某品牌纯碱样品中 的质量分数。取12g纯碱样品放入烧杯中,加水完全溶解,逐滴加入一定溶
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
质质量分数的 溶液。产生沉淀的质量与加入 溶液的质量关系如图所示。
(1)完全反应后,生成沉淀的质量为 g。
(2)计算纯碱样品中 的质量分数。(精确到0.1%)
6.(24-25九年级上·陕西咸阳·期末)兴趣小组加热某不纯的高锰酸钾样品制取氧气,反应过程中固体物
质的质量随时间变化的数据如下表所示:
加热时间/s 0 t₁ t₂ t₃ t₄
固体质
20.0 19.3 18.8 18.4 18.4
量/g
请分析并计算:
(1)生成氧气的总质量为 g。(2)计算该样品中高锰酸钾的质量分数。
7.(24-25九年级上·内蒙古呼伦贝尔·期末)硅钢是变压器、充电器中的核心材料,其主要成分是Fe和
Si。某学生用硅钢样品做了如下实验:取4.2g硅钢样品,将60g稀硫酸分6次加入样品中(其中稀硫酸与硅
及其他杂质不反应),充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下
实验次数 一 二 三 四 五 六
稀硫酸的用量/g 10 10 10 10 10 10
剩余固体的质
M 2.8 2.1 1.4 0.7 0.7
量/g
(1)从以上数据可知,稀硫酸加入第 次充分反应后,铁恰好完全反应。
(2)计算所用稀硫酸中溶质的质量分数(结果精确到0.1%)。
8.(2024九年级上·湖南邵阳·竞赛)某化学兴趣小组的同学为测定石灰石中碳酸钙的质量分数,取50g石
灰石置于重100g的烧杯中,再将100g稀盐酸,分5次加入烧杯中,充分反应,(杂质不溶于水也不参加反
应)实验数据如下:
实验次序 1 2 3 4 5
加入稀盐酸的质量/g 20 20 20 20 20
烧杯及剩余物总质
167.8 185.6 m 221.2 240.1
量/g
请回答:
(1)表中: 。
(2)石灰石中碳酸钙的质量分数(写出计算过程)
9.(24-25九年级上·湖北武汉·期末)“金粉”(铜锌合金)是一种金属颜料,可用于文物修复。某化学
兴趣小组通过实验测定“金粉”中铜的含量:称取25.00g“金粉”样品放入如图装置中,将100.00g稀硫酸
分5次加入,记录每次反应后装置内物质的总质量。实验数据如下表:
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
加入次数 第1次 第2次 第3次 第4次 第5次
加入稀硫酸的质量/g 20.00 20.00 20.00 20.00 20.00
反应后装置内物质总质
44.94 64.88 84.82 104.80 124.80
量/g
回答下列问题:
(1)25.00g“金粉”样品与100.00g稀硫酸充分反应后,生成氢气的质量共有 g;
(2)计算样品中铜的质量分数(写出计算过程,计算结果精确到0.1%)。
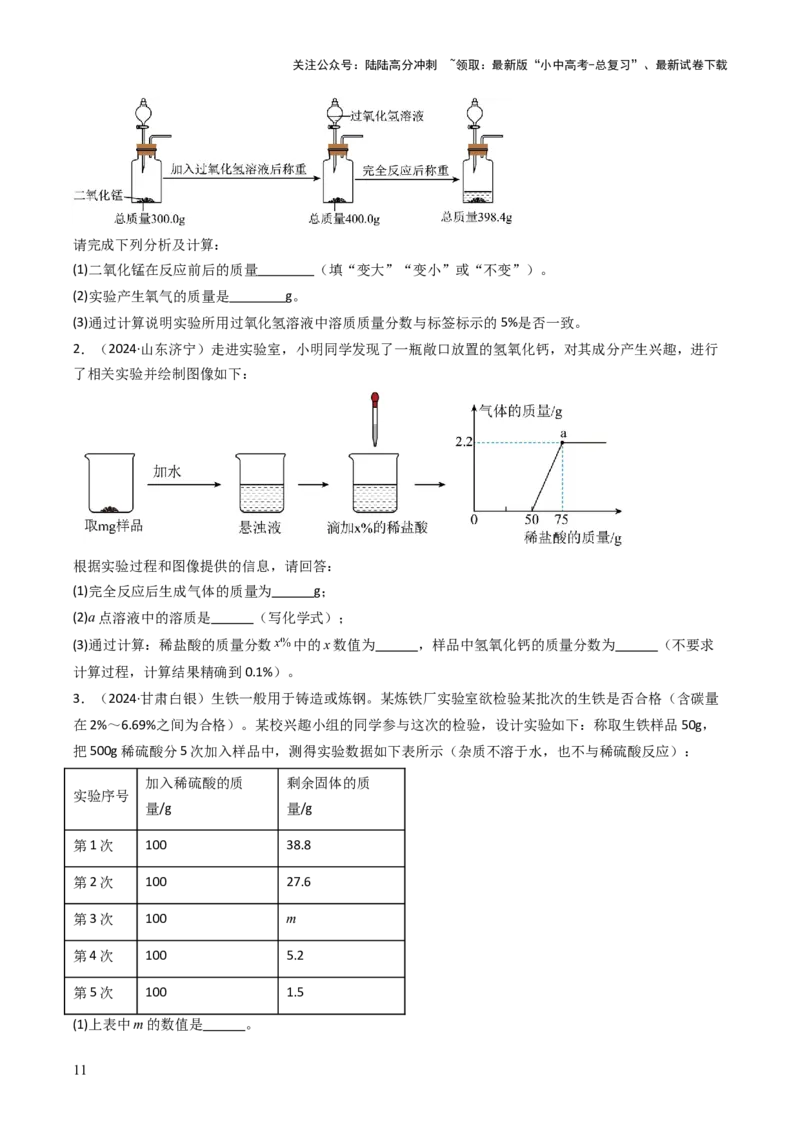
10.(24-25九年级上·江西吉安·阶段练习)同学们从山上采集到一种石灰石,他们取80克该样品进行煅
烧实验(所含杂质在煅烧过程不发生变化),测得反应后固体的质量(m)与反应时间(t)的关系如下表:
反应时间
反应后固体的质量 80 75 70 66 62 58 58
请回答下列问题:
(1)当石灰石完全反应后,生成二氧化碳的质量为 g。
(2)求该石灰石中碳酸钙的质量分数,写出计算过程。
(3)反应过程中固体中钙元素的质量分数 (填“逐渐增大”“逐渐减小”“先增大后不变”“先减
小后不变”或“一直不变”)。
11.(24-25九年级上·重庆彭水·阶段练习)实验室用34g过氧化氢溶液和1g二氧化锰制取氧气,实验的相
关数据如图所示。请回答:
(1)过氧化氢中氢元素和氧元素的质量比 。
(2)反应生成氧气的质量为 。
(3)计算该反应消耗过氧化氢的质量。
12.(24-25九年级上·海南海口·期末)某兴趣小组为测定某石灰石(主要成分是CaCO )的质量分数,做
3
了如下实验:取24g样品放入烧杯中,向其中逐渐加入稀盐酸(杂质不溶于水也不与酸反应),剩余固体
质量随加入稀盐酸质量的变化关系如图所示。
(1)24g该石灰石样品中CaCO 的质量为 克;
3
(2)计算充分反应后产生二氧化碳的质量为 克。
►类型6 溶液溶质质量分数的计算
角度1 所给溶液的溶质质量分数
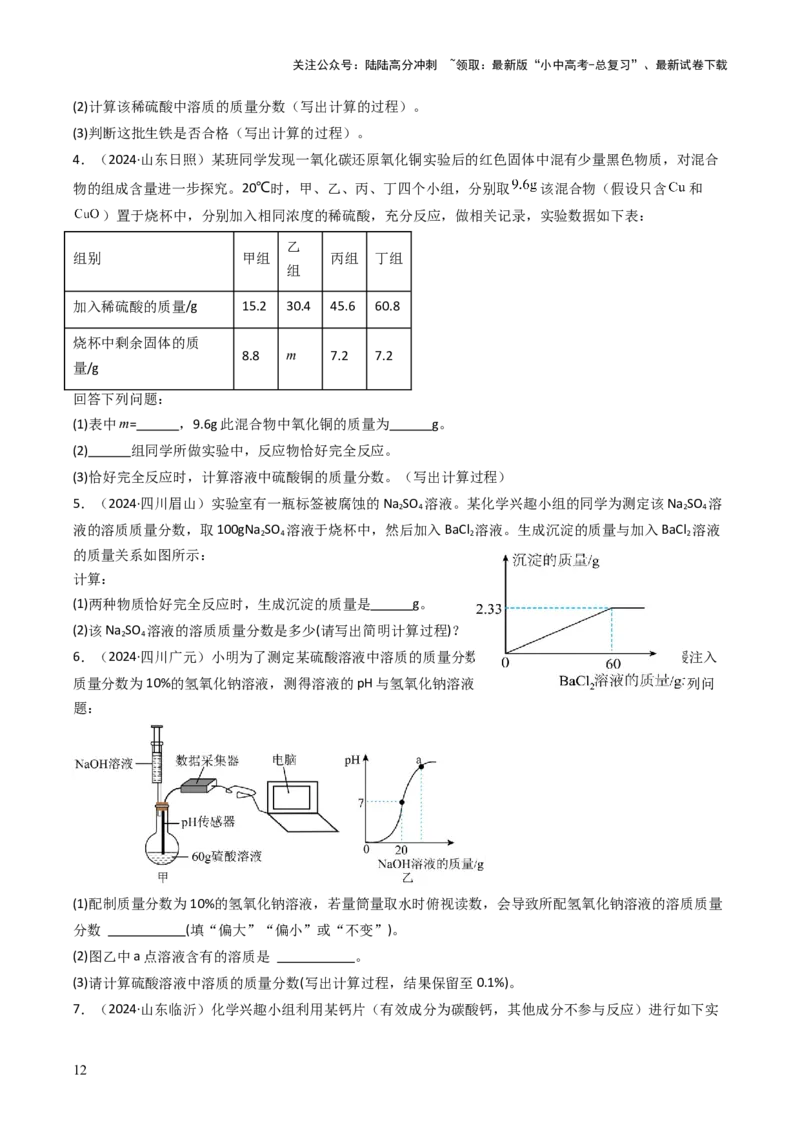
1.(2024·陕西)学习小组用一瓶长久放置、标签标示溶质质量分数为5%的过氧化氢溶液制取氧气,并用
下图所示方法测定实验产生氧气的质量。
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
请完成下列分析及计算:
(1)二氧化锰在反应前后的质量 (填“变大”“变小”或“不变”)。
(2)实验产生氧气的质量是 g。
(3)通过计算说明实验所用过氧化氢溶液中溶质质量分数与标签标示的5%是否一致。
2.(2024·山东济宁)走进实验室,小明同学发现了一瓶敞口放置的氢氧化钙,对其成分产生兴趣,进行
了相关实验并绘制图像如下:
根据实验过程和图像提供的信息,请回答:
(1)完全反应后生成气体的质量为 g;
(2)a点溶液中的溶质是 (写化学式);
(3)通过计算:稀盐酸的质量分数 中的x数值为 ,样品中氢氧化钙的质量分数为 (不要求
计算过程,计算结果精确到0.1%)。
3.(2024·甘肃白银)生铁一般用于铸造或炼钢。某炼铁厂实验室欲检验某批次的生铁是否合格(含碳量
在2%~6.69%之间为合格)。某校兴趣小组的同学参与这次的检验,设计实验如下:称取生铁样品50g,
把500g稀硫酸分5次加入样品中,测得实验数据如下表所示(杂质不溶于水,也不与稀硫酸反应):
加入稀硫酸的质 剩余固体的质
实验序号
量/g 量/g
第1次 100 38.8
第2次 100 27.6
第3次 100 m
第4次 100 5.2
第5次 100 1.5
(1)上表中m的数值是 。
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)计算该稀硫酸中溶质的质量分数(写出计算的过程)。
(3)判断这批生铁是否合格(写出计算的过程)。
4.(2024·山东日照)某班同学发现一氧化碳还原氧化铜实验后的红色固体中混有少量黑色物质,对混合
物的组成含量进一步探究。20℃时,甲、乙、丙、丁四个小组,分别取 该混合物(假设只含 和
)置于烧杯中,分别加入相同浓度的稀硫酸,充分反应,做相关记录,实验数据如下表:
乙
组别 甲组 丙组 丁组
组
加入稀硫酸的质量/g 15.2 30.4 45.6 60.8
烧杯中剩余固体的质
8.8 m 7.2 7.2
量/g
回答下列问题:
(1)表中m= ,9.6g此混合物中氧化铜的质量为 g。
(2) 组同学所做实验中,反应物恰好完全反应。
(3)恰好完全反应时,计算溶液中硫酸铜的质量分数。(写出计算过程)
5.(2024·四川眉山)实验室有一瓶标签被腐蚀的Na SO 溶液。某化学兴趣小组的同学为测定该Na SO 溶
2 4 2 4
液的溶质质量分数,取100gNa SO 溶液于烧杯中,然后加入BaCl 溶液。生成沉淀的质量与加入BaCl 溶液
2 4 2 2
的质量关系如图所示:
计算:
(1)两种物质恰好完全反应时,生成沉淀的质量是 g。
(2)该Na SO 溶液的溶质质量分数是多少(请写出简明计算过程)?
2 4
6.(2024·四川广元)小明为了测定某硫酸溶液中溶质的质量分数,如图甲,向60g硫酸溶液中缓缓注入
质量分数为10%的氢氧化钠溶液,测得溶液的pH与氢氧化钠溶液的质量对应关系如图乙。请回答下列问
题:
(1)配制质量分数为10%的氢氧化钠溶液,若量筒量取水时俯视读数,会导致所配氢氧化钠溶液的溶质质量
分数 (填“偏大”“偏小”或“不变”)。
(2)图乙中a点溶液含有的溶质是 。
(3)请计算硫酸溶液中溶质的质量分数(写出计算过程,结果保留至0.1%)。
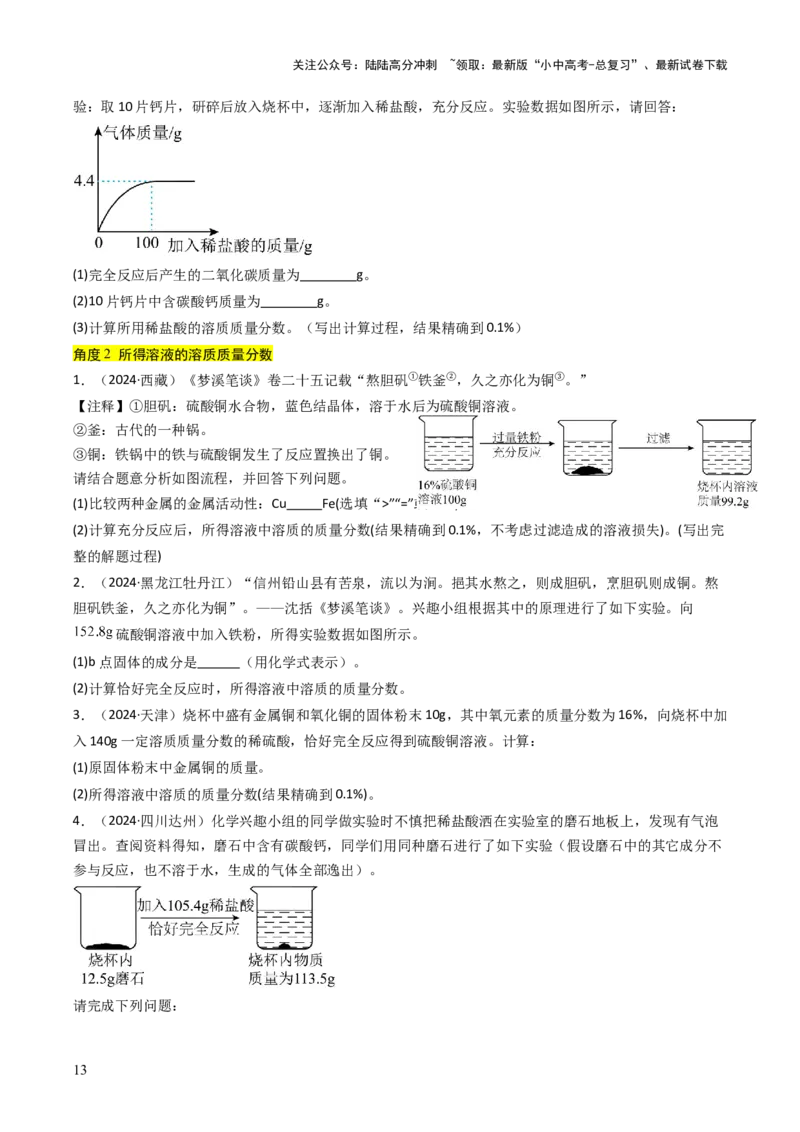
7.(2024·山东临沂)化学兴趣小组利用某钙片(有效成分为碳酸钙,其他成分不参与反应)进行如下实
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
验:取10片钙片,研碎后放入烧杯中,逐渐加入稀盐酸,充分反应。实验数据如图所示,请回答:
(1)完全反应后产生的二氧化碳质量为 g。
(2)10片钙片中含碳酸钙质量为 g。
(3)计算所用稀盐酸的溶质质量分数。(写出计算过程,结果精确到0.1%)
角度2 所得溶液的溶质质量分数
1.(2024·西藏)《梦溪笔谈》卷二十五记载“熬胆矾 铁釜 ,久之亦化为铜 。”
① ② ③
【注释】①胆矾:硫酸铜水合物,蓝色结晶体,溶于水后为硫酸铜溶液。
②釜:古代的一种锅。
③铜:铁锅中的铁与硫酸铜发生了反应置换出了铜。
请结合题意分析如图流程,并回答下列问题。
(1)比较两种金属的金属活动性:Cu Fe(选填“>”“=”或“<”)。
(2)计算充分反应后,所得溶液中溶质的质量分数(结果精确到0.1%,不考虑过滤造成的溶液损失)。(写出完
整的解题过程)
2.(2024·黑龙江牡丹江)“信州铅山县有苦泉,流以为涧。挹其水熬之,则成胆矾,烹胆矾则成铜。熬
胆矾铁釜,久之亦化为铜”。——沈括《梦溪笔谈》。兴趣小组根据其中的原理进行了如下实验。向
硫酸铜溶液中加入铁粉,所得实验数据如图所示。
(1)b点固体的成分是 (用化学式表示)。
(2)计算恰好完全反应时,所得溶液中溶质的质量分数。
3.(2024·天津)烧杯中盛有金属铜和氧化铜的固体粉末10g,其中氧元素的质量分数为16%,向烧杯中加
入140g一定溶质质量分数的稀硫酸,恰好完全反应得到硫酸铜溶液。计算:
(1)原固体粉末中金属铜的质量。
(2)所得溶液中溶质的质量分数(结果精确到0.1%)。
4.(2024·四川达州)化学兴趣小组的同学做实验时不慎把稀盐酸洒在实验室的磨石地板上,发现有气泡
冒出。查阅资料得知,磨石中含有碳酸钙,同学们用同种磨石进行了如下实验(假设磨石中的其它成分不
参与反应,也不溶于水,生成的气体全部逸出)。
请完成下列问题:
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)生成二氧化碳的质量为 g。
(2)计算反应后烧杯内溶液的溶质质量分数(写出计算过程)。
5.(2024·黑龙江)某化学实验小组为测定碳酸钾和氯化钾的固体混合物组成情况,同学们取20g固体混
合物,加入90g水使固体混合物全部溶解,再向该溶液中加入111g溶质质量分数为10%的氯化钙溶液,恰
好完全反应形成不饱和溶液。请计算下列问题:
(1)固体混合物中碳酸钾的质量。
(2)恰好完全反应后所得溶液的溶质质量分数。
►类型7 关于溶液配制的计算问题
角度1 溶液配制的计算
1.(2024·黑龙江牡丹江节选)配制 溶质质量分数为 的蔗糖溶液
(1)需蔗糖 g,水 g。
2.(2024·黑龙江绥化节选)(3)把150g质量分数为16%的氯化钠溶液稀释为8%的氯化钠溶液,需加水的
质量是 g。
3.(2024·四川成都节选)
(3)配制质量分数为7.08%的硝酸钾溶液200g,需要硝酸钾 g(精确到0.1g)。
4.(2024·江苏连云港节选)物质的溶解性与化学变化密切相关。兴趣小组对“CaSO 与NaOH能否发生复
4
分解反应”进行探究。
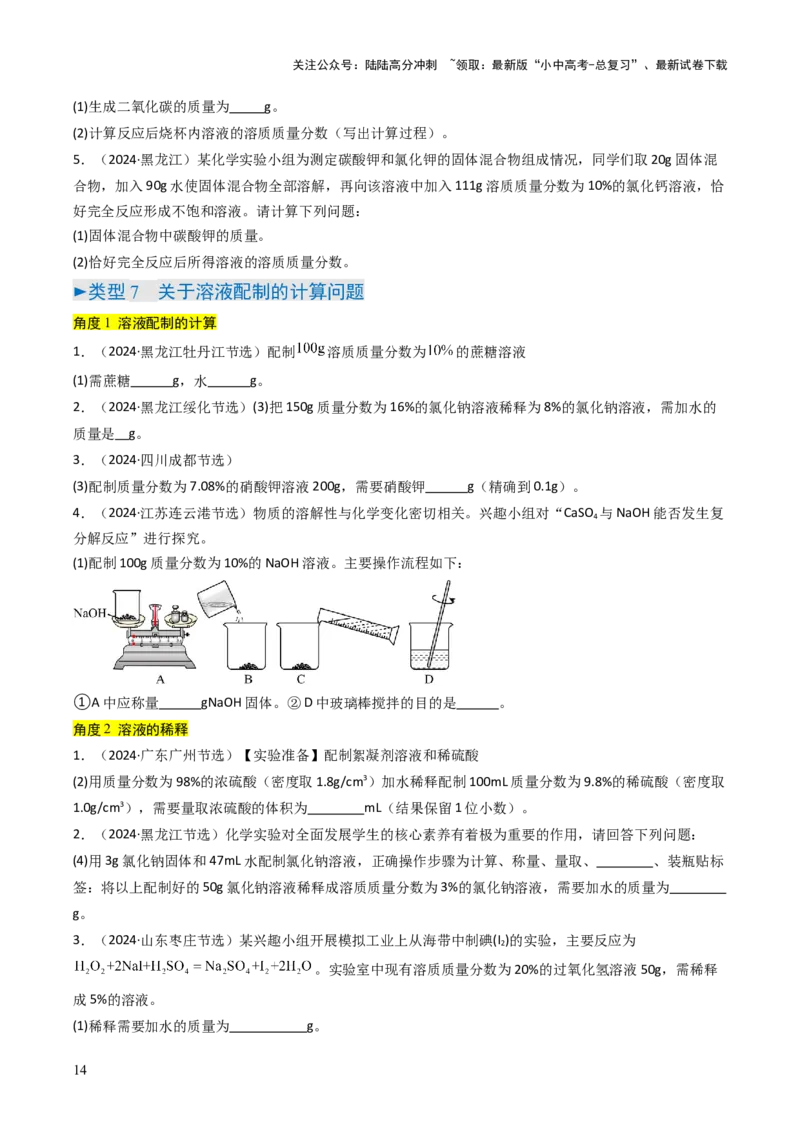
(1)配制100g质量分数为10%的NaOH溶液。主要操作流程如下:
①A中应称量 gNaOH固体。②D中玻璃棒搅拌的目的是 。
角度2 溶液的稀释
1.(2024·广东广州节选)【实验准备】配制絮凝剂溶液和稀硫酸
(2)用质量分数为98%的浓硫酸(密度取1.8g/cm3)加水稀释配制100mL质量分数为9.8%的稀硫酸(密度取
1.0g/cm3),需要量取浓硫酸的体积为 mL(结果保留1位小数)。
2.(2024·黑龙江节选)化学实验对全面发展学生的核心素养有着极为重要的作用,请回答下列问题:
(4)用3g氯化钠固体和47mL水配制氯化钠溶液,正确操作步骤为计算、称量、量取、 、装瓶贴标
签:将以上配制好的50g氯化钠溶液稀释成溶质质量分数为3%的氯化钠溶液,需要加水的质量为
g。
3.(2024·山东枣庄节选)某兴趣小组开展模拟工业上从海带中制碘(I )的实验,主要反应为
2
。实验室中现有溶质质量分数为20%的过氧化氢溶液50g,需稀释
成5%的溶液。
(1)稀释需要加水的质量为 g。
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
15