文档内容
5 氢氧化亚铁制备实验探究
1.制备原理
(1)制备原理:Fe2++2OH-===Fe(OH) ↓。
2
(2)成功关键:溶液中不含O 等氧化性物质;制备过程中,保证生成的 Fe(OH) 在密闭的、
2 2
隔绝空气的体系中。
2.常用方法
(1)有机层隔离法
①反应在试管底部进行(这是唯一一种把胶头滴管插入反应溶液的实验)。
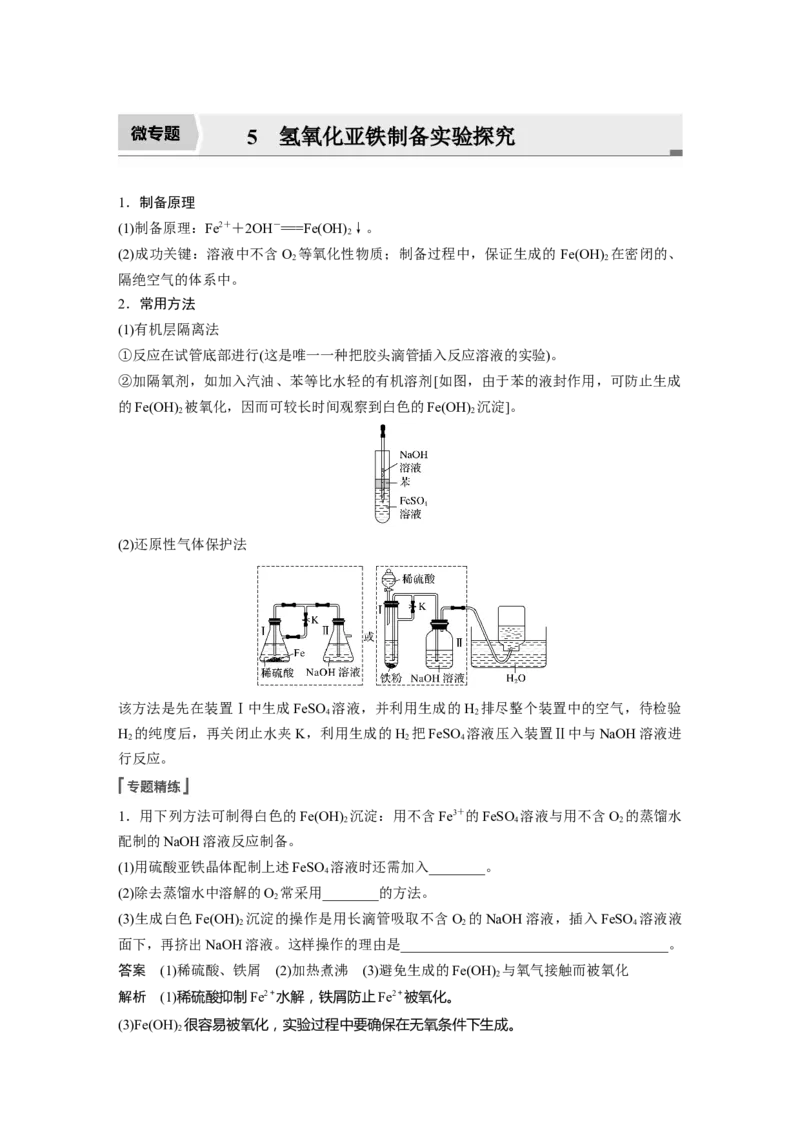
②加隔氧剂,如加入汽油、苯等比水轻的有机溶剂[如图,由于苯的液封作用,可防止生成
的Fe(OH) 被氧化,因而可较长时间观察到白色的Fe(OH) 沉淀]。
2 2
(2)还原性气体保护法
该方法是先在装置Ⅰ中生成FeSO 溶液,并利用生成的H 排尽整个装置中的空气,待检验
4 2
H 的纯度后,再关闭止水夹K,利用生成的H 把FeSO 溶液压入装置Ⅱ中与NaOH溶液进
2 2 4
行反应。
1.用下列方法可制得白色的Fe(OH) 沉淀:用不含Fe3+的FeSO 溶液与用不含O 的蒸馏水
2 4 2
配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述FeSO 溶液时还需加入________。
4
(2)除去蒸馏水中溶解的O 常采用________的方法。
2
(3)生成白色Fe(OH) 沉淀的操作是用长滴管吸取不含O 的NaOH溶液,插入FeSO 溶液液
2 2 4
面下,再挤出NaOH溶液。这样操作的理由是______________________________________。
答案 (1)稀硫酸、铁屑 (2)加热煮沸 (3)避免生成的Fe(OH) 与氧气接触而被氧化
2
解析 (1)稀硫酸抑制Fe2+水解,铁屑防止Fe2+被氧化。
(3)Fe(OH) 很容易被氧化,实验过程中要确保在无氧条件下生成。
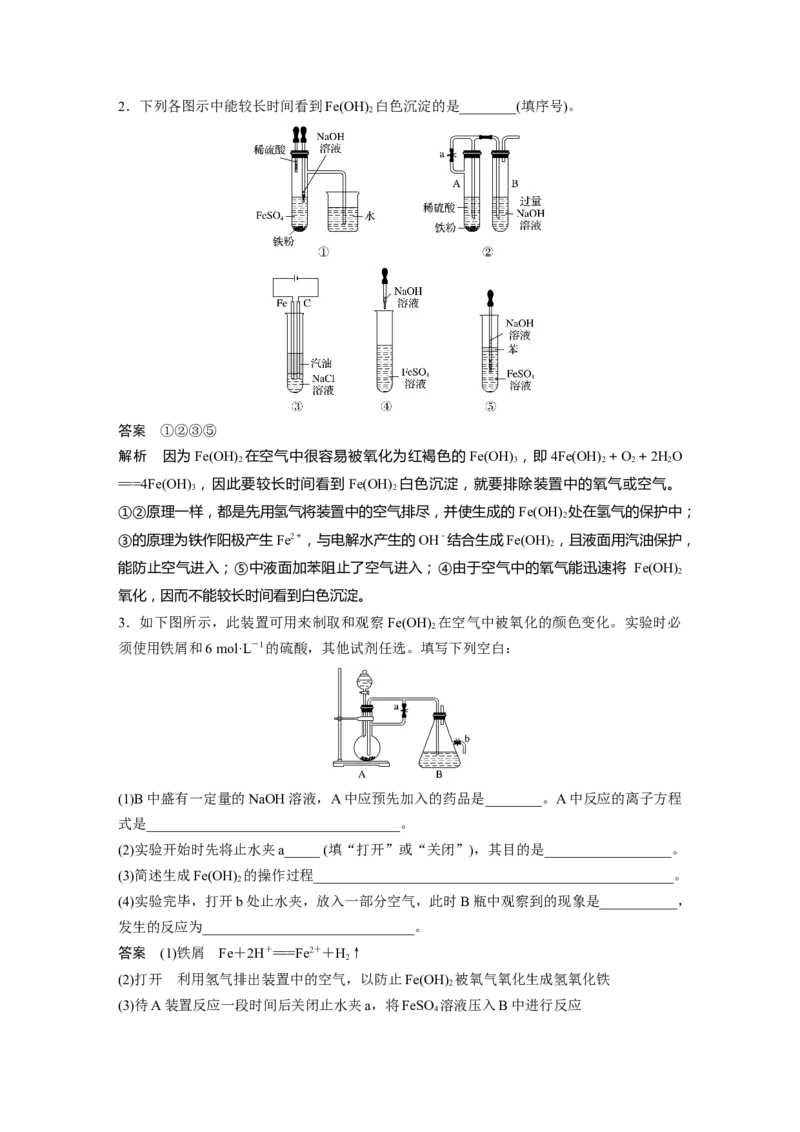
22.下列各图示中能较长时间看到Fe(OH) 白色沉淀的是________(填序号)。
2
答案 ①②③⑤
解析 因为Fe(OH) 在空气中很容易被氧化为红褐色的Fe(OH) ,即4Fe(OH) +O +2HO
2 3 2 2 2
===4Fe(OH) ,因此要较长时间看到 Fe(OH) 白色沉淀,就要排除装置中的氧气或空气。
3 2
①②原理一样,都是先用氢气将装置中的空气排尽,并使生成的 Fe(OH) 处在氢气的保护中;
2
③的原理为铁作阳极产生Fe2+,与电解水产生的OH-结合生成Fe(OH) ,且液面用汽油保护,
2
能防止空气进入;⑤中液面加苯阻止了空气进入;④由于空气中的氧气能迅速将 Fe(OH)
2
氧化,因而不能较长时间看到白色沉淀。
3.如下图所示,此装置可用来制取和观察 Fe(OH) 在空气中被氧化的颜色变化。实验时必
2
须使用铁屑和6 mol·L-1的硫酸,其他试剂任选。填写下列空白:
(1)B中盛有一定量的NaOH溶液,A中应预先加入的药品是________。A中反应的离子方程
式是____________________________________。
(2)实验开始时先将止水夹a_____ (填“打开”或“关闭”),其目的是__________________。
(3)简述生成Fe(OH) 的操作过程___________________________________________________。
2
(4)实验完毕,打开b处止水夹,放入一部分空气,此时B瓶中观察到的现象是___________,
发生的反应为______________________________。
答案 (1)铁屑 Fe+2H+===Fe2++H↑
2
(2)打开 利用氢气排出装置中的空气,以防止Fe(OH) 被氧气氧化生成氢氧化铁
2
(3)待A装置反应一段时间后关闭止水夹a,将FeSO 溶液压入B中进行反应
4(4)白色絮状物迅速变成灰绿色,最后变为红褐色
4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 3