文档内容
第 25 讲 非金属及其化合物知识落实与拓展
复习目标 1.进一步巩固常见非金属及其化合物的性质与应用。2.了解氮族元素磷、砷及其
重要化合物的性质和特点。3.了解氧族元素硒、碲及其化合物的性质。
考点一 非金属及其化合物知识再落实
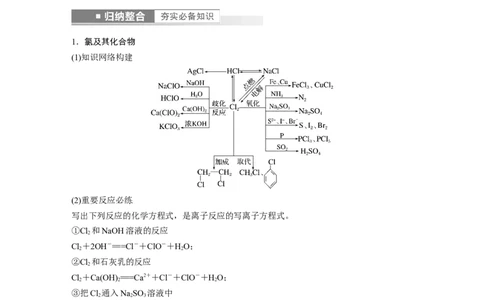
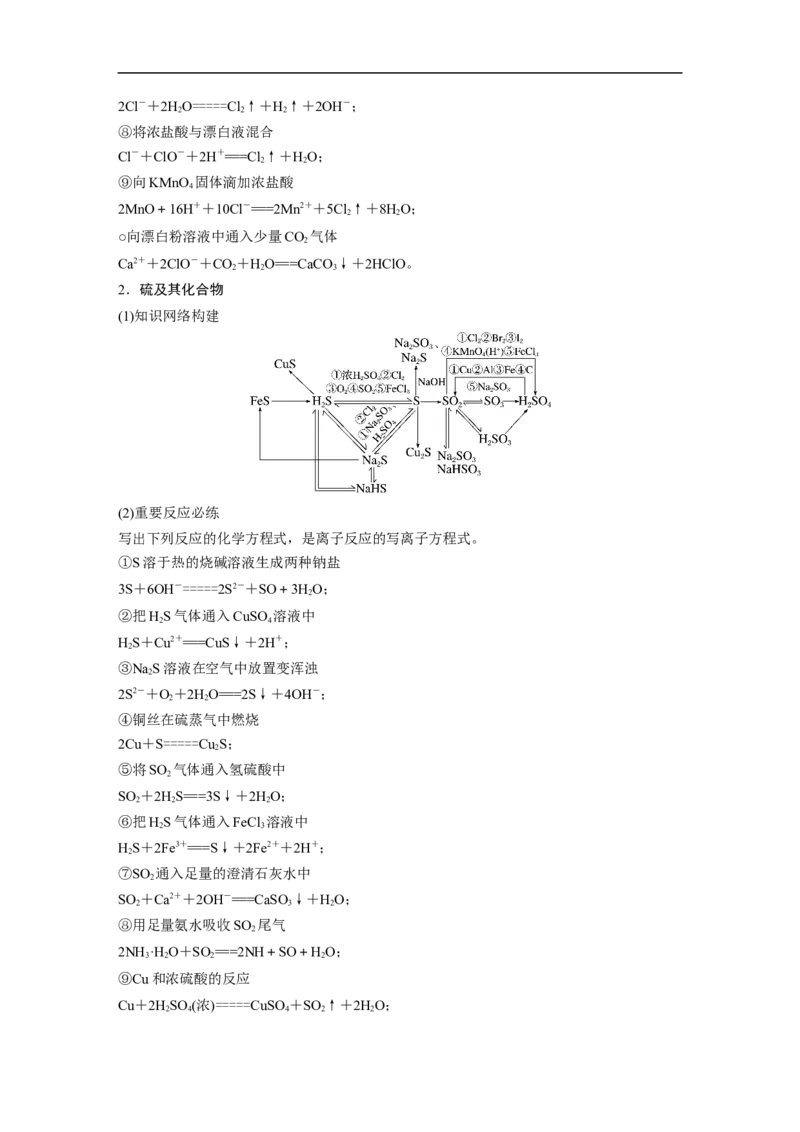
1.氯及其化合物
(1)知识网络构建
(2)重要反应必练
写出下列反应的化学方程式,是离子反应的写离子方程式。
①Cl 和NaOH溶液的反应
2
Cl+2OH-===Cl-+ClO-+HO;
2 2
②Cl 和石灰乳的反应
2
Cl+Ca(OH) ===Ca2++Cl-+ClO-+HO;
2 2 2
③把Cl 通入NaSO 溶液中
2 2 3
Cl+SO+HO===SO+2H++2Cl-;
2 2
④将Cl 和SO 混合通入HO中
2 2 2
SO +Cl+2HO===4H++2Cl-+SO;
2 2 2
⑤将Cl 通入氢硫酸溶液中
2
Cl+HS===S↓+2H++2Cl-;
2 2
⑥将浓盐酸和MnO 混合加热
2
MnO +4H++2Cl-=====Mn2++Cl↑+2HO;
2 2 2
⑦电解饱和食盐水2Cl-+2HO=====Cl↑+H↑+2OH-;
2 2 2
⑧将浓盐酸与漂白液混合
Cl-+ClO-+2H+===Cl↑+HO;
2 2
⑨向KMnO 固体滴加浓盐酸
4
2MnO+16H++10Cl-===2Mn2++5Cl↑+8HO;
2 2
○向漂白粉溶液中通入少量CO 气体
2
Ca2++2ClO-+CO+HO===CaCO ↓+2HClO。
2 2 3
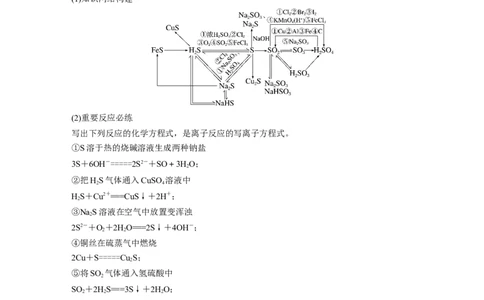
2.硫及其化合物
(1)知识网络构建
(2)重要反应必练
写出下列反应的化学方程式,是离子反应的写离子方程式。
①S溶于热的烧碱溶液生成两种钠盐
3S+6OH-=====2S2-+SO+3HO;
2
②把HS气体通入CuSO 溶液中
2 4
HS+Cu2+===CuS↓+2H+;
2
③NaS溶液在空气中放置变浑浊
2
2S2-+O+2HO===2S↓+4OH-;
2 2
④铜丝在硫蒸气中燃烧
2Cu+S=====Cu S;
2
⑤将SO 气体通入氢硫酸中
2
SO +2HS===3S↓+2HO;
2 2 2
⑥把HS气体通入FeCl 溶液中
2 3
HS+2Fe3+===S↓+2Fe2++2H+;
2
⑦SO 通入足量的澄清石灰水中
2
SO +Ca2++2OH-===CaSO↓+HO;
2 3 2
⑧用足量氨水吸收SO 尾气
2
2NH ·H O+SO ===2NH+SO+HO;
3 2 2 2
⑨Cu和浓硫酸的反应
Cu+2HSO (浓)=====CuSO +SO ↑+2HO;
2 4 4 2 2○C和浓硫酸的反应
C+2HSO (浓)=====CO↑+2SO ↑+2HO;
2 4 2 2 2
⑪把浓HSO 滴到NaSO 固体上
2 4 2 3
HSO (浓)+NaSO ===NaSO +HO+SO ↑。
2 4 2 3 2 4 2 2
3.氮及其化合物
(1)知识网络构建
(2)重要反应必练
写出下列反应的化学方程式,是离子反应的写离子方程式。
①把NH 通入水中
3
NH +HONH ·H ONH+OH-;
3 2 3 2
②实验室利用NH Cl固体、Ca(OH) 固体混合加热制备NH
4 2 3
2NH Cl+Ca(OH) =====2NH ↑+2HO+CaCl ;
4 2 3 2 2
③NH 的催化氧化
3
4NH +5O=====4NO+6HO;
3 2 2
④NO 溶于水
2
3NO +HO===2H++2NO+NO;
2 2
⑤NO 被烧碱溶液吸收生成两种钠盐
2
2NO +2OH-===NO+NO+HO;
2 2
⑥物质的量之比为1∶1的NO和NO 混合气体恰好被烧碱溶液吸收生成一种钠盐
2
NO+NO +2OH-===2NO+HO;
2 2
⑦Cu和稀HNO 的反应
3
3Cu+8H++2NO===3Cu2++2NO↑+4HO;
2
⑧Cu和浓HNO 的反应
3
Cu+4H++2NO===Cu2++2NO ↑+2HO;
2 2
⑨C和浓HNO 的反应
3
C+4H++4NO=====CO↑+4NO ↑+2HO;
2 2 2
⑩浓硝酸见光分解
4HNO=====4NO ↑+O↑+2HO。
3 2 2 2
一、非金属及其化合物性质的综合判断1.下列关于C、N、Si、S等非金属元素及其化合物的说法错误的是( )
A.它们都能以游离态存在于自然界中
B.氮氧化物、二氧化硫是形成酸雨的主要物质
C.它们的最高价氧化物都能与强碱反应生成含氧酸盐
D.加热条件下,碳、硫单质都能与浓硝酸、浓硫酸发生反应
答案 A
解析 硅是亲氧元素,硅元素在自然界中以硅酸盐、二氧化硅的形式存在,C、N、S都能
以游离态存在于自然界中,A项错误;二氧化硫、氮氧化物以及它们在大气中发生反应后的
生成物溶于雨水会形成酸雨,故氮氧化物、二氧化硫是形成酸雨的主要物质,B项正确;
C、N、Si、S的最高价氧化物分别为CO 、NO 、SiO 和SO ,与强碱反应分别生成碳酸盐、
2 2 5 2 3
硝酸盐、硅酸盐和硫酸盐,都是含氧酸盐,C项正确;碳单质和硫单质具有还原性,浓硝酸
和浓硫酸具有氧化性,故碳单质、硫单质在加热条件下能与浓硝酸、浓硫酸发生反应,D项
正确。
2.下列关于Cl、S等非金属元素单质及其化合物的说法正确的是( )
A.漂白粉的成分是次氯酸钙
B.实验室可用浓硫酸干燥硫化氢
C.将浓硫酸滴到浓盐酸中可以快速制取HCl气体
D.氯气、硫与铁反应生成的产物中,铁的化合价相同
答案 C
解析 漂白粉的主要成分是次氯酸钙和氯化钙,有效成分是次氯酸钙,A项错误;浓硫酸具
有强氧化性,硫化氢具有还原性,两者可发生反应,故不能用浓硫酸干燥硫化氢,B项错误;
浓硫酸稀释时放热,可使盐酸挥发,故将浓硫酸滴到浓盐酸中可快速制取HCl气体,C项正
确;氯气具有强氧化性,可将铁氧化为Fe3+,硫的氧化性弱于氯气,只能将铁氧化为Fe2
+,故氯气、硫与铁反应生成的产物中,铁的化合价不同,D项错误。
3.液氨中存在与水的电离类似的电离过程,金属钠投入液氨中可生成氨基钠(NaNH ),下
2
列说法不正确的是( )
A.液氨的电离方程式可表示为2NH NH+NH
3
B.钠与液氨的反应是氧化还原反应,反应中有H 生成
2
C.NaNH 与少量水反应可能有NH 逸出,所得溶液呈弱碱性
2 3
D.NaNH 与一定量稀硫酸充分反应,所得溶液经蒸发浓缩、冷却结晶可能得到四种盐
2
答案 C
解析 HO的电离方程式可表示为 2HOHO++OH-,HO分子电离出的H+与另一个
2 2 3 2
HO分子中O原子的孤电子对成键生成HO+,NH 分子中N原子也有孤电子对,可与H+成
2 3 3
键,A项正确;根据“金属钠投入液氨中可生成氨基钠(NaNH )”可知,钠元素的化合价由
2
0升高为+1,发生了氧化还原反应,则必有元素化合价降低,体系中只有+1价的H能得电子生成 H ,B 项正确;类比乙醇钠与水的反应,NaNH 与水的反应为 NaNH +
2 2 2
2HO===NaOH+NH ·H O,水量较少时,可能有NH 逸出,但所得溶液呈强碱性,C项错
2 3 2 3
误;NaNH 在溶液中会水解生成NaOH和NH ·H O,当加入少量稀硫酸时:2NH ·H O+
2 3 2 3 2
HSO ===(NH )SO +2HO、2NaOH+HSO ===NaSO +2HO,当加入过量稀硫酸时:
2 4 4 2 4 2 2 4 2 4 2
NH ·H O+HSO ===NH HSO +HO、NaOH+HSO ===NaHSO +HO,则可能得到
3 2 2 4 4 4 2 2 4 4 2
(NH )SO 、NaSO 、NH HSO 、NaHSO 四种盐,D项正确。
4 2 4 2 4 4 4 4
4.硫酸铜分解产物受温度影响较大,现将硫酸铜在一定温度下分解,得到的气体产物可能
含有SO 、SO 、O ,得到的固体产物可能含有CuO、Cu O。已知Cu O+2H+===Cu+Cu2+
2 3 2 2 2
+HO,某学习小组对产物进行以下实验,下列有关说法正确的是( )
2
A.将气体通过BaCl 溶液产生白色沉淀,说明混合气体中含有SO
2 3
B.将气体通过酸性高锰酸钾溶液,溶液褪色,说明混合气体中含有SO 与O
2 2
C.固体产物中加稀硝酸溶解,溶液呈蓝色,说明固体产物中含有CuO
D.将气体依次通过饱和NaSO 溶液、灼热的铜网、酸性高锰酸钾溶液可以将气体依次吸
2 3
收
答案 B
解析 SO 、O 与 BaCl 反应也有沉淀生成:2SO +O +2BaCl +2HO===2BaSO↓+
2 2 2 2 2 2 2 4
4HCl,故不能说明混合气体中含有SO ,A项错误;SO 能使酸性高锰酸钾溶液褪色,说明
3 2
混合气体中含有SO ,硫酸铜分解产生SO ,硫元素的化合价由+6降至+4,根据得失电子
2 2
守恒可知,应有元素化合价升高,故硫酸铜分解的产物中一定含有 O ,B项正确;CuO、
2
Cu O 均可与稀硝酸反应生成蓝色的硝酸铜溶液,反应的方程式为 3Cu O+
2 2
14HNO(稀)===6Cu(NO ) +2NO↑+7HO、CuO+2HNO(稀)===Cu(NO ) +HO,故不能说
3 3 2 2 3 3 2 2
明固体产物中含有CuO,C项错误;SO 、SO 均可与饱和NaSO 溶液反应,故不能依次吸
2 3 2 3
收气体,D项错误。
二、非金属及其化合物转化关系的应用
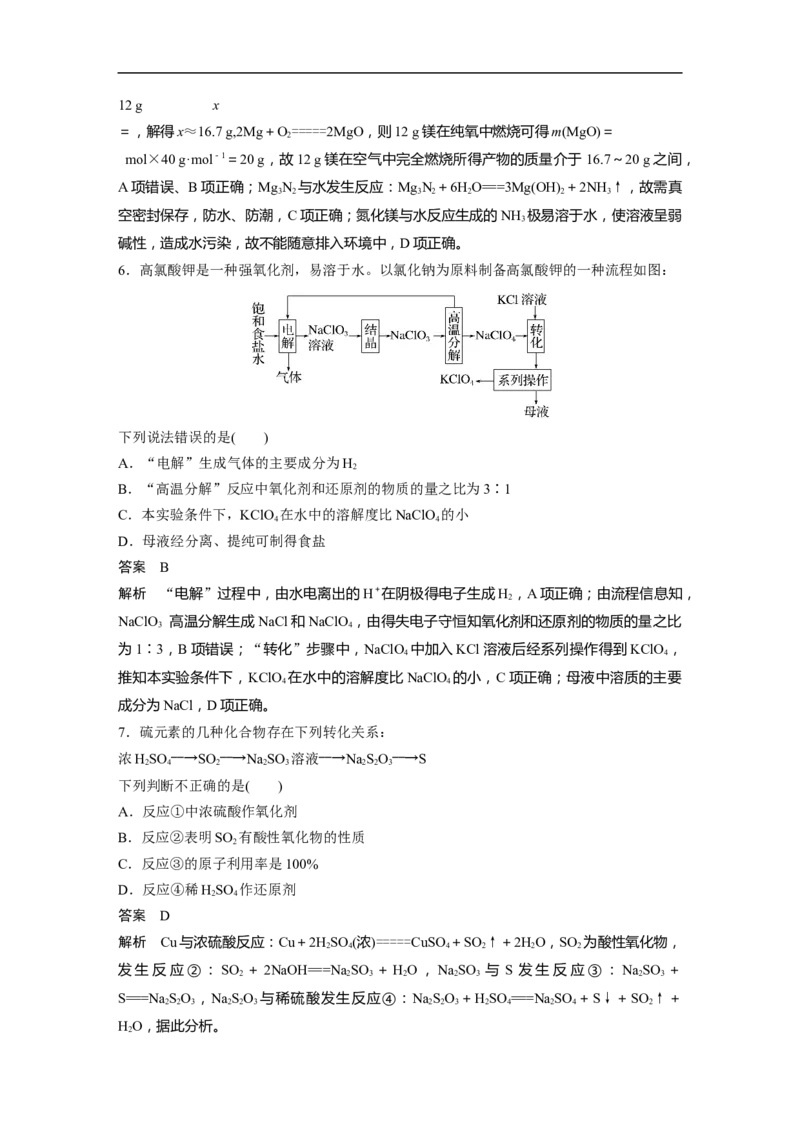
5.氮化镁(Mg N)是由氮和镁所组成的无机化合物。室温下,纯净的氮化镁为黄绿色的粉末,
3 2
能与水反应,但含有氧化镁杂质的氮化镁是灰白色的,能溶于酸,微溶于乙醇和乙醚。下列
说法错误的是( )
A.12 g镁在空气中完全燃烧所得产物的质量大于20 g
B.要制备氮化镁,可将镁带在氮气中燃烧制成
C.氮化镁需要真空密封保存,防水、防潮
D.未经政府许可不能将MgN 排入周围环境
3 2
答案 A
解析 设12 g镁在氮气中完全燃烧生成氮化镁的质量为x,则有:
3Mg+N=====MgN
2 3 2
72 10012 g x
=,解得x≈16.7 g,2Mg+O=====2MgO,则12 g镁在纯氧中燃烧可得m(MgO)=
2
mol×40 g·mol-1=20 g,故12 g镁在空气中完全燃烧所得产物的质量介于 16.7~20 g之间,
A项错误、B项正确;MgN 与水发生反应:MgN +6HO===3Mg(OH) +2NH ↑,故需真
3 2 3 2 2 2 3
空密封保存,防水、防潮,C项正确;氮化镁与水反应生成的NH 极易溶于水,使溶液呈弱
3
碱性,造成水污染,故不能随意排入环境中,D项正确。
6.高氯酸钾是一种强氧化剂,易溶于水。以氯化钠为原料制备高氯酸钾的一种流程如图:
下列说法错误的是( )
A.“电解”生成气体的主要成分为H
2
B.“高温分解”反应中氧化剂和还原剂的物质的量之比为3∶1
C.本实验条件下,KClO 在水中的溶解度比NaClO 的小
4 4
D.母液经分离、提纯可制得食盐
答案 B
解析 “电解”过程中,由水电离出的H+在阴极得电子生成H ,A项正确;由流程信息知,
2
NaClO 高温分解生成NaCl和NaClO ,由得失电子守恒知氧化剂和还原剂的物质的量之比
3 4
为1∶3,B项错误;“转化”步骤中,NaClO 中加入KCl溶液后经系列操作得到KClO ,
4 4
推知本实验条件下,KClO 在水中的溶解度比NaClO 的小,C项正确;母液中溶质的主要
4 4
成分为NaCl,D项正确。
7.硫元素的几种化合物存在下列转化关系:
浓HSO ――→SO ――→NaSO 溶液――→NaSO――→S
2 4 2 2 3 2 2 3
下列判断不正确的是( )
A.反应①中浓硫酸作氧化剂
B.反应②表明SO 有酸性氧化物的性质
2
C.反应③的原子利用率是100%
D.反应④稀HSO 作还原剂
2 4
答案 D
解析 Cu与浓硫酸反应:Cu+2HSO (浓)=====CuSO +SO ↑+2HO,SO 为酸性氧化物,
2 4 4 2 2 2
发生反应②:SO +2NaOH===NaSO +HO,NaSO 与 S 发生反应③:NaSO +
2 2 3 2 2 3 2 3
S===NaSO ,NaSO 与稀硫酸发生反应④:NaSO +HSO ===NaSO +S↓+SO ↑+
2 2 3 2 2 3 2 2 3 2 4 2 4 2
HO,据此分析。
2考点二 氮族元素知识拓展(P、As)
1.磷及其重要化合物
(1)磷有多种同素异形体,常见的有白磷、红磷和黑磷,磷的单质都具有很强的还原性。
(2)P O 是白色粉末状固体,具有很强的吸水性,是常见的酸性干燥剂。
2 5
PO 是磷酸的酸酐,与热水反应生成磷酸,化学方程式为PO+3HO=====2HPO 。
2 5 2 5 2 3 4
(3)常见磷的含氧酸有磷酸(H PO )、亚磷酸(H PO )、次磷酸(H PO )。
3 4 3 3 3 2
①三种酸分别为三元酸、二元酸、一元酸。
②亚磷酸与NaOH反应可能生成盐的化学式为NaHPO 、 NaH PO 。
2 3 2 3
2.砷及其化合物
1.已知:次磷酸(H PO )的电离常数K(H PO )=5.9×10-2。碱性条件下,次磷酸盐可与硝
3 2 a 3 2
酸银溶液反应进行化学镀银。下列说法不正确的是( )
A.次磷酸具有强还原性
B.次磷酸溶液中通入足量氯气,pH增大
C.次磷酸钠溶液滴入酚酞变红色
D.化学镀银的反应为HPO+4Ag++6OH-===PO+4Ag↓+4HO
2 2
答案 B
解析 HPO 中P显+1价,具有还原性,A项正确;HPO 具有还原性,通入足量氯气发生
3 2 3 2
反应:HPO +2Cl +2HO===HPO +4HCl,故溶液pH减小,B项错误;根据K(H PO )=
3 2 2 2 3 4 a 3 2
5.9×10-2可知,HPO 为一元弱酸,故次磷酸钠溶液中HPO水解使溶液显碱性,酚酞遇碱
3 2 2
变红,C项正确;根据“碱性条件下,次磷酸盐可与硝酸银溶液反应进行化学镀银”可知,
该反应中硝酸银溶液中的Ag+得到电子被还原成Ag,HPO失去电子被氧化成PO,该反应
2
在碱性条件下进行,所以还有OH-参与反应,D项正确。
2.砷(As)及其化合物与生产、生活密切相关,广泛应用在杀虫剂以及药物中。回答下列问
题:
(1)砷是第四周期第ⅤA族元素。下列关于第ⅤA族元素及其化合物的说法不正确的是
______(填字母)。
a.沸点:PH <NH
3 3b.酸性:HNO>HAsO
3 3 4
c.As的氧化物的水化物是强碱
d.形成的简单离子半径随着原子序数递增而增大
(2)工业生产中常用“古氏试砷法”检验微量砷,其反应原理如下:
①将含砷化合物转化为具有极强还原性的AsH 。
3
②AsH 与 AgNO 溶液反应产生 As O 与另一种固体,该反应的离子方程式:
3 3 2 3
________________________________________________________________________
________________________________________________________________________。
(3)砷及其化合物几乎都有毒,通常+3价砷化合物的毒性强于+5价砷化合物。海产品中含
有微量+5价砷化合物,食用海鲜后不能马上进食水果的原因是______________________
_____________________________________________________________________________。
(4)砷酸(H AsO )可用于制造杀虫剂、药物。As O 溶于稀硝酸中可得砷酸,此反应的化学方
3 4 2 3
程式:________________________________________________________________________
________________________________________________________________________。
答案 (1)c
(2)2AsH+12Ag++3HO===As O+12H++12Ag↓
3 2 2 3
(3)水果中富含还原性物质(如维生素C等),能把+5价砷化合物还原为毒性更大的+3价砷
化合物
(4)3As O+4HNO+7HO===6HAsO +4NO↑
2 3 3 2 3 4
预测陌生无机物性质的三个角度
(1)依据周期的位置预测氢化物的稳定性,最高价含氧酸的强弱。
(2)依据化合物中元素的化合价预测氧化性及还原性。
(3)依据物质的类别预测物质与酸、碱的反应。
考点三 氧族元素知识拓展(Se、Te)
Se、Te及其化合物
(1)硒及其化合物的性质
①单质硒及其氢化物在空气中燃烧可得到SeO。
2
②SeO 的氧化性比 SO 强,属于中等强度的氧化剂,可氧化 HS、NH 等:SeO +
2 2 2 3 2
2HS===Se+2S+2HO、3SeO+4NH ===3Se+2N+6HO。
2 2 2 3 2 2
③亚硒酸可作氧化剂,能氧化SO :HSeO +2SO +HO===2HSO +Se,但遇到强氧化剂
2 2 3 2 2 2 4
时表现还原性,可被氧化成硒酸:HSeO+Cl+HO===HSeO+2HCl。
2 3 2 2 2 4(2)碲及其化合物的性质
①碲在空气或纯氧中燃烧生成TeO 。
2
②TeO 是不挥发的白色固体,微溶于水,易溶于强酸、强碱,如TeO +2NaOH===NaTeO
2 2 2 3
+HO。
2
③TeO (H TeO )具有氧化性和还原性
2 2 3
HTeO +2SO +HO===2HSO +Te
2 3 2 2 2 4
HTeO +Cl+HO===HTeO +2HCl
2 3 2 2 2 4
(3)硒和碲的化合物均有毒。
1.为防止废弃的硒单质(Se)造成环境污染,通常用浓硫酸将其转化成二氧化硒(SeO ),再用
2
KI溶液处理后回收Se。发生的反应为①Se+2HSO (浓)===2SO ↑+SeO +2HO;②SeO
2 4 2 2 2 2
+4KI+4HNO===4KNO+Se+2I+2HO,下列说法错误的是( )
3 3 2 2
A.①中SO 是还原产物,SeO 是氧化产物
2 2
B.②中KI是还原剂,SeO 是氧化剂
2
C.每生成0.4 mol I 共转移1.2 mol电子
2
D.氧化性由强到弱的顺序是HSO (浓)>SeO >HNO
2 4 2 3
答案 C
解析 反应②中,生成2 mol碘单质,转移4 mol电子,则每生成0.4 mol I 共转移0.8 mol
2
电子,故C错误;在同一反应中氧化剂的氧化性大于氧化产物的氧化性,反应①中氧化性:
HSO (浓)>SeO ,反应②中硝酸既不是氧化剂也不是还原剂,说明氧化性:SeO>HNO ,故
2 4 2 2 3
D正确。
2.碲(Te)广泛用于彩色玻璃和陶瓷。工业上用精炼铜的阳极泥(含有质量分数为 8%的
TeO 、少量Ag、Au)为原料制备单质碲的一种工艺流程如下(已知TeO 微溶于水,易溶于强
2 2
酸和强碱),下列有关说法不正确的是( )
A.将阳极泥研磨、反应适当加热都有利于提高“碱浸”的速率和效率
B.“碱浸”时发生主要反应的离子方程式为TeO +2OH-===TeO+HO
2 2
C.“沉碲”时为使碲元素沉淀充分,应加入过量的硫酸
D.若提取过程碲元素的回收率为90%,则处理1 kg这种阳极泥最少需通入标准状况下SO
2
20.16 L
答案 C
解析 由已知信息可知,TeO 微溶于水,易溶于强酸和强碱,是两性氧化物,与氢氧化钠
2发生类似氧化铝与氢氧化钠的反应,生成TeO,离子方程式为TeO +2OH-===TeO+HO,
2 2
故B正确;在沉碲的过程中,硫酸若过量,可能导致TeO 的溶解,造成产品的损失,故C
2
错误;1 kg阳极泥中含有TeO 的质量为1 000 g×8%=80 g,碲元素的回收率为90%,则有
2
80 g×90%=72 g的TeO 被还原,根据关系式:TeO ~2SO ,V(SO )=×2×
2 2 2 2
22.4 L ·mol-1=20.16 L,故D正确。
1.(2021·河北,10)关于非金属含氧酸及其盐的性质,下列说法正确的是( )
A.浓HSO 具有强吸水性,能吸收糖类化合物中的水分并使其炭化
2 4
B.NaClO、KClO 等氯的含氧酸盐的氧化性会随溶液的pH减小而增强
3
C.加热NaI与浓HPO 混合物可制备HI,说明HPO 比HI酸性强
3 4 3 4
D.浓HNO 和稀HNO 与Cu反应的还原产物分别为NO 和NO,故稀HNO 氧化性更强
3 3 2 3
答案 B
解析 浓硫酸能使蔗糖炭化,体现的是脱水性,而不是吸水性,A错误;NaClO在水溶液中
会发生水解,离子方程式为ClO-+HOHClO+OH-,pH减小,酸性增强,会促使平衡
2
向正反应方向移动,生成氧化性更强的HClO,ClO在酸性条件下可生成具有强氧化性的氯
气、二氧化氯等气体,增强氧化能力,B正确;HI的沸点低、易挥发,加热NaI与浓HPO
3 4
混合物发生反应生成HI利用的是高沸点酸制备低沸点酸的原理,C错误;相同条件下根据
铜与浓硝酸、稀硝酸反应的剧烈程度可知,浓硝酸的氧化性大于稀硝酸的氧化性,D错误。
2.(2021·浙江1月选考,12)下列“类比”合理的是( )
A.Na与HO反应生成NaOH和H,则Fe与HO反应生成Fe(OH) 和H
2 2 2 3 2
B.NaClO溶液与CO 反应生成NaHCO 和HClO,则NaClO溶液与SO 反应生成NaHSO
2 3 2 3
和HClO
C.NaN与盐酸反应生成NaCl和NH Cl,则MgN 与盐酸反应生成MgCl 和NH Cl
3 4 3 2 2 4
D.NaOH溶液与少量AgNO 溶液反应生成Ag O和NaNO ,则氨水与少量AgNO 溶液反应
3 2 3 3
生成Ag O和NH NO
2 4 3
答案 C
解析 Na与水反应生成NaOH和H ,Fe与冷水、热水都不反应,Fe与水蒸气反应生成
2
Fe O 和H ,A不合理;NaClO具有强氧化性,SO 具有较强的还原性,NaClO溶液与SO
3 4 2 2 2
发生氧化还原反应时SO 被氧化成SO,ClO-被还原成Cl-,B不合理;NaN与盐酸反应生
2 3
成 NaCl 和 NH Cl:NaN+4HCl===3NaCl+NH Cl,MgN 与盐酸反应生成 MgCl 和
4 3 4 3 2 2
NH Cl:MgN +8HCl===3MgCl +2NH Cl,C 合理;氨水与少量 AgNO 反应生成
4 3 2 2 4 3
[Ag(NH)]+:Ag++2NH ·H O===[Ag(NH)]++2HO,D不合理。
3 2 3 2 3 2 2
3.(2021·河北,6)BiOCl是一种具有珍珠光泽的材料,利用金属Bi制备BiOCl的工艺流程如图:
下列说法错误的是( )
A.酸浸工序中分次加入稀HNO 可降低反应剧烈程度
3
B.转化工序中加入稀HCl可抑制生成BiONO
3
C.水解工序中加入少量CHCOONa(s)可提高Bi3+水解程度
3
D.水解工序中加入少量NH NO (s)有利于BiOCl的生成
4 3
答案 D
解析 硝酸为强氧化剂,可与金属铋反应,酸浸工序中分次加入稀HNO ,反应物硝酸的量
3
减少,可降低反应剧烈程度,A正确;金属铋与硝酸反应生成的硝酸铋会发生水解反应生成
BiONO ,水解的离子方程式为 Bi3++NO+HOBiONO +2H+,转化工序中加入稀
3 2 3
HCl,使氢离子浓度增大,根据勒夏特列原理,硝酸铋水解平衡左移,可抑制生成
BiONO ,B正确;氯化铋水解生成BiOCl的离子方程式为Bi3++Cl-+HOBiOCl+2H
3 2
+,水解工序中加入少量CHCOONa(s),醋酸根会结合氢离子生成弱电解质醋酸,使氢离子
3
浓度减小,根据勒夏特列原理,氯化铋水解平衡右移,促进Bi3+水解,C正确;水解工序中
加入少量NH NO (s),铵根离子水解生成氢离子,使氢离子浓度增大,根据勒夏特列原理,
4 3
氯化铋水解平衡左移,不利于生成BiOCl,且部分铋离子与硝酸根、水也会发生反应,也不
利于生成BiOCl,D错误。
课时精练
1.下列方程式中,不能正确表达反应颜色变化的是( )
A.将KSCN溶液滴入FeCl 溶液中,溶液变成红色:Fe3++3SCN-Fe(SCN)
3 3
B.淀粉-KI溶液中通入氯气,溶液变为蓝色:2I-+Cl===I+2Cl-
2 2
C.将集满NO 气体的烧瓶放到冰水浴中,烧瓶内气体红棕色变浅:2NO ===2NO+O
2 2 2
D.将金属钠投入硫酸铜溶液中,得到蓝色沉淀:2Na+2HO+Cu2+===Cu(OH) ↓+2Na+
2 2
+H↑
2
答案 C
解析 Fe3+和SCN-结合生成红色的Fe(SCN) ,A项正确;氧化性:Cl >I ,故氯气可将I-
3 2 2
转化为I ,淀粉遇I 呈蓝色,B项正确;NO 与NO 存在转化关系:2NO (g)NO(g)
2 2 2 2 4 2 2 4
ΔH<0,放入冰水浴中,温度降低促使平衡向正反应方向移动,烧瓶中颜色变浅,C项错误;
金属钠投入溶液中,先和水反应生成H 和NaOH,NaOH再与硫酸铜反应生成蓝色絮状的
2
Cu(OH) 沉淀,D项正确。
22.下列有关KHSO 的表述不正确的是( )
4
A.它与Ba(OH) 作用一定生成白色沉淀
2
B.它电解往往生成O 和KSO
2 2 2 8
C.它与Y作用产生有刺激性气味的气体(Y是由相同的四种元素组成的盐,溶液也呈酸性,
但弱于KHSO)
4
D.镁能与它的溶液反应
答案 B
解析 KHSO 电离出的SO与Ba(OH) 电离出的Ba2+反应生成BaSO 白色沉淀,A项正确;
4 2 4
电 解 KHSO , 发 生 氧 化 还 原 反 应 , 若 生 成 物 为 O 和 KSO(S O 的 结 构 为
4 2 2 2 8 2
),则反应过程中只有O的化合价升高,没有元素化合价降低,
不符合得失电子守恒原则,B项错误;由“Y是由相同的四种元素组成的盐,溶液也呈酸性,
但弱于KHSO”可知,Y是KHSO ,发生反应的化学方程式为KHSO +KHSO===KSO +
4 3 4 3 2 4
SO ↑+HO,C项正确;KHSO 在溶液中完全电离为K+、H+和SO,其溶液的酸性与等浓
2 2 4
度的一元强酸相当,可与镁反应放出氢气,D项正确。
3.磷化铝(AlP,熔点:2 000 ℃)通常是作为一种广谱性熏蒸杀虫剂,主要用于熏杀粮食中
的储粮害虫等,下列有关说法正确的是( )
A.AlP属于分子晶体
B.起熏杀作用的物质通常是Al(OH)
3
C.AlP能水解或与稀硫酸作用,且均产生一种无毒气体
D.常用铝与红磷在一定条件下化合制备AlP
答案 D
解析 AlP的熔点为2 000 ℃,比较高,属于共价晶体,A项错误;AlP可发生水解:AlP+
3HO===Al(OH) ↓+PH ↑,Al(OH) 没有氧化性,不能熏杀害虫,PH 有剧毒,可熏杀害虫,
2 3 3 3 3
B项错误;AlP与稀硫酸发生反应:2AlP+3HSO ===Al (SO )+2PH ↑,AlP水解或与稀硫
2 4 2 4 3 3
酸作用均可产生有毒气体PH ,C项错误;红磷和铝粉烧制可得到磷化铝,该反应为化合反
3
应,D项正确。
4.白色固体NaSO 常用于织物的漂白,也能将污水中的某些重金属离子还原为单质除去。
2 2 4
下列关于NaSO 的说法不正确的是( )
2 2 4
A.可以使品红溶液褪色
B.其溶液可用作分析化学中的吸氧剂
C.其溶液可以和Cl 反应,但不能和AgNO 溶液反应
2 3
D.已知隔绝空气加热NaSO 分解可生成SO ,则其残余固体产物中可能有NaSO
2 2 4 2 2 2 3答案 C
解析 NaSO 常用于织物的漂白,故其具有漂白性,能使品红溶液褪色,A项正确;由
2 2 4
NaSO 能将污水中的某些重金属离子还原为单质除去可知,NaSO 具有还原性,易吸收氧
2 2 4 2 2 4
气而被氧化,故可作分析化学中的吸氧剂,B项正确;NaSO 溶液具有还原性,Cl 、
2 2 4 2
AgNO 溶液均具有氧化性,故NaSO 与Cl 、AgNO 溶液均可发生氧化还原反应,C项错
3 2 2 4 2 3
误;由“隔绝空气加热NaSO 分解可生成SO ”可知,S的化合价由+3升至+4,则一定
2 2 4 2
有元素化合价降低的产物,而NaSO 中S显+2价,故NaSO 分解残余固体产物中可能有
2 2 3 2 2 4
NaSO,D项正确。
2 2 3
5.汽车尾气的治理是减轻空气污染的有效途径。科学家研究发现 TiO 的混凝土或沥青可以
2
适度消除汽车尾气中的氮氧化物,其原理如下。下列关于“消除”过程的叙述错误的是(
)
A.部分光能转变为化学能
B.1 mol O比1 mol·OH多9N 个电子(N 为阿伏加德罗常数)
A A
C.使用纳米TiO,产生的光生电子和空穴更多,NO 消除效率更高
2 x
D.消除总反应为4NO+(5-2x)O +2HO=====4HNO
x 2 2 3
答案 B
解析 含TiO 的混凝土或沥青可以部分消除汽车尾气中的氮氧化物,在 TiO 催化作用下,
2 2
紫外线提供能量,发生反应4NO+(5-2x)O +2HO=====4HNO ,纳米TiO 与紫外线接触
x 2 2 3 2
面积更大,反应更充分,反应速率更快,由此分析解答。1 mol O的电子的物质的量为17
mol;而1 mol羟基含有电子的物质的量为9 mol,所以1 mol O比1 mol·OH多8N 个电子,
A
故B错误;纳米TiO 与紫外线接触面积更大,反应更充分,反应速率更快,NO 消除效率
2 x
更 高 , 故 C 正 确 ; 由 上 述 分 析 过 程 可 知 消 除 总 反 应 为 4NO + (5 - 2x)O +
x 2
2HO=====4HNO,故D正确。
2 3
6.(2022·朝阳区模拟)漂白粉和漂粉精是常用的消毒清洁用品,有效成分均为Ca(ClO) ,相
2
应的生产流程如图所示。下列说法不正确的是( )
A.①中阳极的电极反应式为2Cl--2e-===Cl↑
2B.②中反应的化学方程式为2Cl+2Ca(OH) ===Ca(ClO) +CaCl +2HO
2 2 2 2 2
C.上述过程涉及氧化还原反应、化合反应、复分解反应
D.制备漂粉精过程中,Cl 转化为Ca(ClO) 时,Cl的原子利用率为100%
2 2
答案 D
解析 ①②③为氧化还原反应、④为化合反应、⑤为复分解反应,故C正确;漂粉精是常
用的消毒清洁用品,有效成分为Ca(ClO) ,CaCl 是副产物,Cl的原子利用率小于100%,
2 2
故D错误。
7.铋(Bi)位于元素周期表中第ⅤA族。铋酸钠(NaBiO)为姜黄色固体,不溶于冷水,在空
3
气中会逐渐分解,固体产物为氧化铋(Bi O)和氢氧化钠。下列推断不合理的是( )
2 3
A.铋的+3价比较稳定
B.可以用BiO检验溶液中是否有Na+
C.铋酸钠在空气中分解有气态产物生成
D.铋酸钠在酸性条件下可以氧化Mn2+,酸化试剂可用盐酸
答案 D
解析 铋酸钠(NaBiO)在空气中分解得到氧化铋(Bi O),BiO 中的Bi显+3价,则铋的+3
3 2 3 2 3
价比较稳定,A项正确;根据“铋酸钠(NaBiO)为姜黄色固体,不溶于冷水”可知,NaBiO
3 3
是姜黄色沉淀,故可用BiO检验溶液中的Na+,若产生姜黄色沉淀,则溶液中含有Na+,B
项正确;铋酸钠(NaBiO)在空气中分解:HO+2NaBiO===2NaOH+BiO+O↑,C项正确;
3 2 3 2 3 2
NaBiO 具有强氧化性,可将盐酸中的Cl-氧化为Cl,故酸化试剂不可选用盐酸,D项错误。
3 2
8.(2022·辽宁高三模拟)以黄铁矿(主要成分为FeS)为原料生产硫酸,应将产出的炉渣和尾
2
气进行资源化综合利用,减轻对环境的污染,其中一种流程如图所示。下列说法错误的是(
)
A.黄铁矿中的FeS 在煅烧过程中作还原剂
2
B.欲得到更纯的NaHSO,反应①应通入过量的SO 气体
3 2
C.还原铁粉用盐酸溶解后,可用KMnO 溶液滴定法来测定其纯度
4
D.加热NaHSO 制备NaSO 的化学方程式为2NaHSO=====NaSO+HO
3 2 2 5 3 2 2 5 2
答案 C
解析 黄铁矿中的FeS 在煅烧过程中Fe元素的化合价由+2价升至+3价,S元素的化合价
2
由-1价升至+4价,作还原剂,A正确;通入过量二氧化硫保证碱反应完全,得到更纯的
NaHSO ,B正确;盐酸也能与高锰酸钾溶液反应,不能用KMnO 溶液滴定法来测定还原铁
3 4
粉的纯度,C错误。
9.硒(Se)、碲(Te)为第ⅥA族元素,是当今高新技术新材料的主要成分之一,电解精炼铜的阳极泥主要成分为Cu Te、Ag Se和少量金属单质及其他化合物,工业上从其中回收碲、硒
2 2
的一种工艺流程如下:
已知:
Ⅰ.Se 单质难溶于水。TeO 微溶于水,易溶于较浓的强酸和强碱;
2
Ⅱ.元素碲在溶液中主要以Te4+、TeO、HTeO等形式存在;
Ⅲ.25 ℃时,亚碲酸(H TeO )的K =1×10-3,K =2×10-8。
2 3 a1 a2
(1)Se的氢化物的电子式是________________________________________________。
0.1 mol·L-1的HTeO 电离度(当弱电解质在溶液里达到电离平衡时,溶液中已经电离的电
2 3
解质分子数占原来总分子数的百分数叫做电离度) 约为______________。
(2) 加入浓硫酸焙烧前常将阳极泥中大块颗粒先粉碎,其目的是________________。
(3)SeO 与SO 在冷却后通入水中发生反应的化学方程式:____________________
2 2
________________________________________________________________________。
反应后分离出Se单质的操作①为__________________________________________________
________________________________________________________________________(填操作
名称)。
(4)焙砂中碲以TeO 形式存在,与足量NaOH溶液反应后得到的溶液①,其溶质的主要成分
2
为________________________________________________________________________
________________________________________________________________________(填化学
式,过量的NaOH除外)。
工业上也可以通过电解溶液①得到单质碲。已知电解时的电极均为石墨,则阴极的电极反应
式为________________________________________________________________________
________________________________________________________________________。
(5)向溶液①中加入硫酸时控制溶液的pH为4.5~5.0,生成TeO 沉淀,如果HSO 过量,将
2 2 4
导致碲的回收率________(填“偏高”“偏低”或“无影响”)。
(6)将纯净的TeO 先溶于盐酸得到四氯化碲,再将SO 通入溶液中得到Te单质,请写出由四
2 2
氯化碲得到Te单质的离子方程式:________________________________________
________________________________________________________________________。
(7)上述流程中可循环利用的物质是_________________________________________
(填化学式)。
答案 (1) 10%
(2)增大接触面积,加快反应速率
(3)SeO +2SO +2HO===2HSO +Se↓ 过滤
2 2 2 2 4
(4)Na TeO TeO+3HO+4e-===Te+6OH- (5)偏低 (6)Te4++2SO +4HO===Te↓+8H
2 3 2 2 2++2SO (7)H SO 、HCl
2 4
解析 (1)Se与O属于同主族元素,故Se的氢化物的电子式为 。设电离的亚碲
酸为x mol·L-1,亚碲酸(H TeO )的K =1×10-3=,解得x≈0.01,则0.1 mol·
2 3 a1
L-1的HTeO 电离度为×100%=10%。
2 3
(2)加入浓硫酸焙烧前常将阳极泥中大块颗粒先粉碎,可以增大接触面积,加快反应速率。
(3)根据流程图,SeO 与SO 在冷却后通入水中发生反应生成Se,反应的化学方程式为SeO
2 2 2
+2SO +2HO===2HSO +Se↓,Se单质难溶于水,反应后分离出Se单质可以通过过滤分
2 2 2 4
离。
(4)TeO 微溶于水,易溶于较浓的强酸和强碱,焙砂中碲以 TeO 的形式存在,与足量NaOH
2 2
溶液反应后得到的溶液①,其溶质的主要成分为NaTeO ,工业上也可以通过电解溶液①得
2 3
到单质碲,电解时的电极均为石墨,则阴极发生还原反应,TeO得到电子生成Te,电极反
应式为TeO+3HO+4e-===Te+6OH-。
2
(5)TeO 微溶于水,易溶于较浓的强酸和强碱。向溶液①中加入硫酸时控制溶液的pH为4.5
2
~5.0,生成TeO 沉淀,如果HSO 过量,将导致生成的TeO 沉淀偏少,碲的回收率偏低。
2 2 4 2
(6)将纯净的TeO 先溶于盐酸得到四氯化碲,再将SO 通入溶液中得到Te单质,二氧化硫被
2 2
氧化成硫酸,反应的离子方程式为Te4++2SO +4HO===Te↓+8H++2SO。
2 2
10.锡渣的主要成分是SnO,还含有少量Fe、Cu、Sb、Pb、As等元素的氧化物。可用下列
流程中的方法生产锡酸钠。
已知:①砷酸钡难溶于水,K [Ba (AsO)]=10-24
sp 3 4 2
②水碎液中溶质的主要成分为NaSnO 、NaAsO 、NaSbO 、NaPbO
2 3 3 4 3 4 2 2
(1)碱熔就是在锡渣中加NaOH焙烧,SnO转变为NaSnO ,SnO参加反应的化学方程式为
2 3
________________________________________________________________________
________________________________________________________________________。
(2)除杂1的目的是“除砷和铅”,加入硫化钠所发生反应的离子方程式为_____________;
若要使0.001 mol·L-1的AsO沉淀完全(一般认为离子浓度小于10-6 mol·L-1时即沉淀完全),
需等体积加入至少____________ mol·L-1的Ba(OH) 。
2
(3)除杂2中加入Sn粒的目的是___________________________________________
________________________________________________________________________。
(4)已知NaSnO ·3H O可溶于水,难溶于乙醇,加热至140 ℃时会失去结晶水,所以最后一
2 3 2
步从滤液中得到锡酸钠晶体的操作步骤为________________________________、过滤、用__________洗涤、__________。
(5)水碎渣中的铁元素主要以氧化物的形式存在,回收比较容易,而铜冶炼过程中的铜渣中
也有铁元素,但主要以硅酸亚铁的形式存在,回收方法更复杂:需先加CaO作置换剂,发
生钙铁置换反应:CaO+FeO·SiO CaO·SiO +FeO,在反应过程中,加CaO的同时还需
2 2
加入还原剂烟煤,则加入还原剂烟煤的作用是_____________________________________
________________________________________________________________________。
答案 (1)2SnO+4NaOH+O=====2NaSnO +2HO
2 2 3 2
(2)PbO+S2-+2HO===PbS↓+4OH- 0.001 7
2
(3)除去SbO(或除锑)
(4)在140 ℃以下加热蒸发(或蒸发浓缩、冷却结晶) 乙醇 低温干燥
(5)还原FeO以减少生成物,使钙铁置换反应向正反应方向移动
解析 (1)碱熔就是在锡渣中加NaOH焙烧,SnO转变为NaSnO ,在转化过程中,Sn由+2
2 3
价升高到+4价,应有氧化剂参与反应,NaOH不可能作氧化剂,则必有空气中的O 参与反
2
应,由此可写出SnO参加反应的化学方程式为2SnO+4NaOH+O=====2NaSnO +2HO。
2 2 3 2
(2)除杂1的目的是“除砷和铅”,加入的NaS与NaPbO 反应,生成PbS,由此可写出发
2 2 2
生反应的离子方程式:PbO+S2-+2HO===PbS↓+4OH-;若要使0.001 mol·L-1的AsO沉
2
淀完全(一般认为离子浓度小于10-6 mol·L-1时即沉淀完全),加入Ba(OH) 起两个作用,一
2
个是使AsO完全沉淀,由离子方程式:3Ba2++2AsO===Ba (AsO)↓可求出参加反应的
3 4 2
c(Ba2+)==0.001 5 mol·L-1;另一个是溶解在溶液中,使Ba (AsO) 达到沉淀溶解平衡,
1 3 4 2
c(Ba2+)= mol·L-1=10-4 mol·L-1,此为混合溶液中的
2
c(Ba2+),换算为原溶液中的浓度,则为2×10-4 mol·L-1;从而得出c(Ba2+)=0.001 5 mol·L
-1+2×10-4 mol·L-1=0.001 7 mol·L-1。(3)除杂2中加入Sn粒的目的是使NaSbO 转化为
3 4
沉淀,从溶液中除去。(4)最后一步从滤液中得到锡酸钠晶体的操作步骤为在 140 ℃以下加
热蒸发或蒸发浓缩、冷却结晶、过滤,为减少水洗时的溶解损失,应使用乙醇洗涤,最后再
低温干燥。(5)在反应过程中,加CaO的同时还需加入还原剂烟煤,作用是还原FeO,减少
生成物,使平衡正向移动。
11.高纯硝酸锶[Sr(NO)]可用于制造信号灯、光学玻璃等。工业级硝酸锶含硝酸钙、硝酸
3 2
钡等杂质,提纯流程如下:已知:①“滤液1”的主要溶质是Ca(NO );“滤渣1”的成分为Ba(NO )、Sr(NO);“滤
3 2 3 2 3 2
渣2”的主要成分为BaCrO(杂质不与硝酸反应)。②铬酸(H CrO)为弱酸。
4 2 4
(1)“酸浸”不能采用高温的原因是_________________________________________
________________________________________________________________________。
(2)相对于水洗,用浓HNO 洗涤的优点是___________________________________
3
________________________________________________________________________。
(3)“滤液2”中过量的HCrO 被NH 还原为Cr3+,同时放出无污染的气体,写出反应的离
2 4 2 4
子方程式:_____________________________________________________________
________________________________________________________________________。
(4)在溶液中存在以下沉淀溶解平衡:Cr(OH) (s)Cr3+(aq)+3OH-(aq),常温下,Cr(OH)
3 3
的溶度积K =1.0×10-32,当c(Cr3+)降至1.0×10-5 mol·L-1,认为Cr3+已经完全沉淀。现
sp
将还原后溶液的pH调至4,此时Cr3+是否沉淀完全并写出计算过程:__________________。
(5)已知Cr(OH) 类似Al(OH) ,还原后溶液的pH不能大于8的原因是____________________
3 3
________________________________________________________________________
(结合离子方程式说明理由)。
(6)为了测定“滤渣2”中BaCrO 的含量,进行以下实验:
4
m g“滤渣2”―――――→500 mL滤液――――→―――――――――→――→――→――→――→n g
①判断Ba2+完全沉淀的方法:____________________________________________
________________________________________________________________________。
②“滤渣2”中BaCrO 的质量分数为________________(用代数表示)。
4
答案 (1)避免浓HNO 挥发和分解
3
(2)减少Sr(NO) 溶解而造成的损失
3 2
(3)4H CrO+3NH+12H+===4Cr3++3N↑+16HO
2 4 2 4 2 2
(4)c(OH-)=10-10 mol·L-1时,c(Cr3+)= mol·L-1=1.0×10-2 mol·L-1>1.0×
10-5 mol·L-1,此时Cr3+没有沉淀完全
(5)pH大于8时,Cr(OH) 会溶解:Cr(OH) +OH-===CrO+2HO
3 3 2
(6)①静置,向上层清液中继续滴加NaSO 溶液,上层清液中无白色沉淀生成 ②×100%
2 4
解析 (2)根据同离子效应,硝酸锶在浓HNO 中比在水中溶解度小,用浓HNO 洗涤可减少
3 3
硝酸锶溶解而造成的损失。(3)“滤液2”中过量的HCrO 被NH 还原为Cr3+,同时产生一
2 4 2 4
种无污染的气体,为氮气,根据得失电子守恒和原子守恒,反应的离子方程式为 4HCrO +
2 43NH+12H+===4Cr3++3N↑+16HO。(5)已知Cr(OH) 类似Al(OH) ,Cr(OH) 在碱性溶液
2 4 2 2 3 3 3
中会发生反应Cr(OH) +OH-===CrO+2HO而溶解,所以还原后溶液的 pH不能大于8。
3 2
(6)①硝酸钡溶液和NaSO 溶液反应生成硫酸钡和硝酸钠,所以判断Ba2+完全沉淀的方法是
2 4
静置,向上层清液中继续滴加NaSO 溶液,上层清液中无白色沉淀生成。
2 4
②设“滤渣2”中BaCrO 的质量为x,
4
BaCrO ~ BaSO
4 4
253 233
x n g×5
=,解得x= g,所以“滤渣2”中BaCrO 的质量分数为×100%=×100%。
4