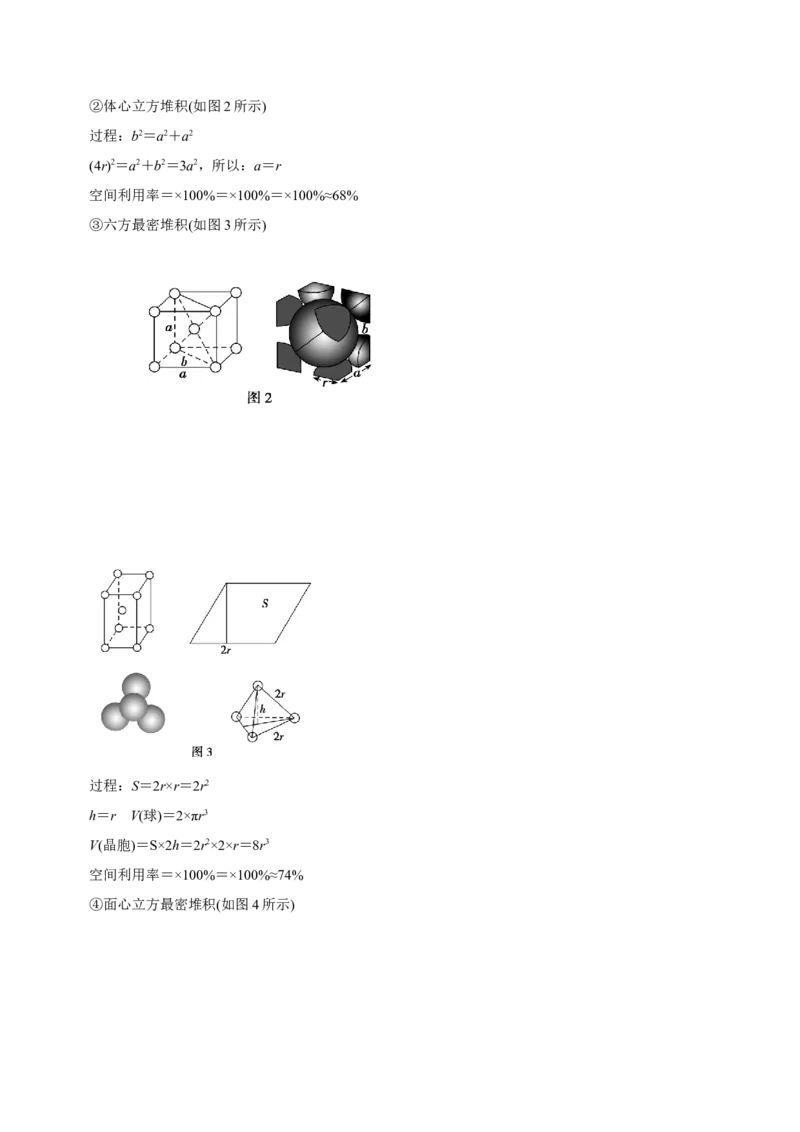
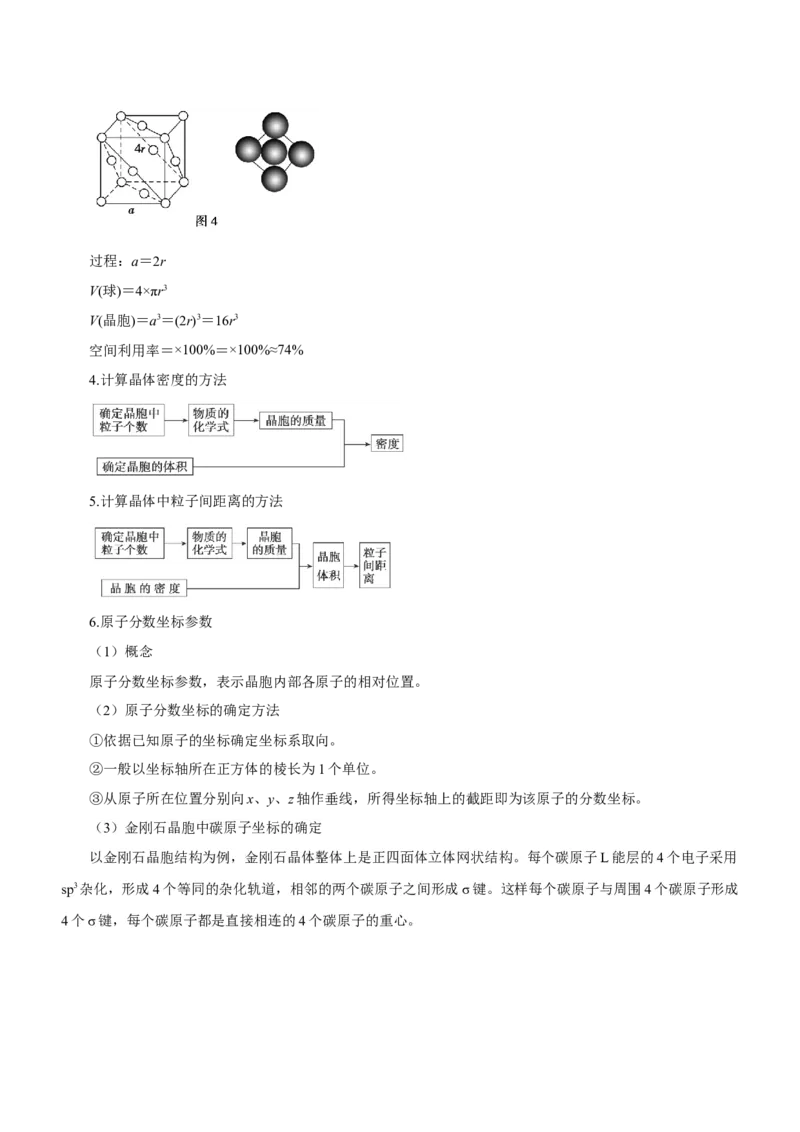
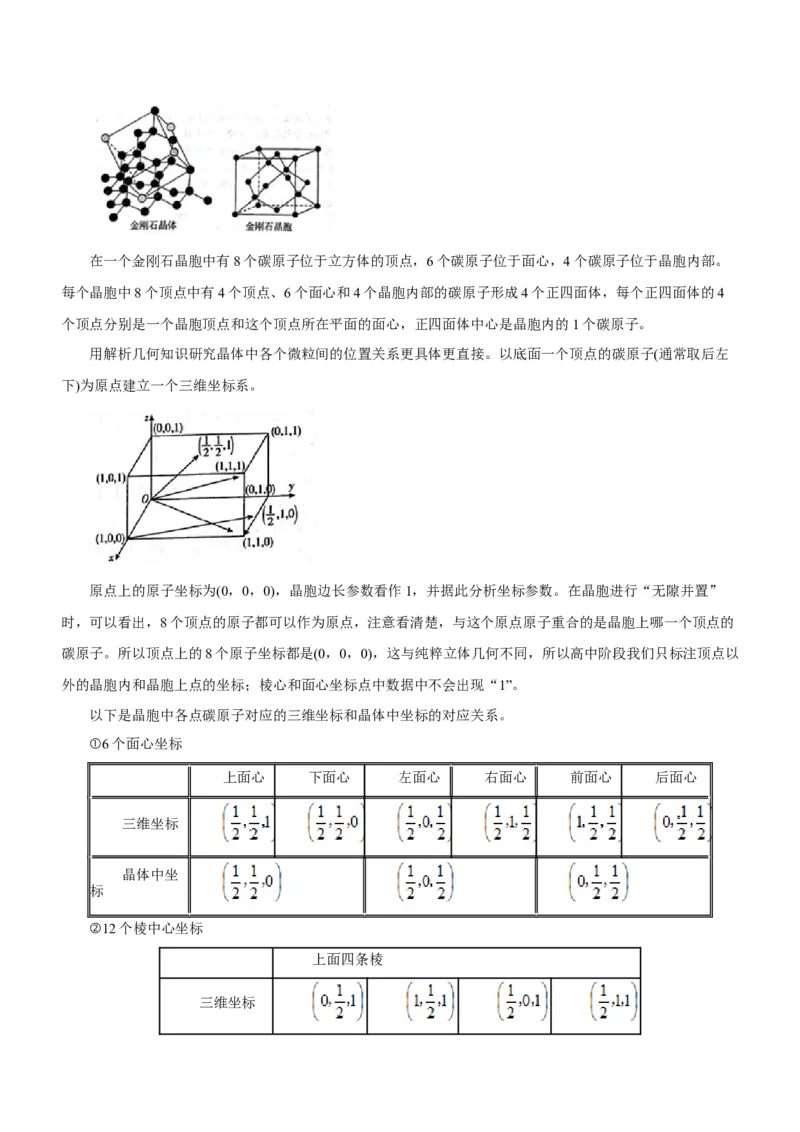
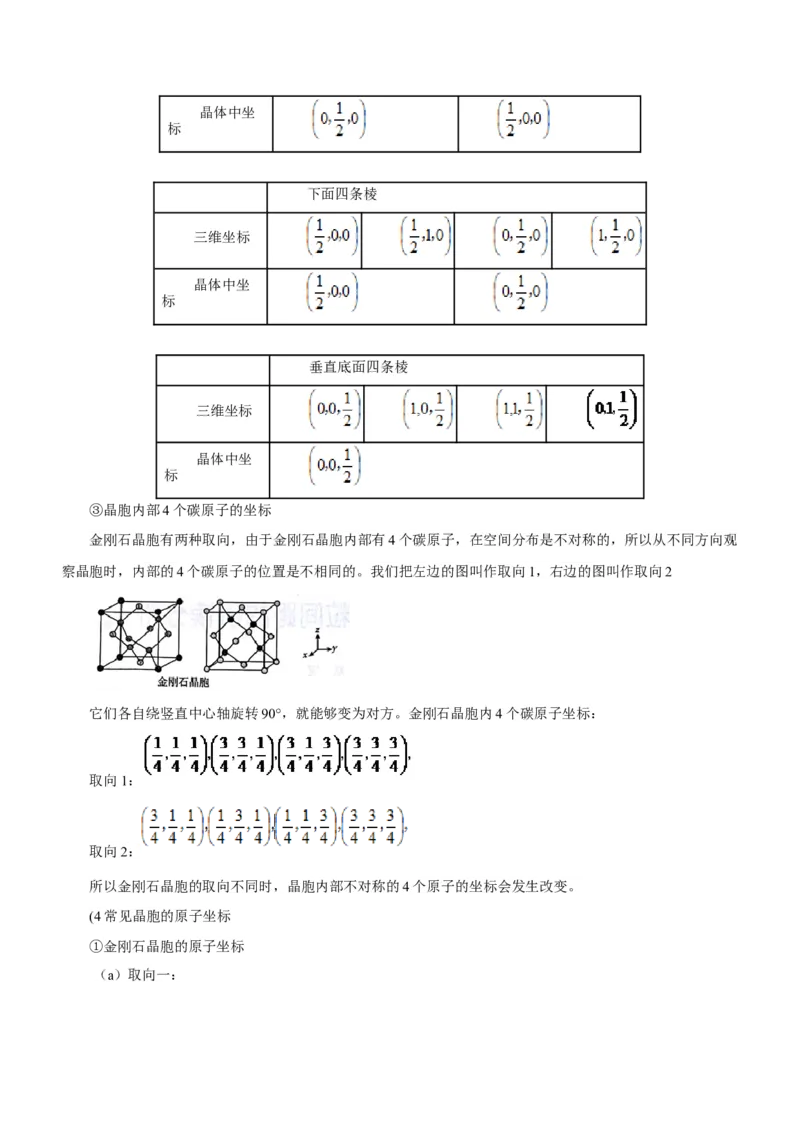
文档内容
专题 16 物质结构与性质综合题
稳定加创新是本专题的基本特点,命题采取结合新科技,新能源等社会热点为背景,命题的形式分为选择
题和填空题,原子的结构与性质、分子的结构与性质和晶体的结构与性质是命题的三大要点。从大题的构成来
看,给出一定的知识背景,然后设置成4—5个小题,每个小题考查一个知识要点是主要的命题模式,内容主
要考查基本概念,如电子排布式,轨道式,电离能,电负性,杂化方式以及空间构型等,也可联系有机考查有
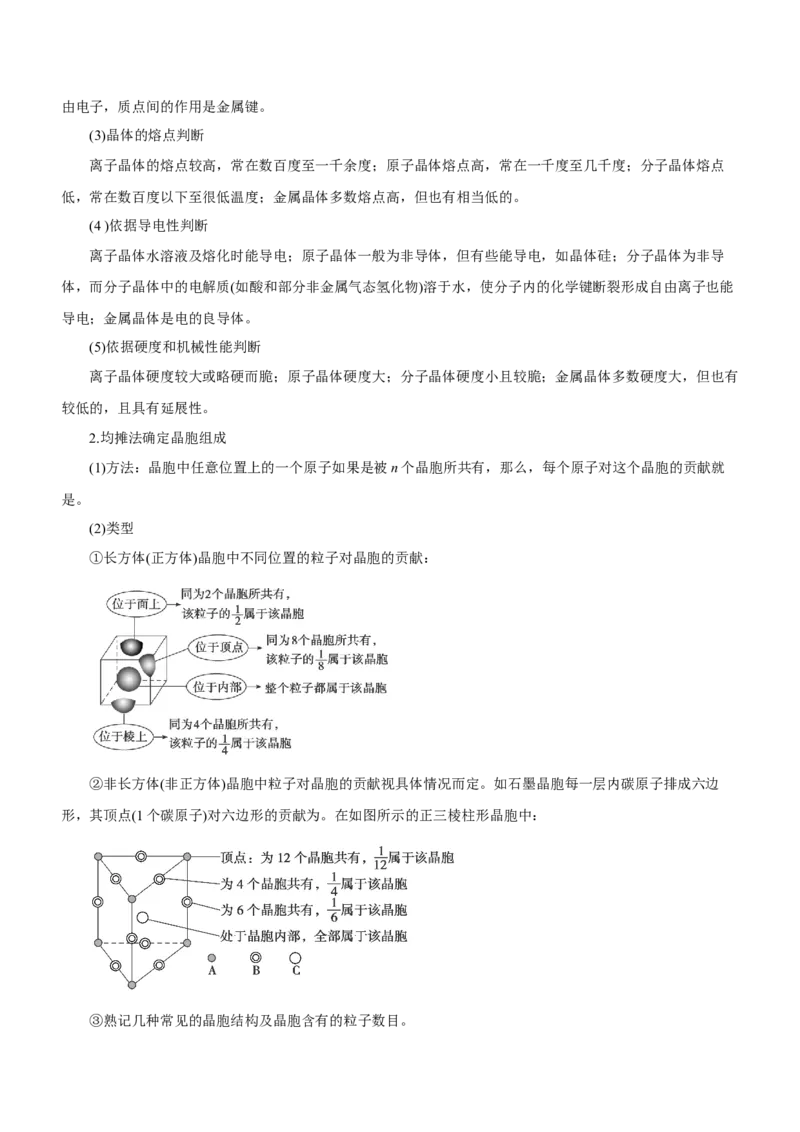
机物中C原子的杂化,联系数学几何知识考查晶体的计算等,一般利用均摊法考查晶胞中的原子个数,或者
考查晶体的化学式的书写、晶体类型的判断等,考查的抽象思维能力、逻辑思维能力;同时培养学生的分析和
推理能力。
高频考点一 原子结构与性质
1.核外电子排布
(1)核外电子排布规律
(2)原子结构示意图
(3)基态原子的核外电子排布原理
①能量最低原理:即电子尽可能地先占有能量低的轨道,然后进入能量高的轨道,使整个原子的能量处于
最低状态。如图为构造原理示意图,即基态原子核外电子在原子轨道上的排布顺序图:②泡利不相容原理
每个原子轨道里最多只能容纳2个电子,且自旋状态相反。
如2s轨道上的电子排布为 ,不能表示为 。
③洪特规则
当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据一个轨道,且自旋状态相同。
如2p3的电子排布为
,不能表示为 或
洪特规则特例:当能量相同的原子轨道在全满(p6、d10、f14)、半满(p3、d5、f7)和全空(p0、d0、f0)状态时,
体系的能量最低,如: Cr的电子排布式为1s22s22p63s23p63d54s1。
24
(4)表示基态原子核外电子排布的四种方法
表示方法 举例
电子排布式 Cr:1s22s22p63s23p63d54s1
简化表示式 Cu:[Ar]3d104s1
价电子排布式 Fe:3d64s2
电子排布图
(或轨道表示式) O:
5.第一电离能、电负性
(1)元素第一电离能的周期性变化规律。
一般 同一周期,随着原子序数的增加,元素的第一电离能呈现增大的趋势,稀有气体元素的第一电离能最
规律 大,碱金属元素的第一电离能最小;同一主族,随着电子层数的增加,元素的第一电离能逐渐减小
特殊 第一电离能的变化与元素原子的核外电子排布有关。通常情况下,当原子核外电子排布在能量相等的轨道上形成全空(p0、d0、f0)、半满(p3、d5、f7)和全满(p6、d10、f14)结构时,原子的能量较低,该元素
情况 具有较大的第一电离能。如同周期主族元素,第ⅡA族元素的原子最外层s能级全充满、ⅤA族元素
的原子最外层p能级半充满,比较稳定,所以其第一电离能大于同周期相邻的主族元素
(2)电负性大小判断。
规律 在周期表中,同周期主族元素电负性从左到右逐渐增大,同主族从上往下逐渐减小
常常应用化合价及物质类别判断电负性的大小,如O与Cl的电负性比较:①HClO中Cl为+1价、O
方法
为-2价,可知O的电负性大于Cl;②Al O 是离子化合物、AlCl 是共价化合物,可知O的电负性大于Cl
2 3 3
核心考点二 分子结构与性质
1.与分子结构有关的两种理论
(1)杂化轨道理论
①基本观点:杂化轨道成键满足原子轨道最大重叠原理;杂化轨道形成的共价键更加牢固。
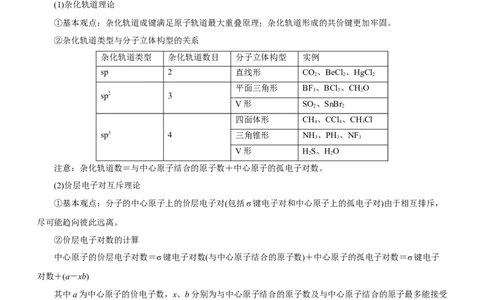
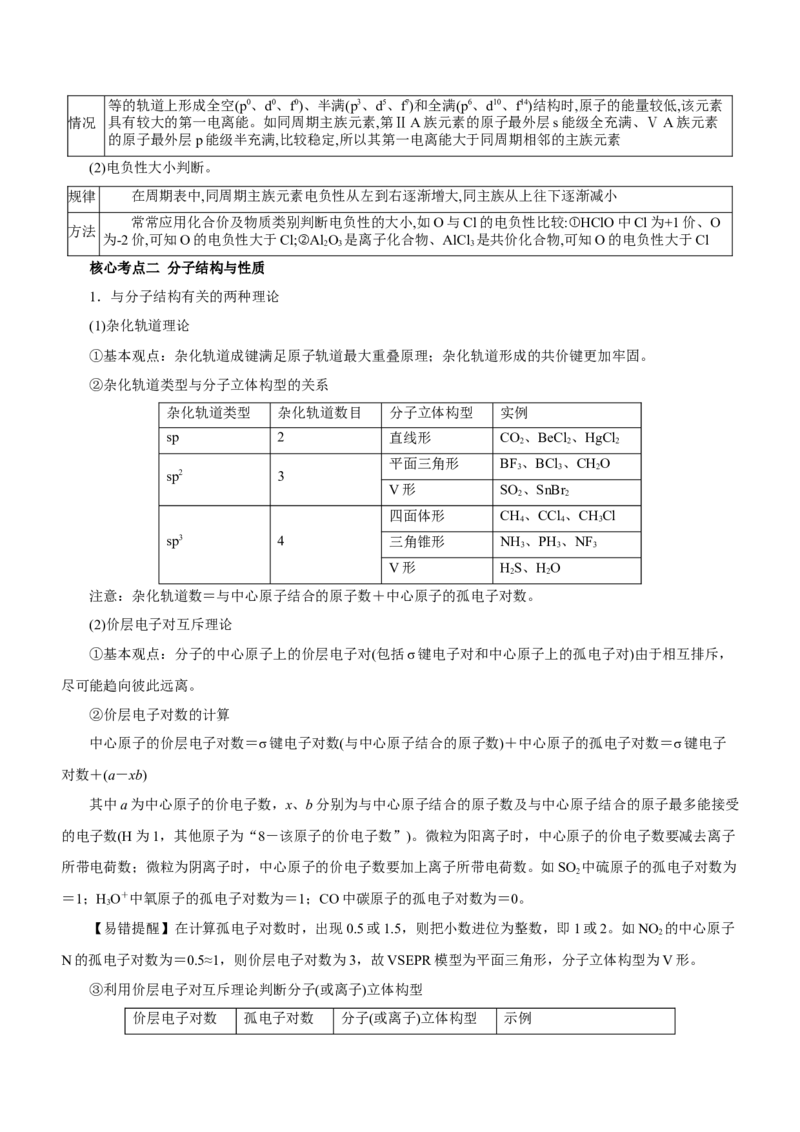
②杂化轨道类型与分子立体构型的关系
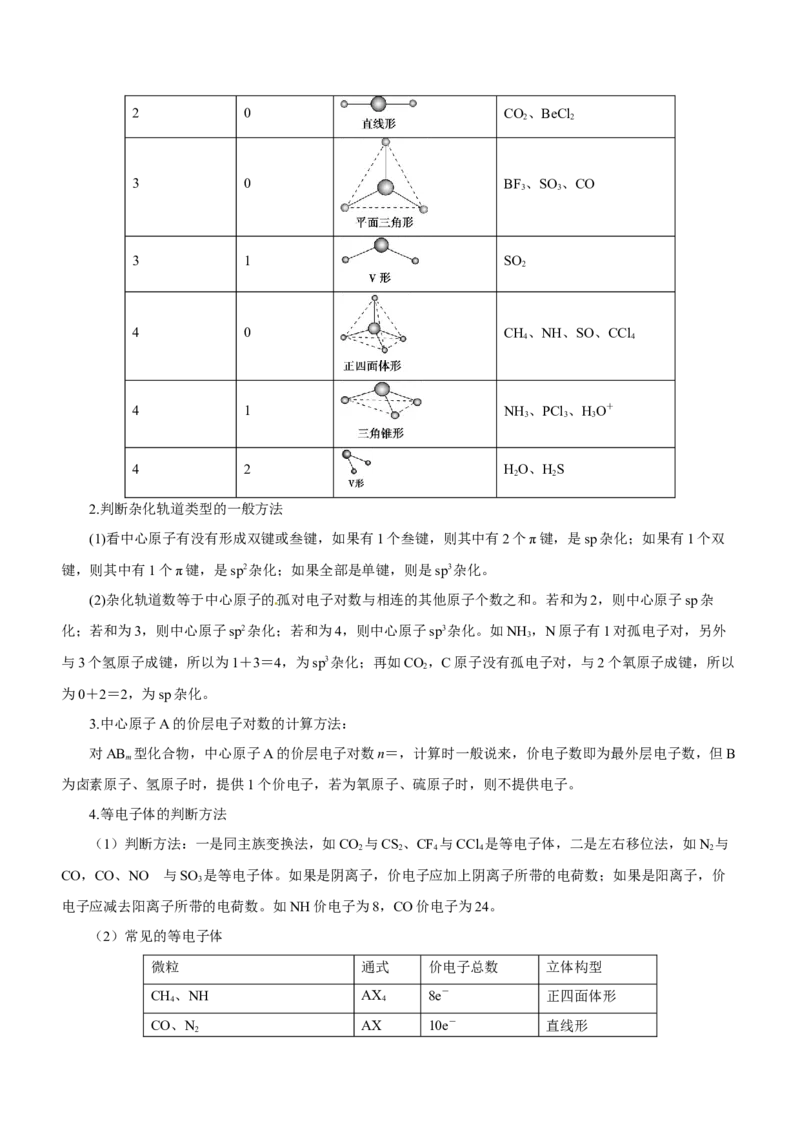
杂化轨道类型 杂化轨道数目 分子立体构型 实例
sp 2 直线形 CO、BeCl 、HgCl
2 2 2
平面三角形 BF、BCl 、CHO
3 3 2
sp2 3
V形 SO 、SnBr
2 2
四面体形 CH、CCl 、CHCl
4 4 3
sp3 4 三角锥形 NH 、PH 、NF
3 3 3
V形 HS、HO
2 2
注意:杂化轨道数=与中心原子结合的原子数+中心原子的孤电子对数。
(2)价层电子对互斥理论
①基本观点:分子的中心原子上的价层电子对(包括σ键电子对和中心原子上的孤电子对)由于相互排斥,
尽可能趋向彼此远离。
②价层电子对数的计算
中心原子的价层电子对数=σ键电子对数(与中心原子结合的原子数)+中心原子的孤电子对数=σ键电子
对数+(a-xb)
其中a为中心原子的价电子数,x、b分别为与中心原子结合的原子数及与中心原子结合的原子最多能接受
的电子数(H为1,其他原子为“8-该原子的价电子数”)。微粒为阳离子时,中心原子的价电子数要减去离子
所带电荷数;微粒为阴离子时,中心原子的价电子数要加上离子所带电荷数。如SO 中硫原子的孤电子对数为
2
=1;HO+中氧原子的孤电子对数为=1;CO中碳原子的孤电子对数为=0。
3
【易错提醒】在计算孤电子对数时,出现0.5或1.5,则把小数进位为整数,即1或2。如NO 的中心原子
2
N的孤电子对数为=0.5≈1,则价层电子对数为3,故VSEPR模型为平面三角形,分子立体构型为V形。
③利用价层电子对互斥理论判断分子(或离子)立体构型
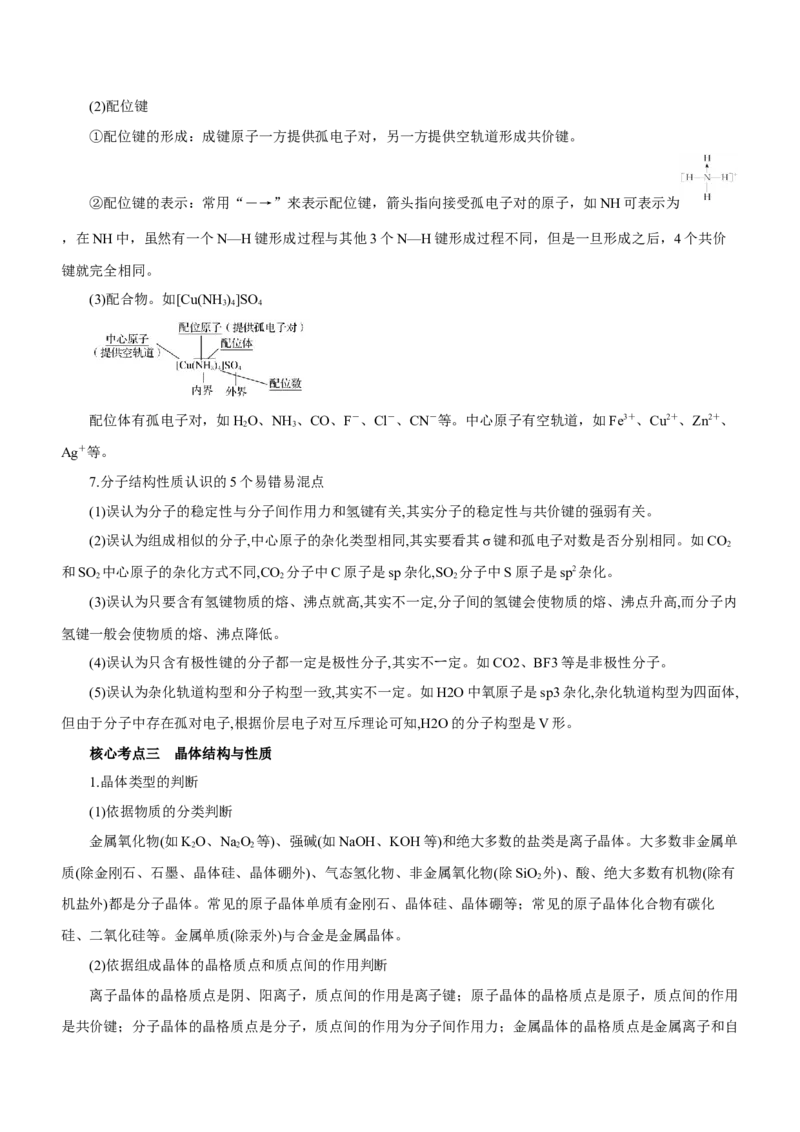
价层电子对数 孤电子对数 分子(或离子)立体构型 示例2 0 CO、BeCl
2 2
3 0 BF、SO 、CO
3 3
3 1 SO
2
4 0 CH、NH、SO、CCl
4 4
4 1 NH 、PCl 、HO+
3 3 3
4 2 HO、HS
2 2
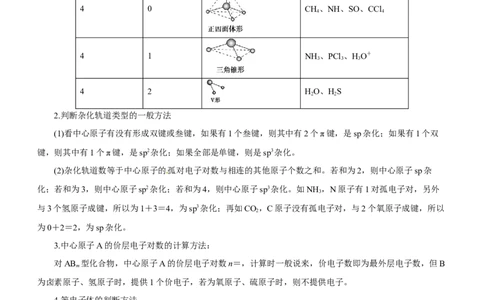
2.判断杂化轨道类型的一般方法
(1)看中心原子有没有形成双键或叁键,如果有1个叁键,则其中有2个π键,是sp杂化;如果有1个双
键,则其中有1个π键,是sp2杂化;如果全部是单键,则是sp3杂化。
(2)杂化轨道数等于中心原子的孤对电子对数与相连的其他原子个数之和。若和为2,则中心原子sp杂
化;若和为3,则中心原子sp2杂化;若和为4,则中心原子sp3杂化。如NH ,N原子有1对孤电子对,另外
3
与3个氢原子成键,所以为1+3=4,为sp3杂化;再如CO,C原子没有孤电子对,与2个氧原子成键,所以
2
为0+2=2,为sp杂化。
3.中心原子A的价层电子对数的计算方法:
对AB 型化合物,中心原子A的价层电子对数n=,计算时一般说来,价电子数即为最外层电子数,但B
m
为卤素原子、氢原子时,提供1个价电子,若为氧原子、硫原子时,则不提供电子。
4.等电子体的判断方法
(1)判断方法:一是同主族变换法,如CO 与CS、CF 与CCl 是等电子体,二是左右移位法,如N 与
2 2 4 4 2
CO,CO、NO 与SO 是等电子体。如果是阴离子,价电子应加上阴离子所带的电荷数;如果是阳离子,价
3
电子应减去阳离子所带的电荷数。如NH价电子为8,CO价电子为24。
(2)常见的等电子体
微粒 通式 价电子总数 立体构型
CH、NH AX 8e- 正四面体形
4 4
CO、N AX 10e- 直线形
2CO、CNS-、NO、N AX 16e- 直线形
2 2
SO 、O、NO AX 18e- V形
2 3 2
CO、NO、SO AX 24e- 平面三角形
3 3
PO、SO、ClO AX 26e- 三角锥形
3
SO、PO AX 32e- 正四面体形
4
5.分子性质
(1)分子极性
1)分子构型与分子极性的关系
2)键的极性与分子极性的关系
类型 实例 两个键之间的夹角 键的极性 分子的极性 空间构型
X H、N - 非极性键 非极性分子 直线型
2 2 2
XY HCl、NO - 极性键 极性分子 直线型
CO、CS 180° 极性键 非极性分子 直线型
2 2
XY (X Y) SO 120° 极性键 极性分子 三角形
2 2 2
HO、HS 104.5° 极性键 极性分子 V形
2 2
BF 120° 极性键 非极性分子 平面三角形
3
XY
3
NH 107.3° 极性键 非极性分子 三角锥形
3
XY CH、CCl 109.5° 极性键 非极性分子 正四面体
4 4 4
(2)溶解性——“相似相溶”规律:非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶剂;
若存在氢键,则溶剂和溶质之间的氢键作用力越大,溶解性越好。
(3)无机含氧酸分子的酸性
无机含氧酸可写成(HO) RO,如果成酸元素R相同,则n值越大,R的正电性越高,使R—O—H中O的
m n
电子向R偏移,在水分子的作用下越易电离出H+,酸性越强,如酸性:HClO