文档内容
专题 24 原电池 化学电源
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 原电池的工作原理及应用
考点二 化学电源
考点一 原电池的工作原理及应用
1.(2023·安徽芜湖·芜湖一中校考模拟预测)光催化微生物燃料电池的工作原理如图所示:
已知:电极a在光激发条件下会产生电子(e-)—空穴(h+)。下列说法错误的是
A.电极电势:电极a>电极b
B.电极b发生的电极反应式为(C H O)-24e-+7H O=6CO↑+24H+
6 10 5 n 2 2
C.光激发时,光生电子会与O 结合,光生空穴会与电极b产生的电子结合
2
D.电池工作一段时间后,右侧溶液pH保持不变(不考虑CO 的溶解)
2
【答案】B
【解析】A.根据题图信息判断,(C H O) 在电极b上失电子,转化为CO,则电极b为负极,电极a为
6 10 5 n 2
正极,原电池中,正极的电极电势高于负极的电极电势,则电极电势:电a>电极b,故A正确;B.根据
得失电子守恒判断,电极b发生的电极反应式为(C H O)-24ne-+7nH O=6nCO↑+24nH+,故B错误;C.
6 10 5 n 2 2
根据题图信息判断,电极a在光激发条件下会产生电子(e-)、空穴(h+),光生电子会与O 结合,光生空穴会
2
与电极b产生的电子结合,故C正确;D.根据电极反应判断,每转移24nmol电子时,右侧溶液中生成
24nmolH+,同时会有24n mol H+通过阳离子交换膜移向左侧溶液,则右侧溶液的pH保持不变,故D正确;
故选B。
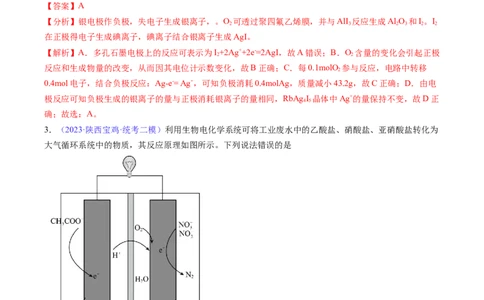
2.(2023·陕西西安·陕西师大附中校考模拟预测)固体电解质在制造全固态电池、探测器方面应用广泛。
一种利用原电池原理测定O 含量的气体传感器示意图如图,RbAg I 是只能传导Ag+的固体电解质。O 可
2 4 5 2
透过聚四氟乙烯膜,并与AlI 反应生成Al O 和I。通过电池电位计的变化可测得O 的含量。下列说法不
3 2 3 2 2
正确的是
1
原创精品资源学科网独家享有版权,侵权必究!A.多孔石墨电极上的反应可表示为I+2Rb++2e-=2RbI
2
B.O 含量的变化会引起电位计示数的变化
2
C.理论上,每0.1molO 参与反应,银电极质量就减小43.2g
2
D.传感器工作时RbAg I 晶体中Ag+的量保持不变
4 5
【答案】A
【分析】银电极作负极,失电子生成银离子,。O 可透过聚四氟乙烯膜,并与AlI 反应生成Al O 和I。I
2 3 2 3 2 2
在正极得电子生成碘离子,碘离子结合银离子生成AgI。
【解析】A.多孔石墨电极上的反应可表示为I+2Ag++2e-=2AgI,故A错误;B.O 含量的变化会引起正极
2 2
反应和生成物量的改变,从而因其电位计示数变化,故B正确;C.每0.1molO 参与反应,电路中转移
2
0.4mol电子,结合负极反应:Ag-e-= Ag+,可知负极消耗0.4molAg,质量减小43.2g,故C正确;D.由电
极反应可知负极生成的银离子的量与正极消耗银离子的量相同,RbAg I 晶体中Ag+的量保持不变,故D正
4 5
确;故选:A。
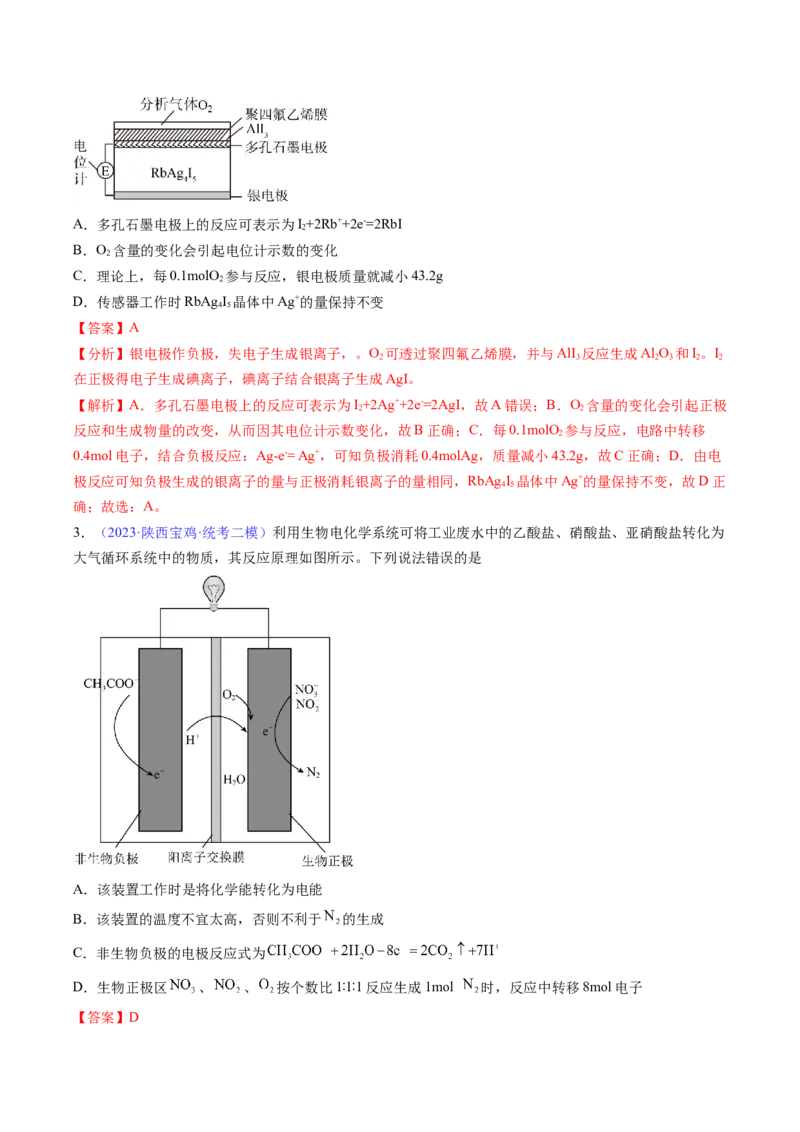
3.(2023·陕西宝鸡·统考二模)利用生物电化学系统可将工业废水中的乙酸盐、硝酸盐、亚硝酸盐转化为
大气循环系统中的物质,其反应原理如图所示。下列说法错误的是
A.该装置工作时是将化学能转化为电能
B.该装置的温度不宜太高,否则不利于 的生成
C.非生物负极的电极反应式为
D.生物正极区 、 、 按个数比1∶1∶1反应生成1mol 时,反应中转移8mol电子
【答案】D【解析】A.原电池是将化学能转化为电能的装置,A项正确;B.温度超过一定范围,生物正极会失去活
性,不利于 的生成,B项正确;C.由电荷守恒和原子守恒,非生物负极的电极反应式为
,C项正确;D.生物正极区生成 的反应式为
,则生成1mol 时,反应中转移12mol ,D项错误;故
选:D。
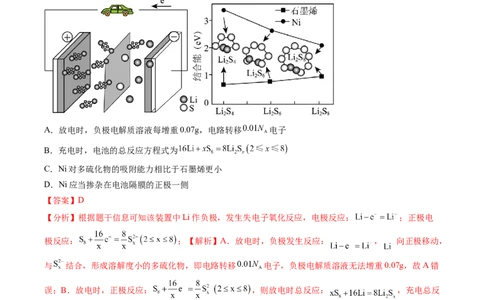
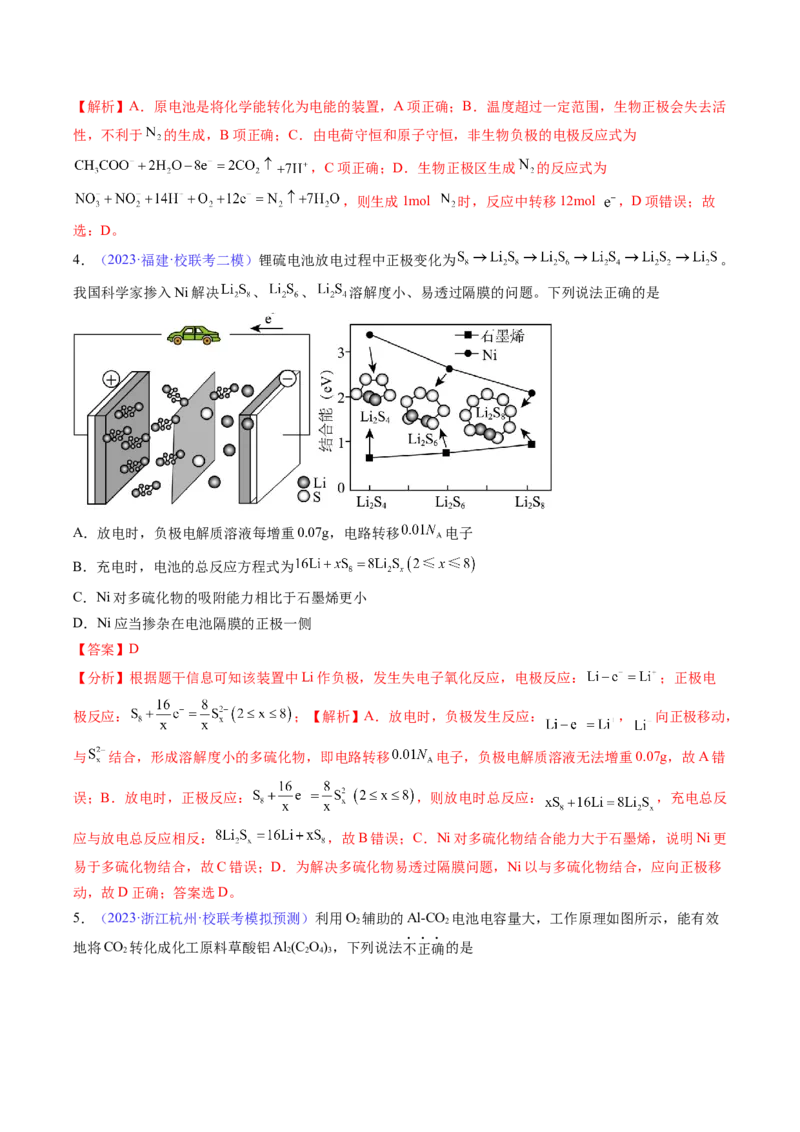
4.(2023·福建·校联考二模)锂硫电池放电过程中正极变化为 。
我国科学家掺入Ni解决 、 、 溶解度小、易透过隔膜的问题。下列说法正确的是
A.放电时,负极电解质溶液每增重0.07g,电路转移 电子
B.充电时,电池的总反应方程式为
C.Ni对多硫化物的吸附能力相比于石墨烯更小
D.Ni应当掺杂在电池隔膜的正极一侧
【答案】D
【分析】根据题干信息可知该装置中Li作负极,发生失电子氧化反应,电极反应: ;正极电
极反应: ;【解析】A.放电时,负极发生反应: , 向正极移动,
与 结合,形成溶解度小的多硫化物,即电路转移 电子,负极电解质溶液无法增重0.07g,故A错
误;B.放电时,正极反应: ,则放电时总反应: ,充电总反
应与放电总反应相反: ,故B错误;C.Ni对多硫化物结合能力大于石墨烯,说明Ni更
易于多硫化物结合,故C错误;D.为解决多硫化物易透过隔膜问题,Ni以与多硫化物结合,应向正极移
动,故D正确;答案选D。
5.(2023·浙江杭州·校联考模拟预测)利用O 辅助的Al-CO 电池电容量大,工作原理如图所示,能有效
2 2
地将CO 转化成化工原料草酸铝Al (C O),下列说法不正确的是
2 2 2 4 3A.多孔碳电极为电池的正极,发生还原反应
B.氧气在反应过程中作为氧化剂,最终转化为
C.电池的负极反应式为Al-3e-=Al3+
D.电池的正极反应可以表示为
【答案】B
【分析】由图可知,Al元素价态升高失电子,故铝电极为负极,电极反应式为Al-3e- =A13+;多空碳电极
为正极,反应为O+4e-=2O2-,继续发生反应:6O2-+6CO = 6O +3 ,正极反应可以表示为2CO+2e-=
2 2 2 2
。
【解析】A.在多空碳电极上氧气得电子被还原,所以多孔碳电极为正极,发生还原反应,A正确;B.
O+4e-=2O2-,继续发生反应6O2-+6CO = 6O +3 ,可见氧气为反应的催化剂,B错误;C.A1元素价
2 2 2
态升高失电子,故铝电极为负极,电极反应式为Al-3e-=Al3+,C正确;D.正极反应为O+4e-=2O2-,继续
2
发生反应6O2-+6CO = 6O +3 ,正极反应可以表示为2CO+2e-= ,D正确;故合理选项是B。
2 2 2
6.(2023·河北保定·校联考三模)采用情性电极,设计双阴极微生物燃料电池进行同步硝化和反硝化脱氮
的装置如图所示。下列说法不正确的是
A.缺氧室和好氧室电极均为燃料电池正极
B.缺氧室中电极发生的反应为2 +12H++10e-=N ↑+6H O
2 2
C.若好氧室消耗标准状况下44.8LO ,则至少有1mol 完全转化为
2
D.理论上,厌氧室消耗1 mol C H O,外电路转移24 mol e-
6 12 6
【答案】C【分析】根据左侧缺氧室 →N 可得N元素化合价降低,则为正极,左侧缺氧阴极发生的电极反应为2
2
+12H++10e-=N ↑+6H O,右侧好氧阴极为正极,发生的反应为O+4e-+4H+=2H O,电极附近还发生
2 2 2 2
NH +2O =NO +2H++H O,中间厌氧阳极为负极,厌氧阳极上有机污染物发生失电子的氧化反应生成CO
2 2 2
和H+。
【解析】A.该装置为原电池,阳离子移向正极,左侧缺氧室和右侧好氧室均为正极,故A正确;B.左
侧缺氧室 →N 中N元素化合价降低,得电子发生还原反应,电极反应式为2 +12H++10e-
2
=N ↑+6H O,故B正确;C.若好氧室消耗标准状况下44.8LO 其物质的量为: =2mol,
2 2 2
+2O = +H O +2H+,由于 和电极之间存在着对O 的竞争,故可知则最多有1mol 完全转化为
2 2 2
,故C错误;D.厌氧阳极上葡萄糖发生失电子的氧化反应生成CO 和H+,电极反应式为
2
C H O+6H O-24e-═6CO +24H+,消耗1 molC H O,外电路转移24 mol e-,故D正确;故答案选C。
6 12 6 2 2 6 12 6
7.(2023·四川巴中·统考模拟预测)一种可用于吸收CO 的电池,其工作原理如图所示。下列说法正确的
2
是
A.电极a上发生的反应为H-2e⁻=2H+
2
B.I室出口处溶液的pH大于入口处
C.该装置可以制取CaCl 和NaHCO
2 3
D.如果将阴离子交换膜改为阳离子交换膜,则电池工作时I室可能有CaCO 沉淀生成
3
【答案】C
【分析】在电极a上H 放电,为负极,由于电极a附近为碱性条件,所以电极a上发生的反应为H-2e-
2 2
+2OH-=2H O;电极b为正极,H+放电生成H,电极b上发生的反应为2H++2e-=H ,以此作答。
2 2 2
【解析】A.由分析可知,电极a上发生的反应为H-2e-+2OH-=2H O,故A错误;B.I室中的OH-在
2 2
电极a上被消耗,导致氢氧根离子减小,出口处溶液的pH小于入口处,故B错误;C.II室的Cl-通过阴
离子交换膜进入I室,可在I室获得CaCl ,II室中水电离产生的氢离子放电,使溶液呈碱性,过量的CO
2 2
与OH-反应生成碳酸氢根,则可在II室获得碳酸氢钠,故C正确;D.II室中有碳酸根离子生成,若将阴
离子交换膜改为阳离子交换膜,则I室中的钙离子通过交换膜进入II室,从而在II室中生成碳酸钙沉淀,
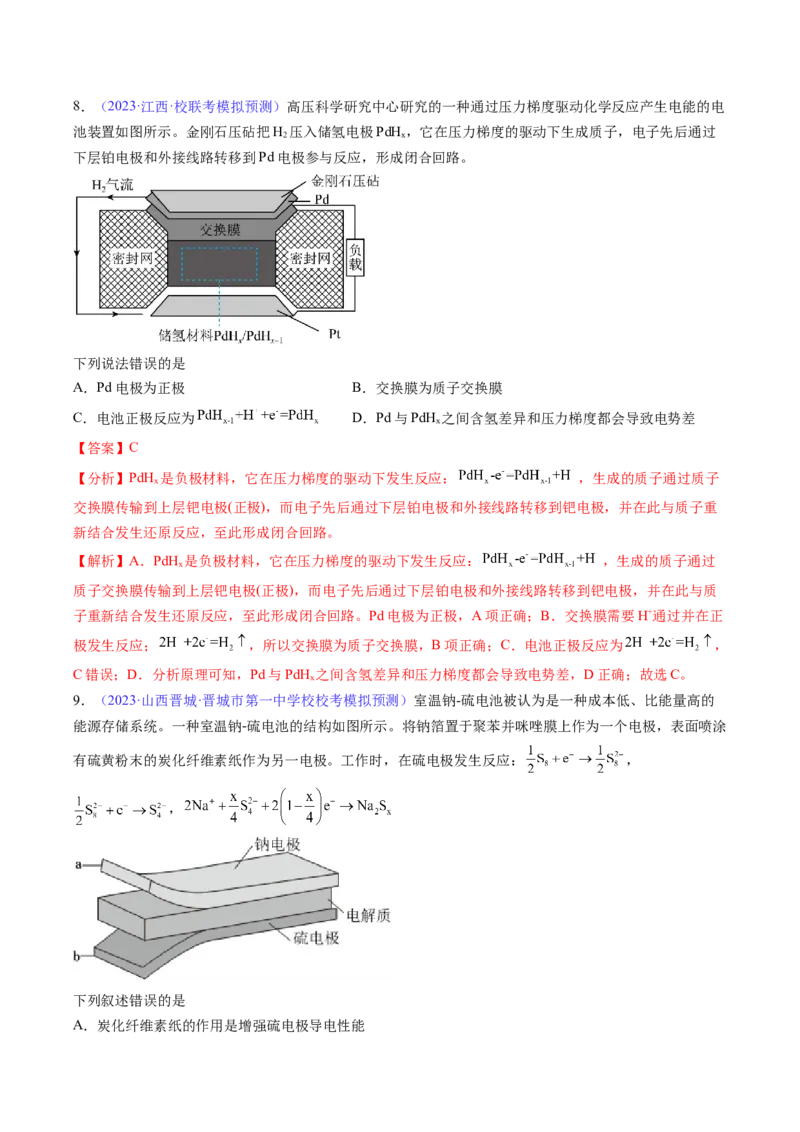
故D错误;故选C。8.(2023·江西·校联考模拟预测)高压科学研究中心研究的一种通过压力梯度驱动化学反应产生电能的电
池装置如图所示。金刚石压砧把H 压入储氢电极PdH ,它在压力梯度的驱动下生成质子,电子先后通过
2 x
下层铂电极和外接线路转移到Pd电极参与反应,形成闭合回路。
下列说法错误的是
A.Pd电极为正极 B.交换膜为质子交换膜
C.电池正极反应为 D.Pd与PdH 之间含氢差异和压力梯度都会导致电势差
x
【答案】C
【分析】PdH 是负极材料,它在压力梯度的驱动下发生反应: ,生成的质子通过质子
x
交换膜传输到上层钯电极(正极),而电子先后通过下层铂电极和外接线路转移到钯电极,并在此与质子重
新结合发生还原反应,至此形成闭合回路。
【解析】A.PdH 是负极材料,它在压力梯度的驱动下发生反应: ,生成的质子通过
x
质子交换膜传输到上层钯电极(正极),而电子先后通过下层铂电极和外接线路转移到钯电极,并在此与质
子重新结合发生还原反应,至此形成闭合回路。Pd电极为正极,A项正确;B.交换膜需要H+通过并在正
极发生反应; ,所以交换膜为质子交换膜,B项正确;C.电池正极反应为 ,
C错误;D.分析原理可知,Pd与PdH 之间含氢差异和压力梯度都会导致电势差,D正确;故选C。
x
9.(2023·山西晋城·晋城市第一中学校校考模拟预测)室温钠-硫电池被认为是一种成本低、比能量高的
能源存储系统。一种室温钠-硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂
有硫黄粉末的炭化纤维素纸作为另一电极。工作时,在硫电极发生反应: ,
,
下列叙述错误的是
A.炭化纤维素纸的作用是增强硫电极导电性能B.放电时负极反应为:
C.充电时 从硫电极向钠电极迁移
D.放电时外电路电子流动的方向是
【答案】B
【分析】钠-硫电池中钠作负极,电极反应式为:Na-e-=Na+,表面喷涂有硫磺粉末的炭化纤维素纸作正极,
电极反应式为: S+e-→ S , S +e-→S ,2Na++ S +2(1- )e-→NaS,充电时,钠电极作阴极,
8 2 x
电极反应式为:Na++e-=Na。
【解析】A.炭化纤维素纸具有导电性,其作用是增强硫电极导电性能,故A正确;B.钠-硫电池中钠作
负极,电极反应式为:Na-e-=Na+,故B错误;C.由分析知,充电时Na电极作为阴极,阳离子移向阴极,
因此充电时Na+从硫电极向钠电极迁移,故C正确;D.放电时,电子由负极流向正极,由分析知,a为负
极,b为正极,因此放电时外电路电子流动的方向是a→b,故D正确;故选B。
10.(2023·海南海口·海南中学校考三模)中科院研究者研发出世界首例室温条件以氢负离子为导体的新
型电池,如以氢化镧(LaH )为电解质的电池的工作原理如图所示:
x
下列说法正确的是
A.电势:Y