文档内容
专题二 能力提升检测卷
1.下列物理量对应的单位符号不正确的是
A.摩尔质量:g/mol B.气体摩尔体积:L/mol
C.物质的量:n D.物质的量浓度:mol/L
2.下列说法中,正确的是
A.S的摩尔质量是32 g
B.常温常压下,1mol SO 的体积是22.4 L
2
C.0.5 mol·L-1 Na SO 溶液中含有1 mol Na+
2 4
D.1 mol N 中含有的分子数约为6.02×1023
2
3.下列叙述中正确的是
A.14gN 中含有1mol氮 B.1molCO中约含有6.02×1023个原子
2
C.氧化钙的摩尔质量为56 D.1molH O和1molH O 所含氢元素质量相等
2 2 2
4.下列说法正确的是
A. 的 溶液与 的 溶液的 浓度相等
B.将 固体溶解在 水中,所得溶液的物质的量浓度恰好是
C.在相同的温度和压强下, 的 和 混合气体与 的 含有相同数目的原子
D.摩尔是国际基本物理量,氯原子的摩尔质量为
5.航天员在太空舱需要的氧气除了从地球运输外,在空间站制取的原理为:① ;
② 。下列有关说法不正确的是A.①②均为氧化还原反应
B.反应①中每生成 ,同时生成
C.反应②中 被还原可得到
D.常温常压下, 的摩尔质量为
6.同温同压下,等容积的两个密闭容器中分别充满了12C18O和14N 两种气体。关于这两个容器中气体的说
2
法正确的是
A.原子数、中子数和质子数都相等 B.分子数和质量均不相等
C.质量、分子数、原子数均相等 D.质子数、原子数相等,质量不等
7.容积不同的A、B两个密闭容器,A中充满氮气,B中充满 和 混合气体,同温同压下测得两容
器中气体密度相同,下列叙述不正确的是
A.容器A和容器B中所含气体质量一定不同
B.容器B中混合气体的密度是同温同压下氢气密度的14倍
C.容器B中 和 的质量之比为33∶16
D.容器A和容器B中所含气体分子数一定不同
8.设N 为阿伏加德罗常数的值,下列叙述正确的是
A
A.1L1mol Ca(ClO) 溶液中含ClO-的数目为0.2N
2 A
B.12g质量分数为25%的甲醛水溶液中含0.1N 个O原子
A
C.已知核反应: U+ n→ Ba+ M+3 n,则0.1molM中含中子的数目为5.3N
A
D.50mL18.4mol•L-1浓硫酸与足量铜微热反应,生成SO 分子的数目为0.46N
2 A
9.已知: 。 代表阿伏加德罗常数的值,下列说法错误的是A.生成 电子转移数为
B.消耗 生成CO分子数为
C.生成标准状况下 ,断开C-H键数为
D.消耗 所生成的气体完全燃烧,需要 分子数为
10.设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.标准状况下,22.4LCH CHO的碳原子数为2N
3 A
B.向FeBr 溶液中通入适量氯气,当有1molBr 生成时,总共转移电子的数目可能为4mol
2 2
C.3.2gCu与S完全反应,转移电子数为0.1N
A
D.O 和O 均只含非极性键,也均为非极性分子
2 3
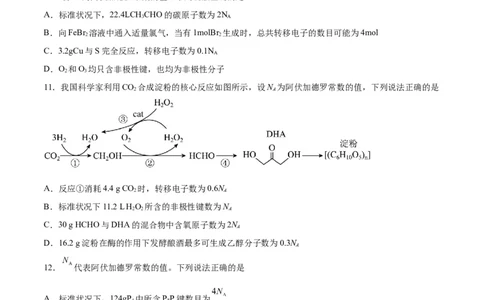
11.我国科学家利用CO 合成淀粉的核心反应如图所示,设N 为阿伏加德罗常数的值,下列说法正确的是
2 A
A.反应①消耗4.4 g CO 时,转移电子数为0.6N
2 A
B.标准状况下11.2 L HO 所含的非极性键数为N
2 2 A
C.30 g HCHO与DHA的混合物中含氧原子数为2N
A
D.16.2 g淀粉在酶的作用下发酵酿酒最多可生成乙醇分子数为0.3N
A
12. 代表阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,124gP 中所含P-P键数目为
4
B. 溶液中所含 的数目小于
C.常温常压下,11.2L甲烷和乙烯混合物中含氢原子数目为
D.48g正丁烷和10g异丁烷的混合物中共价键数目为
13.用N 阿伏加德罗常数,下列说法正确的是
AA.1molCl 与足量Fe反应,转移的电子数为3N
2 A
B.1.5 mol NO 与足量HO反应,转移的电子数为1.5N
2 2 A
C.常温常压下,46 g的NO 和NO 混合气体含有的原子数为3N
2 2 4 A
D.0.10mol Fe粉与足量水蒸气反应生成的H 分子数为0.10N
2 A
14.下列叙述不正确的是
A.常温常压下,等物质的量的N 和CO所含的分子数目均为N
2 A
B.常温常压下,4.6gNO 和NO 混合气体中含有的氧原子数目为0.2N
2 2 4 A
C.25℃1.0LpH=13的Ca(OH) 溶液中含有的OH-数目为0.1N
2 A
D.标准状况下,2.24LHCl与3.4gH S气体分子所含电子数目均为1.8N
2 A
15.N 为阿伏加德罗常数的值,下列说法正确的是
A
A.4.4gC HO中含有 键数目最多为0.7N
2 4 A
B.1.7gH O 中含有氧σ原子数为0.2N
2 2 A
C.向1L0.1mol/LCHCOOH溶液通氨气至中性,铵根离子数为0.1N
3 A
D.标准状况下,11.2LCl 通入水中,溶液中氯离子数为0.5N
2 A
16.关于NaO 的叙述正确的是 (N 表示阿伏加德罗常数)
2 2 A
A.7.8g Na O 含有的共价键数为0.2N
2 2 A
B.7.8 g Na S与NaO 的混合物, 含离子总数为0.3 N
2 2 2 A
C.7.8g Na O 与足量的CO 充分反应, 转移的电数为0.2N
2 2 2 A
D.0.2 mol Na被完全氧化生成7.8g Na O, 转移电子的数目为0.4N
2 2 A
17.阿伏加德罗常数的值为 。下列说法正确的是
A.1L0.1mol· NH Cl溶液中, 的数量为0.1
4
B.2.4gMg与HSO 完全反应,转移的电子数为0.1
2 4
C.标准状况下,2.24LN 和O 的混合气体中分子数为0.2
2 2
D.0.1mol H 和0.1mol I 于密闭容器中充分反应后,其分子总数为0.2
2 2
18.设阿伏加德罗常数的值为N ,下列说法正确的是
A
A.标准状况下,2.24LCH OH分子中共价键的数目为0.5N
3 A
B.1molNa O 与足量CO 充分反应,转移的电子数为2 N
2 2 2 AC.用浓盐酸分别和KMnO 、KClO 反应制备l mol氯气,转移的电子数均为2N
4 3 A
D.5.6gFe粉与足量S粉加热充分反应转移的电子数为0.2N
A
19.某同学欲配制100 mL 0.10 mol/L CuSO 溶液。以下操作①~④是其配制过程及示意图,关于该配制过
4
程,下列说法正确的是
A.操作①中,称取 2.5 g 胆矾晶体,并于烧杯中加水溶解
B.操作②中,容量瓶使用前需用自来水、蒸馏水洗涤,干燥后可用
C.操作③为定容,按图示观察,将导致所配溶液浓度偏高
D.操作④摇匀后静置,发现液面低于刻度线,继续加水至凹液面与刻度线相切
20.某学生配制了100mL1mol·L-1的硫酸,然后对溶液浓度做精确测定,且测定过程中一切操作都正确,
但测得溶液的物质的量浓度小于1mol·L-1.则在配制过程中,下列操作可能导致溶液浓度偏低的是
①量筒用蒸馏水洗净后立即用来量取浓硫酸
②将浓硫酸在烧杯中稀释,转移到100mL的容量瓶中后,没有洗涤烧杯和玻璃棒
③在转移过程中用玻璃棒引流,因操作不慎有少量溶液流到了容量瓶外面
④最后定容时,加水超过了刻度线,马上用胶头滴管吸去多余的水,使溶液凹液面刚好与刻度线相切
A.只有②③④ B.只有③④ C.只有①②③ D.①②③④
21.如图是某学校实验室从化学试剂商店采购的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制100mL
1.5mol/L的稀硫酸。可供选用的仪器有:胶头滴管;烧瓶;烧杯;药匙;量筒;托盘天平。
硫酸化学纯(CP)
(500mL)
品名:硫酸
化学式:HSO
2 4
相对分子质量:98
密度:1.84g/cm3
质量分数:98%
请回答下列问题:
(1)配制稀硫酸时,还缺少的仪器是_______(填写名称)。(2)经计算,配制100mL 1.5mol·L-1的稀硫酸需要量取上述浓硫酸的体积为_______mL。
(3)对所配制的稀硫酸进行测定,发现其浓度大于1.5 mol·L-1,配制过程中下列各项操作可能引起该误差的
有_______(填写字母)。
A.用量筒量取浓硫酸时,仰视刻度线取浓硫酸
B.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
C.将硫酸稀释后立即转入容量瓶后,紧接着就进行以后的实验操作
D.转移溶液时,不慎有少量溶液洒到容量瓶外面
E.定容时,俯视容量瓶刻度线进行定容
F.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
(4)将10.9g Na O和NaO 的固体混合物溶于水得到500mL溶液,所得溶液用100mL 稀硫酸恰好
2 2 2
完全中和。回答下列问题:
①固体混合物中 的质量为_______g。
②固体混合物与水反应生成气体的体积为_______L(标准状况)。
③固体混合物与水反应后,所得NaOH溶液的物质的量浓度_______ 。
22.用质量分数为36.5%的浓盐酸(密度为1.16g·cm-3)配制成1mol·L-1的稀盐酸。现实验室仅需要这种盐酸
220mL,试回答下列问题:
(1)配制稀盐酸时,应选用规格为___________mL的容量瓶。
(2)经计算需要___________mL浓盐酸,在量取时宜选用下列量筒中的___________。
A.5mL B.10mL C.25mL D.50mL
(3)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入选定规格的容量瓶中;
②往容量瓶中小心注入蒸馏水至液面距离容量瓶刻度线1~2cm时,改用胶头滴管滴加蒸馏水,使溶液的
凹液面与瓶颈的刻度线相切;
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅拌,使其混合均匀;
④用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是___________(填序号)。
(4)在上述配制过程中,用刚刚洗涤干净的量筒来量取浓盐酸,则配制的稀盐酸浓度___________(填“偏
高”“偏低”或“无影响”,下同)。若未用蒸馏水洗涤烧杯和玻璃棒或未将洗涤液注入容量瓶,则配制的
稀盐酸浓度___________。23.1984年我国研制出有效杀灭肝炎病毒的消毒液,命名为“84消毒液”。完成下列问题。
(1)实验室“84 消毒液”可通过将氯气通入冷而稀的氢氧化钠溶液获得,写出该反应的离子方程式
_______。
(2)“84消毒液”与洁厕灵(主要成分为盐酸)混用,会产生黄绿色有毒气体。反应离子方程式为_______,氧
化产物与还原产物的物质的量之比为_______。
(3)将“84 消毒液”与 同时用于织物漂白,效果不佳,原因 _______(用离子方程式表示)。
(4)高铁酸钠 是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。
①某兴趣小组欲用 固体配制 的高铁酸钠溶液,需要高铁酸钠固体的质量为
_______g 。配制所用的容量瓶上标有_______、_______、刻度线。
②下列操作导致浓度偏低的是_______。
A.容量瓶用蒸馏水洗净之后,直接用于溶液的配制
B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C.摇匀后,发现液面低于刻度线,又滴加蒸馏水至与刻度线相切
D.定容时,俯视刻度线
24.完成下列填空
(1)9.5 g某二价金属氯化物(ACl )中含有0.2 molCl-,则A的摩尔质量是_______。
2
(2)Al与NaOH溶液的反应化学方程式为_______;铝的氧化物属于_______氧化物(填“碱性”,“酸性”
或“两性”)。
(3)已知某饱和NaCl溶液的体积为VmL。密度为ρ g/cm3,质量分数为w%,物质的量浓度为c mol/L,用w
表示该温度下NaCl的溶解度_______。
(4)有一个储气瓶,装满O 称重为516g,装满Cl 称重为535.5g (均在标况下测定),若相同条件下装满H,
2 2 2
则称重质量为_______。
(5)如图是某学校实验室从化学试剂商店采购的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制240mL1.84mol/ L的稀硫酸。可供选用的仪器有:胶头滴管;烧瓶;烧杯;药匙;量筒;托盘天平。
硫酸化学纯
(CP)(500mL)
品名:硫酸
化学式: HSO
2 4
相对分子质量: 98
密度: 1.84g/cm3
质量分数: 98%
请回答下列问题:
①配制稀硫酸时,还缺少的仪器是_______(填写名称)。
②经计算,配制240mLl.84mol· L-1的稀硫酸需要量取上述浓硫酸的体积为_______mL。
③对所配制的稀硫酸进行测定,发现其浓度大于1.84mol·L-1,配制过程中下列各项操作可能引起该误差的
有_______(填写字母)。
A.用量筒量取浓硫酸时,俯视刻度线取浓硫酸
B.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
C.将硫酸稀释后立即转入容量瓶后,紧接着就进行以后的实验操作
D.用量筒量取浓硫酸后,洗涤量筒并将洗涤液也转移入烧杯中
E.定容时,仰视容量瓶刻度线
F.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处