文档内容
专题八 能力提升检测卷
1.下列电离方程式书写正确的是
A. B.
C. D.
【答案】B
【解析】 为盐,电离出 和 ,电离方程式为 ,故A错误; 为弱
电解质,电离方程式为 ;故B正确; 为弱电解质,分两步电离,电离方程式为
, ;故C错误; 为盐,完全电离,电离方程式为
;故D错误;故选B。
2.下列有关电解质、强电解质、弱电解质的分类正确的是
选项 A B C D
电解质 HO CO NaCl NaOH
2 2
强电解
盐酸 Ba(OH) HClO BaSO
质 2 4 4
弱电解
CHCOOH HO Cu(OH) 氨水
质 3 2 2
【答案】C
【解析】盐酸是混合物,不是电解质,A错误;二氧化碳不是电解质,是非电解质,B错误;氯化钠是电
解质,高氯酸是强酸,是强电解质,Cu(OH) 是弱电解质,C正确;氨水是混合物,不是电解质,D错
2
误;
故选C。
3.下列实验事实不能证明醋酸是弱电解质的是
A.用醋酸溶液做导电实验,灯泡很暗
B.常温下,测得0.1 mol·L-1醋酸溶液的c(H+)=10-4 mol·L-1
C.常温下,将c(H+)=0.1 mol·L-1的醋酸溶液稀释1 000倍测得c(H+)<10-4 mol·L-1D.等c(H+)、等体积的盐酸和醋酸溶液中和碱时,醋酸中和碱的能力强
【答案】A
【解析】如果醋酸的浓度很小,即便完全电离,溶液中离子浓度仍然很小,灯泡也很暗,所以醋酸浓度未
知,不能由灯泡很暗判断醋酸是强电解质还是弱电解质,故A符合题意;常温下,0.1 mol·L-1醋酸溶液的
氢离子浓度为10-4 mol·L-1说明醋酸是在溶液中部分电离的弱电解质,故B不符合题意;常温下,将氢离
子浓度为0.1 mol·L-1的醋酸溶液稀释1 000倍,稀释后溶液的氢离子浓度小于10-4 mol·L-1说明醋酸是在
溶液中部分电离的弱电解质,故C不符合题意;氢离子浓度相等的等体积的盐酸和醋酸溶液中和碱时,醋
酸中和碱的能力强说明醋酸是在溶液中部分电离的弱电解质,故D不符合题意;故选A。
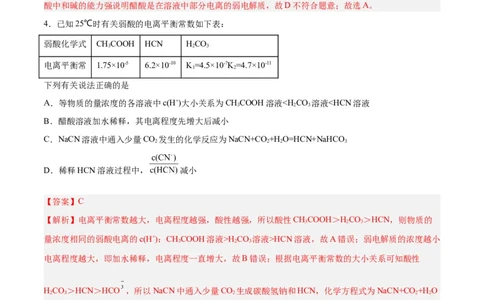
4.已知25℃时有关弱酸的电离平衡常数如下表:
弱酸化学式 CHCOOH HCN HCO
3 2 3
电离平衡常 1.75×10-5 6.2×10-10 K=4.5×10-7K=4.7×10-11
1 2
下列有关说法正确的是
A.等物质的量浓度的各溶液中c(H+)大小关系为CHCOOH溶液H CO 溶液>HCN溶液,故A错误;弱电解质的浓度越小
3 2 3
电离程度越大,即加水稀释,电离程度一直增大,故B错误;根据电离平衡常数的大小关系可知酸性
HCO>HCN>HCO ,所以NaCN中通入少量CO 生成碳酸氢钠和HCN,化学方程式为NaCN+CO+H O
2 3 2 2 2
=HCN+NaHCO ,故C正确; ,加水稀释酸性减弱,氢离子浓度减小,电离平衡常数
3
不变,所以 增大,故D错误;故选C。5. 时, 的电离常数 , 的电离常数 、 。下列说法
不正确的是
A. 溶液和 溶液中离子种类相同
B. 时,反应 的
C. ,物质的量浓度相同的 溶液与 溶液的 :前者小于后者
D.向氯水中加入少量 固体, 增大
【答案】B
【解析】碳酸钠电离出钠离子和碳酸根离子,碳酸根离子水解生成碳酸氢根离子,碳酸氢根离子水解生成
碳酸分子,碳酸氢钠电离出钠离子和碳酸氢根离子,碳酸氢根离子电离出碳酸根离子和氢离子,碳酸氢根
离子水解生成碳酸分子和氢氧根离子,两种溶液中离子种类相同,A正确;25℃时,反应
的 ,B错误;从电离平衡常数分
析,次氯酸的电离平衡常数比碳酸氢根离子的电离平衡常数大,根据越弱越水解分析,碳酸根离子水解程
度大,溶液碱性强,pH大,C正确;氯水中含有盐酸和次氯酸,盐酸能和碳酸氢钠反应,使氯气和水反应
的平衡正向移动,次氯酸的浓度增大,D正确;故选B。
6.下列有关水的电离平衡或pH变化的判断中,正确的是
A.随着温度的升高,Kw 减小
B.随着温度的升高,纯水的pH增大
C.向0.1mol/L氨水的平衡体系中加入少量NH Cl固体,溶液中c(OH-)减小
4
D.向水中通入少量HCl,水的电离平衡向正反应方向移动,c(H+)增大
【答案】C
【解析】水的电离为吸热反应,温度越高,K值越大,A错误;水的电离为吸热反应,温度越高,c(H+)增
大,pH越小,B错误; ,加入NH Cl固体,c( )增大,一水合氨电离平衡逆向
4
移动,c(OH-)减小,C正确; ,加入HCl,水的电离平衡逆向进行,c(H+)增大,D错误;
故选C。7.常温下,下列各组离子在给定溶液中可能大量共存的是
A.麦芽糖溶液中: 、 、 、
B.能使苯酚溶液显紫色的溶液中: 、 、 、
C.水电离出来的 的溶液中: 、 、 、
D.滴加甲基橙显红色的水溶液中: 、 、 、
【答案】C
【解析】麦芽糖具有还原性,酸性条件下 具有强氧化性,两者不能共存,A不符合题意;能使苯酚
溶液显紫色的溶液中含有 ,与 因发生双水解而不能大量共存,B不符合题意;水电离出来的
的溶液可能呈酸性也可能呈碱性,酸性条件下, 和 都能与 反应不能共
存,C符合题意;滴加甲基橙显红色的水溶液呈酸性,在酸性条件下 能发生反应,不能大量共存,D
不符合题意;故选C。
8.水的离子积常数随着温度的变化关系如表:
温度/℃ 25 50 75 100
1.
5.5 20.0 56.0
0
下列说法正确的是
A.纯水中 的大小与温度无关
B.水的电离度a(50℃)K (H CO),故B错误;实验2中发生反应的离子方程式为 + +2OH-= +NH ↑
b 3 2 a1 2 3 3
+2HO,故C错误;析出晶体为NaHCO ,滤液中溶质为NaHCO 、NH Cl,根据元素质量守恒,实验3中
2 3 3 4
物料守恒所得滤液中存在:c( )+c(NH ·H O)=c(Cl—),c(Na+)=c(H CO)+c( )+c( ),c(Na
3 2 2 3
+)c(H CO)+c( )+c( ),故D错误;故选A。
2 3
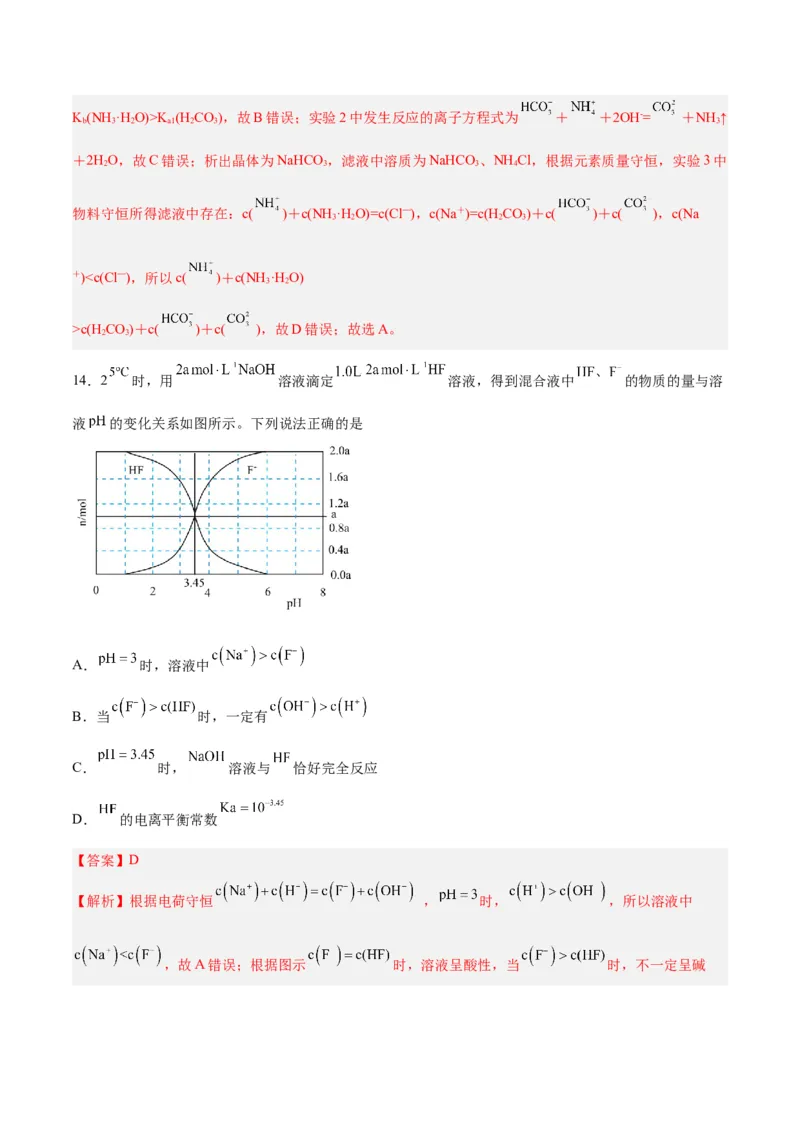
14.2 时,用 溶液滴定 溶液,得到混合液中 的物质的量与溶
液 的变化关系如图所示。下列说法正确的是
A. 时,溶液中
B.当 时,一定有
C. 时, 溶液与 恰好完全反应
D. 的电离平衡常数
【答案】D
【解析】根据电荷守恒 , 时, ,所以溶液中
,故A错误;根据图示 时,溶液呈酸性,当 时,不一定呈碱性,故B错误;氢氧化钠与HF完全反应生成NaF,溶液呈碱性,所以 时,溶液与 没有完全
反应,故C错误; 时, ,则 的电离平衡常数
,故D正确;故选D。
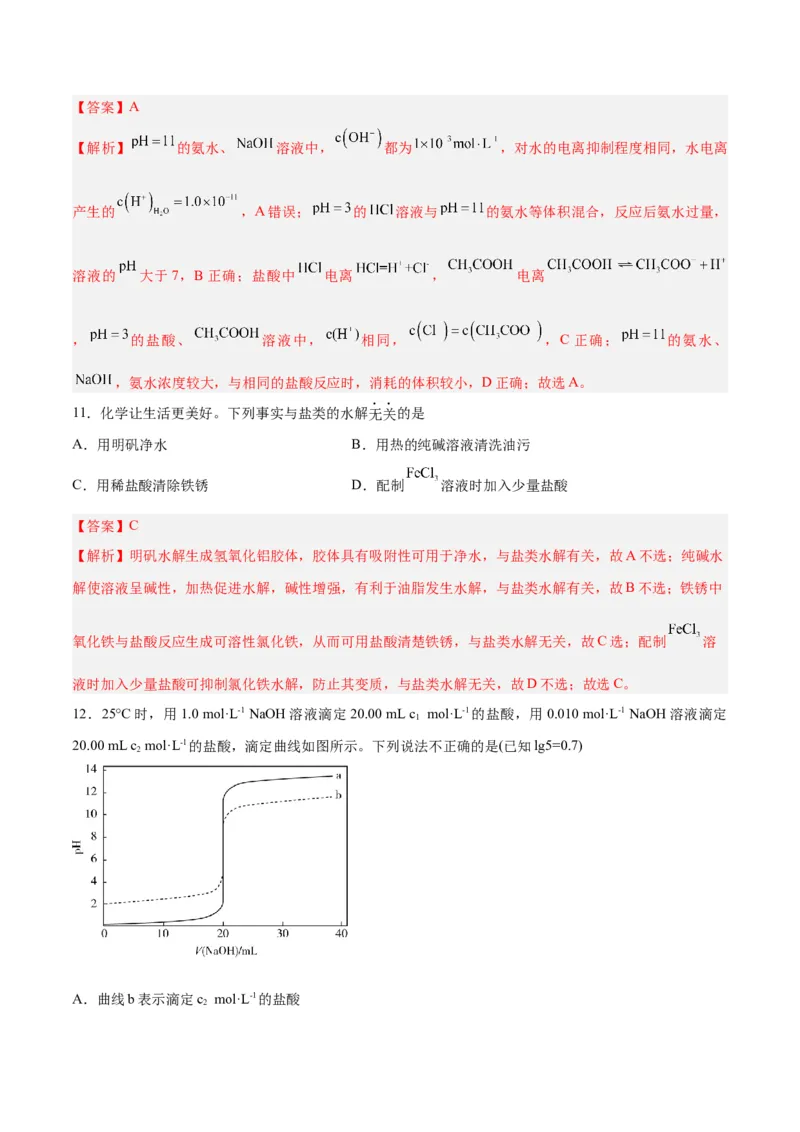
15.T℃时,水的离子积常数K =10-13,该温度下,V mLpH=12的Ba(OH) 稀溶液与V mLpH=2的稀硫酸
w 1 2 2
充分反应(混合后的体积变化忽略不计),恢复到T℃,测得混合溶液的pH=3,则V:V 的值为
1 2
A.9∶101 B.99∶101 C.1∶100 D.1∶10
【答案】A
【解析】T℃时,水的离子积常数 K =10-13,该温度下,V mLpH=12 的 Ba(OH) 稀溶液,c(H+)=10-12
w 1 2
mol/L,则c(OH-)=10-1 mol/L mol/L;V mLpH=2的稀硫酸c(H+)=10-2 mol/L,二者反应后恢复到T℃,测得
2
混合溶液的pH=3,c(H+)=10-3 mol/L,说明酸过量,则 c(H+)= ,解得V :
1
V=9∶101,故选A。
2
16.在0.1mol/LFeCl 溶液中存在Fe3++3H O Fe(OH) +3H+的水解平衡,下列说法中正确的是
3 2 3
A.加FeCl 固体,平衡正向移动,水解程度增大
3
B.稍微加热,促进水解,c(H+)增大,pH减小
C.加NaOH固体,与铁离子反应,平衡逆向移动
D.通入HCl气体,平衡逆向移动,铁离子水解常数减小
【答案】B
【解析】加FeCl 固体,平衡正向移动,但由于溶液浓度增大,所以水解程度减小,故A错误;盐的水解
3
一般是吸热的,微热,水解平衡正向移动,c(H+)增大,pH减小,故B正确;加NaOH固体,OH-与H+反
应,平衡正向移动,故C错误;通入HCl气体,c(H+)增大,平衡逆向移动,但水解常数只与温度有关,铁
离子的水解常数不变,故D错误;故选B。
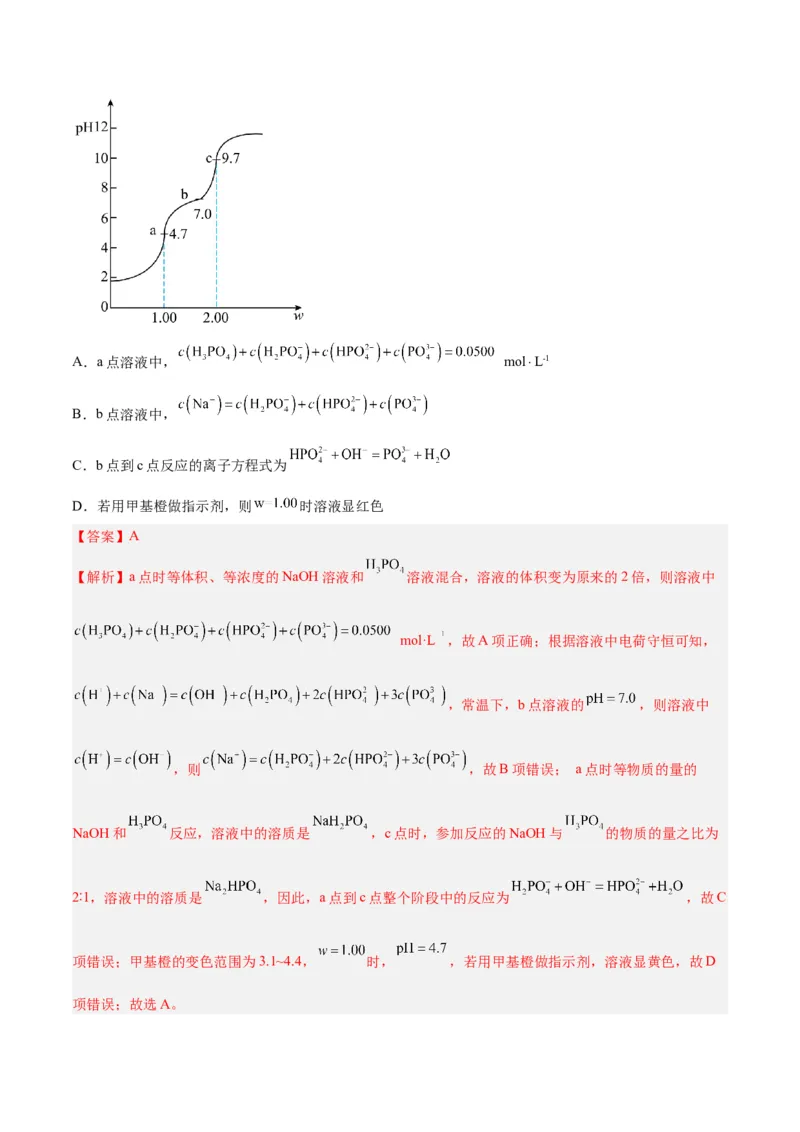
17.常温下,用0.1000 mol⋅L-1的NaOH溶液滴定0.1000 mol⋅L-1的 溶液,获得的滴定曲线如图所
示。横坐标为滴定分数(w),滴定分数是指滴定过程中标准溶液与待测溶液中溶质的物质的量之比。忽略溶
液混合时的体积变化,下列说法正确的是A.a点溶液中, mol⋅L-1
B.b点溶液中,
C.b点到c点反应的离子方程式为
D.若用甲基橙做指示剂,则 时溶液显红色
【答案】A
【解析】a点时等体积、等浓度的NaOH溶液和 溶液混合,溶液的体积变为原来的2倍,则溶液中
mol·L ,故A项正确;根据溶液中电荷守恒可知,
,常温下,b点溶液的 ,则溶液中
,则 ,故B项错误; a点时等物质的量的
NaOH和 反应,溶液中的溶质是 ,c点时,参加反应的NaOH与 的物质的量之比为
2∶1,溶液中的溶质是 ,因此,a点到c点整个阶段中的反应为 ,故C
项错误;甲基橙的变色范围为3.1~4.4, 时, ,若用甲基橙做指示剂,溶液显黄色,故D
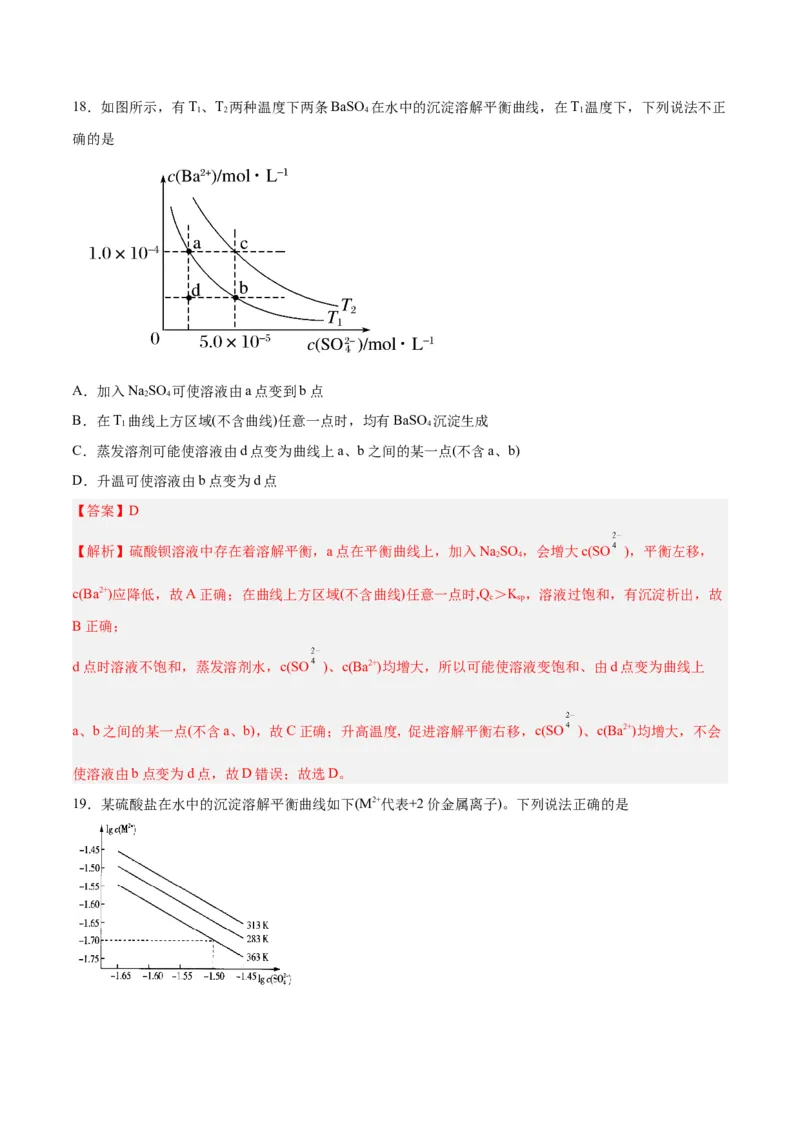
项错误;故选A。18.如图所示,有T、T 两种温度下两条BaSO 在水中的沉淀溶解平衡曲线,在T 温度下,下列说法不正
1 2 4 1
确的是
A.加入NaSO 可使溶液由a点变到b点
2 4
B.在T 曲线上方区域(不含曲线)任意一点时,均有BaSO 沉淀生成
1 4
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
D.升温可使溶液由b点变为d点
【答案】D
【解析】硫酸钡溶液中存在着溶解平衡,a点在平衡曲线上,加入NaSO ,会增大c(SO ),平衡左移,
2 4
c(Ba2+)应降低,故A正确;在曲线上方区域(不含曲线)任意一点时,Q>K ,溶液过饱和,有沉淀析出,故
c sp
B正确;
d点时溶液不饱和,蒸发溶剂水,c(SO )、c(Ba2+)均增大,所以可能使溶液变饱和、由d点变为曲线上
a、b之间的某一点(不含a、b),故C正确;升高温度, 促进溶解平衡右移,c(SO )、c(Ba2+)均增大,不会
使溶液由b点变为d点,故D错误;故选D。
19.某硫酸盐在水中的沉淀溶解平衡曲线如下(M2+代表+2价金属离子)。下列说法正确的是A.363 K时,该硫酸盐的溶度积K 的数量级为10-3
sp
B.温度一定时溶度积K 随c( )的增大而减小
sp
C.313 K下的该盐饱和溶液升温到363 K时有固体析出
D.283 K下的该盐饱和溶液升温到313 K时有固体析出
【答案】C
【解析】363 K时, ,即K 的数量级为10-4,A错误;溶度积常
sp
数只与温度有关,与物质的浓度无关,B错误;由图知,363 K时K 最小,313 K时K 最大,故313 K下
sp sp
的该盐饱和溶液升温到363 K时有固体析出,C正确;由图可知:温度由283 K升高到313 K,物质的溶解
度增大,溶液由饱和溶液变为不饱和溶液,因此不会由固体析出,D错误;故选C。
20.下列说法不正确的是
A.Mg(OH)
2
固体在溶液中存在平衡:Mg(OH)
2
(s)⇌Mg2+(aq)+2OH-,该固体可溶于NH
4
Cl溶液
B.向ZnS沉淀上滴加CuSO 溶液沉淀变为黑色,可推知同温下K (ZnS)K (AgI)
sp sp
【答案】B
【解析】NH Cl为强酸弱碱盐,电离产生的铵根离子与Mg(OH) 产生的氢氧根离子反应生成弱电解质
4 2
NH ▪H O,促使Mg(OH) 溶解平衡正向移动,故Mg(OH) 固体可溶于NH Cl溶液,A说法正确;向ZnS沉
3 2 2 2 4
淀上滴加CuSO 溶液沉淀变为黑色,则发生ZnS(s)+Cu2+(aq)=CuS(s)+Zn2+(aq),可推知同温下K (ZnS)>
4 sp
K (CuS),B说法错误;向AgCl悬浊液中滴加NaS溶液,白色沉淀AgCl变成黑色的Ag S,反应的离子方
sp 2 2
程式为:2AgCl(s)+S2-(aq)⇌Ag
2
S(s)+2Cl-(aq),C说法正确;向2mL浓度均为1.2 mol·L-1的KCl、KI混合溶
液中滴加1~2滴0.01 mol·L-1的AgNO 溶液,振荡沉淀呈黄色,氯离子、碘离子过量,能生成AgI,则AgI
3
更难溶于水,说明K (AgCl)>K (AgI),D说法正确;故选B。
sp sp
21.已知某烧碱样品中含有NaCl杂质,为测定该样品中NaOH的质量分数,进行如下实验:
①称量1.00g样品溶于水配成250mL溶液:
②用碱式滴定管准确量取25.00mL所配溶液于锥形瓶中,滴加2—3滴指示剂:
③用 的标准盐酸滴定并重复三次,每次实验数据记录如下:
滴 定 序 待测液体积/mL 消耗盐酸的体积/mL号
滴定前 滴定后
1 25.00 0.50 20.60
2 25.00 6.00 26.00
3 25.00 1.10 21.00
请回答下列问题:
(1)配制该溶液所需要的主要玻璃仪器为 。
(2)实验步骤②中所滴加的指示剂是 。
(3)滴定管装好溶液后,排除碱式滴定管胶管中气泡的方法是 。滴定过程中用左手控制
。(填仪器及部位),眼睛 ,直至滴定终点。
(4)判断达到滴定终点时的现象为 。
(5)若出现下列情况,导致测定结果偏高的是 (填序号)。
a.滴定前用蒸水冲洗锥形瓶
b.滴定过程中振荡锥形瓶时不慎使瓶内溶液溅出
c.滴定过程中不慎将数滴酸液滴在链形瓶外
d.酸式滴定管中在滴定前有气泡,滴定后气泡消失
e.滴定前仰视读数,滴定后俯视读数
f.酸式滴定管在使用前没有用标准液润洗
(6)通过计算可知该烧碱样品的纯度为 。
【答案】(1)250mL容量瓶、烧杯、玻璃棒、胶头滴管; (2)酚酞(或甲基橙)
(3) 将胶管向上弯曲,用力挤捏玻璃珠,使溶液从尖嘴喷出 酸式滴定管活塞 注视锥形瓶内溶液
颜色的变化
(4)滴入最后半滴盐酸后,锥形瓶中溶液的颜色由红(浅红、粉红)色变为无色且半分钟内不恢复原色(或滴入
最后半滴盐酸后,锥形瓶中溶液的颜色由黄色变为橙色且半分钟内不恢复原色)
(5)c、d、f (6)80%
【解析】(1)配制一定物质的量浓度的溶液的操作步骤为计算、称量、溶解、冷却、转移、洗涤、定
容、摇匀等,用到的主要玻璃仪器为烧杯、玻璃棒、250mL容量瓶、胶头滴管。
(2)强酸滴定强碱可用酚酞或甲基橙作指示剂。
(3)滴定管装好溶液后,排除碱式滴定管胶管中气泡的方法是将胶管向上弯曲,用力捏挤玻璃珠,使溶
液从尖嘴喷出;滴定过程中用左手控制酸式滴定管活塞,眼睛注视锥形瓶内溶液颜色的变化,直至滴定终点。
(4)滴定时,若用酚酞作指示剂,则滴入最后半滴盐酸后,锥形瓶中溶液的颜色由浅红色变为无色且半
分钟内不恢复原色,可说明达到滴定终点,若用甲基橙作指示剂,则滴入最后半滴盐酸后,锥形瓶中溶液
的颜色由黄色变为橙色且半分钟内不恢复原色,可说明达到滴定终点。
(5)滴定前用蒸馏水冲洗锥形瓶,待测液的物质的量不变,所用标准液的体积不变,则测定值不变,故 a
项错误;在振荡锥形瓶时不慎使瓶内溶液溅出,会导致所用标准液的体积偏小,则测定值偏低,故 b项错
误;若在滴定过程中不慎将数滴酸液滴在锥形瓶外,会导致所用标准液的体积偏大,则测定值偏高,故 c
项正确;酸式滴定管中在滴定前有气泡,滴定后气泡消失,造成V(标准)偏大,则测定值偏高,故d项正
确;滴定前仰视读数,滴定后俯视读数,会导致标准液的体积偏小,则测定值偏低,故 e项错误;酸式滴
定管在使用前没有用标准液润洗,则标准液被蒸馏水稀释,会导致所用标准液的体积偏大,则测定值偏
高,故f项正确。
(6)0.1000 mol•L-1标准盐酸滴定三次,消耗盐酸的平均体积为(20.10+20.00+19.90)/3=20.00mL,由关系式
HCI~NaOH可知,n(NaOH)=0.100 0 mol•L-1×0.02 L=0.002 mol,则该烧碱样品的纯度为80%。
22.回答下列问题:
(1)已知:HS:K =1.3×10﹣7 K =7.1×10−15; HCO:K =4.3×10﹣7 K =5.6×10−11;
2 a1 a2 2 3 a1 a2
CHCOOH:K=1.8×10﹣5 NH •H O:K=1.8×10﹣5。
3 a 3 2 b
①常温下,0.1 mol∙L−1NaS溶液和0.1 mol∙L−1NaCO 溶液,碱性更强的是 。
2 2 3
②25℃时,NaHCO 溶液的pH (填“大于”或“小于”)CHCOONa溶液的pH。
3 3
③NH HCO 溶液显 性。
4 3
(2)25℃时,HSO +H+的电离常数K=1.0×10−2,则该温度下NaHSO 的水解常数K=
2 3 a 3 h
。
(3)能证明NaSO 溶液中存在 +H O +OH﹣水解平衡的事实是 (填字母,下同)。
2 3 2
A.滴入酚酞溶液变红,再加HSO 溶液红色褪去
2 4
B.滴入酚酞溶液变红,再加BaCl 溶液后产生沉淀且红色褪去
2
C.滴入酚酞溶液变红,再加氯水后红色褪去
(4)氯化铝水溶液呈 性(填“酸”、“中”、“碱”),把AlCl 溶液蒸干、灼烧后,得到的主要
3
固体产物是 。
(5)①写出1mol/L的NaH PO 溶液中的电荷守恒表达式: 。
2 4
②泡沫灭火器[里面装饱和NaHCO 溶液和Al (SO )]的工作原理: (用离子方程式
3 2 4 3表示)。
【答案】(1)Na S 大于 碱 (2)1.0×10-12 (3)B (4) 酸 Al O
2 2 3
(5)c(Na+) + c(H+) = c( ) + 2c( )+ 3c( )+c(OH-) Al3+ + 2 = Al(OH) +3CO ↑
3 2
【解析】(1)①由电离常数数据可知酸性:HS-”“=”或“<”)c(Al3+)+c[Al(OH) ];2c( )-c( )-3c(Al3+)=
3 2 3
mol·L-1(填数值)。
③80 ℃时,0.1 mol·L-1NH Al(SO ) 溶液的pH小于3,分析导致pH随温度变化的原因是 。
4 4 2
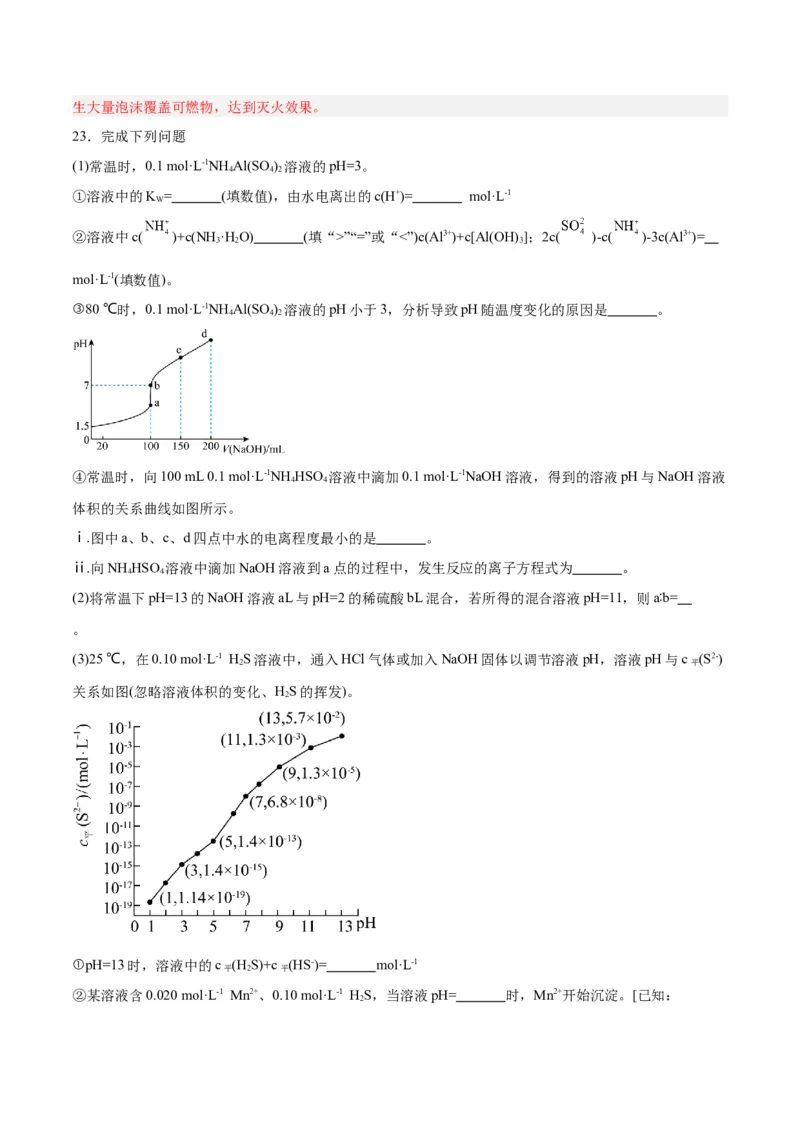
④常温时,向100 mL 0.1 mol·L-1NH HSO 溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液
4 4
体积的关系曲线如图所示。
ⅰ.图中a、b、c、d四点中水的电离程度最小的是 。
ⅱ.向NH HSO 溶液中滴加NaOH溶液到a点的过程中,发生反应的离子方程式为 。
4 4
(2)将常温下pH=13的NaOH溶液aL与pH=2的稀硫酸bL混合,若所得的混合溶液pH=11,则a∶b=
。
(3)25 ℃,在0.10 mol·L-1 HS溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c (S2-)
2 平
关系如图(忽略溶液体积的变化、HS的挥发)。
2
①pH=13时,溶液中的c (H S)+c (HS-)= mol·L-1
平 2 平
②某溶液含0.020 mol·L-1 Mn2+、0.10 mol·L-1 HS,当溶液pH= 时,Mn2+开始沉淀。[已知:
2K (MnS)=2.8×10-15]
sp
【答案】(1) 1×10-14 1×10-3 = 1×10-3 温度升高,N 、Al3+的水解平衡正向移动,溶液
中c(H+)增大 d H++OH-=H O
2
(2)1:9 (3)0.043 5
【解析】(1)①常温时,溶液中的K =1×10-14;0.1mol•L-1NH Al(SO ) 溶液的pH=3的原因是铵根离子和
w 4 4 2
铝离子的水解导致的,溶液中的氢离子全部来自于水的电离,故由水电离出的c(H+)=1×10-3mol•L-1;
②NH Al(SO ) 中氮元素与铝元素是1:1,故溶液中c(NH )+c(NH•H O)=c(Al3+)+c[Al(OH) ];溶液呈电中
4 4 2 3 2 3
性,2c(SO )+c(OH-)= c(NH )+3c(Al3+)+c(H+),2c(SO )-c(NH )-3c(Al3+)= c(H+)-c(OH-)=1×10-3-1×10-
11mol•L-1 1×10-3mol•L-1;
③pH随温度变化的原因是温度升高,NH 、Al3+的水解平衡正向移动,溶液中c(H+)增大;
④ⅰ水的电离程度受溶液中溶质的影响,酸碱抑制水的电离,有弱离子的盐促进水的电离,向
100mL0.1mol•L-1NH HSO 溶液中滴加0.1mol•L-1NaOH溶液100mL对应的a点只有硫酸铵的盐,水的电离
4 4
程度最大,a点之后继续滴加NaOH溶液,水的电离受到抑制,因此水的电离程度最小的是d;
ⅱ向NH HSO 溶液中滴加NaOH溶液到a点的过程中,发生反应的离子方程式为H++OH-=H O;
4 4 2
(2)常温下,pH=13的NaOH溶液中,c(OH-)为0.1mol·L-;pH=2的硫酸溶液c(H+)=0.01mol·L-1,所得溶
液的pH=11,溶液中的c(OH-)= mol·L-, ,a:b=1:9;
(3)①物料守恒有c (H S)+c (HS-)+ c (S2-)=0.10 mol·L-1,由图可知pH=13时,c (S2-)=5.7×10-2
平 2 平 平 平
mol·L-1,则c (H S)+c (HS-)=0.10 mol·L-1-5.7×10-2 mol·L-1=0.043 mol·L-1;
平 2 平
②开始沉淀时c(S2-)= =1.4×10-13 mol·L-1,由图可知c(S2-)=1.4×10-13 mol·L-1时,
pH=5。
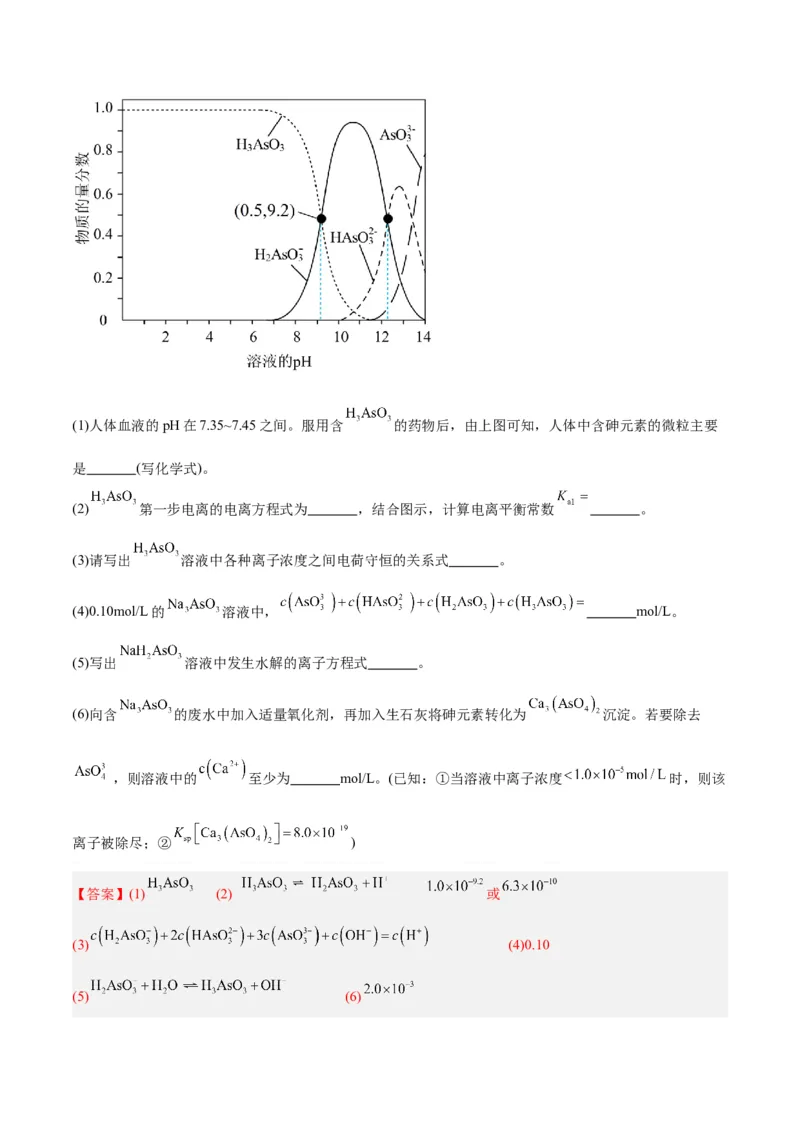
24.常温下,向一定量的 ( 为三元弱酸)溶液中逐滴加入NaOH溶液,含砷元素的各种微粒
物质的量分数与溶液pH的关系如图所示。(1)人体血液的pH在7.35~7.45之间。服用含 的药物后,由上图可知,人体中含砷元素的微粒主要
是 (写化学式)。
(2) 第一步电离的电离方程式为 ,结合图示,计算电离平衡常数 。
(3)请写出 溶液中各种离子浓度之间电荷守恒的关系式 。
(4)0.10mol/L的 溶液中, mol/L。
(5)写出 溶液中发生水解的离子方程式 。
(6)向含 的废水中加入适量氧化剂,再加入生石灰将砷元素转化为 沉淀。若要除去
,则溶液中的 至少为 mol/L。(已知:①当溶液中离子浓度 时,则该
离子被除尽;② )
【答案】(1) (2) 或
(3) (4)0.10
(5) (6)【解析】(1)根据图中曲线知pH在7.35~7.45之间时含砷元素的微粒主要是 。
(2) 第一步电离的电离方程式为 。根据图中 时,
, ,第一步电离的电离平衡常数
。
(3) 溶液中各种离子浓度之间电荷守恒的关系式是:
。
(4)根据As原子守恒得0.10mol/L的 中,
。
(5) 溶液中发生水解的离子方程式: 。
(6)当 时,根据 得
,若要除去 ,则溶液中的 至少为 。