文档内容
第 35 讲 分子的性质 配合物与超分子
[复习目标] 1.理解分子的极性。2.掌握范德华力的含义及对物质性质的影响。3.理解氢键的
含义, 能列举存在氢键的物质,并能解释氢键对物质性质的影响。4.理解配位键的含义。
5.了解超分子的概念。
考点一 键的极性与分子极性
1.键的极性
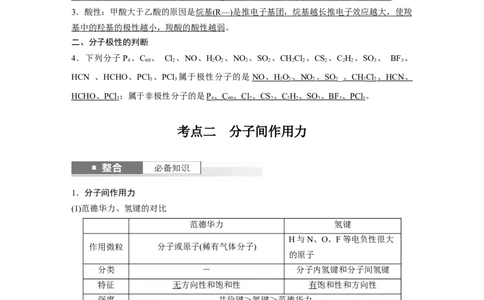
(1)极性键与非极性键的比较
极性键 非极性键
成键原子 不同种元素的原子间 同种元素的原子间
电子对 发生偏移(电荷分布不均匀) 不发生偏移(电荷分布均匀)
成键原子的电性 H—Cl 呈电中性
思考 如何判断共价键极性的强弱?
提示 成键元素电负性值差异越大,共价键的极性越强。
(2)键的极性对化学性质的影响
键的极性对羧酸酸性大小的影响实质是通过改变羧基中羟基的极性而实现的,羧基中羟基的
极性越大,越 容易电离出 H + ,则羧酸的酸性越强。
①与羧基相邻的共价键的极性越大,羧基中羟基的极性越大,则羧酸的酸性越强。
②烷基是推电子基团,从而减小羧基中羟基的极性,导致羧酸的酸性减小。一般地,烷基越
长,推电子效应越大,羧酸的酸性越弱。
2.极性分子和非极性分子
(1)概念
极性分子:分子的正电中心和负电中心不重合,键的极性的向量和不等于零。
非极性分子:分子的正电中心和负电中心重合,键的极性的向量和等于零。
(2)极性分子和非极性分子的判断方法
①A—A型分子一定是非极性分子、A—B型分子一定是极性分子。
②判断AB 型分子极性的两条经验规律
n
a.中心原子A化合价的绝对值等于该元素原子最外层电子数,则为非极性分子,反之则为
极性分子。
b.中心原子A没有孤电子对,则为非极性分子,反之则为极性分子。一、有关羧酸酸性强弱的判断及归因分析
1.试比较下列有机酸的酸性强弱。
①CFCOOH ②CCl COOH ③CHCl COOH ④CHClCOOH ⑤CHCOOH
3 3 2 2 3
⑥CHCHCOOH
3 2
答案 ①>②>③>④>⑤>⑥
2.酸性:氟乙酸大于氯乙酸的原因是 电负性: F>C l , C—F 的极性大于 C—C l 的极性,导致
氟乙酸羧基中的羟基的极性更大,更易电离出 H + ,故氟乙酸的酸性大于氯乙酸的酸性 。
3.酸性:甲酸大于乙酸的原因是 烷基 (R— ) 是推电子基团,烷基越长推电子效应越大,使羧
基中的羟基的极性越小,羧酸的酸性越弱。
二、分子极性的判断
4.下列分子P 、C 、 Cl 、NO、HO 、NO 、SO 、CHCl 、CS 、C H 、SO 、 BF 、
4 60 2 2 2 2 2 2 2 2 2 2 3 3
HCN 、HCHO、PCl 、PCl 属于极性分子的是 NO 、 H O 、 NO 、 SO _ 、 CH Cl 、 HCN 、
5 3 2 2 2 2 2 2
HCHO 、 PCl ;属于非极性分子的是P 、 C 、 C l 、 CS 、 C H 、 SO 、 BF 、 PC l 。
3 4 60 2 2 2 2 3 3 5
考点二 分子间作用力
1.分子间作用力
(1)范德华力、氢键的对比
范德华力 氢键
H与N、O、F等电负性很大
作用微粒 分子或原子(稀有气体分子)
的原子
分类 - 分子内氢键和分子间氢键
特征 无方向性和饱和性 有饱和性和方向性
强度 共价键>氢键>范德华力
①组成和结构相似的物质,相对分子质
影响其强 X—H…Y强弱与X和Y的电
量越大,范德华力越大;
度的因素 负性有关
②分子的极性越大,范德华力越大
对物质性
主要影响物理性质(如熔、沸点)
质的影响
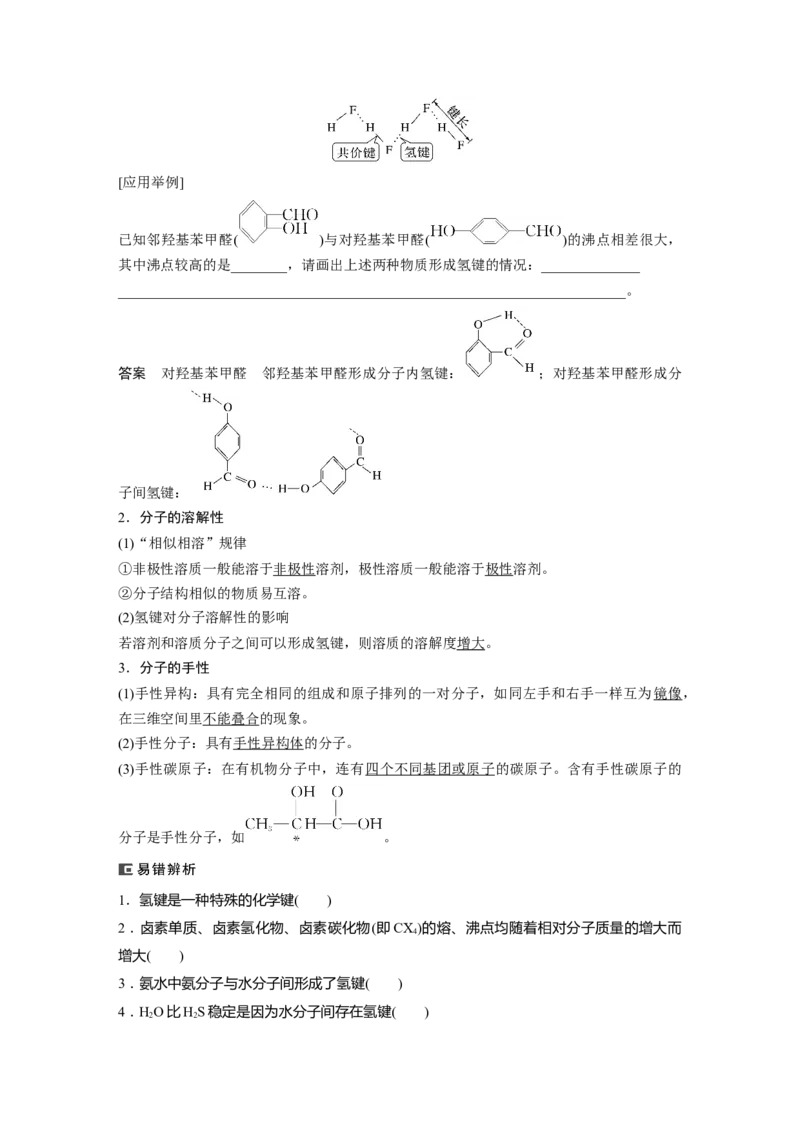
(2)氢键的表示方法(以HF分子间氢键为例)[应用举例]
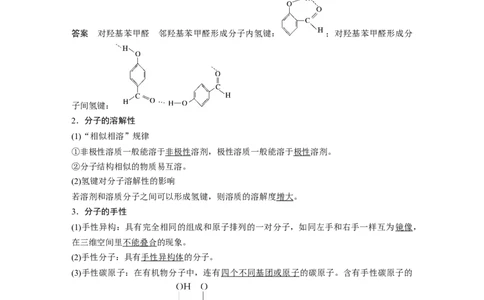
已知邻羟基苯甲醛( )与对羟基苯甲醛( )的沸点相差很大,
其中沸点较高的是________,请画出上述两种物质形成氢键的情况:______________
________________________________________________________________________。
答案 对羟基苯甲醛 邻羟基苯甲醛形成分子内氢键: ;对羟基苯甲醛形成分
子间氢键:
2.分子的溶解性
(1)“相似相溶”规律
①非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶剂。
②分子结构相似的物质易互溶。
(2)氢键对分子溶解性的影响
若溶剂和溶质分子之间可以形成氢键,则溶质的溶解度增大。
3.分子的手性
(1)手性异构:具有完全相同的组成和原子排列的一对分子,如同左手和右手一样互为镜像,
在三维空间里不能叠合的现象。
(2)手性分子:具有手性异构体的分子。
(3)手性碳原子:在有机物分子中,连有四个不同基团或原子的碳原子。含有手性碳原子的
分子是手性分子,如 。
1.氢键是一种特殊的化学键( )
2.卤素单质、卤素氢化物、卤素碳化物(即CX)的熔、沸点均随着相对分子质量的增大而
4
增大( )
3.氨水中氨分子与水分子间形成了氢键( )
4.HO比HS稳定是因为水分子间存在氢键( )
2 25.氢键的存在一定能使物质的熔、沸点升高( )
答案 1.× 2.× 3.√ 4.× 5.×
一、分子间作用力与物质性质原因分析
1.下列说法正确的是( )
A.可燃冰(CH·8H O)中甲烷分子与水分子间形成了氢键
4 2
B.“X—H…Y”三原子不在一条直线上时,不可能形成氢键
C.萃取剂CCl 的沸点高于CH 的沸点
4 4
D.卤素单质、碱金属单质的熔、沸点均随着摩尔质量的增大而升高
答案 C
解析 甲烷分子与水分子间不能形成氢键,A错误;“X—H…Y”三原子不在一条直线上
时,也可能形成氢键,B错误;卤素单质随着摩尔质量的增大,分子间作用力增大,熔、沸
点升高,碱金属单质的熔沸点随着摩尔质量的增大而降低,D错误。
2.下列关于氢键的说法正确的是( )
A.每一个水分子内含有两个氢键
B.冰和干冰分子间都存在氢键
C.DNA中的碱基互补配对是通过氢键来实现的
D.HO是一种非常稳定的化合物是因为水分子间可以形成氢键
2
答案 C
解析 水分子内不存在氢键,氢键存在于水分子之间,故 A错误;干冰为二氧化碳,分子
间不存在氢键,故B错误;HO是一种稳定的化合物,是由于O—H键能较大的原因,与氢
2
键无关,氢键只影响物质的物理性质,故D错误。
3.有关分子的溶解性,解答下列各题:
(1)H O 难溶于CS,简要说明理由_________________________________________。
2 2 2
(2)NH 、CHCHOH、CHCHO都极易溶于水的原因是_______________________
3 3 2 3
________________________________________________________________________。
答案 (1)H O 为极性分子,而CS 为非极性溶剂,根据“相似相溶”规律,HO 难溶于CS
2 2 2 2 2 2
(2)NH 、CHCHOH、CHCHO都是极性分子,且都能与HO形成氢键
3 3 2 3 2
4.有关物质的熔、沸点,解答下列问题。
(1)有机物A( )的结构可以表示为 (虚线表示氢键),而有机物B( )
只能形成分子间氢键。工业上用水蒸气蒸馏法将A和B进行分离,首先被蒸出的成分是____ , 原 因 是 :
________________________________________________________________________
________________________________________________________________________。
(2)苯胺( )与甲苯( )的相对分子质量相近,但苯胺的熔点(-5.9
℃)、沸点(184.4 ℃)分别高于甲苯的熔点(-95.0 ℃)、沸点(111 ℃),原因是
________________________________________________________________________。
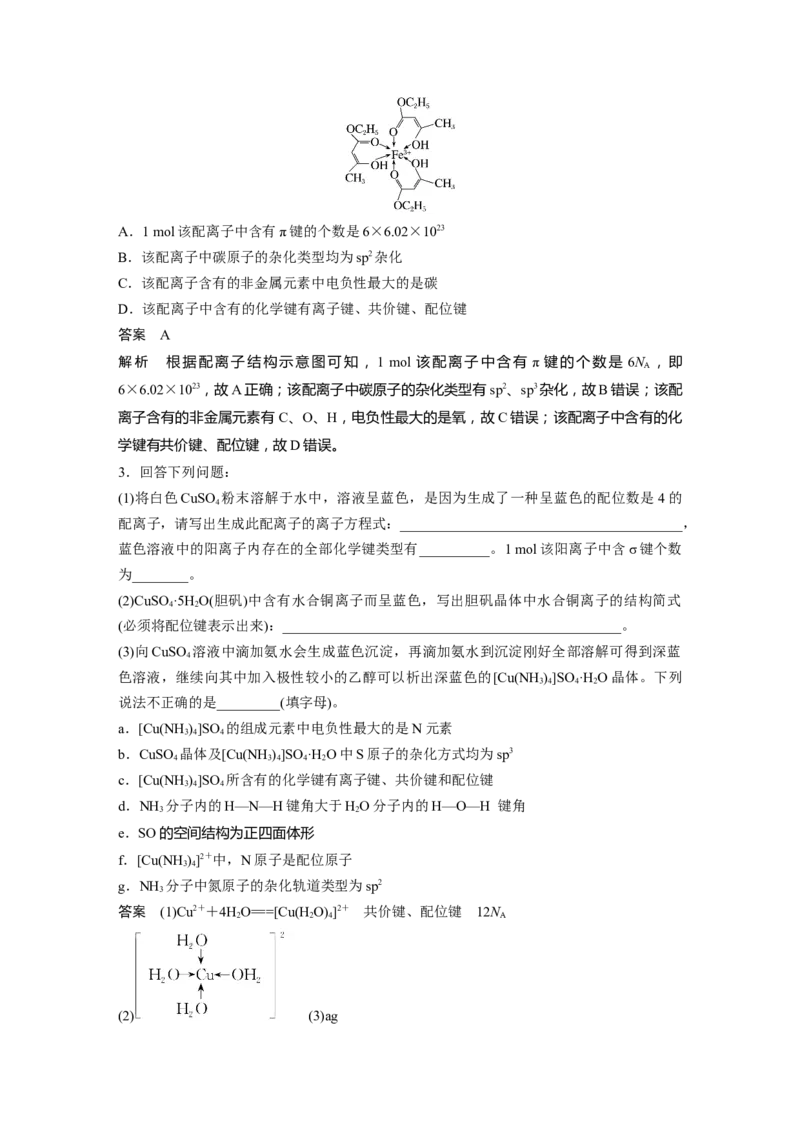
(3)如图为 S 的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为
8
________________________________________________________________________。
(4)在CO 低压合成甲醇反应(CO +3H===CHOH+HO)所涉及的4种物质中,沸点从高到
2 2 2 3 2
低的顺序为________________,原因是_____________________________________
________________________________________________________________________。
答案 (1)A A易形成分子内氢键,B易形成分子间氢键,所以B的沸点比A的高
(2)苯胺分子间存在氢键
(3)S 相对分子质量大,分子间范德华力大
8
(4)H O>CHOH>CO >H HO与CHOH均为极性分子,HO中氢键比甲醇多;CO 与
2 3 2 2 2 3 2 2
H 均为非极性分子,CO 相对分子质量较大,范德华力较大
2 2
二、手性碳的判断
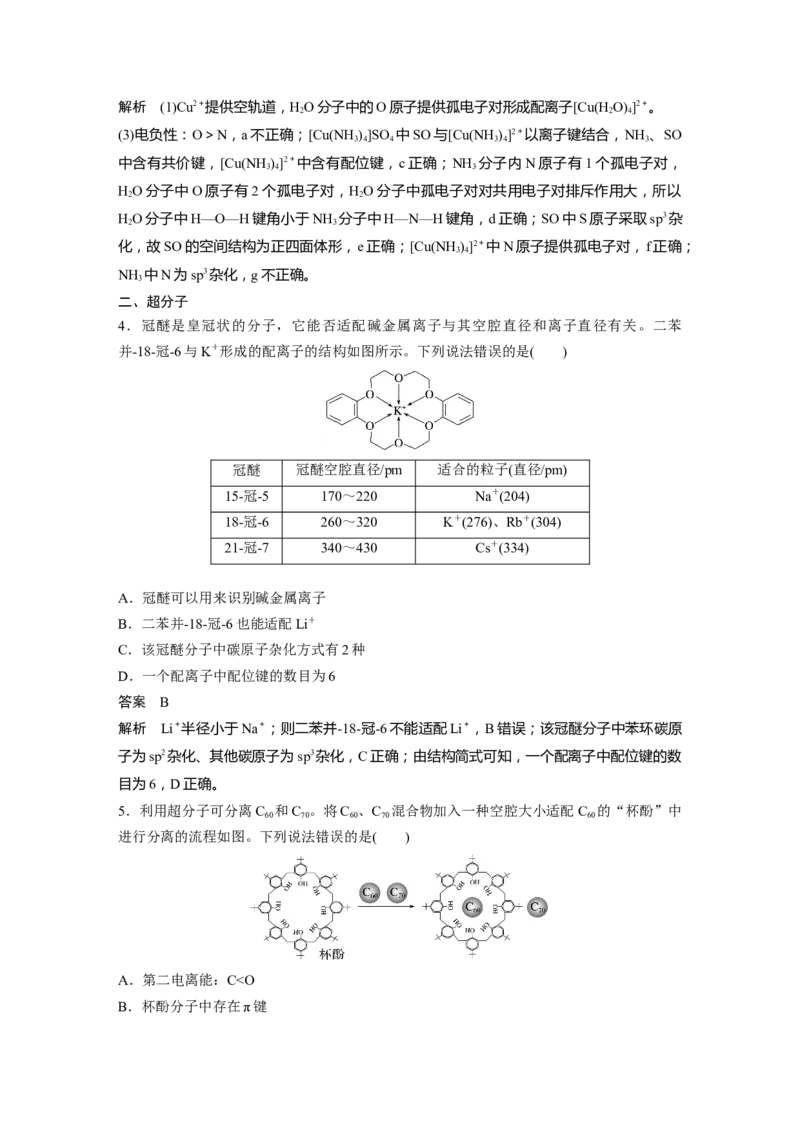
5.(2023·海南,12改编) 闭花耳草是海南传统药材,具有消炎功效。车叶草苷酸是其活性
成分之一,结构简式如图所示。用“*”标出分子中的手性碳原子。
答案考点三 配合物、超分子
1.配位键
(1)形成:由一个原子单方面提供孤电子对而另一个原子接受孤电子对形成的共价键,即
“电子对给予—接受”键被称为配位键。
(2)表示方法:常用“→”来表示配位键,箭头指向接受孤电子对的原子,如 NH可表示为
,在NH中,虽然有一个N—H形成过程与其他3个N—H形成过程不同,
但是一旦形成之后,4个共价键就完全相同。
2.配位化合物
(1)概念:金属离子或原子(称为中心离子或原子)与某些分子或离子(称为配体或配位体)以配
位键结合形成的化合物。如[Cu(NH )]SO :
3 4 4
(2)形成条件
①中心离子或原子:有空轨道,一般是带正电的金属离子,特别是过渡金属离子,如 Fe3
+、Cu2+、Zn2+、Ag+等,但也有电中性的原子等。
②配位体:其中的配位原子(配位体中直接同中心离子或原子配合的原子)有孤电子对。配位
体可以是分子,如CO、NH 、HO等,也可以是离子,如F-、Cl-、Br-、I-、CN-、SCN
3 2
-、OH-等。
(3)配位原子及配位数
①配位原子:配位体中提供孤对电子的原子叫配位原子,如:HO中的O原子,NH 中的N
2 3
原子。
②配位数:作为配位体直接与中心原子结合的离子或分子的数目,即形成的配位键的数目称
为配位数。如:[Cu(NH )]2+的配位数为4,[Ag(NH)]+的配位数为2。
3 4 3 2
(4)内界和外界:配合物分为内界和外界,其中中心离子或原子与配位体组成的部分称为内
界,与内界发生电性匹配的阳离子(或阴离子)称为外界,如:[Cu(NH )]SO 的内界是
3 4 4
[Cu(NH )]2+,外界是SO,配合物在水溶液中电离成内界和外界两部分。
3 4
即:[Cu(NH )]SO ===[Cu(NH )]2++SO,而内界很难电离,其电离程度很小,[Cu(NH )]2+
3 4 4 3 4 3 4Cu2++4NH 。
3
3.超分子
(1)概念
超分子是由两种或两种以上的分子通过分子间相互作用形成的分子聚集体。
(2)超分子内分子间的作用力
多数人认为,超分子内部分子之间通过非共价键相结合,包括氢键、静电作用、疏水作用以
及一些分子与金属离子形成的弱配位键等。
(3)超分子的两个重要特征是分子识别和自组装。
(4)超分子的应用
在分子水平上进行分子设计,有序组装甚至复制出一些新型的分子材料。
1.配位键实质上是一种特殊的共价键( )
2.提供孤电子对的微粒既可以是分子,也可以是离子( )
3.有配位键的化合物就是配位化合物( )
4.配位化合物都很稳定( )
5.在配合物[Co(NH )Cl]Cl 中的Cl-均可与AgNO 反应生成AgCl沉淀( )
3 5 2 3
6.Ni(CO) 是配合物,它是由中心原子与配体构成的( )
4
答案 1.√ 2.√ 3.× 4.× 5.× 6.√
一、配合物
1.关于化学式为[TiCl(H O) ]Cl ·H O的配合物,下列说法正确的是( )
2 5 2 2
A.配位体是Cl-和HO,配位数是8
2
B.中心离子是Ti4+,配离子是[TiCl(H O) ]2+
2 5
C.内界和外界中Cl-的数目比是1∶2
D.在1 mol该配合物中加入足量AgNO 溶液,可以得到3 mol AgCl沉淀
3
答案 C
解析 配合物[TiCl(H O) ]Cl ·H O中配位体是Cl-和HO,配位数是6,故A错误;中心离
2 5 2 2 2
子是Ti3+,故B错误;加入足量AgNO 溶液,外界Cl-与Ag+反应,内界Cl-不与Ag+反应,
3
1 mol该配合物只能生成2 mol AgCl沉淀,故D错误。
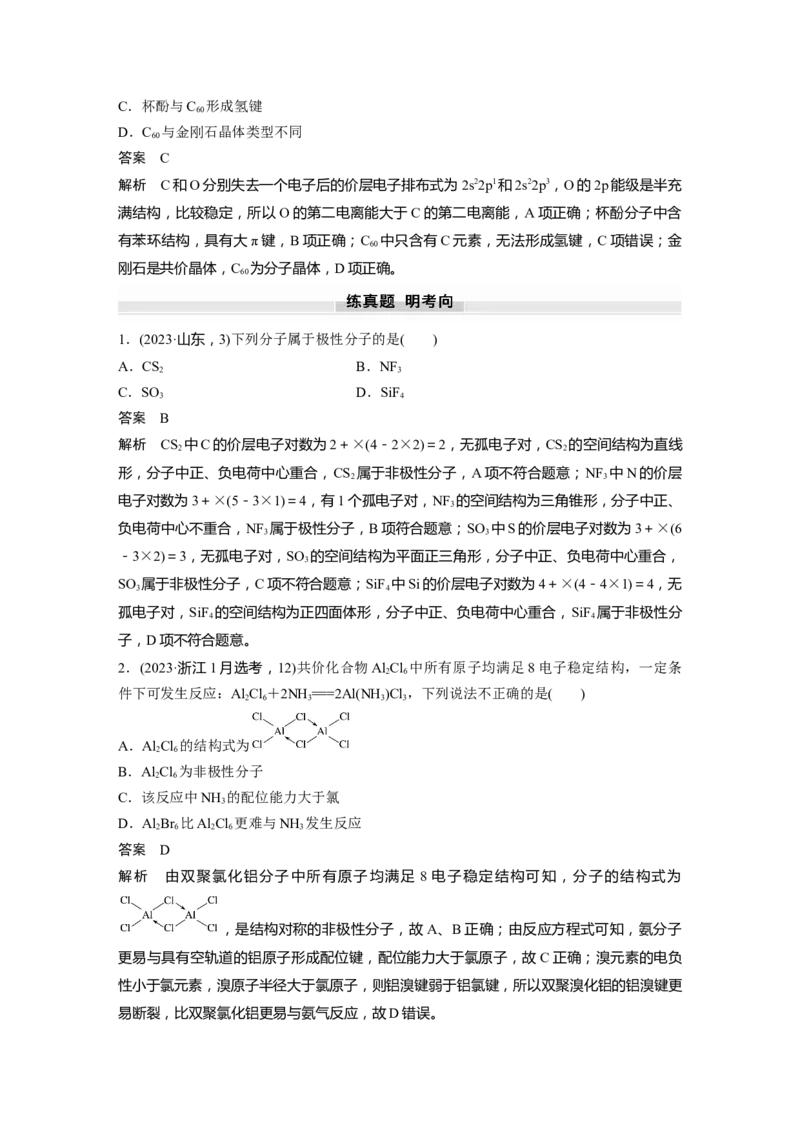
2.(2023·烟台模拟)过渡金属配合物的一些特有性质的研究正受到许多研究人员的关注,因为
这方面的研究无论是理论上还是工业应用上都有重要意义。氯化铁溶液用于检验食用香精乙
酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示。下列有关该配离子的说法正确
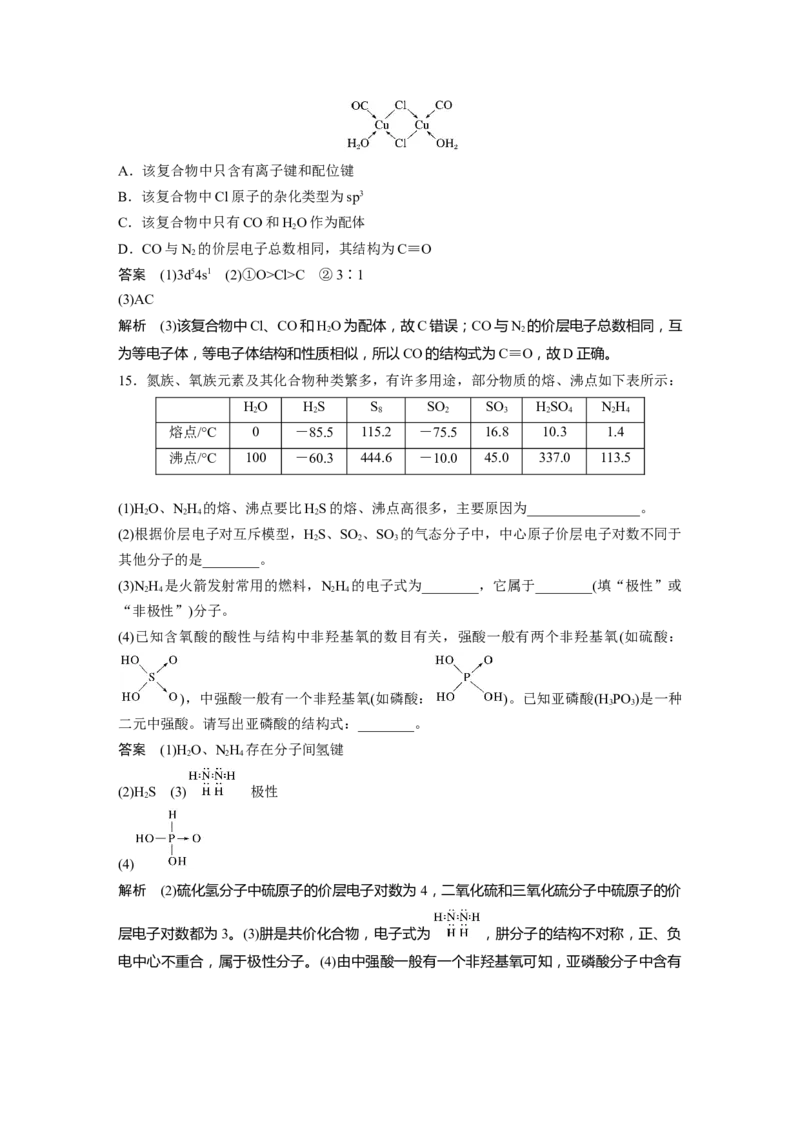
的是( )A.1 mol该配离子中含有π键的个数是6×6.02×1023
B.该配离子中碳原子的杂化类型均为sp2杂化
C.该配离子含有的非金属元素中电负性最大的是碳
D.该配离子中含有的化学键有离子键、共价键、配位键
答案 A
解析 根据配离子结构示意图可知,1 mol 该配离子中含有 π 键的个数是 6N ,即
A
6×6.02×1023,故A正确;该配离子中碳原子的杂化类型有sp2、sp3杂化,故B错误;该配
离子含有的非金属元素有C、O、H,电负性最大的是氧,故C错误;该配离子中含有的化
学键有共价键、配位键,故D错误。
3.回答下列问题:
(1)将白色CuSO 粉末溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配位数是4的
4
配离子,请写出生成此配离子的离子方程式:________________________________________,
蓝色溶液中的阳离子内存在的全部化学键类型有__________。1 mol该阳离子中含σ键个数
为________。
(2)CuSO ·5H O(胆矾)中含有水合铜离子而呈蓝色,写出胆矾晶体中水合铜离子的结构简式
4 2
(必须将配位键表示出来):________________________________________________。
(3)向CuSO 溶液中滴加氨水会生成蓝色沉淀,再滴加氨水到沉淀刚好全部溶解可得到深蓝
4
色溶液,继续向其中加入极性较小的乙醇可以析出深蓝色的[Cu(NH )]SO ·H O晶体。下列
3 4 4 2
说法不正确的是_________(填字母)。
a.[Cu(NH )]SO 的组成元素中电负性最大的是N元素
3 4 4
b.CuSO 晶体及[Cu(NH )]SO ·H O中S原子的杂化方式均为sp3
4 3 4 4 2
c.[Cu(NH )]SO 所含有的化学键有离子键、共价键和配位键
3 4 4
d.NH 分子内的H—N—H键角大于HO分子内的H—O—H 键角
3 2
e.SO的空间结构为正四面体形
f.[Cu(NH )]2+中,N原子是配位原子
3 4
g.NH 分子中氮原子的杂化轨道类型为sp2
3
答案 (1)Cu2++4HO===[Cu(H O) ]2+ 共价键、配位键 12N
2 2 4 A
(2) (3)ag解析 (1)Cu2+提供空轨道,HO分子中的O原子提供孤电子对形成配离子[Cu(H O) ]2+。
2 2 4
(3)电负性:O>N,a不正确;[Cu(NH )]SO 中SO与[Cu(NH )]2+以离子键结合,NH 、SO
3 4 4 3 4 3
中含有共价键,[Cu(NH )]2+中含有配位键,c正确;NH 分子内N原子有1个孤电子对,
3 4 3
HO分子中O原子有2个孤电子对,HO分子中孤电子对对共用电子对排斥作用大,所以
2 2
HO分子中H—O—H键角小于NH 分子中H—N—H键角,d正确;SO中S原子采取sp3杂
2 3
化,故SO的空间结构为正四面体形,e正确;[Cu(NH )]2+中N原子提供孤电子对,f正确;
3 4
NH 中N为sp3杂化,g不正确。
3
二、超分子
4.冠醚是皇冠状的分子,它能否适配碱金属离子与其空腔直径和离子直径有关。二苯
并-18-冠-6与K+形成的配离子的结构如图所示。下列说法错误的是( )
冠醚 冠醚空腔直径/pm 适合的粒子(直径/pm)
15-冠-5 170~220 Na+(204)
18-冠-6 260~320 K+(276)、Rb+(304)
21-冠-7 340~430 Cs+(334)
A.冠醚可以用来识别碱金属离子
B.二苯并-18-冠-6也能适配Li+
C.该冠醚分子中碳原子杂化方式有2种
D.一个配离子中配位键的数目为6
答案 B
解析 Li+半径小于Na+;则二苯并-18-冠-6不能适配Li+,B错误;该冠醚分子中苯环碳原
子为sp2杂化、其他碳原子为sp3杂化,C正确;由结构简式可知,一个配离子中配位键的数
目为6,D正确。
5.利用超分子可分离C 和C 。将C 、C 混合物加入一种空腔大小适配C 的“杯酚”中
60 70 60 70 60
进行分离的流程如图。下列说法错误的是( )
A.第二电离能:CPH NH 分子间氢键强于PH 分子间作用力
3 3 3 3
C Cl—Cl的键长小于Br—Br的键长 Cl—Cl的键能小于Br—Br的键能
烷基(R—)越长推电子效应越大,使羧基
D 酸性:CHCOOH>CH CHCOOH
3 3 2
中羟基的极性越小,羧酸的酸性越弱
答案 D
解析 水分子中O上有2个孤电子对,氨分子中N上有1个孤电子对,孤电子对数越多,
对成键电子对的排斥作用越大,键角越小,所以水分子中键角比氨分子中键角小,A错误;
N与P为同主族元素,N的非金属性比P强,则热稳定性:NH >PH ,分子的热稳定性与分
3 3
子间的作用力无关,B错误;Cl的原子半径小于Br的原子半径,则Cl—Cl的键长小于Br—Br的键长,Cl—Cl的键能大于Br—Br的键能,C错误。
9.(2023·山东滨州模拟)螯合剂能与人体内有毒的金属离子结合形成稳定螯合物,从而治疗
与急性或慢性中毒相关的损伤。乙二胺四乙酸(EDTA)是常见的螯合剂之一,其四价阴离子
形成的螯合物结构如图。下列说法正确的是( )
A.原子半径:O>N>C>H
B.N、C、O的氢化物分子间均存在氢键
C.M的配位数为6,配位原子为 N和O
D.螯合物中每两个氮碳键(N—C)的夹角均为107°
答案 C
解析 同周期元素,从左到右原子半径依次减小,则原子半径:C>N>O,故A错误;碳元
素的氢化物不能形成分子间氢键,故B错误;由图可知,螯合物中Mn+与氮原子和氧原子
形成配位键,配位数为6,故C正确;由图可知,螯合物中氮原子的杂化方式都为sp3杂化,
孤电子对用于形成配位键,则氮碳键的夹角均大于107°,故D错误。
10.吡啶( )含有与苯环类似的大π键,下列说法或实验操作不正确的是( )
A.吡啶中N原子的价层孤电子对占据了一个未参与杂化的p轨道
B.吡啶是极性分子且能与水形成氢键,故吡啶在水中的溶解度比苯大
C.除去苯中含有的少量吡啶:用盐酸洗涤、分液、干燥有机层
D. 、 的碱性随N原子电子云密度的增大而增强,故 碱性较强
答案 A
解析 吡啶( )含有与苯环类似的大π键,则吡啶中N原子也发生sp2杂化,所以价层孤
电子对占据了一个参与杂化的p轨道,A不正确;吡啶是极性分子且能与水分子间形成氢键,
而苯为非极性分子,故吡啶在水中的溶解度比苯大,B正确;因为吡啶呈碱性,能与盐酸反
应生成水溶性物质,所以除去苯中含有的少量吡啶,可用盐酸洗涤、分液、干燥有机层,C
正确;烷基是推电子基团, 分子中N原子电子云密度比 大,故 碱性较强,
D正确。11.(2023·浙江嘉兴模拟)BF(三氟化硼)熔点-127 ℃,沸点-100 ℃,水解生成HBO(硼
3 3 3
酸,结构如图)和HBF (氟硼酸),与氨气相遇立即生成白色的BF·NH (氨合三氟化硼)固体。
4 3 3
下列说法不正确的是( )
A.BF 和BF中心硼原子杂化方式不同
3
B.1 mol H BO 晶体含有6 mol氢键
3 3
C.HBO 显酸性原因:HBO+HOB(OH)+H+
3 3 3 3 2
D.BF·NH 结构式为
3 3
答案 B
解析 BF 中心原子价层电子对数为3+×(3-3×1)=3,采取sp2杂化,BF中心原子价层电
3
子对数为4+×(3+1-4×1)=4,采取sp3杂化,二者中心硼原子杂化方式不同,故A正确
1个HBO 参与6个氢键的形成,每个氢键形成于两个硼酸分子之间,则1 mol H BO 晶体
3 3 3 3
中含有6 mol×=3 mol氢键,故B错误;HBO 是一元弱酸,在水溶液中电离产生H+使溶
3 3
液呈酸性,电离方程式为HBO +HOB(OH)+H+,故C正确;BF·NH 中N原子为sp3
3 3 2 3 3
杂化,N原子上有一个孤电子对,B原子为sp3杂化,提供一个空轨道,与NH 形成配位键,
3
BF·NH 结构式为 ,故D正确。
3 3
12.(2023·江苏徐州模拟)我国科学家成功利用CO 人工合成淀粉,使淀粉生产方式从农耕种
2
植转变为工业制造成为可能,其部分转化过程如下:
已知:ZnO是两性氧化物;ZrCl 水解可制得ZrO。
4 2下列有关物质的说法正确的是( )
A.H 和HCHO均属于非极性分子
2
B.CO 的空间结构为V形
2
C.HO 和HO中均含极性键和非极性键
2 2 2
D.CHOH的熔点高于HCHO
3
答案 D
解析 HCHO中C原子价层电子对数为3+=3,不含孤电子对,为平面三角形结构,正、
负电荷中心不重合,为极性分子,H 为直线形分子,为非极性分子,选项A错误;CO 分
2 2
子中C原子的价层电子对数为2+=2,无孤电子对,空间结构为直线形,选项B错误;
HO不含非极性键,选项C错误;分子晶体相对分子质量越大,熔点越高,分子间含有氢键
2
时熔点较高,CHOH分子间存在氢键,则熔点为HCHOCl>C ②3∶1
(3)AC
解析 (3)该复合物中Cl、CO和HO为配体,故C错误;CO与N 的价层电子总数相同,互
2 2
为等电子体,等电子体结构和性质相似,所以CO的结构式为C≡O,故D正确。
15.氮族、氧族元素及其化合物种类繁多,有许多用途,部分物质的熔、沸点如下表所示:
HO HS S SO SO HSO NH
2 2 8 2 3 2 4 2 4
熔点/°C 0 -85.5 115.2 -75.5 16.8 10.3 1.4
沸点/°C 100 -60.3 444.6 -10.0 45.0 337.0 113.5
(1)H O、NH 的熔、沸点要比HS的熔、沸点高很多,主要原因为________________。
2 2 4 2
(2)根据价层电子对互斥模型,HS、SO 、SO 的气态分子中,中心原子价层电子对数不同于
2 2 3
其他分子的是________。
(3)N H 是火箭发射常用的燃料,NH 的电子式为________,它属于________(填“极性”或
2 4 2 4
“非极性”)分子。
(4)已知含氧酸的酸性与结构中非羟基氧的数目有关,强酸一般有两个非羟基氧(如硫酸:
),中强酸一般有一个非羟基氧(如磷酸: )。已知亚磷酸(H PO )是一种
3 3
二元中强酸。请写出亚磷酸的结构式:________。
答案 (1)H O、NH 存在分子间氢键
2 2 4
(2)H S (3) 极性
2
(4)
解析 (2)硫化氢分子中硫原子的价层电子对数为4,二氧化硫和三氧化硫分子中硫原子的价
层电子对数都为3。(3)肼是共价化合物,电子式为 ,肼分子的结构不对称,正、负
电中心不重合,属于极性分子。(4)由中强酸一般有一个非羟基氧可知,亚磷酸分子中含有一个非羟基氧和2个羟基,有一个氢原子直接与磷原子相连,结构式为 。