文档内容
驻马店市高三阶段性检测
化学
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要
求的。
1.化学与生活密切相关,下列物质不是由金属材料制成的是( )
A.青铜雁鱼灯 B.蒜头纹银盒 C.黄河大铁牛 D.秦朝兵马俑
2.氮及其化合物在生产生活中具有广泛的应用。在给定条件下,下列选项所示物质间的转化能实现的是(
)
A. B.
C. D.
3.下列叙述正确的是( )
A.我国科学家发现飞尘颗粒物中含 核素,其中子数与质子数之差为30
B.钠在过量的氧气中燃烧生成的产物的电子式为
C.氧是地壳中最丰富、分布最广的元素,简单氧离子的结构示意图为
D.标准状况下,密度约为 的烃的结构简式为
4.香港回归祖国25周年之际,筹备多年的香港故宫文化博物馆也正式对公众开放。清代圆雕玉器的代表作
——带皮白玉桐荫仕女图山子(如图)也在这次展览中与观众见面。下列叙述正确的是( )
已知:汉白玉就是纯白色的大理石,是一种石灰石形态,内含内光晶体,主要由 、 和
组成,也包含少量 、 等。
A. 、 、 、 、 五种化合物在高温下都能稳定存在B. 、 均既能与强酸反应又能与强碱反应
C.“带皮白玉桐萌仕女图山子”可被酸雨腐蚀
D.将汉白玉雕刻成该文物的样式的过程中发生了化学变化
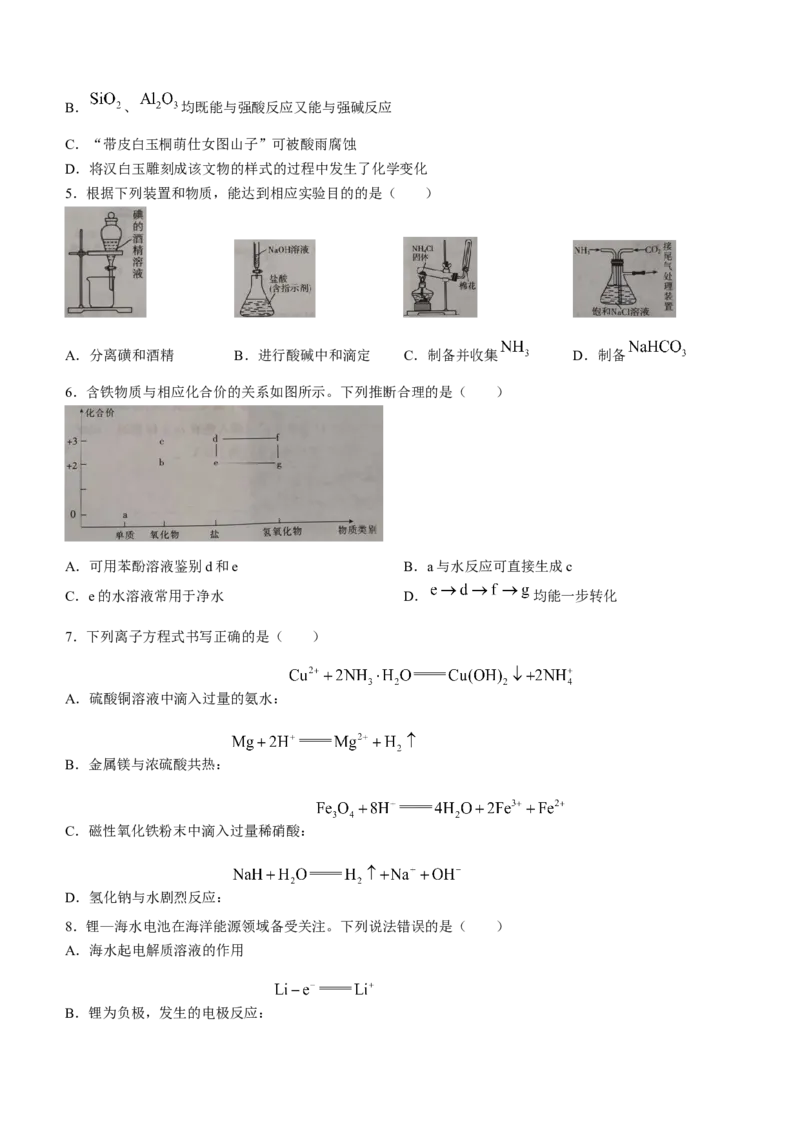
5.根据下列装置和物质,能达到相应实验目的的是( )
A.分离磺和酒精 B.进行酸碱中和滴定 C.制备并收集 D.制备
6.含铁物质与相应化合价的关系如图所示。下列推断合理的是( )
A.可用苯酚溶液鉴别d和e B.a与水反应可直接生成c
C.e的水溶液常用于净水 D. 均能一步转化
7.下列离子方程式书写正确的是( )
A.硫酸铜溶液中滴入过量的氨水:
B.金属镁与浓硫酸共热:
C.磁性氧化铁粉末中滴入过量稀硝酸:
D.氢化钠与水剧烈反应:
8.锂—海水电池在海洋能源领域备受关注。下列说法错误的是( )
A.海水起电解质溶液的作用
B.锂为负极,发生的电极反应:C.锂电极应与海水直接接触
D.正极反应式:
9.设 是阿伏加德罗常数的值。下列说法正确的是( )
A.1LPH=1的硫酸溶液中含有 的数目为
B.标准状况下, 中含有的质子数为
C.一定条件下,1molFe分别在足量的氧气、氯气中燃烧,转移电子数均为
D.用惰性电极电解足量 溶液时,若阴极增重12.8g,则理论上阳极产生的气体分子数为
10.T℃时,在恒容密闭容器中通入一定量的 和 ,发生反应:
,测得 和 的浓度变化如表:
时间/s 0 2 4 6
1.00 0.25 0.10 0.10
4.60 1.6 1.00 1.00
下列说法中一定正确的是( )
A.若升高温度,则反应达到平衡的时间将缩短
B.0~2s内,用 表示的平均速率为
C.若使用催化剂,则2s时的 将大于
D.4s时,反应恰好达到该条件下的最大限度,且气体压强不再变化
11.根据下列实验现象和有关数据,推断错误的是( )
A.原混合物中含 B.白色沉淀M为
C. 和 都是非极性分子 D.气体R是大气污染物
12.根据下列实验活动与现象得出的结论正确的是( )
选项 实验活动与现象 结论
A
溶液中依次滴入稀硫酸、KSCN溶液后,溶液变 已变质红色
B 向某待测液中滴加盐酸,产生白色沉淀
该待测液中一定含有
C
溶于稀硫酸得到红色固体和蓝色溶液 具有氧化性和还原性
D
向少量酸性 溶液中滴入适量白葡萄酒,溶液褪色 白葡萄酒中一定含有
13.X、Y、Z、W是原子序数依次增大的前20号元素,由它们组成的化合物的结构简式如图,其中 与
位于相邻主族,下列说法正确的是( )
A.原子半径:
B. 的最高价氧化物对应的水化物为强酸
C.化合物WYX中只含有离子键
D.W与Y形成的化合物不可能具有强氧化性
14.西北干旱地区地下水丰富,某同学取某山区的地下水进行检验。已知水中存在 、 、 、
、 、 、 、 、 中的五种离子,且浓度均为 。检验过程如图所示
(部分产物省略),溶液 与地下水 所含的阴离子种类相同。
下列说法正确的是( )
A.气体甲转变为气体乙的过程中发生了复分解反应
B.该地下水中可能含有 ,一定没有
C.该地下水中含两种阳离子和三种阴离子
D.将足量的气体乙分别通入沉淀甲和沉淀乙的悬浊液中,沉淀甲溶解,沉淀乙不溶解
二、非选择题:本题共4小题,共58分。
15.(14分)X、Y、Z、M、N五种主族元素位于前四周期,且原子序数依次增大。其中X、Y、Z、M为短
周期元素,这四种元素的最外层电子数之和为16,其中M的最外层电子数为Z的两倍,Y、M位于同一主族,
X、N也位于同一主族,只有Z、M位于同一周期。回答下列问题:
(1)N位于第______周期______族。
(2)Y______(填元素符号,下同),Y、Z、M中原子半径最大的是______。
(3)沸点: ______(填“>”或“<”) .
(4)M的最高价氧化物对应水化物的稀溶液与Z反应时,氧化产物的化学式为______。(5) 可作为氧气源用于呼吸面罩, 与水反应的化学方程式为______,若反应过程中转移0.3mol电
子,则得到标准状况下氧化产物的体积为______L。
(6)加热时,单质M与NYX反应的离子方程式为______,该反应中氧化剂与还原剂的物质的量之比为
______。
16.(14分)尿素 是目前使用量较大的一种化学氮肥。某化学实验小组以尿素为原料制备
(水合肼)并验证水合肼还原性的实验流程如图1所示:
已知① 沸点用196.6℃;
② 沸点为118℃,且能与NaClO剧烈反应生成 。
I. 的制备
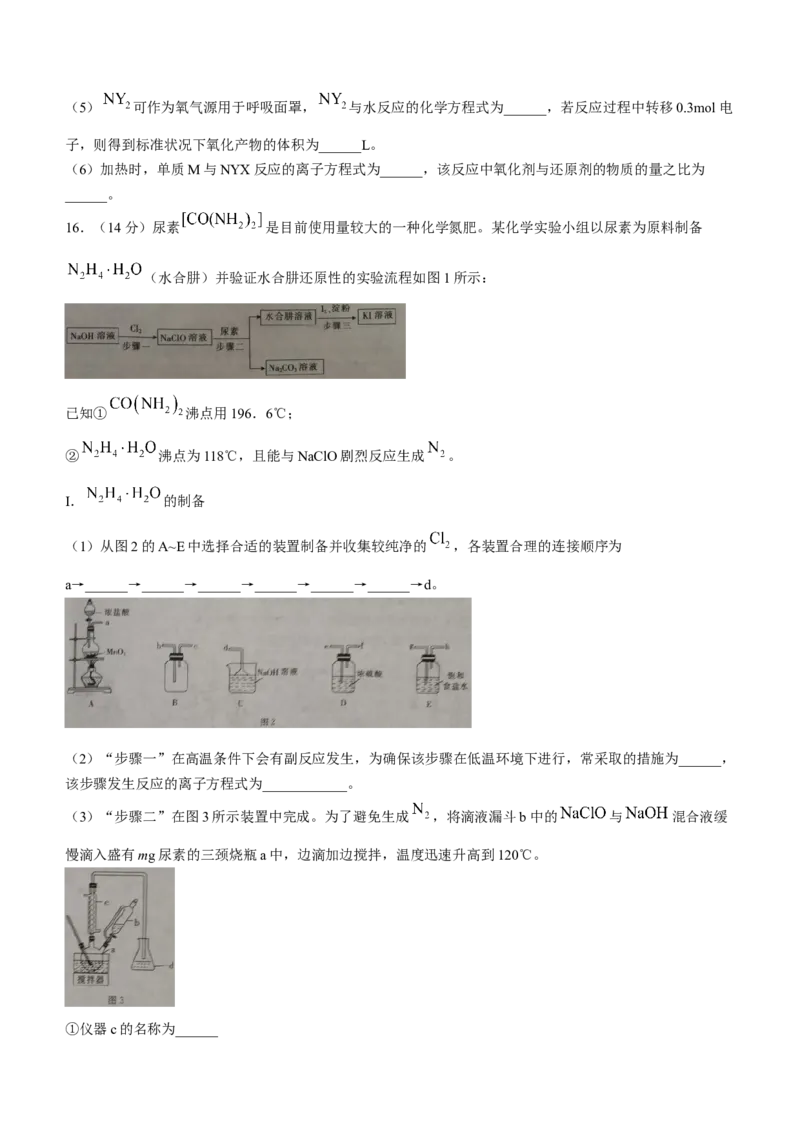
(1)从图2的A~E中选择合适的装置制备并收集较纯净的 ,各装置合理的连接顺序为
a→______→______→______→______→______→______→d。
(2)“步骤一”在高温条件下会有副反应发生,为确保该步骤在低温环境下进行,常采取的措施为______,
该步骤发生反应的离子方程式为____________。
(3)“步骤二”在图3所示装置中完成。为了避免生成 ,将滴液漏斗b中的 与 混合液缓
慢滴入盛有mg尿素的三颈烧瓶a中,边滴加边搅拌,温度迅速升高到120℃。
①仪器c的名称为______②生成水合肼的化学方程式为____________。
Ⅱ.验证 的还原性
(4)将“步骤二”制得的水合肼配成1000mL落液,移出25mL于锥形瓶中,滴加2滴淀粉溶液,用
的 溶液滴定,当滴定完全时,消耗 溶液VmL。
①滴定过程中水合肼被氧化为 ,反应的化学方程式为_______________________。
②配成的水合肼的浓度 ______ (用含V的代数式表示)。
③ 的产率为____________(用含m、V的代数式表示)。
17.(15分)已知: 为短周期主族元素中某元素的氧化物。根据下列信息,回答相关问题:
(1)若镁条在 中燃烧生成黑色粉末(单质)和白色粉末,则 的化学式为______。
(2)若常温下, 能与氢氟酸反应生成一种气体和一种液态化合物。 和纯碱混合在铁坩埚中熔融生
成R的含氧酸盐, 和纯碱反应的化学方程式为_______________________。
(3)若向酸性 溶液,含酚酞的烧碱溶液中分别通入无色气体 ,两溶液颜色均逐渐褪去。酸性
溶液吸收 的离子方程式为_______________________;向烧碱溶液中通入过量 的离子方程
式为_______________________。
(4)设 为阿伏加德罗常数的值。若烧杯中固体W为银粉,向该烧杯中通入 ,固体W逐渐溶解(如
图所示),则 的化学式为______,向某密闭容器中充入2molRO和 ,则产物的分子数______
(填“大于”、“小于”或“等于”) 。
(5)若 是一种绿色饮用水消毒剂,则 具有______性而能杀菌消毒;工业上,常用+5价R的含氧
酸的钠盐和HR的浓溶液在常温下反应制备气态 ,同时还有R单质和水生成,该反应的离子方程式为
______________________________。18.(15分)我国科学家开发催化剂 ,来提高 燃料电池的性能。某小组以含镍废料(主要
含Ni、NiO,以及少量CuO、FeO, 、MgO、ZnO、 和 等)为原料提取镍的流程如下:
请回答下列问题:
(1)“酸浸”中产生了一种还原性气体,它是______(填化学式)。
(2)“固体2”中除CuS、ZnS外,还可能含硫单质等物质,生成硫单质的离子方程式为
__________________。
(3)为提高原料利用率,“电沉积”得到的“废液”可以循环用于______(填名称)工序。
(4)在“除铁铝”中, 作______(填“氧化剂”或“还原剂”), 最终转化为______(填化学
式)。
(5)可以通过电解法提纯镍,粗镍作______(填“阳”或“阴”)极,阴极的电极反应式为______。
(6)氢氧化氧镍(NiOOH)是镍电池的正极活性材料。在 溶液加入NaOH和NaCIO混合液可以制备
NiOOH,其离子方程式为__________________。
驻马店市高三阶段性检测
化学参考答案
1.D 2.A 3.C 4.
5.D 6.A 7.D 8.C
9.D 10.A 11.A 12.C
13.A 14.C
15.(1)四(1分);IA(1分) (2)O(1分);Al(1分)
(3)>(1分)
(4) (写“ ”也给分,1分)
(5) (2分);6.72(分)
(6) (2分);2:1(2分)
16.(1)g;h;e;f;b;c(2分)(2)冰水浴(或冷水浴,1分); (2分)
(3)①(球形)冷凝管(1分)
② (不打“↑”不扣分,2分)
(4)① (2分)
② (2分) ③ (2分)
17.(1) (2分)
(2) (2分)
(3) (2分); (2分)
(4) (2分);小于(2分)
(5)强氧化(1分); (2分)
18.(1) (2分)
(2) (2分)
(3)酸浸(2分) (4)氧化剂(2分); (2分)
(5)阳(1分); (2分)