文档内容
热点专项 平衡常数(或速率常数)的计算及应用
目录
01考情透视·目标导航........................................................................................................................
02知识导图·思维引航........................................................................................................................
03核心精讲·题型突破........................................................................................................................
题型一 速率常数及相关计算..................................................................................................................................
【真题研析】..............................................................................................................................................................
【核心精讲】..............................................................................................................................................................
1.速率常数................................................................................................................................................................
2.速率方程................................................................................................................................................................
3.速率常数与化学平衡之间的关系........................................................................................................................
【命题预测】..............................................................................................................................................................
考向1速率常数概念与计算......................................................................................................................................
考向2速率常数综合应用..........................................................................................................................................
题型二 压强平衡常数及相关计算..........................................................................................................................
【真题研析】..............................................................................................................................................................
【核心精讲】..............................................................................................................................................................
1.气体的分压p(B)....................................................................................................................................................
2.分压平衡常数(K ).................................................................................................................................................
P
3.常用的四个公式....................................................................................................................................................
【命题预测】..............................................................................................................................................................
考向1分压平衡常数的计算......................................................................................................................................
考向2平衡常数K(lg K)与T()关系曲线...................................................................................................................
考点要求 考题统计 考情分析
速率常数 压强平衡常数与速率常数是在化学平
2024·山东卷,15,4分;2024·河北
及相关计 衡常数基础上的延伸和拓展,它是定卷,17(2);2023•山东卷,20(2);2022•
算
河北省选择性卷,11; 量研究平衡移动的重要手段。各平衡
常数的应用和计算是高考的热点和难
2024·福建卷,14(3);2024· 贵州卷, 点。以化学平衡原理为指导,以判断
17(5);2024·湖南卷,18(3);2024·湖北 平衡移动的方向为线索,以勒夏特列
原理和相关守恒定律为计算依据,以
卷,17(2);2023•全国乙卷,28(3)(4);
压强平衡 各平衡常数之间的联系为突破口,联
2023•湖北省选择性考试,19(4);2023•
常数及相 系元素及化合物知识,串点成线,结
辽宁省选择性考试,18(2)(ⅲ);2023•
关计算 线成网,形成完整的认识结构体系,
全国新课标卷,29(4);2023·全国乙
就能势如破竹,水到渠成。
卷,28(3)(4);2022·全国甲卷,28(1)
(2);2022·湖南,16(1);
题型一 速率常数及相关计算
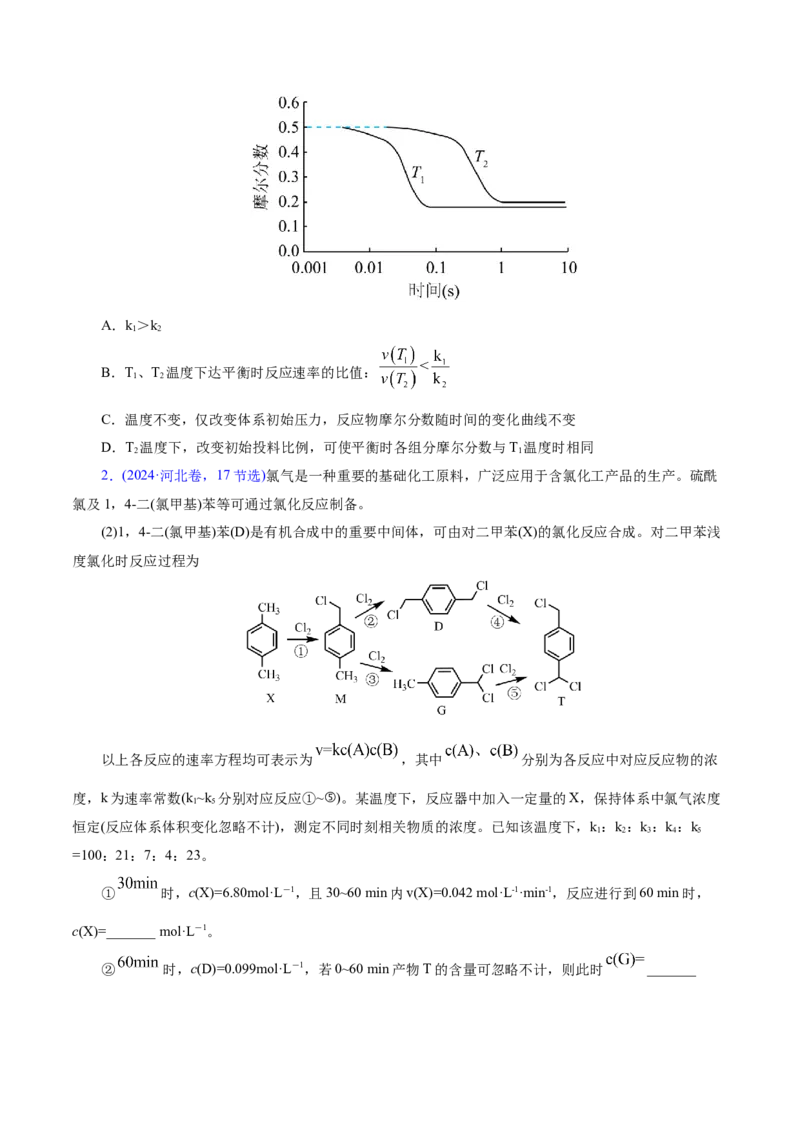
1.(2024·山东卷,15,4分)(双选)逆水气变换反应:CO(g)+H(g) CO(g)+HO(g) ΔH>0。一
2 2 2
定压力下,按CO,H 物质的量之比n(CO):n(H )=1:1投料,T、T 温度时反应物摩尔分数随时间变化
2 2 2 2 1 2
关系如图所示。已知该反应的速率方程为v=kc0.5(H )c(CO),T、T 温度时反应速率常数k分别为k、k。
2 2 1 2 1 2
下列说法错误的是( )A.k>k
1 2
B.T、T 温度下达平衡时反应速率的比值:
1 2
C.温度不变,仅改变体系初始压力,反应物摩尔分数随时间的变化曲线不变
D.T 温度下,改变初始投料比例,可使平衡时各组分摩尔分数与T 温度时相同
2 1
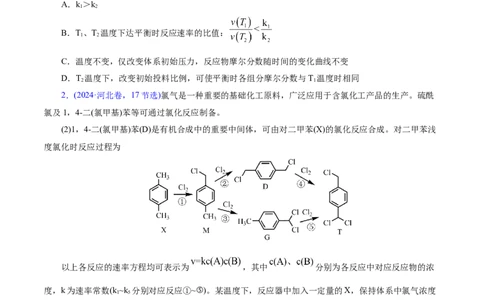
2.(2024·河北卷,17节选)氯气是一种重要的基础化工原料,广泛应用于含氯化工产品的生产。硫酰
氯及1,4-二(氯甲基)苯等可通过氯化反应制备。
(2)1,4-二(氯甲基)苯(D)是有机合成中的重要中间体,可由对二甲苯(X)的氯化反应合成。对二甲苯浅
度氯化时反应过程为
以上各反应的速率方程均可表示为 ,其中 分别为各反应中对应反应物的浓
度,k为速率常数(k~k 分别对应反应①~⑤)。某温度下,反应器中加入一定量的X,保持体系中氯气浓度
1 5
恒定(反应体系体积变化忽略不计),测定不同时刻相关物质的浓度。已知该温度下,k:k:k:k:k
1 2 3 4 5
=100:21:7:4:23。
① 时,c(X)=6.80mol·L-1,且30~60 min内v(X)=0.042 mol·L-1·min-1,反应进行到60 min时,
c(X)=_______ mol·L-1。
② 时,c(D)=0.099mol·L-1,若0~60 min产物T的含量可忽略不计,则此时 _______mol·L-1;60 min后,随T的含量增加, _______(填“增大”“减小”或“不变”)。
3.(2023•山东卷,20节选)一定条件下,水气变换反应CO+HO CO+H 的中间产物是
2 2 2
HCOOH。为探究该反应过程,研究 水溶液在密封石英管中的分子反应:
Ⅰ.HCOOH CO+HO(快)
2
Ⅱ.HCOOH CO+H (慢)
2 2
研究发现,在反应Ⅰ、Ⅱ中,H+仅对反应Ⅰ有催加速作用;反应Ⅰ速率远大于反应Ⅱ,近似认为反应
Ⅰ建立平衡后始终处于平衡状态。忽略水电离,其浓度视为常数。
(2)反应Ⅰ正反应速率方程为: ,k为反应速率常数。T 温度下,HCOOH电离
1
平衡常数为K,当HCOOH平衡浓度为x mol·L-1时,H+浓度为_____ mol·L-1,此时反应Ⅰ应速率 _____
a
mol·L-1·h -1 (用含K、x和k的代数式表示)。
a
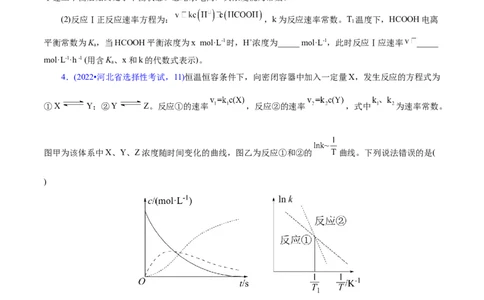
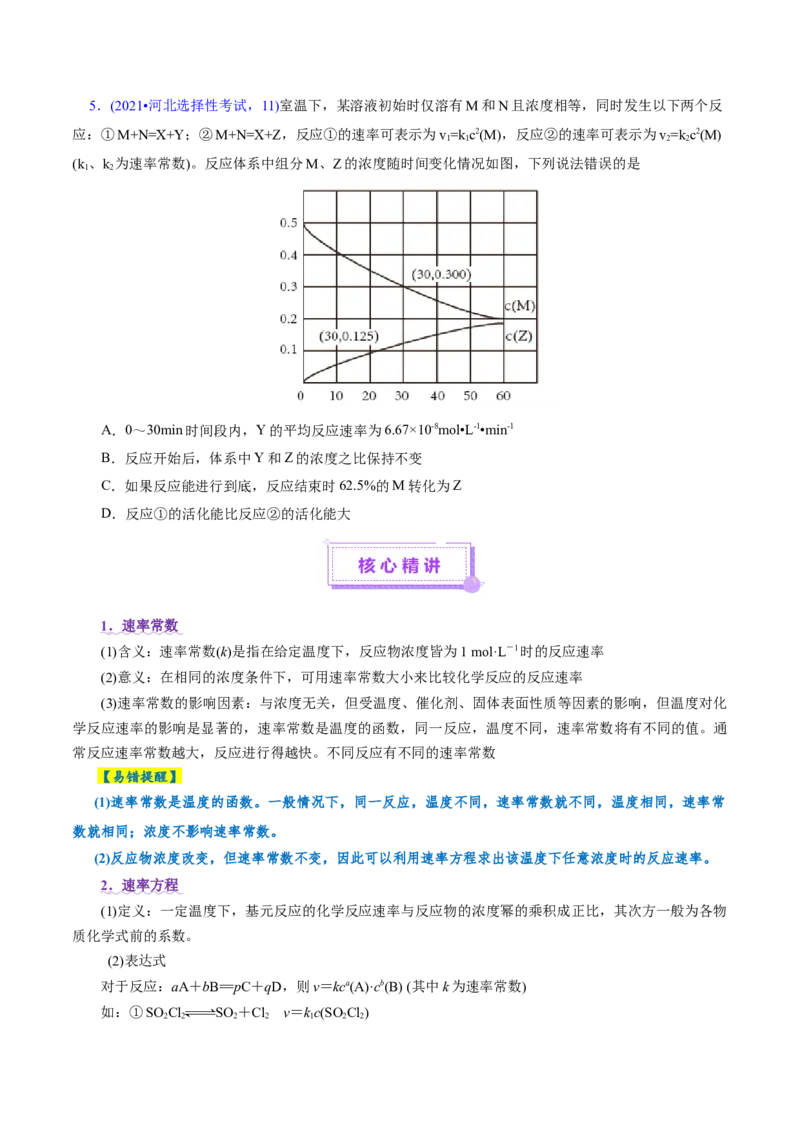
4.(2022•河北省选择性考试,11)恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式为
①X Y;②Y Z。反应①的速率 ,反应②的速率 ,式中 为速率常数。
图甲为该体系中X、Y、Z浓度随时间变化的曲线,图乙为反应①和②的 曲线。下列说法错误的是(
)
A.随 的减小,反应①、②的速率均降低
B.体系中
C.欲提高Y的产率,需提高反应温度且控制反应时间
D.温度低于T 时,总反应速率由反应②决定
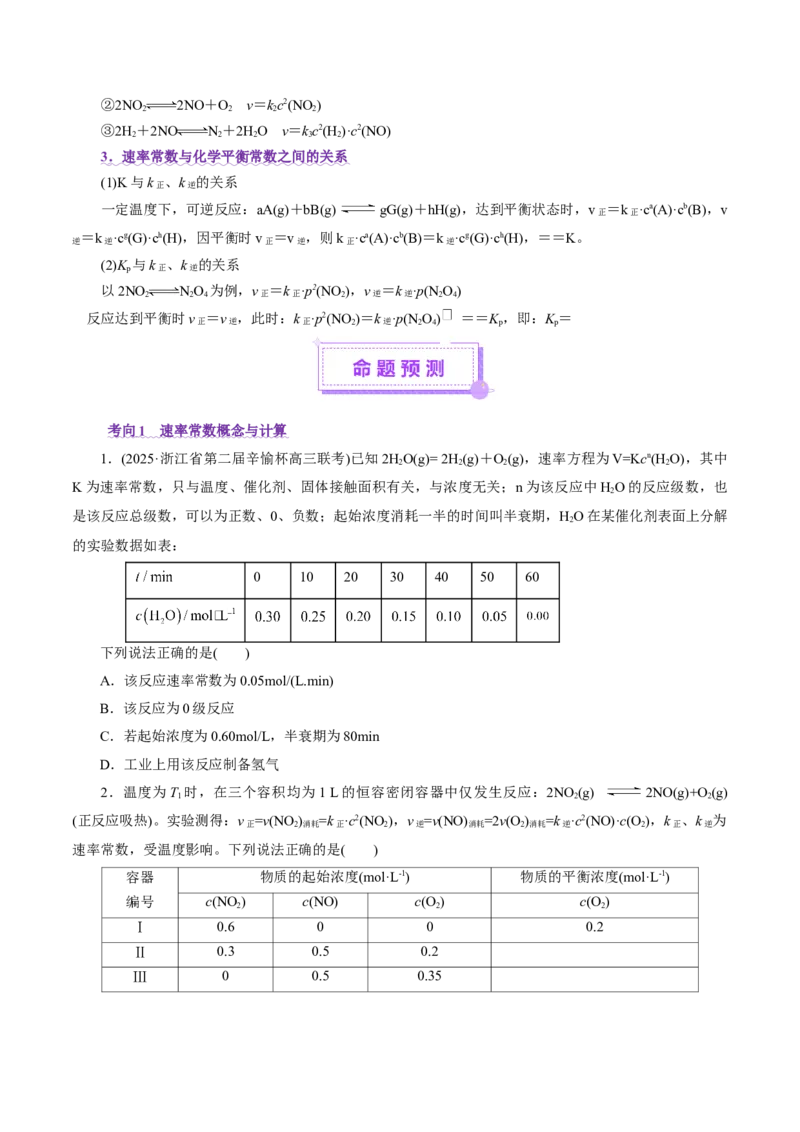
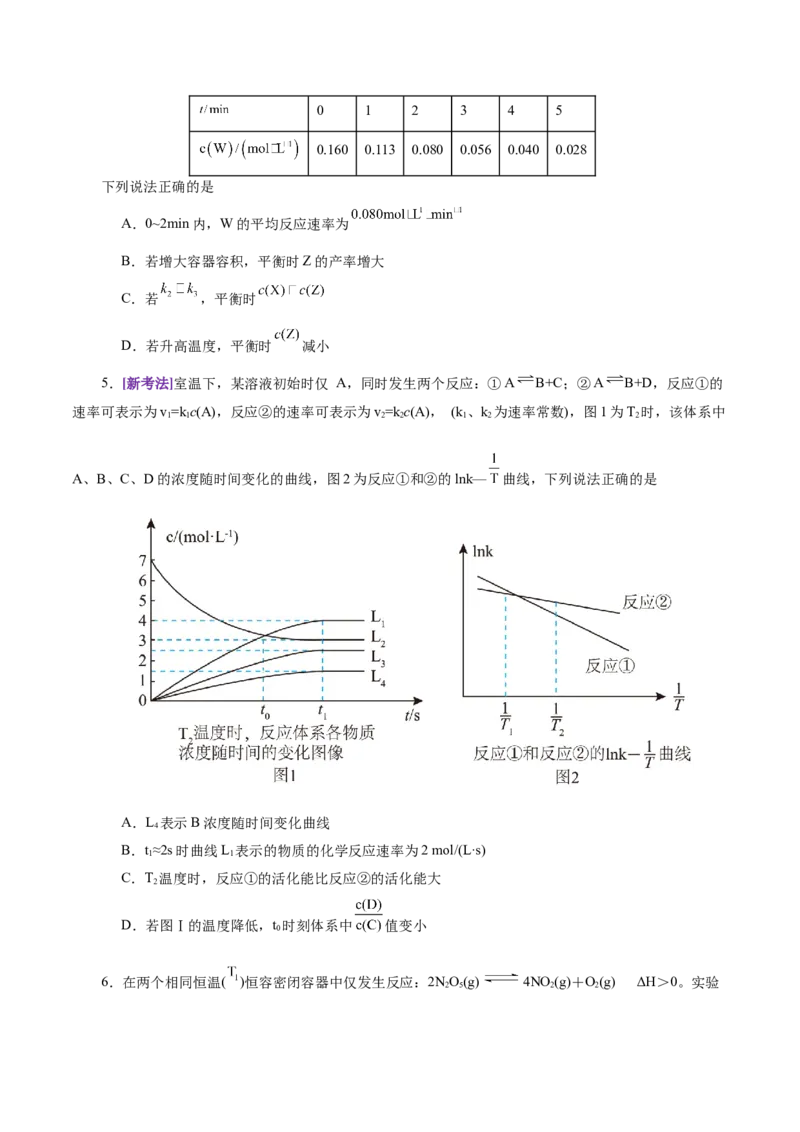
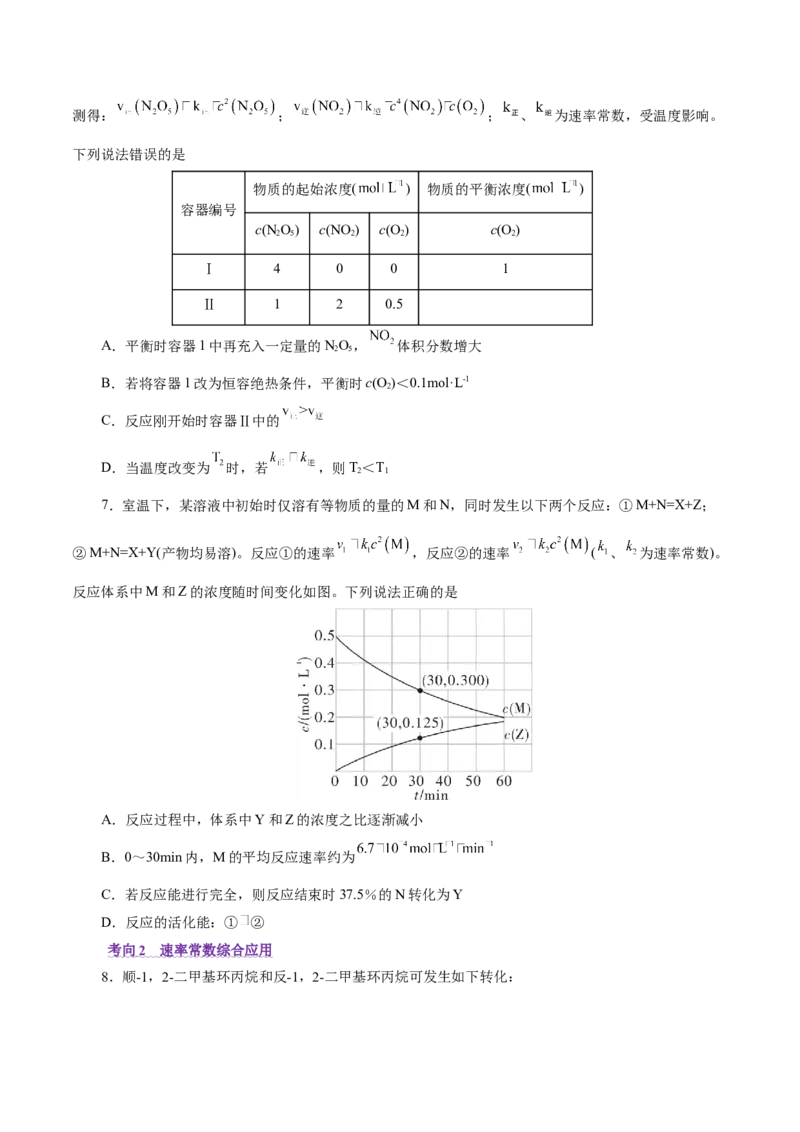
15.(2021•河北选择性考试,11)室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反
应:①M+N=X+Y;②M+N=X+Z,反应①的速率可表示为v=kc2(M),反应②的速率可表示为v=kc2(M)
1 1 2 2
(k、k 为速率常数)。反应体系中组分M、Z的浓度随时间变化情况如图,下列说法错误的是
1 2
A.0~30min时间段内,Y的平均反应速率为6.67×10-8mol•L-1•min-1
B.反应开始后,体系中Y和Z的浓度之比保持不变
C.如果反应能进行到底,反应结束时62.5%的M转化为Z
D.反应①的活化能比反应②的活化能大
1 .速率常数
(1)含义:速率常数(k)是指在给定温度下,反应物浓度皆为1 mol·L-1时的反应速率
(2)意义:在相同的浓度条件下,可用速率常数大小来比较化学反应的反应速率
(3)速率常数的影响因素:与浓度无关,但受温度、催化剂、固体表面性质等因素的影响,但温度对化
学反应速率的影响是显著的,速率常数是温度的函数,同一反应,温度不同,速率常数将有不同的值。通
常反应速率常数越大,反应进行得越快。不同反应有不同的速率常数
【易错提醒】
(1)速率常数是温度的函数。一般情况下,同一反应,温度不同,速率常数就不同,温度相同,速率常
数就相同;浓度不影响速率常数。
(2)反应物浓度改变,但速率常数不变,因此可以利用速率方程求出该温度下任意浓度时的反应速率。
2 .速率方程
(1)定义:一定温度下,基元反应的化学反应速率与反应物的浓度幂的乘积成正比,其次方一般为各物
质化学式前的系数。
(2)表达式
对于反应:aA+bB==pC+qD,则v=kca(A)·cb(B) (其中k为速率常数)
如:①SO Cl SO +Cl v=kc(SO Cl)
2 2 2 2 1 2 2②2NO 2NO+O v=kc2(NO )
2 2 2 2
③2H+2NO N+2HO v=kc2(H )·c2(NO)
2 2 2 3 2
3 .速率常数与化学平衡常数之间的关系
(1)K与k 、k 的关系
正 逆
一定温度下,可逆反应:aA(g)+bB(g) gG(g)+hH(g),达到平衡状态时,v =k ·ca(A)·cb(B),v
正 正
=k ·cg(G)·ch(H),因平衡时v =v ,则k ·ca(A)·cb(B)=k ·cg(G)·ch(H),==K。
逆 逆 正 逆 正 逆
(2)K 与k 、k 的关系
p 正 逆
以2NO NO 为例,v =k ·p2(NO ),v =k ·p(NO)
2 2 4 正 正 2 逆 逆 2 4
反应达到平衡时v =v ,此时:k ·p2(NO )=k ·p(N O) ==K ,即:K =
正 逆 正 2 逆 2 4 p p
考向 1 速率常数概念与计算
1.(2025·浙江省第二届辛愉杯高三联考)已知2HO(g)= 2H (g)+O(g),速率方程为V=Kcn(H O),其中
2 2 2 2
K为速率常数,只与温度、催化剂、固体接触面积有关,与浓度无关;n为该反应中HO的反应级数,也
2
是该反应总级数,可以为正数、0、负数;起始浓度消耗一半的时间叫半衰期,HO在某催化剂表面上分解
2
的实验数据如表:
0 10 20 30 40 50 60
下列说法正确的是( )
A.该反应速率常数为0.05mol/(L.min)
B.该反应为0级反应
C.若起始浓度为0.60mol/L,半衰期为80min
D.工业上用该反应制备氢气
2.温度为T 时,在三个容积均为1 L的恒容密闭容器中仅发生反应:2NO (g) 2NO(g)+O (g)
1 2 2
(正反应吸热)。实验测得:v =v(NO ) =k ·c2(NO ),v =v(NO) =2v(O ) =k ·c2(NO)·c(O ),k 、k 为
正 2 消耗 正 2 逆 消耗 2 消耗 逆 2 正 逆
速率常数,受温度影响。下列说法正确的是( )
容器 物质的起始浓度(mol·L-1) 物质的平衡浓度(mol·L-1)
编号 c(NO ) c(NO) c(O ) c(O )
2 2 2
Ⅰ 0.6 0 0 0.2
Ⅱ 0.3 0.5 0.2
Ⅲ 0 0.5 0.35k
逆
A.设K为该反应的化学平衡常数,则有K=
k
正
B.达平衡时,容器Ⅱ与容器Ⅲ中的总压强之比为20∶17
C.容器Ⅱ中起始时平衡正向移动,达到平衡时,容器Ⅱ中NO 的转化率比容器Ⅰ中的小
2
D.若改变温度为T,且T>T ,则k ∶k <0.8
2 2 1 正 逆
3.硫酸工业中,将SO 氧化为SO 是生产工艺中的重要环节。在温度为T 条件下,在三个容积均为
2 3 1
1L的恒容密闭容器中仅发生反应:2SO (g)+O(g) 2SO (g)ΔH<0,实验测得:v =k ·c2(SO )·c(O),v
2 2 3 正 正 2 2
=k ·c2(SO )。
逆 逆 3
起始浓度/(mol·L-1) 平衡浓度/(mol·L-1)
容器编号
c(SO ) c(O) C(SO ) c(O)
2 2 3 2
I 0.6 0.3 0 0.2
II 0.5 x 0.3
III 0.3 0.25 0.2
已知:k 、k 为速率常数,仅受温度的影响。
正 逆
下列说法错误的是( )
A.达到平衡时,平衡常数和速率常数的关系:
B.若容器II中达到平衡时 =1,则x=0.85
C.容器III中达到平衡时,c(O)<0.25mol·L-1
2
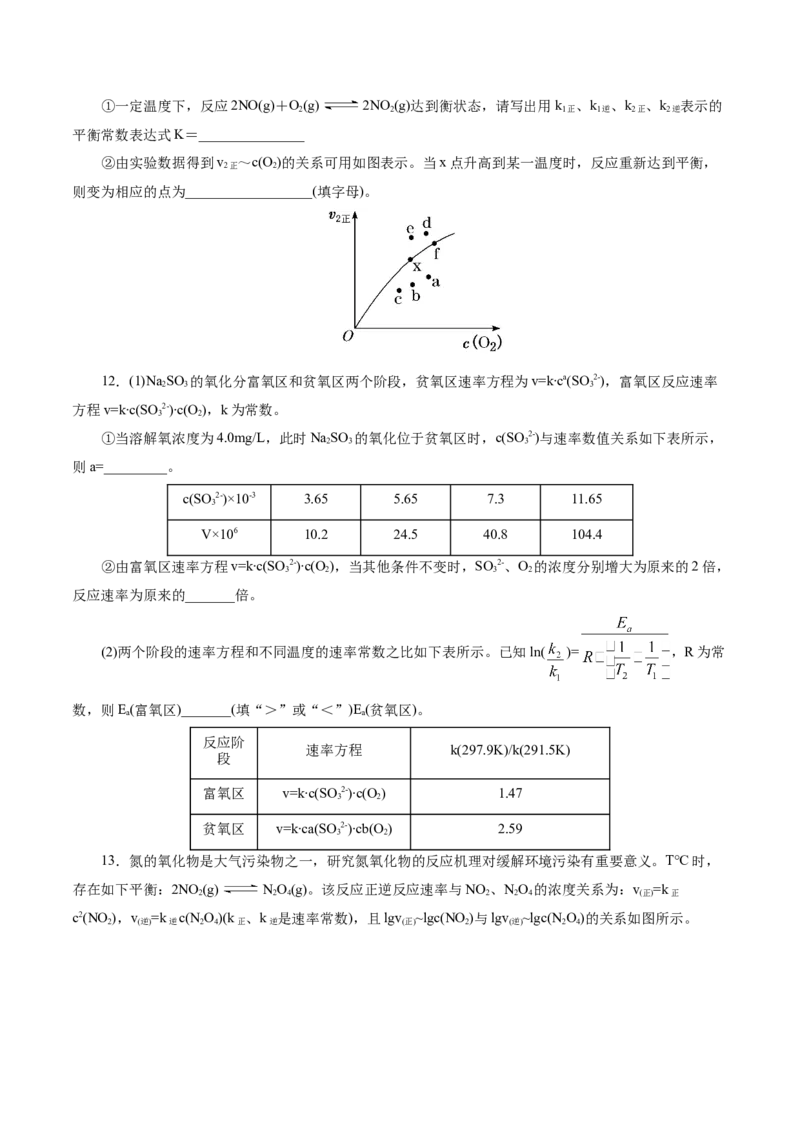
D.当温度升高为T 时,k 、k 分别增大m倍和n倍,则m”“<”或“=”),升高温度,k 增大的倍数
正 逆 3 2 2 4 2 正
________k 增大的倍数(填“>”“<”或“=”)。
逆
②温度为T 时,测定平衡体系中c(HO)=0.25 mol·L−1,则:k /k =__________L·mol−1。
1 2 正 逆
15.航天员呼吸产生的CO 用下列反应处理,可实现空间站中O 的循环利用。
2 2
Sabatior反应:CO(g)+4H(g) CH(g)+2HO(g)
2 2 4 2
水电解反应:2HO(g) 2H(g)+O(g)
2 2 2
一种新的循环利用方案是用Bosch反应CO(g)+2H(g) C(s)+2HO(g) H<0代替Sabatier反应,
2 2 2
再电解水实现O 2 的循环利用。 △
350℃时,向体积为2L的恒容密闭容器中通入8molH 和4molCO 发生以上反应,若反应起始和平衡
2 2
时温度相同(均为350℃),测得反应过程中压强随时间的变化如表所示:
时间/min 0 10 20 30 40 50 60
压强 6.00P 5.60P 5.30P 5.15P 5.06P 5.00P 5.00P
①350℃时Bosch反应的K=_________________(K 为用气体的分压表示的平衡常数,分压=气体的体
p p积分数×体系总压)
②Bosch反应的速率方程:v =k •c(CO)•c2(H ),v =k •c2(H O)(k是速率常数,只与温度有关)。
正 正 2 2 逆 逆 2
30min时, _________________ (填“>”“<”或“=”);升高温度,k 增大的倍数
正
_________________k 增大的倍数。(填“>”“<”或“=”)
逆
题型二 压强平衡常数及相关计算
1.(2024·福建卷,14节选)SiHCl 是制造多晶硅的原料,可由 Si和SiCl 耦合加氢得到,相关反应如
3 4
下:
Ⅰ.SiCl (g)+H(g)= SiHCl (g)+HCl(g) ΔH =52kJ·mol−1
4 2 3 1
Ⅱ.Si(s)+3HCl(g)= SiHCl (g)+H(g) ΔH =-236kJ·mol−1
3 2 2
Ⅲ.Si(s)+SiCl (g)+2H(g)=2SiH Cl(g) ΔH =16kJ·mol−1
4 2 2 2 3
Ⅳ.Si(s)+3SiCl (g)+2H(g)=4SiHCl (g) ΔH =-80 kJ·mol−1
4 2 3 4
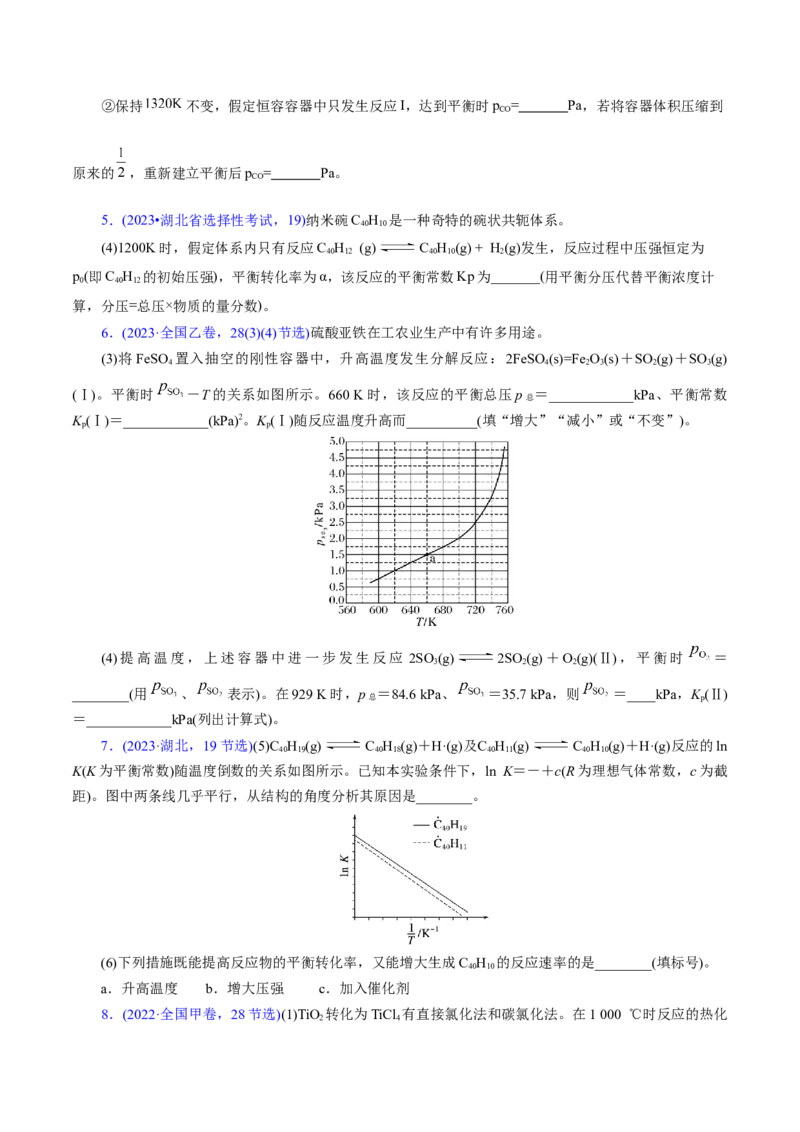
(3)在压强为p 的恒压体系中通入2molH 和1molSiCl ,达到平衡时,气体组分的物质的量分数随温度
0 2 4
变化如图所示(忽略气体组分在硅表面的吸附量)。已知:K 为用气体分压表示的平衡常数,分压=物质的量
p
分数×总压。
①图中n代表的组分为_______。(填化学式)
② 时,反应Ⅲ的平衡常数K=_______。(列出计算式)
p
③ 时,SiCl 的平衡转化率为f,消耗硅的物质的量为_______mol。(列出计算式)
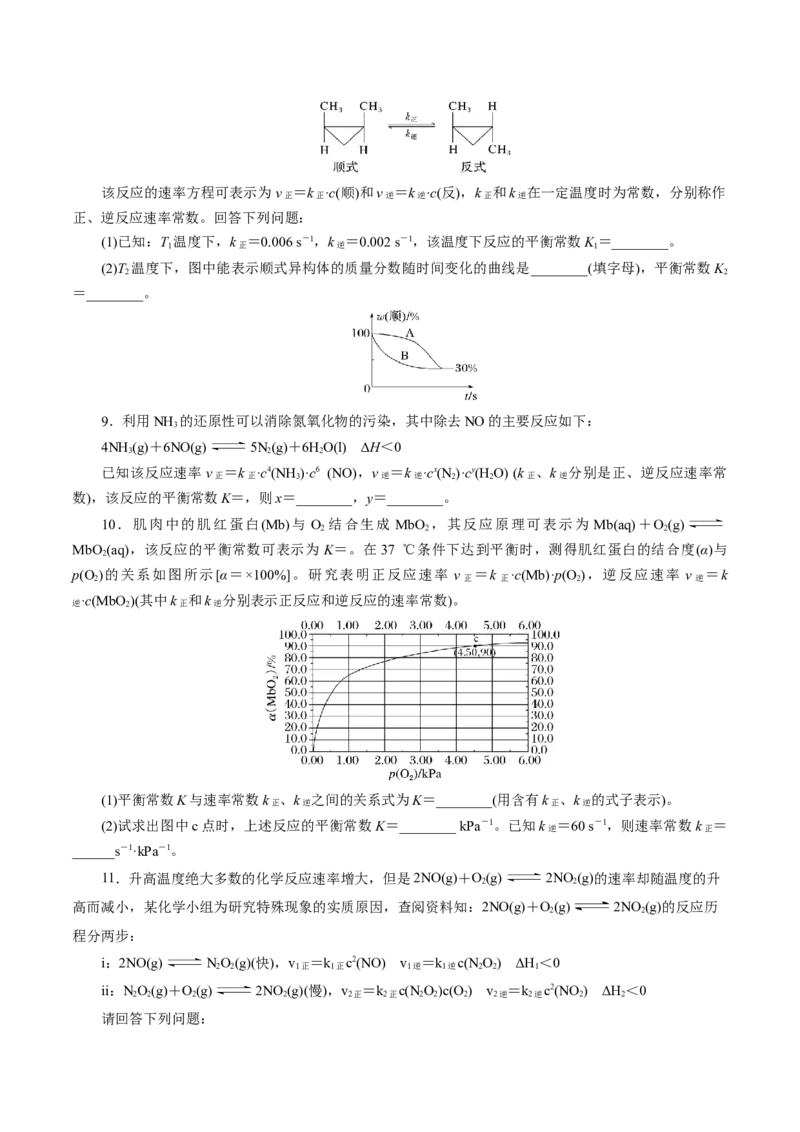
42.(2024· 贵州卷,17节选)在无氧环境下,CH 经催化脱氢芳构化可以直接转化为高附加值的芳烃产
4
品。一定温度下,CH 芳构化时同时存在如下反应:
4
ⅰ.CH(g) →C(s)+2H(g) ΔH =+74.6kJ·mol−1 ΔS=+80.84J·mol-1·K-1
4 2 1
ⅱ.6CH(g) →C H(l)+H(g) ΔH
4 6 6 2 2
(5) 下,在某密闭容器中按 n(C H):n(CH)=1:5 充入气体,发生反应 C H(g)+
6 6 4 6 6
CH(g)→C H(g)+H(g),平衡时C H(g)与C H(g)的分压比为4:1,则C H(g)的平衡转化率为 ,
4 7 8 2 6 6 7 8 6 6
平衡常数K= (用平衡分压代替平衡浓度计算,分压 总压 物质的量分数,列出计算式即可)。
p
3.(2024·湖南卷,18)丙烯腈(CH=CHCN)是一种重要的化工原料。
2
(3)催化剂TiO 再生时会释放CO,可用氨水吸收获得NH HCO 。现将一定量的NH HCO 固体(含
2 2 4 3 4 3
0.72g水)置于密闭真空容器中,充入CO 和NH ,其中CO 的分压为 ,在 ℃下进行干燥。为保证
2 3 2
NH HCO 不分解,NH 的分压应不低于 (已知 NH HCO
4 3 3 4 3
分解的平衡常数K= 4×104(kPa)3);
p
4.(2024·湖北卷,17节选)用BaCO 和焦炭为原料,经反应I、Ⅱ得到BaC ,再制备乙炔是我国科研
3 2
人员提出的绿色环保新路线。
反应I:BaCO(s)+C(s) BaO(s)+2CO(g)
3
反应Ⅱ:BaO(s)+3C(s) BaC (s)+CO(g)
2
(2)已知 、 (n是 的化学计量系数)。反应、Ⅱ的 与温度的关系曲线见图
1。
①反应BaCO(s)+4C(s) BaC (s)+3CO(g)在 的K = Pa3。
3 2 P②保持 不变,假定恒容容器中只发生反应I,达到平衡时p = Pa,若将容器体积压缩到
CO
原来的 ,重新建立平衡后p = Pa。
CO
5.(2023•湖北省选择性考试,19)纳米碗C H 是一种奇特的碗状共轭体系。
40 10
(4)1200K时,假定体系内只有反应C H (g) C H (g) + H(g)发生,反应过程中压强恒定为
40 12 40 10 2
p(即C H 的初始压强),平衡转化率为α,该反应的平衡常数Kp为_______(用平衡分压代替平衡浓度计
0 40 12
算,分压=总压×物质的量分数)。
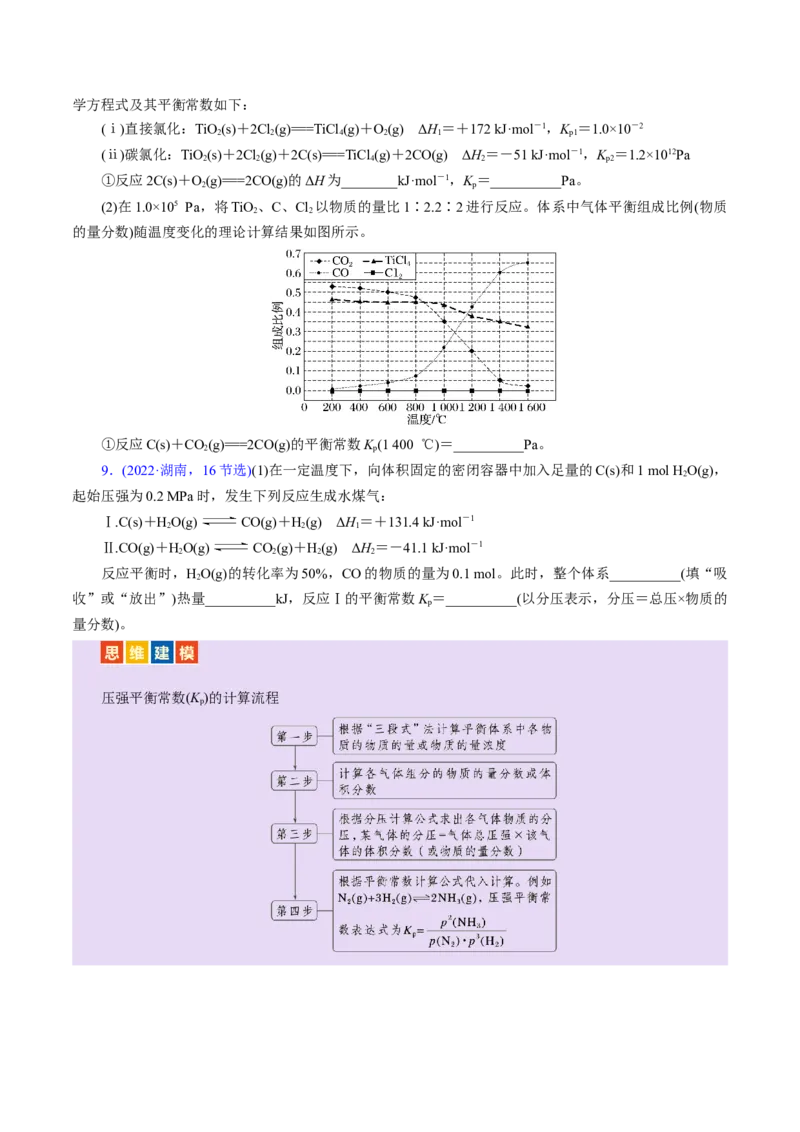
6.(2023·全国乙卷,28(3)(4)节选)硫酸亚铁在工农业生产中有许多用途。
(3)将FeSO 置入抽空的刚性容器中,升高温度发生分解反应:2FeSO (s)=Fe O(s)+SO (g)+SO (g)
4 4 2 3 2 3
(Ⅰ)。平衡时 -T的关系如图所示。660 K时,该反应的平衡总压p =____________kPa、平衡常数
总
K (Ⅰ)=____________(kPa)2。K (Ⅰ)随反应温度升高而__________(填“增大”“减小”或“不变”)。
p p
(4)提高温度,上述容器中进一步发生反应 2SO (g) 2SO (g)+O(g)(Ⅱ),平衡时 =
3 2 2
________(用 、 表示)。在929 K时,p =84.6 kPa、 =35.7 kPa,则 =____kPa,K (Ⅱ)
总 p
=____________kPa(列出计算式)。
7.(2023·湖北,19节选)(5)C H (g) C H (g)+H·(g)及C H (g) C H (g)+H·(g)反应的ln
40 19 40 18 40 11 40 10
K(K为平衡常数)随温度倒数的关系如图所示。已知本实验条件下,ln K=-+c(R为理想气体常数,c为截
距)。图中两条线几乎平行,从结构的角度分析其原因是________。
(6)下列措施既能提高反应物的平衡转化率,又能增大生成C H 的反应速率的是________(填标号)。
40 10
a.升高温度 b.增大压强 c.加入催化剂
8.(2022·全国甲卷,28节选)(1)TiO 转化为TiCl 有直接氯化法和碳氯化法。在1 000 ℃时反应的热化
2 4学方程式及其平衡常数如下:
(ⅰ)直接氯化:TiO(s)+2Cl(g)===TiCl (g)+O(g) ΔH=+172 kJ·mol-1,K =1.0×10-2
2 2 4 2 1 p1
(ⅱ)碳氯化:TiO(s)+2Cl(g)+2C(s)===TiCl (g)+2CO(g) ΔH=-51 kJ·mol-1,K =1.2×1012Pa
2 2 4 2 p2
①反应2C(s)+O(g)===2CO(g)的ΔH为________kJ·mol-1,K =__________Pa。
2 p
(2)在1.0×105 Pa,将TiO 、C、Cl 以物质的量比1∶2.2∶2进行反应。体系中气体平衡组成比例(物质
2 2
的量分数)随温度变化的理论计算结果如图所示。
①反应C(s)+CO(g)===2CO(g)的平衡常数K (1 400 ℃)=__________Pa。
2 p
9.(2022·湖南,16节选)(1)在一定温度下,向体积固定的密闭容器中加入足量的C(s)和1 mol H O(g),
2
起始压强为0.2 MPa时,发生下列反应生成水煤气:
Ⅰ.C(s)+HO(g) CO(g)+H(g) ΔH=+131.4 kJ·mol-1
2 2 1
Ⅱ.CO(g)+HO(g) CO(g)+H(g) ΔH=-41.1 kJ·mol-1
2 2 2 2
反应平衡时,HO(g)的转化率为50%,CO的物质的量为0.1 mol。此时,整个体系__________(填“吸
2
收”或“放出”)热量__________kJ,反应Ⅰ的平衡常数K =__________(以分压表示,分压=总压×物质的
p
量分数)。
压强平衡常数(K )的计算流程
p1 . 气体的分压 p (B)
相同温度下,当某组分气体B单独存在且具有与混合气体总体积相同的体积时,该气体B所具有的压
强,称为气体B的分压强,简称气体B的分压,符号为p(B),单位为Pa或kPa或MPa。
气体B的分压p(B)=气体总压p×B的体积分数=气体总压p×B的物质的量分数。
2 .分压平衡常数 (K )
P
一定条件下,若平衡体系中有气体物质,也可用其分压代替浓度,所求得的平衡常数为分压平衡常数,
以K 表示。
p
对于反应aA(g)+bB(g) cC(g)+dD(g):
压强平衡常数表达式为K =[p(X):X在平衡体系中物质的量分数(或体积分数)×总压强]。
p
cc(C)·cd(D) n
浓 度 平 衡 常 数 与 压 强 平 衡 常 数 的 关 系 : K= , 又 p= RT=cRT , 则
c ca(A)·cb(B) V
K =K·(RT)Δn[Δn=(c+d)-(a+b)]。
p c
3 . 常用的四个公式
公式 备注
反应物的转化率 ×100%=×100%
①平衡量可以是物质的
生成物的产率 ×100%
量、气体的体积;
平衡时混合物组分的百
×100% ②某组分的体积分数,
分含量
也可以是物质的量分数
某组分的体积分数 ×100%
【名师提醒】
解答有关平衡常数的计算
(1)结合题意,运用“三段式”,分析计算、确定各物理量的变化。
(2)多重平衡体系的计算用好连续计算法(分设变量)、守恒法两种方法。
(3)多重平衡体系达到整体综合平衡后,每种平衡组分都只能有一个平衡浓度。
考向 2 分压平衡常数的计算
1.[新考法] (2025·浙江省第二届辛愉杯高三测试,节选)“碳达峰”“碳中和”是近年来的热门话题,
以二氧化氮和氢气为原料反应时,通常存在以下几个反应:
I.CO(g)+H(g) CO(g)+HO(g) ΔH =+41.2kJ·mol−1
2 2 2 1
II.CO(g)+3H(g) CHOH(g)+HO(g) ΔH =-48.8kJ·mol−1
2 2 3 2 2
III.2CO(g)+6H(g) CHOCH (g)+3HO(g) ΔH =-123.2kJ·mol−1
2 2 3 3 2 3IV.2CHOH(g) CHOCH (g)+HO(g) ΔH
3 3 3 2 4
(2)假设只发生反应I、反应II,一定条件下,向体积为 的恒容密闭容器中通入1 molCO 和4 molH
2 2
发生反应,初始压强为2.5 kPa,达到平衡时,CO 的转化率为80%,CO浓度为0.3 mol·Lˉ1,则反应I的
2
K = 。
P
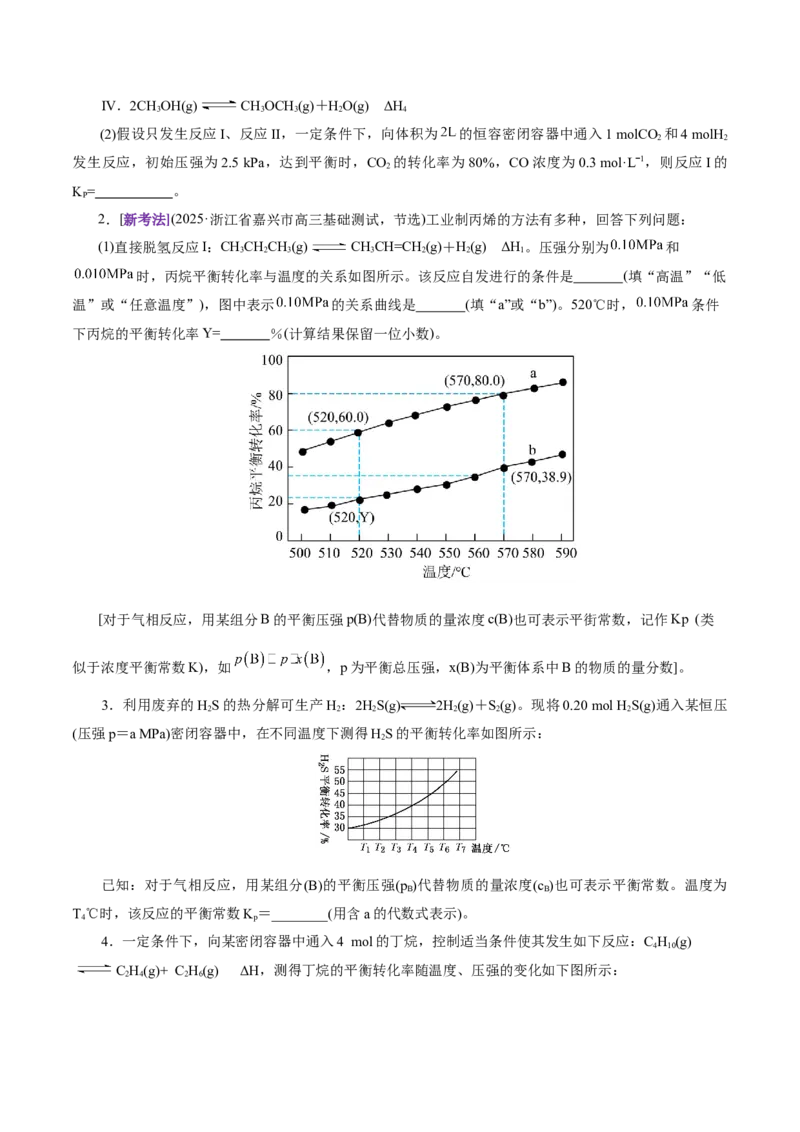
2.[新考法](2025·浙江省嘉兴市高三基础测试,节选)工业制丙烯的方法有多种,回答下列问题:
(1)直接脱氢反应I:CHCHCH(g) CHCH=CH(g)+H(g) ΔH 。压强分别为 和
3 2 3 3 2 2 1
时,丙烷平衡转化率与温度的关系如图所示。该反应自发进行的条件是 (填“高温”“低
温”或“任意温度”),图中表示 的关系曲线是 (填“a”或“b”)。520℃时, 条件
下丙烷的平衡转化率Y= %(计算结果保留一位小数)。
[对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平街常数,记作Kp (类
似于浓度平衡常数K),如 ,p为平衡总压强,x(B)为平衡体系中B的物质的量分数]。
3.利用废弃的HS的热分解可生产H :2HS(g) 2H(g)+S(g)。现将0.20 mol H S(g)通入某恒压
2 2 2 2 2 2
(压强p=a MPa)密闭容器中,在不同温度下测得HS的平衡转化率如图所示:
2
已知:对于气相反应,用某组分(B)的平衡压强(p )代替物质的量浓度(c )也可表示平衡常数。温度为
B B
T℃时,该反应的平衡常数K=________(用含a的代数式表示)。
4 p
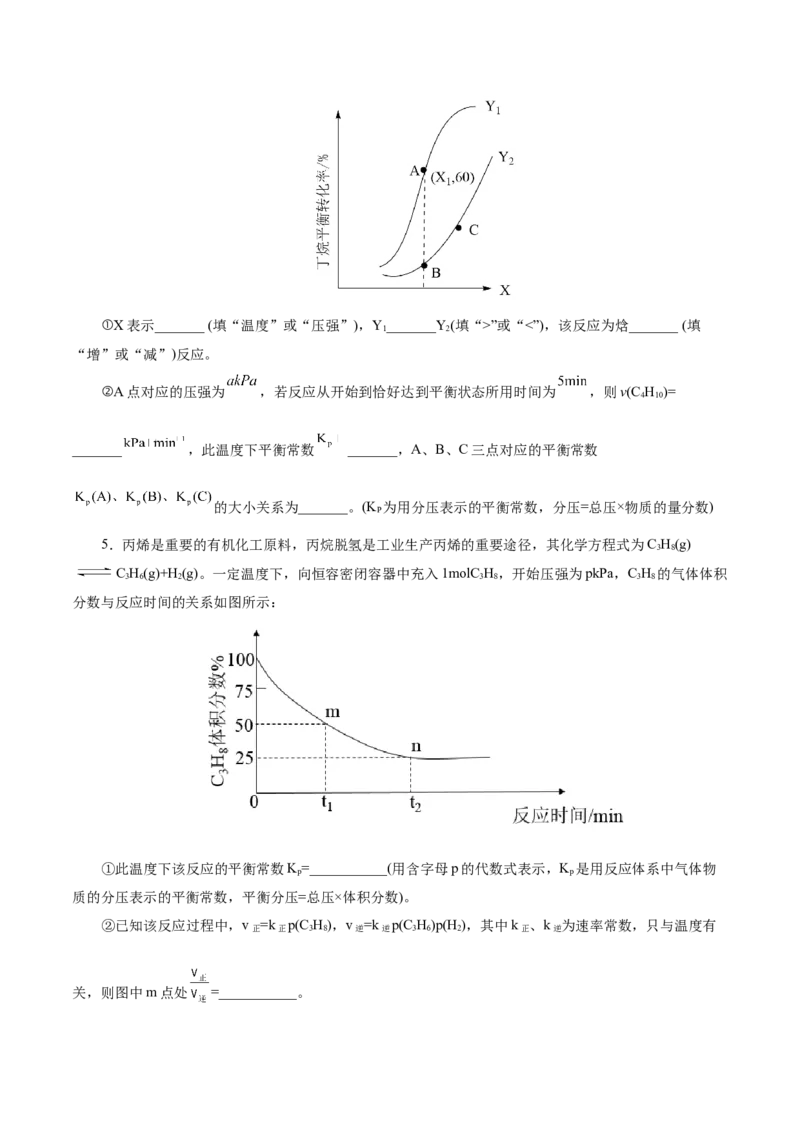
4.一定条件下,向某密闭容器中通入4 mol的丁烷,控制适当条件使其发生如下反应:C H (g)
4 10
C H(g)+ C H(g) ΔH,测得丁烷的平衡转化率随温度、压强的变化如下图所示:
2 4 2 6①X表示_______ (填“温度”或“压强”),Y_______Y(填“>”或“<”),该反应为焓_______ (填
1 2
“增”或“减”)反应。
②A点对应的压强为 ,若反应从开始到恰好达到平衡状态所用时间为 ,则v(C H )=
4 10
_______ ,此温度下平衡常数 _______,A、B、C三点对应的平衡常数
的大小关系为_______。(K 为用分压表示的平衡常数,分压=总压×物质的量分数)
P
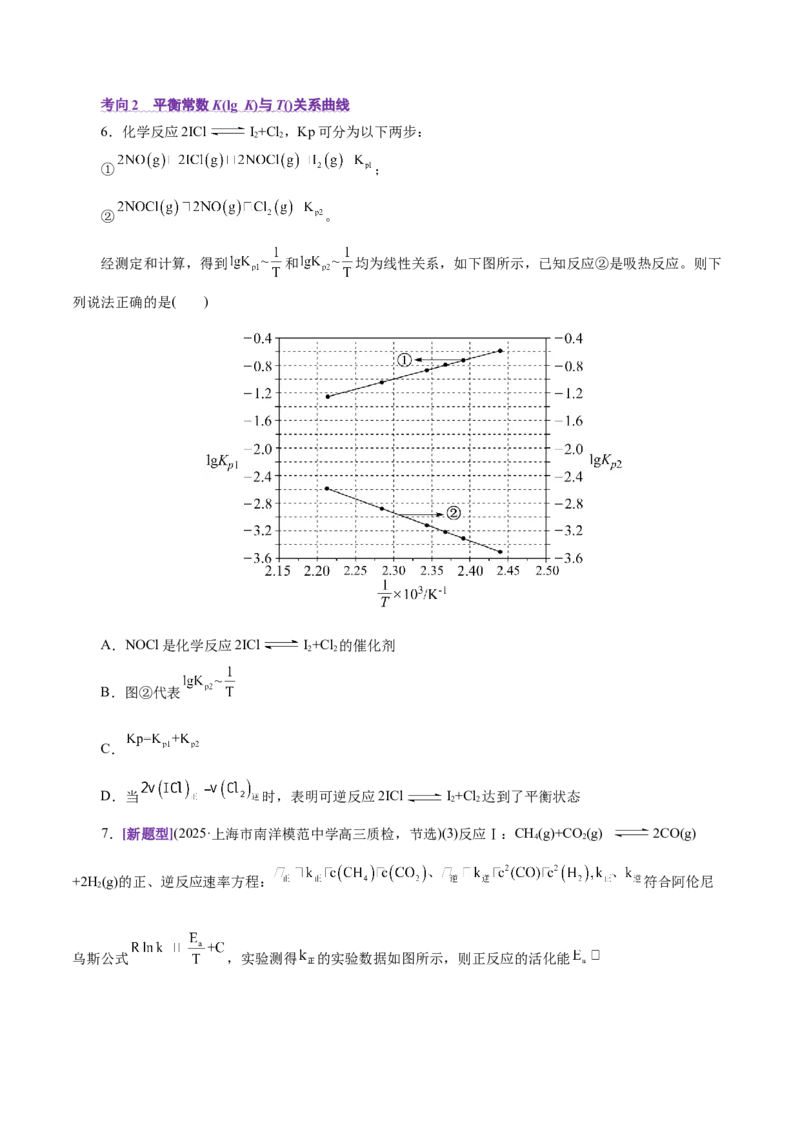
5.丙烯是重要的有机化工原料,丙烷脱氢是工业生产丙烯的重要途径,其化学方程式为C H(g)
3 8
C H(g)+H(g)。一定温度下,向恒容密闭容器中充入1molC H,开始压强为pkPa,C H 的气体体积
3 6 2 3 8 3 8
分数与反应时间的关系如图所示:
①此温度下该反应的平衡常数K=___________(用含字母p的代数式表示,K 是用反应体系中气体物
p p
质的分压表示的平衡常数,平衡分压=总压×体积分数)。
②已知该反应过程中,v =k p(C H),v =k p(C H)p(H ),其中k 、k 为速率常数,只与温度有
正 正 3 8 逆 逆 3 6 2 正 逆
关,则图中m点处 =___________。考向 2 平衡常数 K (lg K ) 与 T ( ) 关系曲线
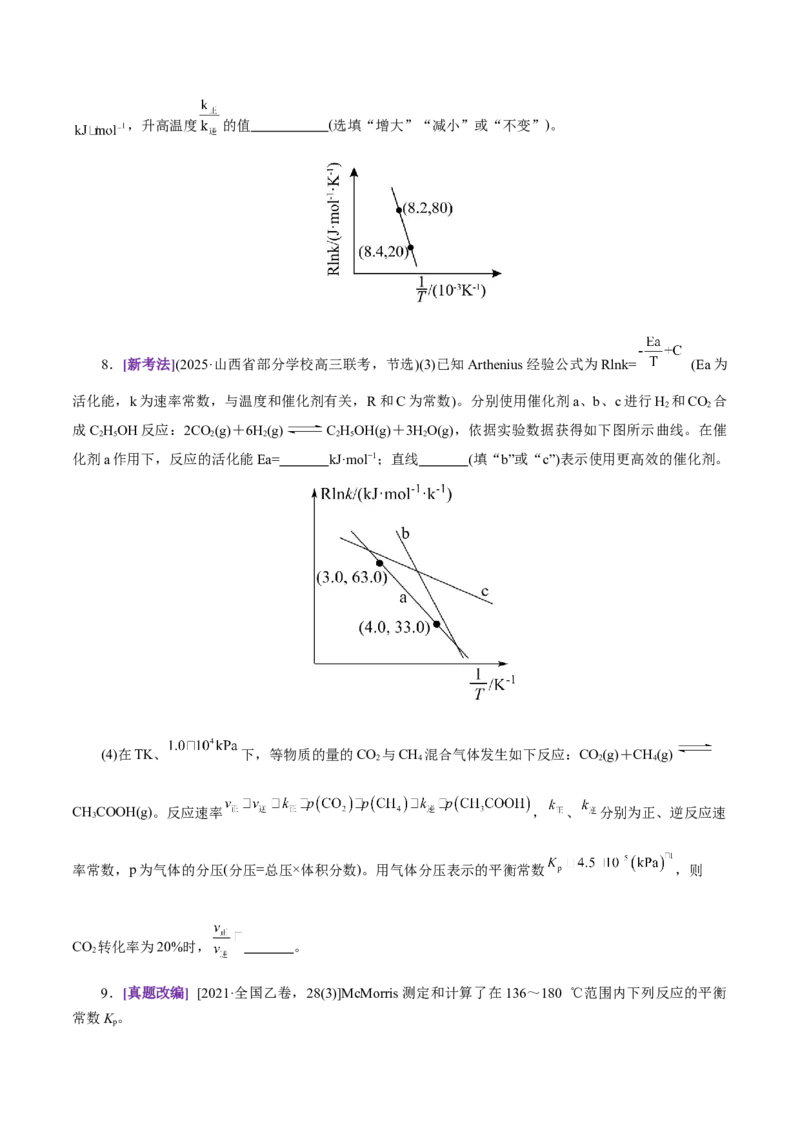
6.化学反应2ICl I+Cl,Kp可分为以下两步:
2 2
① ;
② 。
经测定和计算,得到 和 均为线性关系,如下图所示,已知反应②是吸热反应。则下
列说法正确的是( )
A.NOCl是化学反应2ICl I+Cl 的催化剂
2 2
B.图②代表
C.
D.当 时,表明可逆反应2ICl I+Cl 达到了平衡状态
2 2
7.[新题型](2025·上海市南洋模范中学高三质检,节选)(3)反应Ⅰ:CH(g)+CO (g) 2CO(g)
4 2
+2H (g)的正、逆反应速率方程: 符合阿伦尼
2
乌斯公式 ,实验测得 的实验数据如图所示,则正反应的活化能,升高温度 的值 (选填“增大”“减小”或“不变”)。
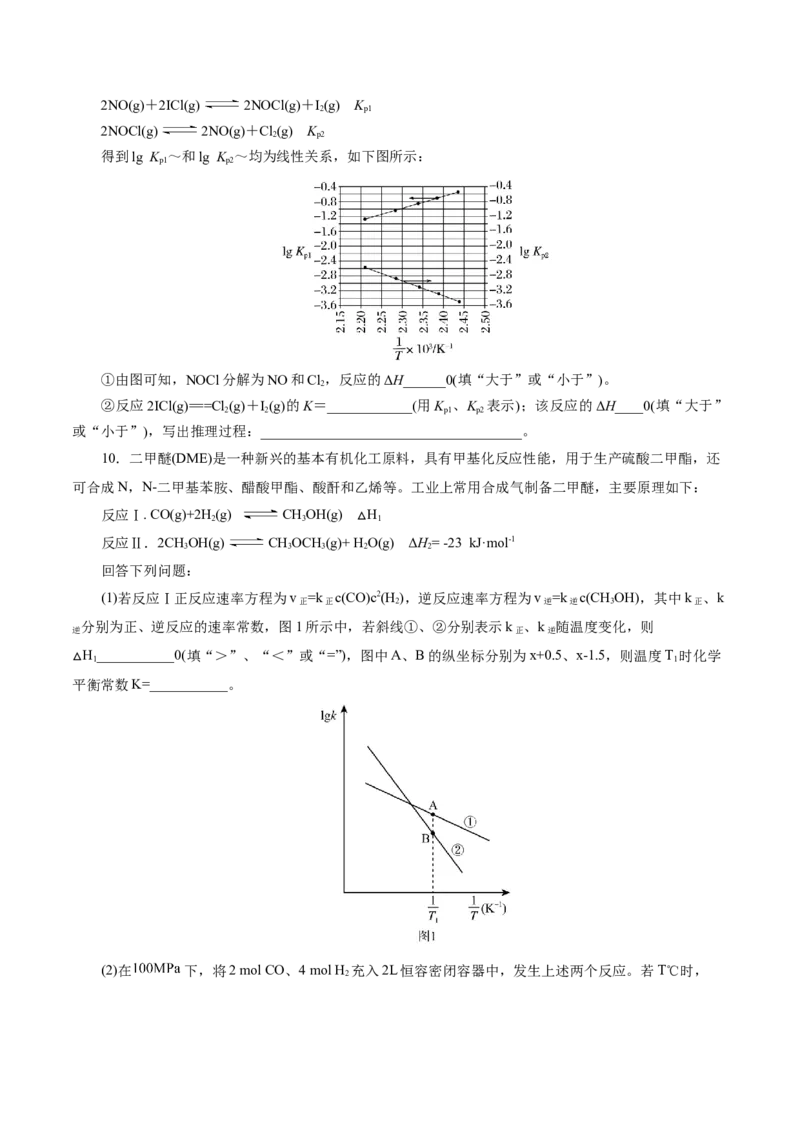
8.[新考法](2025·山西省部分学校高三联考,节选)(3)已知Arthenius经验公式为Rlnk= (Ea为
活化能,k为速率常数,与温度和催化剂有关,R和C为常数)。分别使用催化剂a、b、c进行H 和CO 合
2 2
成C HOH反应:2CO(g)+6H(g) C HOH(g)+3HO(g),依据实验数据获得如下图所示曲线。在催
2 5 2 2 2 5 2
化剂a作用下,反应的活化能Ea= kJ·mol−1;直线 (填“b”或“c”)表示使用更高效的催化剂。
(4)在TK、 下,等物质的量的CO 与CH 混合气体发生如下反应:CO(g)+CH(g)
2 4 2 4
CHCOOH(g)。反应速率 , 、 分别为正、逆反应速
3
率常数,p为气体的分压(分压=总压×体积分数)。用气体分压表示的平衡常数 ,则
CO 转化率为20%时, 。
2
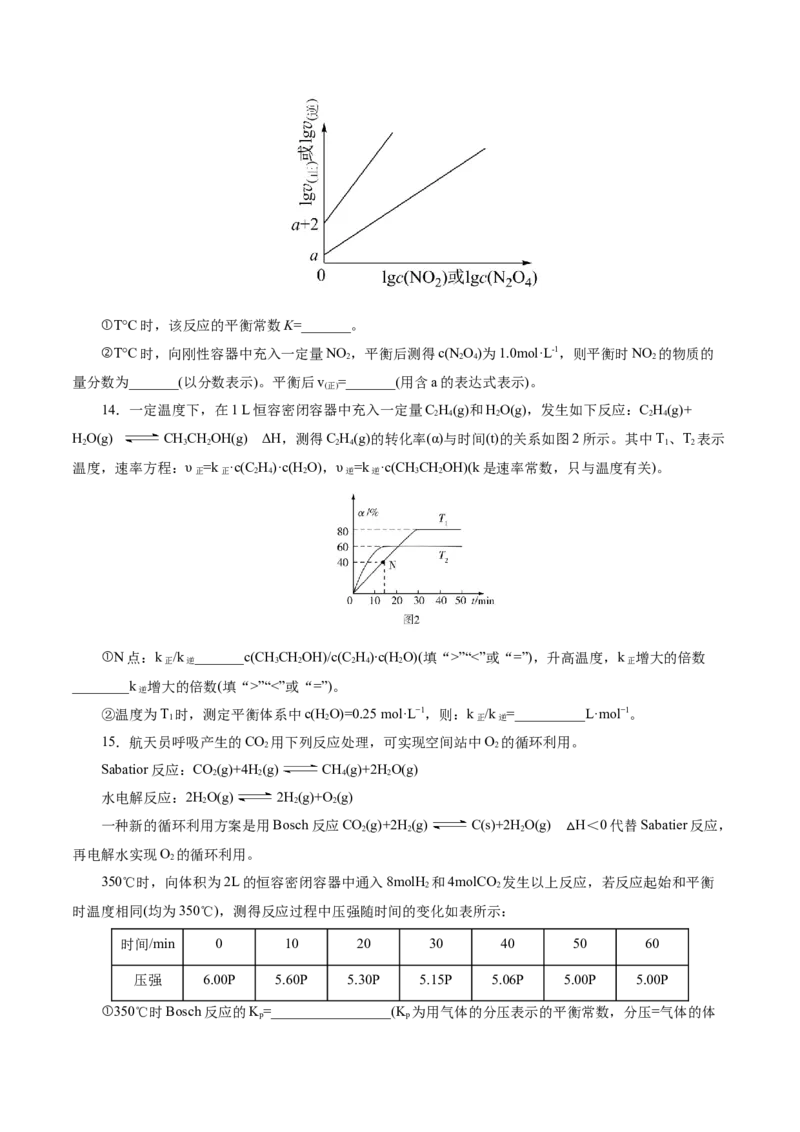
9.[真题改编] [2021·全国乙卷,28(3)]McMorris测定和计算了在136~180 ℃范围内下列反应的平衡
常数K 。
p2NO(g)+2ICl(g) 2NOCl(g)+I(g) K
2 p1
2NOCl(g) 2NO(g)+Cl(g) K
2 p2
得到lg K ~和lg K ~均为线性关系,如下图所示:
p1 p2
①由图可知,NOCl分解为NO和Cl,反应的ΔH______0(填“大于”或“小于”)。
2
②反应2ICl(g)===Cl(g)+I(g)的K=____________(用K 、K 表示);该反应的ΔH____0(填“大于”
2 2 p1 p2
或“小于”),写出推理过程:_____________________________________。
10.二甲醚(DME)是一种新兴的基本有机化工原料,具有甲基化反应性能,用于生产硫酸二甲酯,还
可合成N,N-二甲基苯胺、醋酸甲酯、酸酐和乙烯等。工业上常用合成气制备二甲醚,主要原理如下:
反应Ⅰ. CO(g)+2H (g) CHOH(g) H
2 3 1
反应Ⅱ.2CH
3
OH(g) CH
3
OCH
3
(g)+ H△2 O(g) ΔH
2
= -23 kJ·mol-1
回答下列问题:
(1)若反应Ⅰ正反应速率方程为v =k c(CO)c2(H ),逆反应速率方程为v =k c(CHOH),其中k 、k
正 正 2 逆 逆 3 正
分别为正、逆反应的速率常数,图1所示中,若斜线①、②分别表示k 、k 随温度变化,则
逆 正 逆
H___________0(填“>”、“<”或“=”),图中A、B的纵坐标分别为x+0.5、x-1.5,则温度T 时化学
1 1
△平衡常数K=___________。
(2)在 下,将2 mol CO、4 mol H 充入2L恒容密闭容器中,发生上述两个反应。若T℃时,
210min达到平衡,测得c(H )=0.8mol·L-1、c(H O)=0.15mol·L-1,则v(CO)= ___________ ,反应I
2 2
平衡常数Kp=___________ (Kp为用气体分压表示的平衡常数,分压=总压×物质的量分数;列计算
式)。
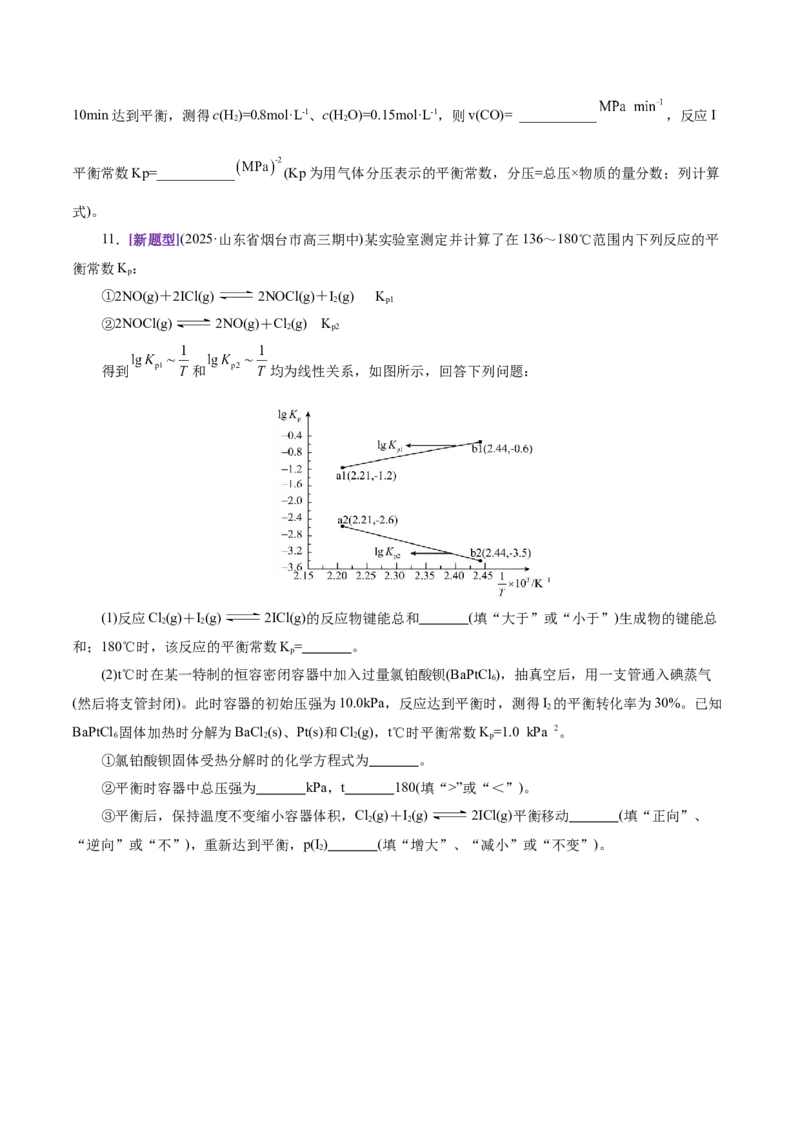
11.[新题型](2025·山东省烟台市高三期中)某实验室测定并计算了在136~180℃范围内下列反应的平
衡常数K:
p
①2NO(g)+2ICl(g) 2NOCl(g)+I(g) K
2 p1
②2NOCl(g) 2NO(g)+Cl(g) K
2 p2
得到 和 均为线性关系,如图所示,回答下列问题:
(1)反应Cl(g)+I(g) 2ICl(g)的反应物键能总和 (填“大于”或“小于”)生成物的键能总
2 2
和;180℃时,该反应的平衡常数K= 。
p
(2)t℃时在某一特制的恒容密闭容器中加入过量氯铂酸钡(BaPtCl ),抽真空后,用一支管通入碘蒸气
6
(然后将支管封闭)。此时容器的初始压强为10.0kPa,反应达到平衡时,测得I 的平衡转化率为30%。已知
2
BaPtCl 固体加热时分解为BaCl (s)、Pt(s)和Cl(g),t℃时平衡常数K=1.0 kPa 2。
6 2 2 p
①氯铂酸钡固体受热分解时的化学方程式为 。
②平衡时容器中总压强为 kPa,t 180(填“>”或“<”)。
③平衡后,保持温度不变缩小容器体积,Cl(g)+I(g) 2ICl(g)平衡移动 (填“正向”、
2 2
“逆向”或“不”),重新达到平衡,p(I) (填“增大”、“减小”或“不变”)。
2