文档内容
专题 09 化学反应速率与化学平衡
化学平衡的相关计
内容 化学反应速率 化学平衡 化学反应进行的方向
算
1.了解化学反应速率的概念和 1.了解化学反应的可逆性及化学平衡的建立
课
定量表示方法 1.能正确计算化学
2.掌握化学平衡的特征
标
2.了解反应活化能的概念,了
反应的转化率(α)
解 解催化剂的重要作用 3.理解外界条件(浓度、温度、压强、催化剂
解读 2.了解化学平衡常
等)对化学平衡的影响,能用相关理论解释其一
读 3.理解外界条件(浓度、温度、 数(K)的含义,能
般规律
压强、催化剂等)对反应速率的 利用化学平衡常数
影响,能用相关理论解释其一
4.了解化学反应速率和化学平衡的调控在生进行相关计算
般规律 活、生产和科学研究领域中的重要作用
本专题主要结合实际生产命题,以定性、定量相结合的方式综合考查化学反应速率和化学平衡,
包括化学反应速率的计算、影响化学平衡的因素及规律、平衡状态的判断、平衡常数和转化率
考情分析
的计算,同时渗透对计算能力、数形结合能力、语言组织能力等的考查。考查学生对信息的提
取、应用能力。
本专题涉及化学反应速率、化学平衡的相关计算及化学平衡移动的影响因素,主要考查学生运
备考策略
用图表、图形分析和解决化学问题的能力。
高频考点一 化学反应速率和化学平衡的影响因素
1.特殊条件的改变对化学反应速率和化学平衡的影响
(1)纯液体和固体浓度视为常数,它们的量的改变不会影响化学反应速率和平衡移动。但固体颗粒的大小
导致接触面积的大小发生变化,故影响反应速率。但仍不影响平衡移动。
(2)对于有固、液参加的反应,改变压强不会影响其反应速率和平衡移动。
(3)使用催化剂催化的化学反应,由于催化剂只有在适宜的温度下活性最大,反应速率才能达到最大,故
在许多工业生产中温度的选择还需考虑催化剂的活性温度范围。但催化剂的改变不影响平衡移动。
(4)“惰气”对反应速率和平衡的影响。
①恒温恒容,充入“惰气”,不改变反应速率和平衡移动。
②恒温恒压,充入“惰气”体积增大(相当于压强减小),v 、v 均减小,平衡向气体分子数增多的方向
正 逆
移动。
2.突破化学平衡状态的判断标志
(1)等——“正逆相等”(三种表述)。
①同一物质(两种表述):v =v 、断键数=成键数。
正 逆
②不同物质:=
(2)定——“变量不变”:如果一个量是随反应进行而改变的(即变量),当其“不变”时反应就达到平衡状
态,即“变量”不变可说明达到平衡状态。(3)依Q(浓度商)与K关系判断:若Q=K,反应处于平衡状态。
3.平衡移动方向判断两方法
(1)根据v 与v 的相对大小
正 逆
①若外界条件改变,引起v >v ,此时正反应占优势,则化学平衡向正反应方向(或向右)移动;
正 逆
②若外界条件改变,引起v K,平衡逆向移动;
②若Q=K,平衡不移动;
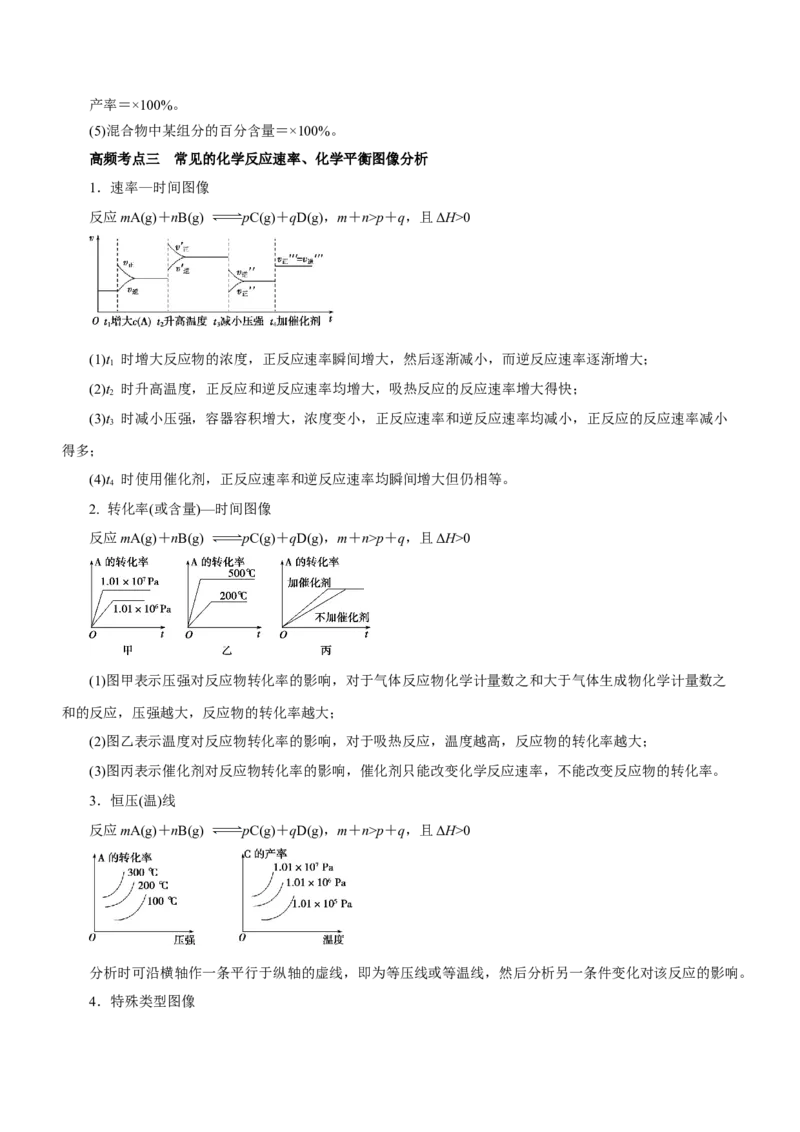
③若Qp+q,且ΔH>0
(1)t 时增大反应物的浓度,正反应速率瞬间增大,然后逐渐减小,而逆反应速率逐渐增大;
1
(2)t 时升高温度,正反应和逆反应速率均增大,吸热反应的反应速率增大得快;
2
(3)t 时减小压强,容器容积增大,浓度变小,正反应速率和逆反应速率均减小,正反应的反应速率减小
3
得多;
(4)t 时使用催化剂,正反应速率和逆反应速率均瞬间增大但仍相等。
4
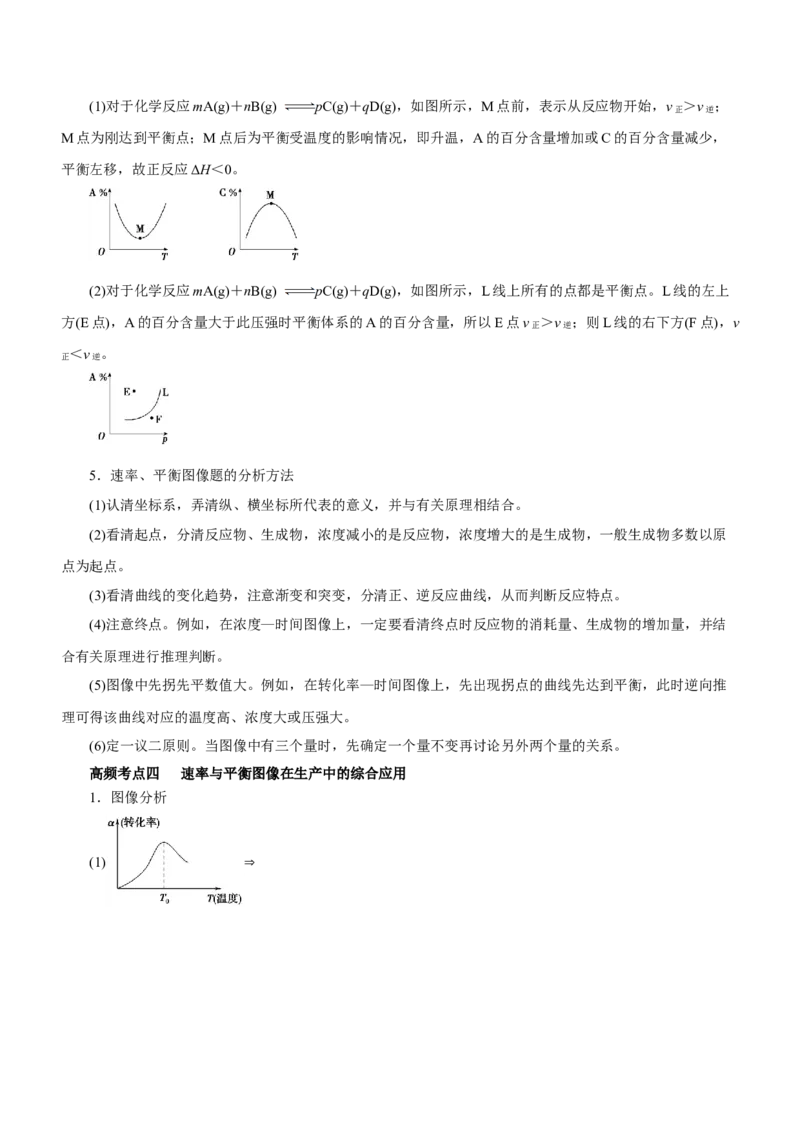
2. 转化率(或含量)—时间图像
反应mA(g)+nB(g) pC(g)+qD(g),m+n>p+q,且ΔH>0
(1)图甲表示压强对反应物转化率的影响,对于气体反应物化学计量数之和大于气体生成物化学计量数之
和的反应,压强越大,反应物的转化率越大;
(2)图乙表示温度对反应物转化率的影响,对于吸热反应,温度越高,反应物的转化率越大;
(3)图丙表示催化剂对反应物转化率的影响,催化剂只能改变化学反应速率,不能改变反应物的转化率。
3.恒压(温)线
反应mA(g)+nB(g) pC(g)+qD(g),m+n>p+q,且ΔH>0
分析时可沿横轴作一条平行于纵轴的虚线,即为等压线或等温线,然后分析另一条件变化对该反应的影响。
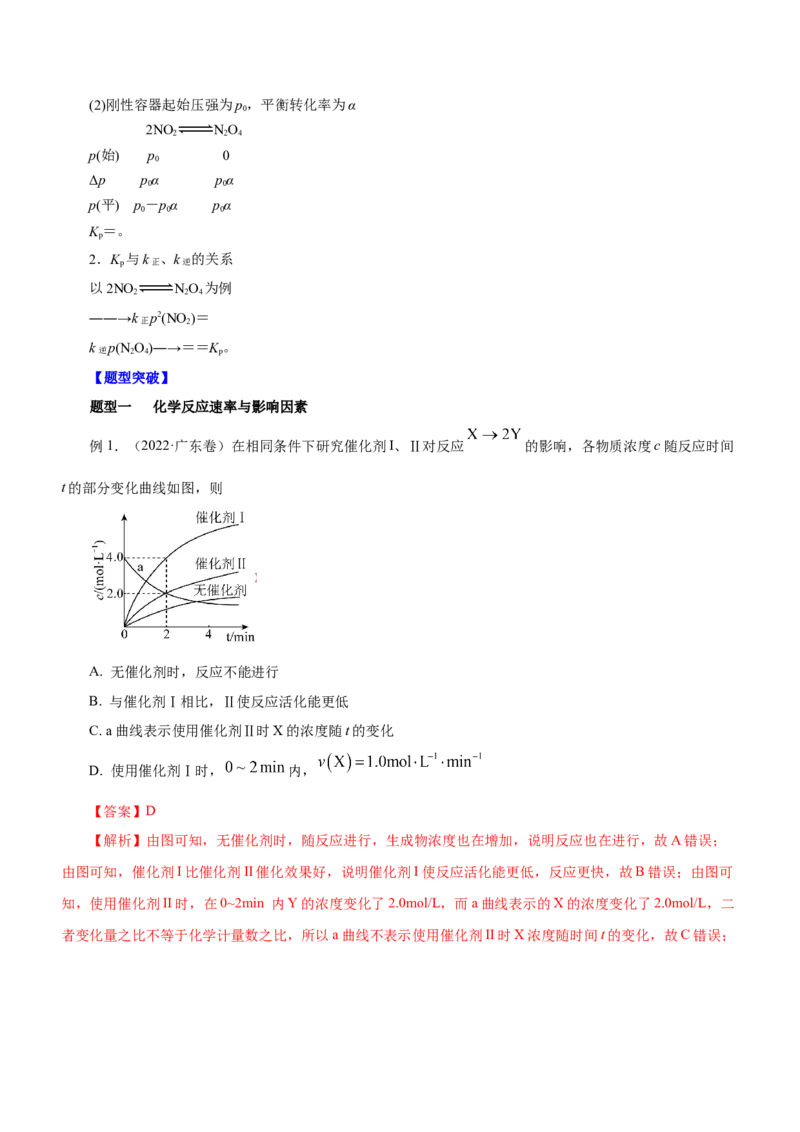
4.特殊类型图像(1)对于化学反应mA(g)+nB(g) pC(g)+qD(g),如图所示,M点前,表示从反应物开始,v >v ;
正 逆
M点为刚达到平衡点;M点后为平衡受温度的影响情况,即升温,A的百分含量增加或C的百分含量减少,
平衡左移,故正反应ΔH<0。
(2)对于化学反应mA(g)+nB(g) pC(g)+qD(g),如图所示,L线上所有的点都是平衡点。L线的左上
方(E点),A的百分含量大于此压强时平衡体系的A的百分含量,所以E点v >v ;则L线的右下方(F点),v
正 逆
<v 。
正 逆
5.速率、平衡图像题的分析方法
(1)认清坐标系,弄清纵、横坐标所代表的意义,并与有关原理相结合。
(2)看清起点,分清反应物、生成物,浓度减小的是反应物,浓度增大的是生成物,一般生成物多数以原
点为起点。
(3)看清曲线的变化趋势,注意渐变和突变,分清正、逆反应曲线,从而判断反应特点。
(4)注意终点。例如,在浓度—时间图像上,一定要看清终点时反应物的消耗量、生成物的增加量,并结
合有关原理进行推理判断。
(5)图像中先拐先平数值大。例如,在转化率—时间图像上,先出现拐点的曲线先达到平衡,此时逆向推
理可得该曲线对应的温度高、浓度大或压强大。
(6)定一议二原则。当图像中有三个量时,先确定一个量不变再讨论另外两个量的关系。
高频考点四 速率与平衡图像在生产中的综合应用
1.图像分析
(1) ⇒(2) ⇒
(3)对于A(g)+2B(g) C(g)
⇒
(4) ⇒
2.图像题的一般分析思路
(1)一审题:审明各物质的状态(有无固体、液体),明确气体分子数的变化(变大、变小、不变),正反应是
吸热还是放热。
(2)二析图像
(3)三想方法规律
①三步分析法:一看反应速率是增大还是减小;二看v(正)、v(逆)的相对大小;三看化学平衡移动的方向。
②先拐先平数值大:在含量(转化率)-时间曲线中,先出现拐点的反应则先达到平衡,说明该曲线反应速
率快,表示温度较高、有催化剂、压强较大等。
③定一议二:当图像中有三个量时,先确定一个量不变,再讨论另外两个量的关系,有时还需要作辅助线。
④想规律做判断:联想化学反应速率、化学平衡移动规律,将图表与原理结合,对照得出结论。
高频考点五 分压平衡常数(K )与速率常数(k 、k )
p 正 逆
1.K 的两种计算模板
p
(1)平衡总压为p
N + 3H 2NH
2 2 3
n(平) a b c
p(分压) p p p
0 0 0
K =。
p(2)刚性容器起始压强为p,平衡转化率为α
0
2NO NO
2 2 4
p(始) p 0
0
Δp pα pα
0 0
p(平) p-pα pα
0 0 0
K =。
p
2.K 与k 、k 的关系
p 正 逆
以2NO NO 为例
2 2 4
――→k p2(NO )=
正 2
k p(N O)―→==K 。
逆 2 4 p
【题型突破】
题型一 化学反应速率与影响因素
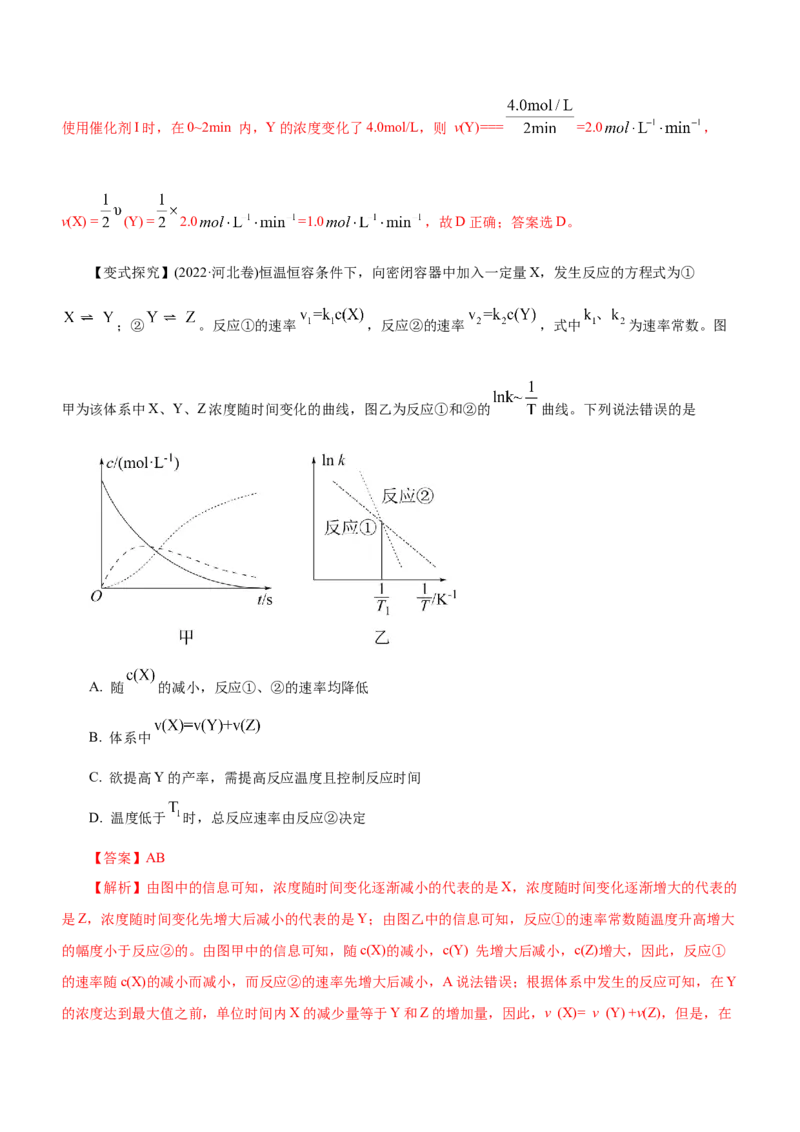
例1.(2022·广东卷)在相同条件下研究催化剂I、Ⅱ对反应 的影响,各物质浓度c随反应时间
t的部分变化曲线如图,则
A. 无催化剂时,反应不能进行
B. 与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C. a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D. 使用催化剂Ⅰ时, 内,
【答案】D
【解析】由图可知,无催化剂时,随反应进行,生成物浓度也在增加,说明反应也在进行,故A错误;
由图可知,催化剂I比催化剂II催化效果好,说明催化剂I使反应活化能更低,反应更快,故B错误;由图可
知,使用催化剂II时,在0~2min 内Y的浓度变化了2.0mol/L,而a曲线表示的X的浓度变化了2.0mol/L,二
者变化量之比不等于化学计量数之比,所以a曲线不表示使用催化剂II时X浓度随时间t的变化,故C错误;使用催化剂I时,在0~2min 内,Y的浓度变化了4.0mol/L,则 v(Y)=== =2.0 ,
v(X) = (Y) = 2.0 =1.0 ,故D正确;答案选D。
【变式探究】(2022·河北卷)恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式为①
;② 。反应①的速率 ,反应②的速率 ,式中 为速率常数。图
甲为该体系中X、Y、Z浓度随时间变化的曲线,图乙为反应①和②的 曲线。下列说法错误的是
A. 随 的减小,反应①、②的速率均降低
B. 体系中
C. 欲提高Y的产率,需提高反应温度且控制反应时间
D. 温度低于 时,总反应速率由反应②决定
【答案】AB
【解析】由图中的信息可知,浓度随时间变化逐渐减小的代表的是X,浓度随时间变化逐渐增大的代表的
是Z,浓度随时间变化先增大后减小的代表的是Y;由图乙中的信息可知,反应①的速率常数随温度升高增大
的幅度小于反应②的。由图甲中的信息可知,随c(X)的减小,c(Y) 先增大后减小,c(Z)增大,因此,反应①
的速率随c(X)的减小而减小,而反应②的速率先增大后减小,A说法错误;根据体系中发生的反应可知,在Y
的浓度达到最大值之前,单位时间内X的减少量等于Y和Z的增加量,因此,v (X)= v (Y) +v(Z),但是,在Y的浓度达到最大值之后,单位时间内Z的增加量等于Y和X的减少量,故v (X) + v (Y) = v(Z),B说法错
误;升高温度可以可以加快反应①的速率,但是反应①的速率常数随温度升高增大的幅度小于反应②的,且反
应②的的速率随着Y的浓度的增大而增大,因此,欲提高Y的产率,需提高反应温度且控制反应时间,C说
法正确;由图乙信息可知,温度低于T时,k>k,反应②为慢反应,因此,总反应速率由反应②决定,D说
1 2
法正确;综上所述,本题选AB 。
【变式探究】(2022·浙江卷)在恒温恒容条件下,发生反应A(s)+2B(g ) 3X(g),c(B)随时间的变化如
图中曲线甲所示。下列说法不正确的是
A.从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率
B.从b点切线的斜率可求得该化学反应在反应开始时的瞬时速率
在
C. 不同时刻都存在关系:2v(B)=3v(X)
D.维持温度、容积、反应物起始的量不变,向反应体系中加入催化剂,c(B)随时间变化关系如图中曲线乙
所示
【答案】C
【解析】图像中可以得到单位时间内的浓度变化,反应速率是单位时间内物质的浓度变化计算得到,从
a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率,选项A正确;b点处的切线的斜率是此时刻
物质浓度除以此时刻时间,为反应物B的瞬时速率,选项B正确;化学反应速率之比等于化学方程式计量数
之比分析,3v(B)=2v(X),选项C不正确;维持温度、容积不变,向反应体系中加入催化剂,平衡不移动,反
应速率增大,达到新的平衡状态,平衡状态与原来的平衡状态相同,选项D错误;故选C。
题型二 化学平衡常数
例2.(2022·海南卷)某温度下,反应 在密闭容器中达到平
衡,下列说法正确的是
A. 增大压强, ,平衡常数增大B. 加入催化剂,平衡时 的浓度增大
的
C. 恒容下,充入一定量 ,平衡向正反应方向移动
D. 恒容下,充入一定量的 , 的平衡转化率增大
【答案】C
【解析】该反应是一个气体分子数减少的反应,增大压强可以加快化学反应速率,正反应速率增大的幅度
大于逆反应的,故v > v ,平衡向正反应方向移动,但是因为温度不变,故平衡常数不变,A不正确;催化
正 逆
剂不影响化学平衡状态,因此,加入催化剂不影响平衡时CHCHOH(g)的浓度,B不正确;恒容下,充入一定
3 2
量的HO(g),HO(g)的浓度增大,平衡向正反应方向移动,C正确;恒容下,充入一定量的CH=CH (g),平
2 2 2 2
衡向正反应方向移动,但是CH=CH (g)的平衡转化率减小,D不正确;综上所述,本题选C。
2 2
【变式探究】(2022·江苏卷)用尿素水解生成的 催化还原 ,是柴油机车辆尾气净化的主要方
法。反应为 ,下列说法正确的是
A. 上述反应
B. 上述反应平衡常数
C. 上述反应中消耗 ,转移电子的数目为
D. 实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气污染程度越小
【答案】B
【解析】由方程式可知,该反应是一个气体分子数增大的反应,即熵增的反应,反应△S>0,故A错
误;由方程式可知,反应平衡常数 ,故B正确;由方程式可知,反应每消耗
4mol氨气,反应转移12mol电子,则反应中消耗1mol氨气转移电子的数目为3mol×4×
×6.02×1023=3×6.02×1023,故C错误;实际应用中,加入尿素的量越多,尿素水解生成的氨气过量,柴油机车辆排放的氨气对空气污染程度增大,故D错误;故选B。
题型三 化学平衡转化率
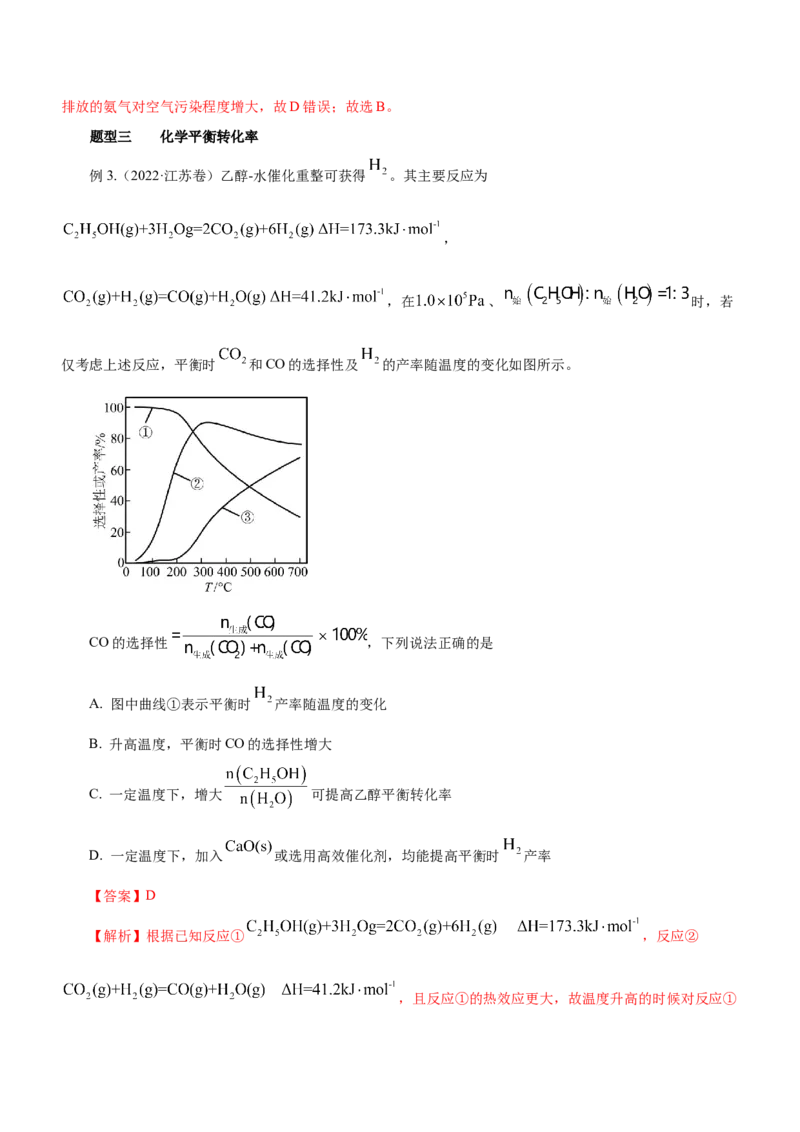
例3.(2022·江苏卷)乙醇-水催化重整可获得 。其主要反应为
,
,在 、 时,若
仅考虑上述反应,平衡时 和CO的选择性及 的产率随温度的变化如图所示。
CO的选择性 ,下列说法正确的是
A. 图中曲线①表示平衡时 产率随温度的变化
B. 升高温度,平衡时CO的选择性增大
C. 一定温度下,增大 可提高乙醇平衡转化率
D. 一定温度下,加入 或选用高效催化剂,均能提高平衡时 产率
【答案】D
【解析】根据已知反应① ,反应②
,且反应①的热效应更大,故温度升高的时候对反应①影响更大一些,即CO 选择性增大,同时CO的选择性减小,根据CO的选择性的定义可知③代表CO 的选择
2 2
性,①代表CO的选择性,②代表H 的产率,以此解题。由分析可知②代表H 的产率,A错误;由分析可知
2 2
升高温度,平衡时CO的选择性减小,B错误;两种物质参加反应增大一种物质的浓度,会降低该物质的平衡
转化率,C错误;加入 与水反应放热,对反应①影响较大,可以增大 产率,或者选用对反应①影
响较大的高效催化剂,也可以增大 产率,D正确;故选D。
【变式探究】(2021·海南卷)制备水煤气的反应 ,下列说法正
确的是
A.该反应 B.升高温度,反应速率增大
C.恒温下,增大总压,HO(g)的平衡转化率不变 D.恒温恒压下,加入催化剂,平衡常数增大
2
【答案】B
【解析】该反应的正反应是气体体积增大的反应,所以△S>0,A错误;升高温度,物质的内能增加,分
子运动速率加快,有效碰撞次数增加,因此化学反应速率增大,B正确;恒温下,增大总压,化学平衡向气体
体积减小的逆反应方向移动,使HO(g)的平衡转化率减小,C错误;恒温恒压下,加入催化剂,化学平衡不移
2
动,因此化学平衡常数不变,D错误;故选B。
题型四 化学图像图表综合分析
例4. (2022·湖南卷)反应物(S)转化为产物(P或P·Z)的能量与反应进程的关系如下图所示:
下列有关四种不同反应进程的说法正确的是
A. 进程Ⅰ是放热反应 B. 平衡时P的产率:Ⅱ>Ⅰ
C. 生成P的速率:Ⅲ>Ⅱ D. 进程Ⅳ中,Z没有催化作用
【答案】AD
【解析】由图中信息可知,进程Ⅰ中S的总能量大于产物P的总能量,因此进程I是放热反应,A说法正
确;进程Ⅱ中使用了催化剂X,但是催化剂不能改变平衡产率,因此在两个进程中平衡时P的产率相同,B说法不正确;进程Ⅲ中由S•Y转化为P•Y的活化能高于进程Ⅱ中由S•X转化为P•X的活化能,由于这两步反应
分别是两个进程的决速步骤,因此生成P的速率为Ⅲ<Ⅱ,C说法不正确;由图中信息可知,进程Ⅳ中S吸附
到Z表面生成S•Z,然后S•Z转化为产物P•Z,由于P•Z没有转化为P+Z,因此,Z没有表现出催化作用,D
说法正确;综上所述,本题选AD。
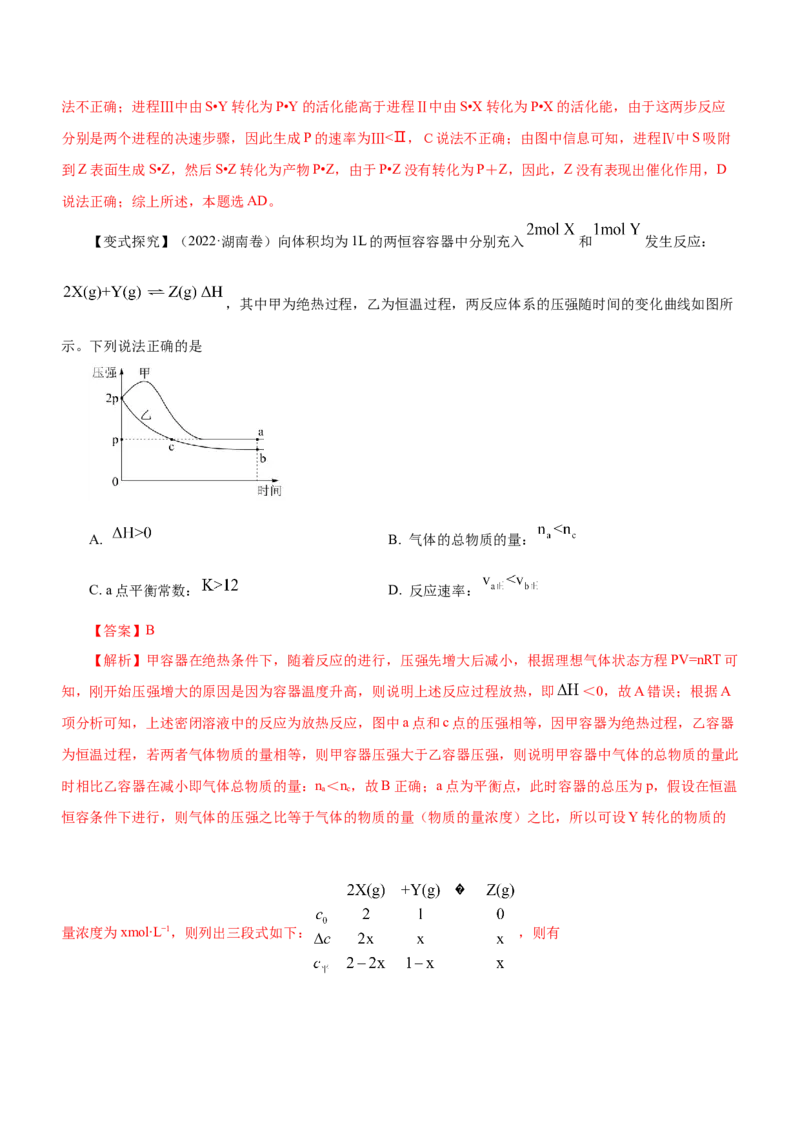
【变式探究】(2022·湖南卷)向体积均为1L的两恒容容器中分别充入 和 发生反应:
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所
示。下列说法正确的是
A. B. 气体的总物质的量:
C. a点平衡常数: D. 反应速率:
【答案】B
【解析】甲容器在绝热条件下,随着反应的进行,压强先增大后减小,根据理想气体状态方程PV=nRT可
知,刚开始压强增大的原因是因为容器温度升高,则说明上述反应过程放热,即 <0,故A错误;根据A
项分析可知,上述密闭溶液中的反应为放热反应,图中a点和c点的压强相等,因甲容器为绝热过程,乙容器
为恒温过程,若两者气体物质的量相等,则甲容器压强大于乙容器压强,则说明甲容器中气体的总物质的量此
时相比乙容器在减小即气体总物质的量:n<n,故B正确;a点为平衡点,此时容器的总压为p,假设在恒温
a c
恒容条件下进行,则气体的压强之比等于气体的物质的量(物质的量浓度)之比,所以可设Y转化的物质的
量浓度为xmol∙L−1,则列出三段式如下: ,则有,计算得到x=0.75,那么化学平衡常数K=
,又甲容器为绝热条件,等效为恒温条件下升温,平衡逆向移动,则平衡常数减小即平衡常数K<12,故C错
误;根据图像可知,甲容器达到平衡的时间短,温度高,所以达到平衡的速率相对乙容器的快,即V >V
a正 b
,故D错误。综上所述,答案为B。
正
【变式探究】(2022·浙江卷)恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下
列说法不正确的是
A.实验①, ,
B.实验②, 时处于平衡状态,
C.相同条件下,增加氨气的浓度,反应速率增大
D.相同条件下,增加催化剂的表面积,反应速率增大
【答案】C
【解析】实验①中,0~20min,氨气浓度变化量为2.40×10-3mol/L-2.00×10-3mol/L=
4.00×10-4mol/L,v(NH )= =2.00×10-5mol/(L·min),反应速率之比等于化学计量数之比,
3
v(N )=v(NH )=1.00×10-5mol/(L·min),A正确;催化剂表面积大小只影响反应速率,不影响平衡,实验③中氨气
2 3
初始浓度与实验①中一样,实验③达到平衡时氨气浓度为4.00×10-4mol/L,则实验①达平衡时氨气浓度也为
4.00×10-4mol/L,而恒温恒容条件下,实验②相对于实验①为减小压强,平衡正向移动,因此实验②60min时
处于平衡状态,x<0.4,即x≠0.4,B正确;实验①、实验②中0~20min、20min~40min氨气浓度变化量都是
4.00×10-4mol/L,实验②中60min时反应达到平衡状态,实验①和实验②催化剂表面积相同,实验①中氨气初始浓度是实验②中氨气初始浓度的两倍,实验①60min时反应未达到平衡状态,相同条件下,增加氨气浓度,
反应速率并没有增大,C错误;对比实验①和实验③,氨气浓度相同,实验③中催化剂表面积是实验①中催化
剂表面积的2倍,实验③先达到平衡状态,实验③的反应速率大,说明相同条件下,增加催化剂的表面积,反
应速率增大,D正确;故选C。