文档内容
第四章 非金属及其化合物
第11讲 碳、硅及无机非金属材料(精讲)
【考情分析】
本讲内容在高考中碳、硅及其化合物的知识单独考查的题目较少。常与晶体结构、元素周期律、化学
方程式及化工流程相结合,重在考查考生创新思维以及理论联系实际的能力。题型以选择题、推断题为主,
难度适中。
【核心素养分析】
1.变化观念与平衡思想:根据碳、硅的结构,预测在一定条件下碳、硅及其化合物可能发生的化学变化。
2.科学态度与社会责任:关注与碳、硅有关的热点问题(如光导纤维、硅电池、半导体材料),形成可持
续发展的意识;知道碳、硅及其化合物对社会发展的重大贡献。
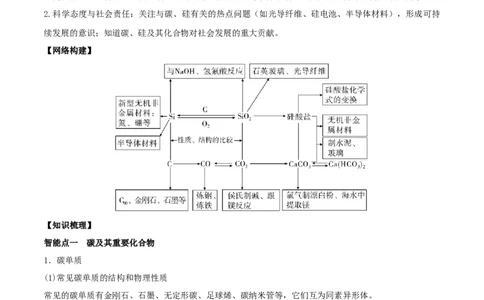
【网络构建】
【知识梳理】
智能点一 碳及其重要化合物
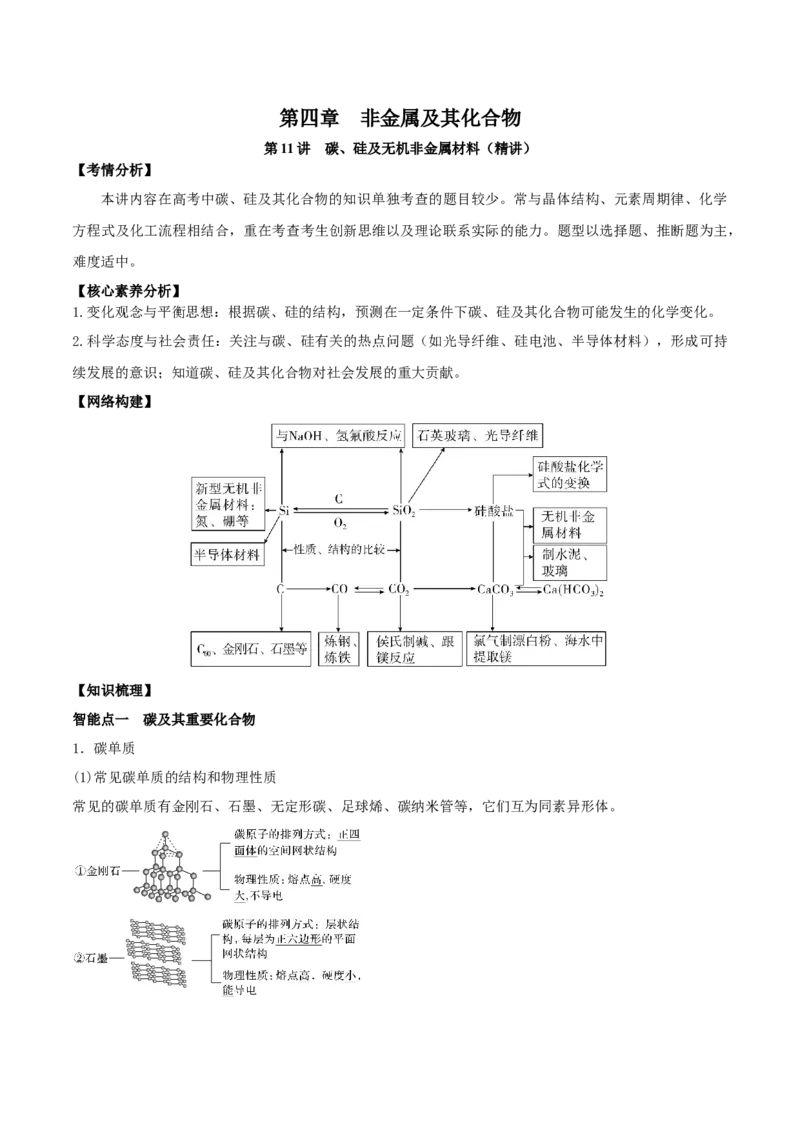
1.碳单质
(1)常见碳单质的结构和物理性质
常见的碳单质有金刚石、石墨、无定形碳、足球烯、碳纳米管等,它们互为同素异形体。(2)化学性质
a.与O 的反应(用化学方程式表示):
2
①O 不足:2C+O=====2CO;
2 2
②O 充足:C+O=====CO。
2 2 2
b.与氧化物反应(用化学方程式表示):
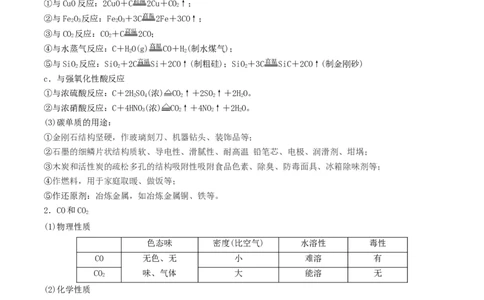
①与CuO反应:2CuO+C 2Cu+CO↑;
2
②与FeO 反应:FeO+3C 2Fe+3CO↑;
2 3 2 3
③与CO 反应:CO+C 2CO;
2 2
④与水蒸气反应:C+HO(g) CO+H(制水煤气);
2 2
⑤与SiO 反应:SiO+2C Si+2CO↑(制粗硅);SiO+3C SiC+2CO↑(制金刚砂)
2 2 2
c.与强氧化性酸反应
①与浓硫酸反应:C+2HSO(浓) CO↑+2SO↑+2HO。
2 4 2 2 2
②与浓硝酸反应:C+4HNO(浓) CO↑+4NO↑+2HO。
3 2 2 2
(3)碳单质的用途:
①金刚石结构坚硬,作玻璃刻刀、机器钻头、装饰品等;
②石墨的细鳞片状结构质软、导电性、滑腻性、耐高温 铅笔芯、电极、润滑剂、坩埚;
③木炭和活性炭的疏松多孔的结构吸附性吸附食品色素、除臭、防毒面具、冰箱除味剂等;
④作燃料,用于家庭取暖、做饭等;
⑤作还原剂:冶炼金属,如冶炼金属铜、铁等。
2.CO和CO
2
(1)物理性质
色态味 密度(比空气) 水溶性 毒性
CO 无色、无 小 难溶 有
CO 味、气体 大 能溶 无
2
(2)化学性质
①CO具有较强的还原性,可以与O、金属氧化物等发生反应。
2
如与FeO 反应:FeO+3CO=====2Fe+3CO。
2 3 2 3 2
②CO 是典型的酸性氧化物,也具有氧化性。
2
a.酸性氧化物
①与水反应:CO +H O H CO
2 2 2 3
②与碱反应:CO 少量:CO +2NaOH===Na CO +H O;CO 足量:CO +NaOH===NaHCO
2 2 2 3 2 2 2 3
③与碱性氧化物反应:CO +CaO=CaCO
2 3④与Ca(ClO) 盐溶液反应:Ca(ClO) +CO +H O===CaCO ↓+2HClO(CO 少量);
2 2 2 2 3 2
Ca(ClO) +2CO +2H O===Ca(HCO ) +2HClO(CO 过量);
2 2 2 3 2 2
b.氧化性
①与C反应:CO+C 2CO;
2
②与Mg反应:2Mg+CO 2MgO+C
2
【特别提醒】溶液中通入CO 气体产生沉淀的问题:向BaCl 或CaCl 溶液中通入CO 气体,由于盐酸的酸性
2 2 2 2
比碳酸的强,不会产生BaCO 或CaCO 沉淀。
3 3
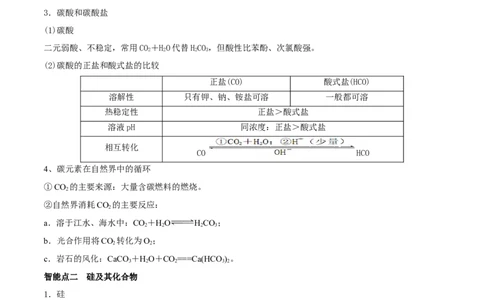
3.碳酸和碳酸盐
(1)碳酸
二元弱酸、不稳定,常用CO+HO代替HCO,但酸性比苯酚、次氯酸强。
2 2 2 3
(2)碳酸的正盐和酸式盐的比较
正盐(CO) 酸式盐(HCO)
溶解性 只有钾、钠、铵盐可溶 一般都可溶
热稳定性 正盐>酸式盐
溶液pH 同浓度:正盐>酸式盐
相互转化
CO HCO
4、碳元素在自然界中的循环
①CO 的主要来源:大量含碳燃料的燃烧。
2
②自然界消耗CO 的主要反应:
2
a.溶于江水、海水中:CO+HO HCO;
2 2 2 3
b.光合作用将CO 转化为O;
2 2
c.岩石的风化:CaCO +HO+CO===Ca(HCO)。
3 2 2 3 2
智能点二 硅及其化合物
1.硅
(1)硅的结构与物理性质
(2)化学性质a.常温
①与氢氟酸反应的化学方程式:Si+4HF===SiF ↑+2H ↑;
4 2
②与NaOH溶液反应的化学方程式:Si+2NaOH+H O===Na SiO +2H ↑;
2 2 3 2
③与F 反应的化学方程式:Si+2F ===SiF
2 2 4
b.高温
①与O 反应:Si+O SiO 。
2 2 2
②与Cl 反应:Si+Cl SiCl
2 2 4
(3)硅的工业制法
①原料:石英砂和焦炭
②制备:SiO+2C=====Si(粗)+2CO↑
2
③提纯:Si(粗)+2Cl SiCl ;SiCl +2H Si(纯)+4HCl
2 4 4 2
【特别提醒】①用焦炭还原SiO,产物是CO而不是CO。
2 2
②粗硅中含碳等杂质,与Cl 反应生成的SiCl 中含有CCl 等杂质,经过分馏提纯SiCl 后,再用H 还原,
2 4 4 4 2
得到高纯度硅。
(4)用途:半导体材料、太阳能电池、计算机芯片和耐酸设备等。
2.二氧化硅
(1)存在:硅石、石英、水晶、玛瑙、沙子等
(2)二氧化硅的结构特点
在SiO 晶体中,每个Si周围结合4个O,Si在中心,O在4个顶角;许多这样的 四面体又通
2
过顶角的O相连接,每个O为两个四面体所共有,即每个O与2个Si相结合。实际上,SiO 晶体是由Si
2
和O按1∶2的比例所组成的立体网状结构的晶体。由结构可知,二氧化硅的化学性质很稳定。
(3)物理性质:熔点高,硬度大,不溶于水
(4)化学性质:
a.酸性氧化物
①与碱反应:SiO +2NaOH===Na SiO +H O;
2 2 3 2
②与CaO碱性氧化物反应:SiO +CaO CaSiO
2 3
③与盐反应:SiO +Na CO Na SiO +CO ↑;SiO +CaCO CaSiO +CO ↑(工业制玻璃)
2 2 3 2 3 2 2 3 3 2
b.氧化性:
高温
①与碳反应:SiO
2
+2C Si+2CO↑(制粗硅);SiO
2
+3C SiC+2CO↑(制金刚砂);
②与Mg反应:4Mg+SiO 2MgSi+2MgO;MgSi+2H O=SiH ↑+2Mg(OH)(制硅化氢);
2 2 2 2 4 2c.特性:
与氢氟酸反应:SiO+4HF===SiF ↑+2H O
2 4 2
(5)用途
①水晶可用于电子工业的部件、光学仪器、工艺品
②SiO 是制光导纤维的重要原料
2
③较纯的石英用于制造石英玻璃
④石英砂用于制玻璃的原料及建筑材料
【特别提醒】(1)由于玻璃的成分中含有SiO,故实验室盛放碱液的试剂瓶用橡皮塞而不用玻璃塞。
2
(2)未进行磨砂处理的玻璃,在常温下是不易被强碱腐蚀的。
(3)因为氢氟酸腐蚀玻璃,与玻璃中的SiO 反应,所以氢氟酸不能用玻璃瓶保存,而应保存在塑料瓶或
2
铅皿中。
(4)SiO 是HSiO 的酸酐,但SiO 不与水反应,不能用SiO 直接与水作用制备HSiO。
2 2 3 2 2 2 3
3.硅酸
(1)物理性质:硅酸是一种白色胶状物质,不溶于水,能形成胶体。新制备的硅酸为透明、胶冻状,硅
酸经干燥脱水形成硅酸干凝胶——“硅胶”。
(2)化学性质:
a.弱酸性:硅酸的酸性很弱,比碳酸的酸性还弱,在与碱反应时只能与强碱反应。如 :
HSiO+2NaOH==Na SiO+2H O。
2 3 2 3 2
b.不稳定性:硅酸的热稳定性很差,受热分解为SiO 和HO:HSiO=====SiO+HO。
2 2 2 3 2 2
(3)制备:
由于SiO 不溶于水,所以硅酸是通过可溶性硅酸盐与其他酸反应制得的。
2
NaSiO+2HCl==H SiO↓+2NaCl,
2 3 2 3
NaSiO+CO +H O==H SiO↓+Na CO(证明酸性:HCO>HSiO)。
2 3 2 2 2 3 2 3 2 3 2 3
(4)用途:硅胶可作催化剂的载体和袋装食品、瓶装药品的干燥剂。
4.硅酸盐
(1)硅酸钠
①物理性质:白色、可溶于水的粉末状固体,其水溶液俗称水玻璃,有黏性,水溶液显碱性。
②化学性质——与酸性较硅酸强的酸反应:
a.与盐酸反应的化学方程式:
NaSiO+2HCl===2NaCl+HSiO↓。
2 3 2 3
b.与CO 水溶液反应的化学方程式:
2
NaSiO+HO+CO===Na CO+HSiO↓。
2 3 2 2 2 3 2 3
③用途:黏合剂(矿物胶)、防腐剂和耐火阻燃材料。
【特别提醒】①NaSiO 的水溶液是一种黏合剂,是制备硅胶和木材防火剂等的原料;NaSiO 易与空气中
2 3 2 3
的CO、HO反应,要密封保存。
2 2
②可溶性碳酸盐、硅酸盐的水溶液呈碱性,保存该溶液的试剂瓶不能用玻璃塞,应用橡胶塞。(2)硅酸盐的氧化物表示法:
氧化物的书写顺序:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水,不同氧化物间以“·”隔开。
如硅酸钠(NaSiO)可表示为NaO·SiO,
2 3 2 2
长石(KAlSiO)可表示为KO·AlO·6SiO。
3 8 2 2 3 2
【特别提醒】(1)氧化物之间以“· ”隔开;(2)计量数配置出现分数应化为整数。硅酸盐改写为氧
化物形式时,各元素的化合价保持不变,且满足化合价代数和为零,各元素原子个数比符合原来的组成。
当系数配置出现分数时一般应化为整数。如上例中 KAlSiO ,将 KO·AlO·3SiO ,要写成
3 8 2 2 3 2
KO·AlO·6SiO。
2 2 3 2
智能点三 无机非金属材料
1.传统无机非金属材料,如水泥、玻璃、陶瓷等硅酸盐材料。
水泥 玻璃 陶瓷
主要原料 黏土、石灰石、石膏 石灰石、石英砂、纯碱 黏土
主要设备 水泥回转窑 玻璃窑 陶瓷窑
复杂的物理、化学变 主要反应:NaCO+SiO=====NaSiO+ 复杂的物理、化
变化 2 3 2 2 3
化过程 CO↑、CaCO+SiO=====CaSiO+CO↑ 学变化过程
2 3 2 3 2
硅酸三钙
(3CaO·SiO)
2
硅酸二钙
组成 硅酸钠、硅酸钙和二氧化硅 硅酸盐
(2CaO·SiO)
2
铝酸三钙
3CaO·AlO)
2 3
在工农业、科
用途 重要的建筑材料 制化学实验用的玻璃仪器、窗玻璃等 技、生活、实验
室中使用广泛
2.新型无机非金属材料,如高温结构陶瓷、光导纤维、生物陶瓷、压电陶瓷等。
材料类别 主要特性 示例 用途
高温结构陶 能承受高温,
氮化硅陶瓷 汽轮机叶片、轴承、永久性模具等
瓷 强度高
半导体陶瓷 具有电学特性 二氧化锡陶瓷 集成电路中的半导体
光学材料 具有光学特性 光导纤维 光缆通讯、医疗、照明等
生物陶瓷 具有生物功能 氧化铝陶瓷 人造骨骼、人造关节、接骨螺钉
智能点四 碳、硅及其化合物性质“反常”小结
(1)一般情况下,非金属元素单质熔、沸点低,硬度小,但晶体硅、金刚石熔、沸点高,硬度大,其中金
刚石为自然界中硬度最大的物质。
(2)一般情况下,非金属单质为绝缘体,但硅为半导体,石墨为电的良导体。
(3)Si的还原性强于C,但C在高温下能还原出Si:SiO+2C=====Si+2CO↑。
2
(4)非金属单质与碱反应一般既作氧化剂又作还原剂,且无氢气放出,但硅与强碱溶液反应只作还原剂,
且放出氢气:Si+2NaOH+HO===NaSiO+2H↑。
2 2 3 2(5)非金属单质一般不与非氧化性酸反应,但硅能跟氢氟酸反应:Si+4HF===SiF↑+2H↑。
4 2
(6)一般情况下,碱性氧化物+酸―→盐+水,二氧化硅是酸性氧化物,却能与氢氟酸反应:SiO +
2
4HF===SiF↑+2HO(SiF 不属于盐,故SiO 不是两性氧化物)。
4 2 4 2
(7)一般情况下,无机酸能溶于水,但硅酸却难溶于水。
(8)一般情况下,较强酸+较弱酸的盐―→较弱酸+较强酸的盐(溶液中的反应)。
因碳酸的酸性强于硅酸,所以水玻璃在空气中易变质:NaSiO+HO+CO===NaCO+HSiO(胶体)。
2 3 2 2 2 3 2 3
但在高温下,可发生反应NaCO+SiO=====NaSiO+CO↑(CO 离开反应体系促进反应的正向进行)。
2 3 2 2 3 2 2
(9)一般情况下,金属(Na、K)能置换出水中的氢,但C在高温下也能置换出HO中的氢:C+HO(g)=====H
2 2 2
+CO。
(10)一般情况下,酸性氧化物与水反应生成相应的含氧酸,但二氧化硅不溶于水,也不与水反应。
智能点五 CO 与碱、盐溶液的反应规律
2
1、与碱溶液的反应
(1)反应原理
NaOH――→NaCO――→NaHCO
2 3 3
(2)反应后溶质成分的判断
x= 溶质成分
x≤1∶1 NaHCO
3
1∶12∶1 NaOH、NaCO
2 3
也可用数轴来表示:
①CO+NaCO+HO===2NaHCO
2 2 3 2 3
②CO+NaSiO+2HO===HSiO↓+NaCO
2 2 3 2 4 4 2 3
或CO+NaSiO+HO===HSiO↓+NaCO
2 2 3 2 2 3 2 3
当CO 过量时,发生反应如下:
2
2CO+NaSiO+2HO===HSiO↓+2NaHCO
2 2 3 2 2 3 3
③CO+Ca(ClO)+HO===CaCO↓+2HClO
2 2 2 3
2、与盐溶液的反应
(1)CO 与盐溶液的常见反应
2
碳酸是一种弱酸,其酸性比盐酸、醋酸要弱,因此,盐酸、醋酸能与碳酸盐反应;其酸性又比硅酸、次氯
酸、苯酚、偏铝酸等强,因此,将CO 气体通入NaSiO 、NaClO、 、NaAlO 等盐溶液中,均能发生反
2 2 3 2
应而生成相应的弱酸和碳酸(氢)盐,这就是“强酸制弱酸”原理的应用。如:
①CO+NaCO+HO===2NaHCO
2 2 3 2 3
②CO+NaSiO+2HO===HSiO↓+NaCO
2 2 3 2 4 4 2 3
或CO+NaSiO+HO===HSiO↓+NaCO
2 2 3 2 2 3 2 3当CO 过量时,发生反应如下:
2
2CO+NaSiO+2HO===HSiO↓+2NaHCO
2 2 3 2 2 3 3
③CO+Ca(ClO)+HO===CaCO↓+2HClO
2 2 2 3
当CO 过量时,发生反应如下:
2
2CO+Ca(ClO)+2HO===Ca(HCO)+2HClO
2 2 2 3 2
④CO+ +HO―→ +NaHCO
2 2 3
⑤CO+NaAlO+2HO===Al(OH)↓+NaHCO(CO 过量时)
2 2 2 3 3 2
CO+2NaAlO+3HO===2Al(OH)↓+NaCO(CO 少量时)
2 2 2 3 2 3 2
(2)注意事项
①“强酸制弱酸”是一个重要的化学反应规律,但不可认为弱酸就不能“制取”强酸。在某些条件下,当
弱酸的酸根阴离子被沉淀或被氧化后,H+就被“释放”出来,从而生成了强酸。如将HS通入CuSO 溶液中
2 4
或向氢硫酸中滴加氯水,均由氢硫酸这种弱酸生成了强酸:HS+CuSO===CuS↓+HSO(S2-与Cu2+结合成
2 4 2 4
难溶的CuS),HS+Cl===S↓+2HCl(S2-被氧化)。
2 2
②CO 与 溶液反应的产物与CO 的用量无关,都生成NaHCO,因为酸性HCO> >HCO。
2 2 3 2 3
③ CO 与 NaClO 溶液反应的产物与 CO 的量无关,也只能生成 NaHCO ,不能生成 NaCO ,因为酸性
2 2 3 2 3
HCO>HClO>HCO。
2 3
④CO、SO 通入CaCl 或BaCl 溶液均不反应,无沉淀产生。
2 2 2 2
【典例剖析】
高频考点1 考查碳及及其化合物性质和应用
例1、下列有关碳及其化合物的说法正确的是( )
A.CO 是导致酸雨的主要气体
2
B.CO和CO 组成元素相同,所以他们的化学性质相同
2
C.金刚石、石墨是碳的单质,而C 是碳的化合物
60
D.在高温条件下,碳能使CO 转变成CO
2
【变式训练1】(碳循环)(2021·福建高三三模)海洋碳循环是全球碳循环的重要组成部分,是影响全
球气候变化的关键控制环节。下图为海洋中碳循环的简单原理图。下列说法错误的是
A.海洋碳循环过程中能将太阳能转化为化学能
B.钙化释放CO 的离子方程式:2HCO +Ca2+=CaCO↓+CO↑+HO
2 3 2 2C.影响海洋碳循环的因素主要有海水的酸碱性、水温、藻类生物的分布等
D.光合作用,每生成0.1mol(CHO) 转移电子数为4N(N表示阿伏伽德罗常数)
2 x A A
【变式训练2】(碳的氧化物的性质及应用)(2020·湘赣皖十五校第一次联考模拟题)通过资源化利用的方
式将CO 转化为具有工业应用价值的产品(如图所示),是一种较为理想的减排方式,下列说法中正确的是(
2
)
A.CO 经催化分解为C、CO、O 的反应为放热反应
2 2
B.除去NaCO 固体中少量NaHCO 可用热分解的方法
2 3 3
C.过氧化尿素和SO 都能使品红溶液褪色,其原理相同
2
D.由CO 和H 合成甲醇,原子利用率达100%
2 2
高频考点2 考查硅及其化合物的性质和应用
例2.下列表述正确的是( )
①人造刚玉熔点很高,可用作高级耐火材料,主要成分是二氧化硅
②化学家采用玛瑙研钵摩擦固体反应物进行无溶剂合成,玛瑙的主要成分是硅酸盐,③提前建成的三峡大
坝使用了大量水泥,水泥是硅酸盐材料,④夏天到了,游客佩戴由添加氧化亚铜的二氧化硅玻璃制作的变
色眼镜来保护眼睛,⑤太阳能电池可采用硅材料制作,其应用有利于环保、节能
A.①②③ B.②④ C.③④⑤ D.③⑤
【变式训练1】(二氧化硅的性质和用途)二氧化硅广泛存在于自然界中,在日常生活、生产、科研及新
型材料等方面有着重要的用途。a~e是对①~⑤反应中SiO 所表现的化学性质或作用进行的判断,其中正
2
确的是( )
①SiO+2NaOH===Na SiO+HO
2 2 3 2
②SiO+2C=====Si+2CO↑
2
③SiO+4HF===SiF ↑+2HO
2 4 2
④NaCO+SiO=====NaSiO+CO↑
2 3 2 2 3 2
⑤SiO+3C=====SiC+2CO↑
2
a.反应①中SiO 作为玻璃的成分被消耗,用于刻蚀玻璃
2
b.反应②中SiO 表现出氧化性
2c.反应③中SiO 表现出酸性氧化物的通性
2
d.反应④符合用难挥发性的酸酐制取易挥发性的酸酐的道理
e.反应⑤中SiO 未参加氧化还原反应
2
A.ace B.bde C.cde D.ab
【变式训练2】(硅酸盐的性质和表示方法)(2020·湖南怀化市高三期末)青石棉是一种致癌物质,是《鹿
特丹公约》中受限制的46种化学品之一,其化学式为NaFeSiO (OH) 。青石棉用稀硝酸处理时,还原产
2 5 8 22 2
物只有NO,下列说法不正确的是( )
A.青石棉是一种硅酸盐产品
B.青石棉中含有一定量的石英晶体
C.青石棉的化学组成可表示为NaO·3FeO·FeO·8SiO·HO
2 2 3 2 2
D.1 mol青石棉能还原1 mol HNO
3
高频考点3 考查无机非金属材料的分类和应用
例3.下列关于无机非金属材料的说法中不正确的是( )
A.传统无机非金属材料是指玻璃、水泥、陶瓷等硅酸盐材料
B.新型无机非金属材料克服了传统无机非金属材料的许多缺点
C.高温结构材料具有耐高温、耐酸碱腐蚀、硬度大、耐磨损、密度小等优点
D.传统无机非金属材料和新型无机非金属材料的主要成分都是硅酸盐
【变式训练1】(传统无机非金属材料)陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与
化学有着密切的关系。下列说法错误的是
A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁
B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成
C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐
D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点
【变式训练2】(新型无机非金属材料)平昌冬奥会“北京8分钟”主创团队用石墨烯制作了-20 ℃能发
热4 h的智能服饰;用铝合金管材和碳纤维制作了高2.35 m、重量仅为10 kg的熊猫木偶,向世界展现了新
时代的中国形象。下列说法中,不正确的是( )
A.石墨烯是能导热的金属材料
B.铝合金是密度较小的金属材料
C.碳纤维是耐低温的无机非金属材料
D.新型材料种类多、用途广
高频考点4 考查CO 通入碱溶液中反应产物的判断及计算
2
例4.(2020·湘赣皖十五校第一次联考)往含0.2 mol NaOH和0.1 mol Ba(OH) 的混合溶液中持续稳定地通
2入CO 气体6.72 L(标准状况下),则在这一过程中,下列有关溶液中离子总物质的量(n)随通入CO 气体体
2 2
积(V)的变化曲线中正确的是(离子水解忽略不计)( )
【变式训练】(2020·吉林模拟)将足量CO 通入KOH和Ca(OH) 的混合稀溶液中,生成沉淀的物质的量(n)
2 2
和通入CO 体积(V)的关系正确的是( )
2