文档内容
2022—2023 学年度(上)六校高三期初考试
化学试题
考试时间:75分钟 满分:100分
可能用到的相对原子质量:H—1 C—12 O—16 Na—23 S—16
一、选择题(每题3分,共45分。每小题只有一个选项符合题意)
1.生活中处处有化学。下列叙述正确的是
A.HB铅笔芯的成分为二氧化铅
B.焰火中紫色来源于钠盐灼烧
C.漂白粉与盐酸可混合使用以提高消毒效果
D.碳酸氢钠可做食品膨松剂
2.下列表示正确的是
A.乙醛的结构简式:
B. 丁烯的键线式:
C.基态碳原子的轨道表示式:
D.过氧化钠的电子式:
3.N 为阿伏加德罗常数的值,下列说法正确的是
A
A.8g CH 含有中子数为3N
4 A
B.0.1mol/L HClO 溶液中含有的H+数为0.1N
4 A
C.1.2g NaHSO 中含有0.02N 个阳离子
4 A
D.0.1mol H 和0.1mol I 于密闭容器中充分反应后,HI分子总数为0.2N
2 2 A
4.下列关于有机物的说法正确的是
A.苯、乙烯和乙酸都能与H 发生加成反应
2
B.苯乙烯( )易溶于水及苯
C. 的一氯代物有四种
D.CH =CH−CH=CH 中所有原子不可能共平面
2 2
5.W、X、Y、Z为原子序数依次增大的短周期元素,四种元素的核外电子总
数满足X+Y=W+Z;化合物XW 与WZ相遇会产生白烟。下列叙述正确的是
3
A.元素的电负性:W>X>Y
B.原子半径:Z>Y>X>W
下载最新免费模拟卷,到公众号:一枚试卷君C.最高价氧化物的水化物的酸性:X>Z
D.Y和W、X、Z均可形成离子化合物
6.关于反应 ,下列说法正确的是
A.H SO 是还原剂
2 4
B.氧化产物与还原产物的物质的量之比为2∶1
C.0.5mol Na S O 发生反应,转移1mol电子
2 2 3
D.Na S O 与稀硝酸也能发生类似反应
2 2 3
7.下列“类比”合理的是
A.Na与H O反应生成NaOH和H ,则Al与H O反应生成Al(OH) 和H
2 2 2 3 2
B.Na N与盐酸反应生成NaCl和NH Cl,则Mg N 与盐酸反应生成MgCl 和
3 4 3 2 2
NH Cl
4
C.NaClO溶液与CO 反应生成NaHCO 和HClO,则NaClO溶液与SO 反应
2 3 2
生成NaHSO 和HClO
3
D.NaOH溶液与少量 AgNO 溶液反应生成 Ag O和NaNO ,则氨水与少量
3 2 3
AgNO 溶液反应生成Ag O和NH NO
3 2 4 3
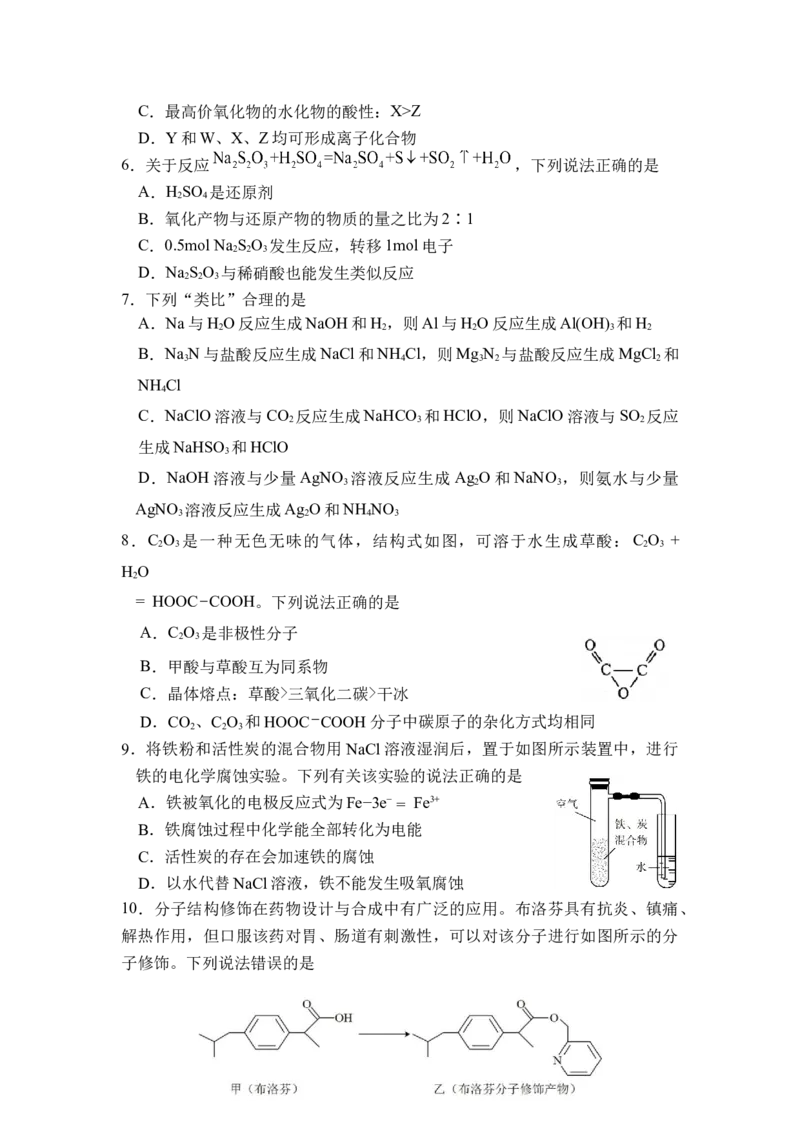
8.C O 是一种无色无味的气体,结构式如图,可溶于水生成草酸:C O +
2 3 2 3
H O
2
= HOOC−COOH。下列说法正确的是
A.C O 是非极性分子
2 3
B.甲酸与草酸互为同系物
C.晶体熔点:草酸>三氧化二碳>干冰
D.CO 、C O 和HOOC−COOH分子中碳原子的杂化方式均相同
2 2 3
9.将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图所示装置中,进行
铁的电化学腐蚀实验。下列有关该实验的说法正确的是
A.铁被氧化的电极反应式为Fe−3e− = Fe3+
B.铁腐蚀过程中化学能全部转化为电能
C.活性炭的存在会加速铁的腐蚀
D.以水代替NaCl溶液,铁不能发生吸氧腐蚀
10.分子结构修饰在药物设计与合成中有广泛的应用。布洛芬具有抗炎、镇痛、
解热作用,但口服该药对胃、肠道有刺激性,可以对该分子进行如图所示的分
子修饰。下列说法错误的是A.甲的分子式为C H O
13 18 2
B.甲分子中最多有8个碳原子共平面
C.甲和乙都能与氢氧化钠溶液发生反应
D.甲修饰成乙可降低对胃、肠道的刺激
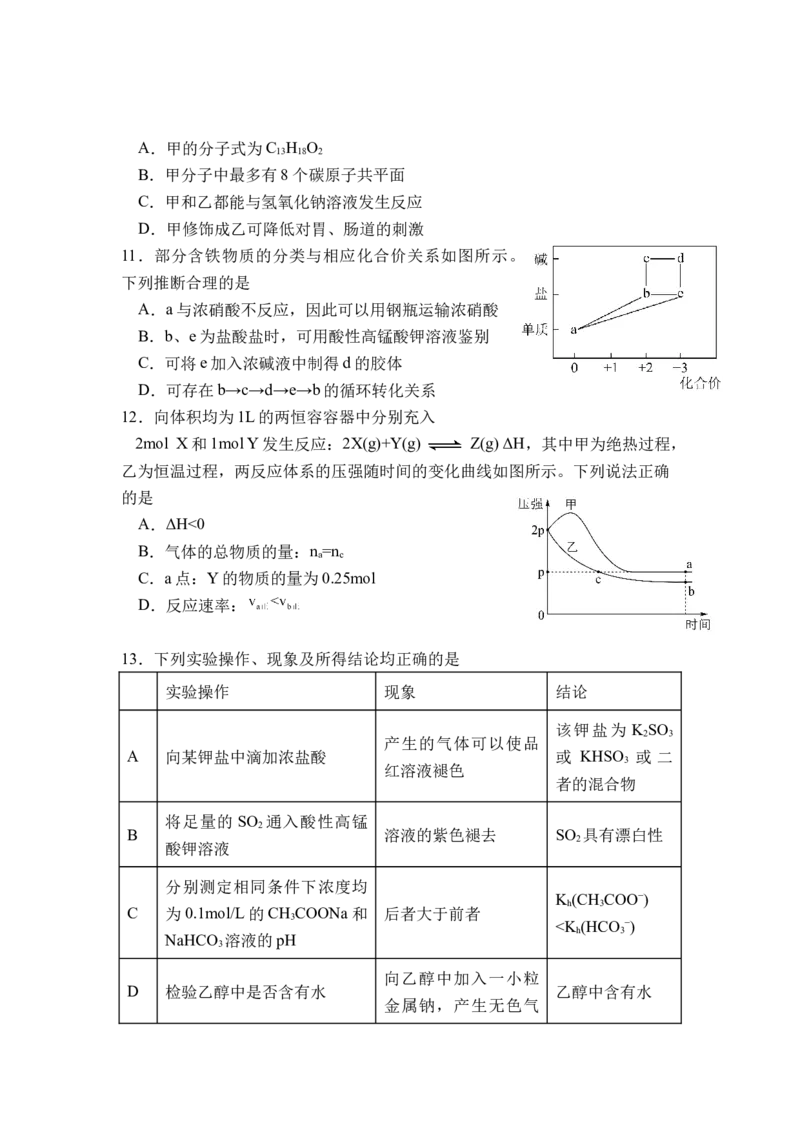
11.部分含铁物质的分类与相应化合价关系如图所示。
下列推断合理的是
A.a与浓硝酸不反应,因此可以用钢瓶运输浓硝酸
B.b、e为盐酸盐时,可用酸性高锰酸钾溶液鉴别
C.可将e加入浓碱液中制得d的胶体
D.可存在b→c→d→e→b的循环转化关系
12.向体积均为1L的两恒容容器中分别充入
2mol X和1mol Y发生反应:2X(g)+Y(g) Z(g) ΔH,其中甲为绝热过程,
乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确
的是
A.ΔH<0
B.气体的总物质的量:n =n
a c
C.a点:Y的物质的量为0.25mol
D.反应速率:
13.下列实验操作、现象及所得结论均正确的是
实验操作 现象 结论
该钾盐为 K SO
2 3
产生的气体可以使品
A 向某钾盐中滴加浓盐酸 或 KHSO 或 二
3
红溶液褪色
者的混合物
将足量的 SO 通入酸性高锰
2
B 溶液的紫色褪去 SO 具有漂白性
2
酸钾溶液
分别测定相同条件下浓度均
K (CH COO−)
h 3
C 为0.1mol/L的CH COONa和 后者大于前者
3
c(B+)>c(BOH)
第 II 卷(非选择题,共 55 分)
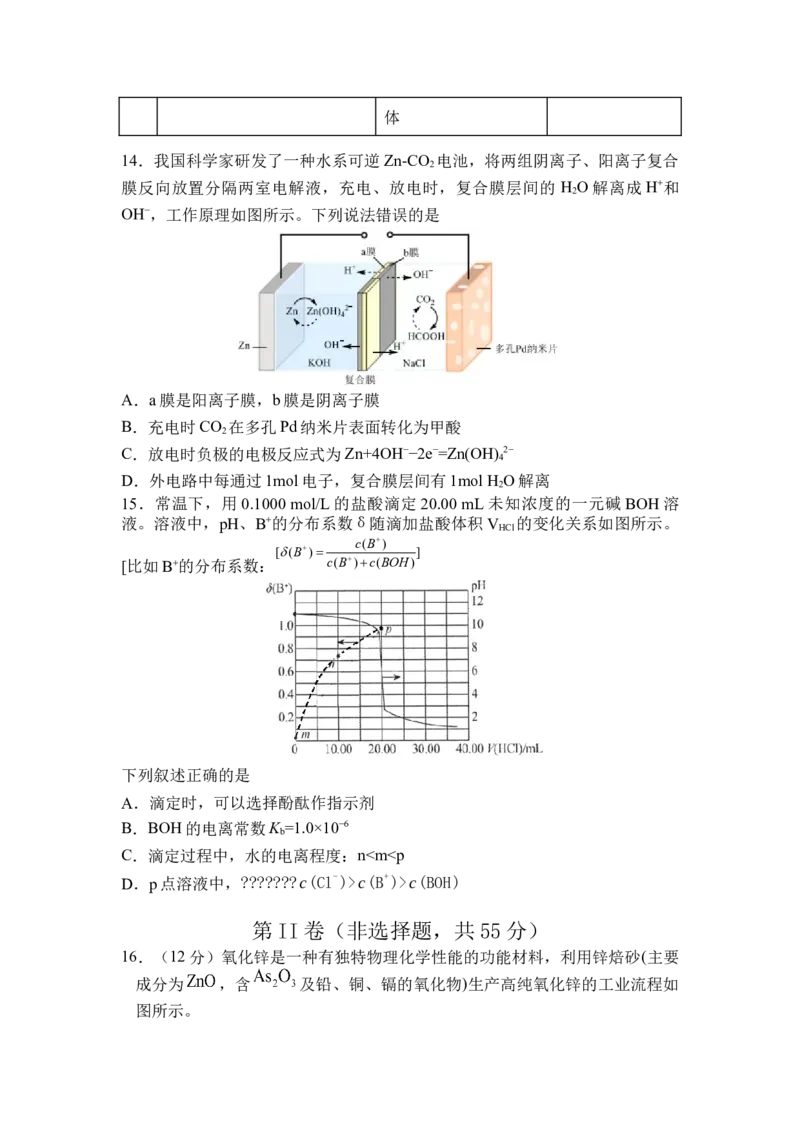
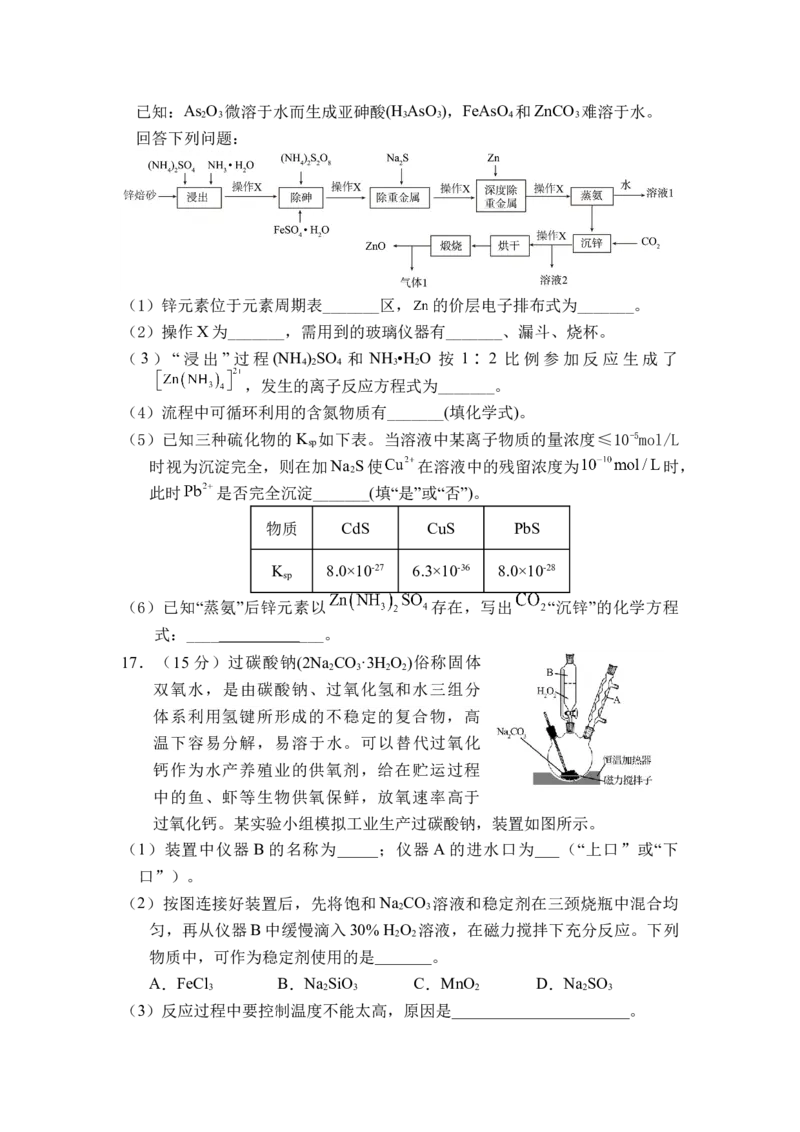
16.(12分)氧化锌是一种有独特物理化学性能的功能材料,利用锌焙砂(主要
成分为 ,含 及铅、铜、镉的氧化物)生产高纯氧化锌的工业流程如
图所示。已知:As O 微溶于水而生成亚砷酸(H AsO ),FeAsO 和ZnCO 难溶于水。
2 3 3 3 4 3
回答下列问题:
(1)锌元素位于元素周期表_______区, 的价层电子排布式为_______。
(2)操作X为_______,需用到的玻璃仪器有_______、漏斗、烧杯。
(3)“浸出”过程(NH ) SO 和 NH •H O 按 1∶2 比例参加反应生成了
4 2 4 3 2
,发生的离子反应方程式为_______。
(4)流程中可循环利用的含氮物质有_______(填化学式)。
(5)已知三种硫化物的K 如下表。当溶液中某离子物质的量浓度≤10-5mol/L
sp
时视为沉淀完全,则在加Na S使 在溶液中的残留浓度为 时,
2
此时 是否完全沉淀_______(填“是”或“否”)。
物质 CdS CuS PbS
K 8.0×10-27 6.3×10-36 8.0×10-28
sp
(6)已知“蒸氨”后锌元素以 存在,写出 “沉锌”的化学方程
式:____ ___。
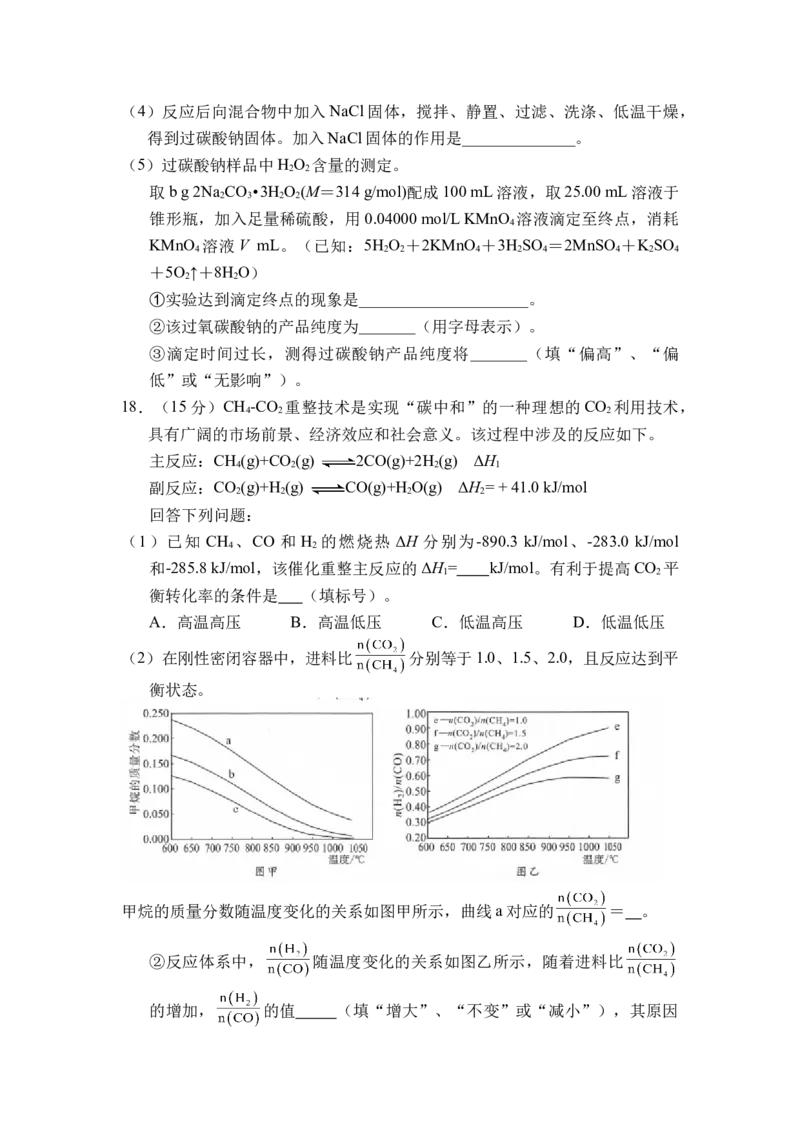
17.(15 分)过碳酸钠(2Na CO ·3H O )俗称固体
2 3 2 2
双氧水,是由碳酸钠、过氧化氢和水三组分
体系利用氢键所形成的不稳定的复合物,高
温下容易分解,易溶于水。可以替代过氧化
钙作为水产养殖业的供氧剂,给在贮运过程
中的鱼、虾等生物供氧保鲜,放氧速率高于
过氧化钙。某实验小组模拟工业生产过碳酸钠,装置如图所示。
(1)装置中仪器 B 的名称为_____;仪器 A 的进水口为___(“上口”或“下
口”)。
(2)按图连接好装置后,先将饱和Na CO 溶液和稳定剂在三颈烧瓶中混合均
2 3
匀,再从仪器B中缓慢滴入30% H O 溶液,在磁力搅拌下充分反应。下列
2 2
物质中,可作为稳定剂使用的是_______。
A.FeCl B.Na SiO C.MnO D.Na SO
3 2 3 2 2 3
(3)反应过程中要控制温度不能太高,原因是______________________。(4)反应后向混合物中加入NaCl固体,搅拌、静置、过滤、洗涤、低温干燥,
得到过碳酸钠固体。加入NaCl固体的作用是______________。
(5)过碳酸钠样品中H O 含量的测定。
2 2
取b g 2Na CO •3H O (M=314 g/mol)配成100 mL溶液,取25.00 mL溶液于
2 3 2 2
锥形瓶,加入足量稀硫酸,用0.04000 mol/L KMnO 溶液滴定至终点,消耗
4
KMnO 溶液V mL。(已知:5H O +2KMnO +3H SO =2MnSO +K SO
4 2 2 4 2 4 4 2 4
+5O ↑+8H O)
2 2
①实验达到滴定终点的现象是_____________________。
②该过氧碳酸钠的产品纯度为_______(用字母表示)。
③滴定时间过长,测得过碳酸钠产品纯度将_______(填“偏高”、“偏
低”或“无影响”)。
18.(15分)CH -CO 重整技术是实现“碳中和”的一种理想的CO 利用技术,
4 2 2
具有广阔的市场前景、经济效应和社会意义。该过程中涉及的反应如下。
主反应:CH (g)+CO (g) 2CO(g)+2H (g) ΔH
4 2 2 1
副反应:CO (g)+H (g) CO(g)+H O(g) ΔH = + 41.0 kJ/mol
2 2 2 2
回答下列问题:
(1)已知 CH 、CO 和 H 的燃烧热 ΔH 分别为-890.3 kJ/mol、-283.0 kJ/mol
4 2
和-285.8 kJ/mol,该催化重整主反应的ΔH = kJ/mol。有利于提高CO 平
1 2
衡转化率的条件是 (填标号)。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
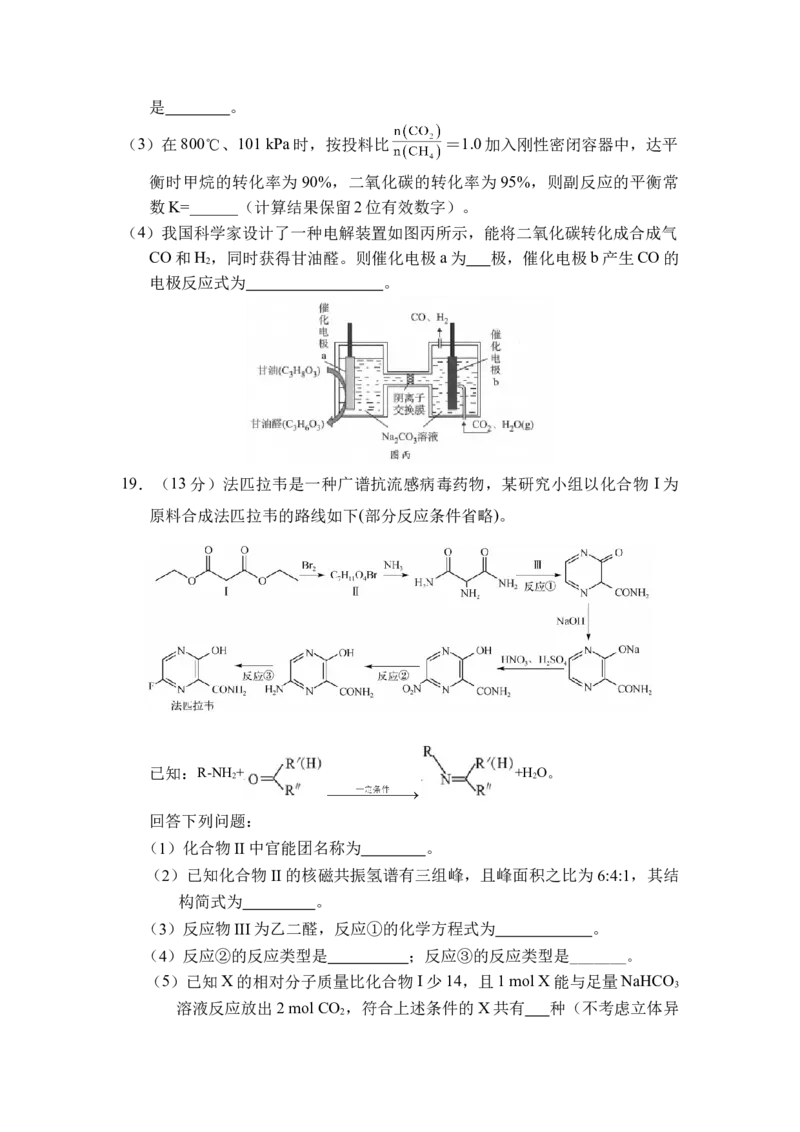
(2)在刚性密闭容器中,进料比 分别等于1.0、1.5、2.0,且反应达到平
衡状态。
甲烷的质量分数随温度变化的关系如图甲所示,曲线a对应的 = 。
②反应体系中, 随温度变化的关系如图乙所示,随着进料比
的增加, 的值 (填“增大”、“不变”或“减小”),其原因是 。
(3)在800℃、101 kPa时,按投料比 =1.0加入刚性密闭容器中,达平
衡时甲烷的转化率为90%,二氧化碳的转化率为95%,则副反应的平衡常
数K=______(计算结果保留2位有效数字)。
(4)我国科学家设计了一种电解装置如图丙所示,能将二氧化碳转化成合成气
CO和H ,同时获得甘油醛。则催化电极a为 极,催化电极b产生CO的
2
电极反应式为 。
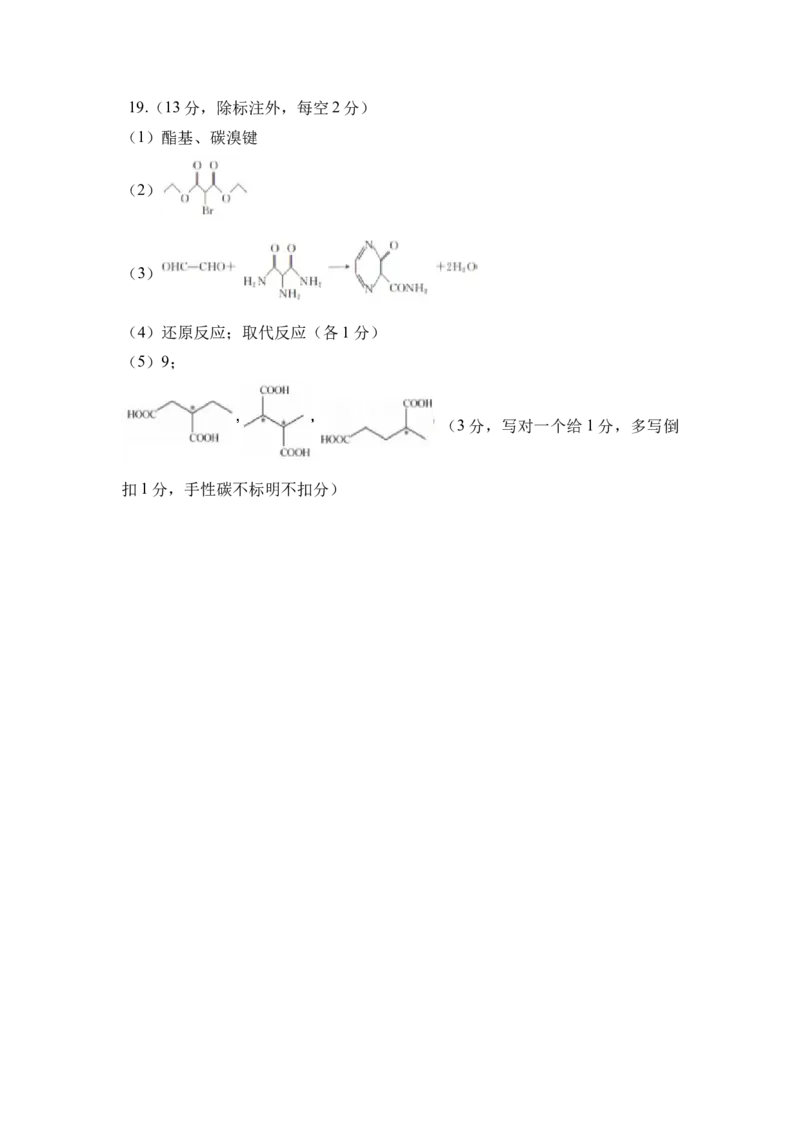
19.(13分)法匹拉韦是一种广谱抗流感病毒药物,某研究小组以化合物 I为
原料合成法匹拉韦的路线如下(部分反应条件省略)。
已知:R-NH + +H O。
2 2
回答下列问题:
(1)化合物II中官能团名称为 。
(2)已知化合物II的核磁共振氢谱有三组峰,且峰面积之比为6:4:1,其结
构简式为 。
(3)反应物III为乙二醛,反应①的化学方程式为 。
(4)反应②的反应类型是 ;反应③的反应类型是_______。
(5)已知X的相对分子质量比化合物I少14,且1 mol X能与足量NaHCO
3
溶液反应放出2 mol CO ,符合上述条件的X共有 种(不考虑立体异
2构),写出含有手性碳原子的所有可能的结构简式: 。(手性碳
原子是指连有4个不同的原子或原子团的饱和碳原子)化学试题参考答案
一、选择题:本题共15小题,每小题3分,共45分。
1 2 3 4 5 6 7 8
D D A C D C B C
9 10 11 12 13 14 15
C B D A C B D
二、非选择题:本题共4小题,共55分。
16.(12分,除标注外,每空2分)
(1)① (1分) ② (1分)
(2)①过滤(1分) ②玻璃棒(1分)
(3)
(4) 、
(5)否
(6)
17. (15分,除标注外,每空2分)
(1)恒压滴液漏斗;下口(1分) (2)B
(3)防止过氧化氢和过碳酸钠发生分解(答防止过氧化氢分解给1分)
(4)增大溶液中C(Na+),降低过碳酸钠的溶解度,有利于过碳酸钠的析出(答
出“降低过碳酸钠的溶解度”即可给分)
(5)①滴入最后半滴KMnO 溶液,溶液由无色变为浅红(浅紫,紫,粉红)
4
色,且半分钟内不褪色
② ×100%(或 、 、 )
③偏低
18. (15分,除标注外,每空2分)
(1)+247.3; B(1分)
(2)① 1.0 ② 减小;随着投料比n(CO )/n(CH )的增加,主反应生成CO和
2 4
H 的量相同,但随着 n(CO )增大,副反应平衡正向移动,导致 n(CO)增多,
2 2
n(H )减少,n(H )/n(CO)减小。
2 2
(3)1.1
(4)阳;CO +H O+2e−===CO+2OH- (或2CO +2e−===CO+CO)
2 2 219.(13分,除标注外,每空2分)
(1)酯基、碳溴键
(2)
(3)
(4)还原反应;取代反应(各1分)
(5)9;
(3分,写对一个给1分,多写倒
扣1分,手性碳不标明不扣分)下载最新免费模拟卷,到公众号:一枚试卷君