文档内容
重难点 10 元素推断与元素周期律
►命题趋势►解题策略►真题回眸►限时检测
考向一 根据“微粒结构式”推断
考向二 根据“文字叙述”推断
元素推断与元素周期律 考向三 根据“元素周期表片段”推断
考向四 根据“原子结构”推断
考向五 根据“物质性质”推断
元素推断与元素周期律因涉及元素“位—构—性”的关系,考察知识面比较广,历来都是高考的重点
和热点。它既考查元素在周期表中的位置,又考查元素原子结构,还考查元素及其化合物的重要性质,更
为重要的是考查三者之间的内在联系及元素周期性的变化规律。
预测2024年高考试题,仍然以短周期元素为背景,考查原子结构、元亲周期律和常见物质的相关性
质。主要有一下几种考察形式:
(1)以“残缺的”元素周期表或元素性质的递变规律为切入点,考查元素的“位-构-性”关系;
(2)结合元素化合物的特殊性质,采用框图或文字叙述形式,考查元素推断、元素周期律的综合运
用;
(3)结合陌生复杂化合物的结构式,从化学键角度进行元素推断,进而对原子结构、元素周期表和
元素周期律进行考查。
题型依然会以选择题为主,难度变化不大。
【策略1】熟练掌握原子结构、核素、同位素的概念
(1)原子的构成
(2)抓住描述对象,突破“四同”判断①同位素——原子,如 H、H。
②同素异形体——单质,如O、O。
2 3
③同系物——化合物,如CHCH、CHCHCH。
3 3 3 2 3
④同分异构体——化合物,如正戊烷、新戊烷。
(3)常见的重要核素及其应用
核素 U C H H O
核燃
用途 用于考古断代 制氢弹 示踪原子
料
(4)核反应方程示例:核聚变、核裂变属于核反应,不是化学变化。
碳14的β衰变 C→N+e
钋209的α衰变 Po→Pb+He
卢瑟福发现质子 N+He→O+H
查德威克发现中子 Be+He→C+n
铀核裂变反应 U+n→Kr+Ba+3n
核反应遵循的两守恒:①反应前后质量数之和不变。
②反应前后质子数之和不变。
【策略2】牢记10e-和18e-微粒的判断与应用
(1)寻找10电子微粒和18电子微粒的方法
①10电子微粒:以Ne为核心,推断同周期的非金属元素的化合物和下一周期的金属元素的化合物。
②18电子微粒:以Ar为核心,推断同周期的非金属元素的化合物和下一周期的金属元素的化合物。CH—CH、HN—NH、HO—OH、F—F、F—CH 、CH—OH……
3 3 2 2 3 3
(2)记忆其他等电子微粒
“2电子”的粒子:He、H-、Li+、Be2+、H。
2
“9电子”的粒子:—F、—OH、—NH 、—CH(取代基)。
2 3
“14电子”的粒子:Si、N、CO。
2
“16电子”粒子:S、O、C H、HCHO。
2 2 4
【策略3】掌握元素周期表的结构特点
注意事项:
①ⅠA族元素不等同于碱金属元素,H元素不属于碱金属元素。
②元素周期表第18列是0族,不是ⅧA族,第8、9、10三列是Ⅷ族,不是ⅧB族。
(1)周期(7个横行,7个周期)
短周期 长周期
周期序数 1 2 3 4 5 6 7
元素种数 2 8 8 18 18 32 32
0族元素原子序数 2 10 18 36 54 86 118
(2)族(18个纵列,16个族)①主族:由短周期元素和长周期元素共同组成的族:ⅠA~ⅦA族。
②副族:仅由长周期元素组成的族:ⅠB~ⅦB族。
③Ⅷ族:包括8、9、10三个纵列。
④0族:第18纵列,该族元素又称为稀有气体元素。
(3)元素周期表的应用
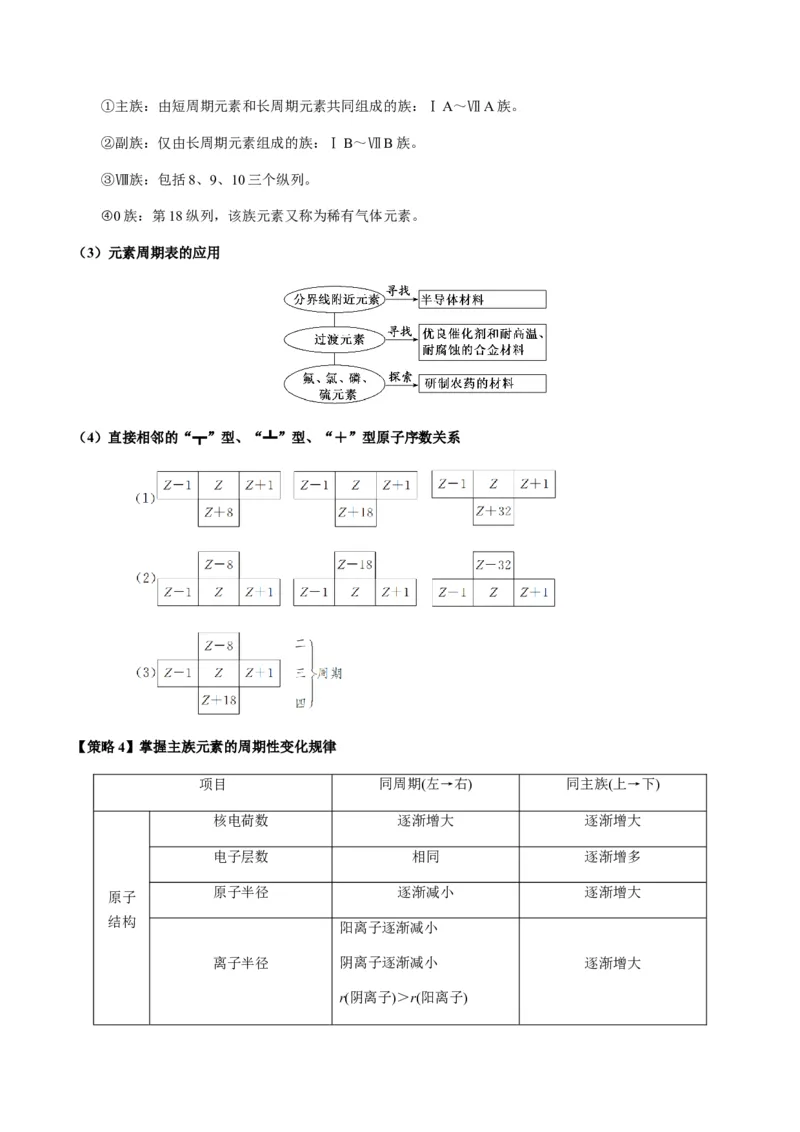
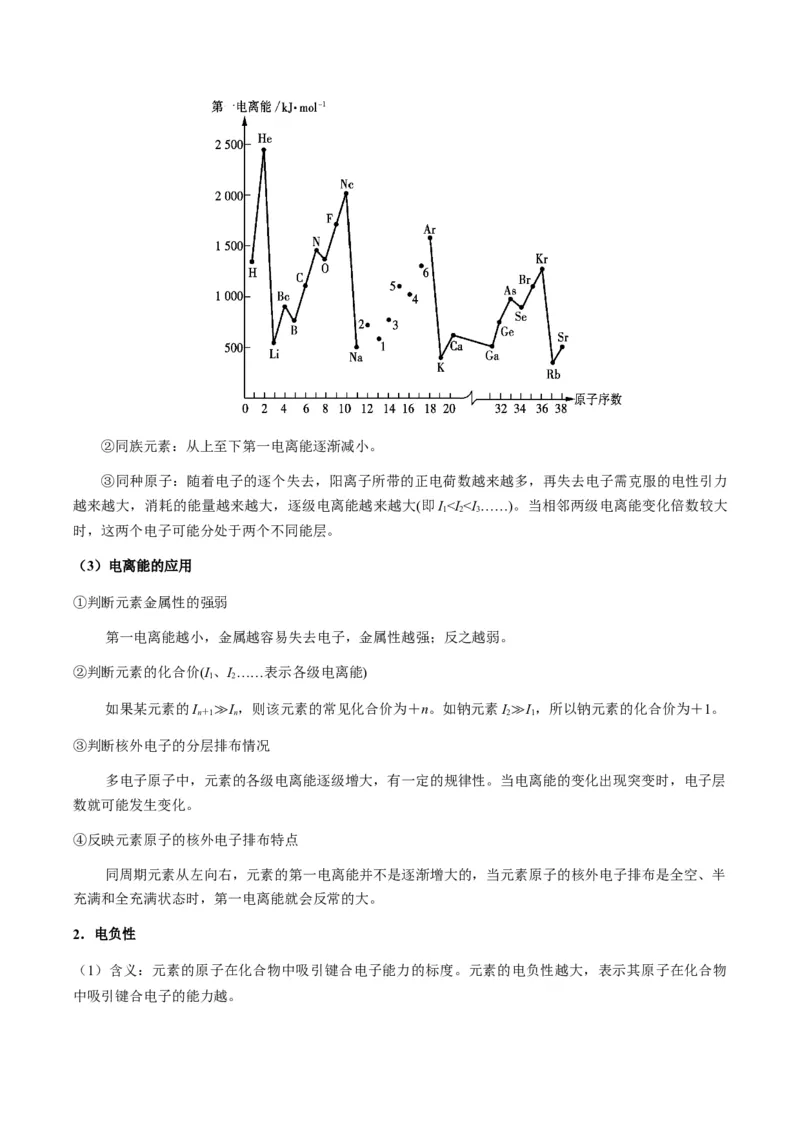
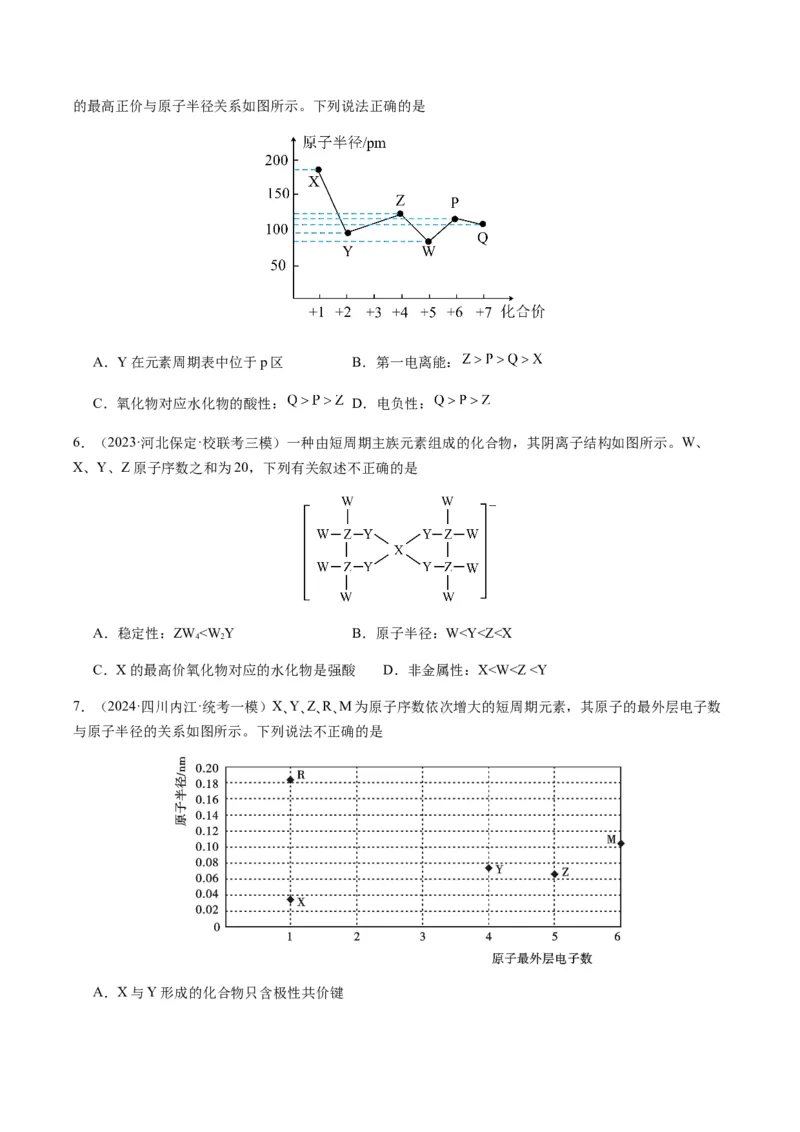
(4)直接相邻的“┳”型、“┻”型、“+”型原子序数关系
【策略4】掌握主族元素的周期性变化规律
项目 同周期(左→右) 同主族(上→下)
核电荷数 逐渐增大 逐渐增大
电子层数 相同 逐渐增多
原子半径 逐渐减小 逐渐增大
原子
结构
阳离子逐渐减小
离子半径 阴离子逐渐减小 逐渐增大
r(阴离子)>r(阳离子)最高正化合价由+1→+7 相同,
化合价 (O、F除外) 最高正化合价=主族序数
负化合价=-(8-主族序数) (O、F除外)
金属性逐渐减弱 金属性逐渐增强
元素的金属性和非金属性
非金属性逐渐增强 非金属性逐渐减弱
性质
阳离子氧化性逐渐增强 阳离子氧化性逐渐减弱
离子的氧化性、还原性
阴离子还原性逐渐减弱 阴离子还原性逐渐增强
气态氢化物的稳定性 逐渐增强 逐渐减弱
碱性逐渐减弱 碱性逐渐增强
最高价氧化物对应的水化
物的酸碱性
酸性逐渐增强 酸性逐渐减弱
(1)“三看”法快速判断简单微粒半径的大小
一看电子层数:最外层电子数相同时,电子层数越多,半径越大。
二看核电荷数:当电子层结构相同时,核电荷数越大,半径越小。
三看核外电子数:当电子层数和核电荷数均相同时,核外电子数越多,半径越大。
(2)对角线规则
在元素周期表中,某些主族元素与右下方的主族元素有些性质是相似的,如:
(3)规避金属性和非金属性判断中的易错点
①关注关键词“最高价”,根据元素氧化物对应水化物的酸碱性的强弱判断元素非金属性或金属性的
强弱时,必须是其最高价氧化物的水化物。
②关注关键词“难易”,判断元素非金属性或金属性的强弱,依据是元素原子在化学反应中得失电子
的难易而不是得失电子的多少。
(4)元素金属性和非金属性强弱的判断方法
本质 原子越易失电子,金属性越强
金属性比较
判断依据 ①在金属活动性顺序中位置越靠前,金属性越强②单质与水或非氧化性酸反应越剧烈,金属性越强
③单质还原性越强或简单阳离子氧化性越弱,金属性越强
④最高价氧化物对应水化物的碱性越强,金属性越强
⑤若Xn++Y→X+Ym+,则Y的金属性比X强
本质 原子越易得电子,非金属性越强
①与H 化合越容易或气态氢化物越稳定,非金属性越强
2
非金属性比较 ②单质氧化性越强或简单阴离子还原性越弱,非金属性越强
判断依据
③最高价氧化物对应水化物的酸性越强,非金属性越强
④若An-+B→Bm-+A,则B的非金属性比A强
【策略5】熟悉电离能、电负性的概念及变化规律
1.电离能
(1)规律
①同周期:第一种元素的第一电离能最小,最后一种元素的第一电离能最大,从左到右总体呈现增大
的变化趋势。同周期主族元素,第ⅡA族(ns2np0)和第ⅤA族(ns2np3),因p轨道处于全空或半充满状态,比
较稳定,所以其第一电离能分别大于同周期相邻的第ⅢA族和第ⅥA族元素,如第一电离能:Mg>Al,
P>S。②同族元素:从上至下第一电离能逐渐减小。
③同种原子:随着电子的逐个失去,阳离子所带的正电荷数越来越多,再失去电子需克服的电性引力
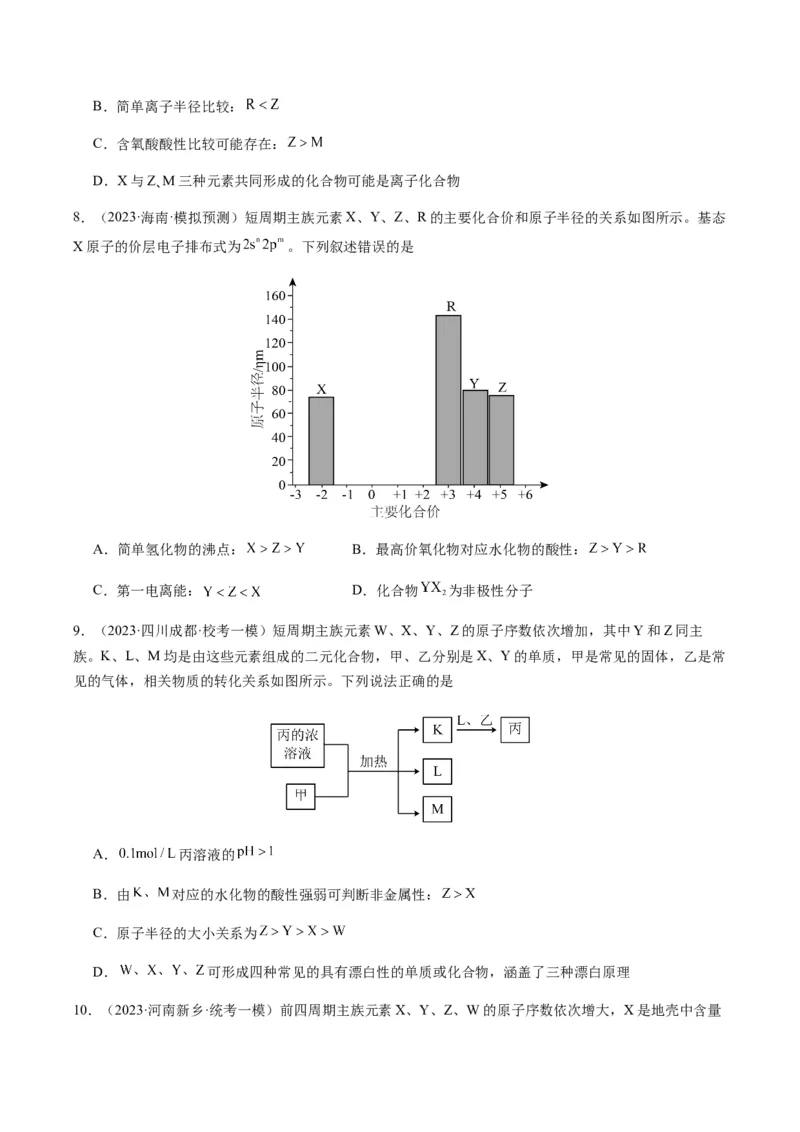
越来越大,消耗的能量越来越大,逐级电离能越来越大(即IY>Z>W
B.原子半径:XY>Z B.电负性:W>X>Y
C.氢化物的沸点:X>Y D.W与Y形成的化合物为分子晶体
2.(2023·河北·校联考二模)短周期元素W、X、Y、Z的原子序数依次增大,它们组成一种团簇分子,
结构如图所示。W、Z的族序数均等于周期序数,X原子核外最外层电子数是其电子总数的 ,下列说法
正确的是A.电负性:XY>Z B.离子半径:W>Z>Y
C.A与C可以反应生成B D.X和Y组成的二元化合物中不含有非极性键
15.(2023·浙江·校联考模拟预测)LDFCB是电池的一种电解质,该电解质阴离子由同周期元素原子W、
X、Y、Z且原子序数依次增大,其结构如下图,Y的最外层电子数等于X的核外电子总数,四种原子最外
层电子数之和为20,下列说法正确的是
A.X的杂化方式是
B.四种元素形成的简单氢化物中Z的沸点最高
C.电负性:
D.元素Z的最高价氧化物的水化物为一元强酸