文档内容
重难点 10 “位、构、性”综合推断
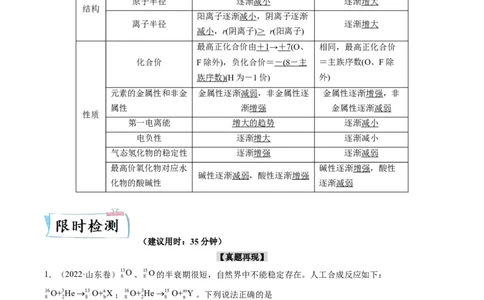
主族元素的周期性变化规律
项目 同周期(左→右) 同主族(上→下)
核电荷数 逐渐增大 逐渐增大
电子层数 相同 逐渐增多
原子
原子半径 逐渐减小 逐渐增大
结构
阳离子逐渐减小,阴离子逐渐
离子半径 逐渐增大
减小,r(阴离子)> r(阳离子)
最高正化合价由 + 1→ + 7(O、 相同,最高正化合价
化合价 F除外),负化合价= - ( 8 -主 =主族序数(O、F除
族序数 )(H为-1价) 外)
元素的金属性和非金 金属性逐渐减弱,非金属性逐 金属性逐渐增强,非
属性 渐增强 金属性逐渐减弱
性质
第一电离能 增大的趋势 逐渐减小
电负性 逐渐增大 逐渐减小
气态氢化物的稳定性 逐渐增强 逐渐减弱
最高价氧化物对应水 碱性逐渐增强,酸性
碱性逐渐减弱,酸性逐渐增强
化物的酸碱性 逐渐减弱
(建议用时:35分钟)
【真题再现】
1.(2022·山东卷)
13O、15O的半衰期很短,自然界中不能稳定存在。人工合成反应如下:
8 8
16O+3He13 O+aX;16O+3He15 O+mY。下列说法正确的是
8 2 8 b 8 2 8 n
A.X的中子数为2
B.X、Y互为同位素
C.
13O、15O可用作示踪原子研究化学反应历程
8 8
D.自然界不存在
13O
、
15O
分子是因其化学键不稳定
8 2 8 2
【答案】B
【解析】根据质量守恒可知,X微粒为6He,Y微粒为 4He,据此分析解题。
2 2
A. 由分析可知,X微粒为6He,根据质量数等于质子数加中子数可知,该微粒的中子数为4,A错误;
2
1
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限公司B. 由分析可知,X微粒为6He,Y微粒为 4He,二者具有相同的质子数而不同的中子数的原子,故互为同
2 2
位素,B正确;
C.由题干信息可知,
13O与15O的半衰期很短,故不适宜用作示踪原子研究化学反应历程,C错误;
8 8
D.自然界中不存在
13O
与
15O
并不是其化学键不稳定,而是由于
13O与15O的半衰期很短,很容易发生核变
8 2 8 2 8 8
化,转化为气体其他原子,O=O的键能与形成该键的核素无关,D错误;
故答案为:B。
2.(2022·广东卷)甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对
应的水化物为强酸。下列说法不正确的是
A.原子半径:丁>戊>乙
B.非金属性:戊>丁>丙
C.甲的氢化物遇氯化氢一定有白烟产生
D.丙的最高价氧化物对应的水化物一定能与强碱反应
【答案】C
【解析】甲~戊是短周期元素,戊中的最高价氧化物对应水化物为强酸,则可能是硫酸或高氯酸,若是高
氯酸,则戊为Cl,甲为N、乙为F、丙为P、丁为S,若是硫酸,则戊为S,甲为C、乙为O、丙为Si、丁
为P。
A.根据层多径大,同电子层结构核多径小原则,则原子半径:丁>戊>乙,故A正确;
B.根据同周期从左到右非金属性逐渐增强,则非金属性:戊>丁>丙,故B正确;
C.甲的氢化物可能为氨气,可能为甲烷、乙烷等,若是氨气,则遇氯化氢一定有白烟产生;若是甲烷、
乙烷等,则遇氯化氢不反应,没有白烟生成,故C错误;
D.丙的最高价氧化物对应的水化物可能是硅酸、也可能是磷酸,都一定能与强碱反应,故D正确。
综上所述,答案为C。
3.(2022·全国甲卷)Q、X、Y、Z是原子序数依次增大的短周期主族元素,其最外层电子数之和为19。
Q与X、Y、Z位于不同周期,X、Y相邻,Y原子最外层电子数是Q原子内层电子数的2倍。下列说法正
确的是
A.非金属性:X>Q B.单质的熔点:X>Y
C.简单氢化物的沸点:Z>Q D.最高价含氧酸的酸性:Z>Y
【答案】D
【解析】Q、X、Y、Z为原子序数依次增大的短周期主族元素,Q与X、Y、Z不在同一周期,Y原子最外
层电子数为Q元原子内层电子数的2倍,则Q应为第二周期元素,X、Y、Z位于第三周期,Y的最外层电
子数为4,则Y为Si元素,X、Y相邻,且X的原子序数小于Y,则X为Al元素,Q、X、Y、Z的最外层
电子数之和为19,则Q、Z的最外层电子数之和为19-3-4=12,主族元素的最外层电子数最多为7,若Q的
2
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限公司最外层电子数为7,为F元素,Z的最外层电子数为5,为P元素,若Q的最外层电子数为6,为O元素,
则Z的最外层电子数为6,为S元素,若Q的最外层电子数为5,为N元素,Z的最外层电子数为7,为Cl
元素;综上所述,Q为N或O或F,X为Al,Y为Si,Z为Cl或S或P,据此分析解题。
A.X为Al,Q为N或O或F,同一周期从左往右元素非金属性依次增强,同一主族从上往下依次减弱,
故非金属性:Q>X,A错误;
B.由分析可知,X为Al属于金属晶体,Y为Si属于原子晶体或共价晶体,故单质熔点Si>Al,即Y>X,
B错误;
C.含有氢键的物质沸点升高,由分析可知Q为N或O或F,其简单氢化物为HO或NH 或HF,Z为Cl
2 3
或S或P,其简单氢化物为HCl或HS或PH ,由于前者物质中存在分子间氢键,而后者物质中不存在,
2 3
故沸点Q>Z,C错误;
D.元素的非金属性越强,其最高价含氧酸的酸性越强,P、S、Cl的非金属性均强于Si,因此最高价含氧
酸酸性:Z>Y,D正确;
故答案为:D。
4.(2022·湖南卷)科学家合成了一种新的共价化合物(结构如图所示),X、Y、Z、W为原子序数依次增
大的短周期元素,W的原子序数等于X与Y的原子序数之和。下列说法错误的是
A.原子半径:X>Y>Z
B.非金属性:Y>X>W
C.Z的单质具有较强的还原性
D.原子序数为82的元素与W位于同一主族
【答案】C
【解析】由共价化合物的结构可知,X、W形成4个共价键,Y形成2个共价键,Z形成1个共价键,X、
Y、Z、W是原子序数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和,则X为C元素、
Y为O元素、Z为F元素、W为Si元素。
A.同周期元素,从左到右原子半径依次减小,则C、O、F的原子半径大小顺序为C>O>F,故A正确;
B.同周期元素,从左到右元素的非金属性依次增强,同主族元素,从上到下元素的非金属性依次减弱,
则C、O、Si的非金属性强弱顺序为O>C>Si,故B正确;
C.位于元素周期表右上角的氟元素的非金属性最强,单质具有很强的氧化性,故C错误;
D.原子序数为82的元素为铅元素,与硅元素都位于元素周期表ⅣA族,故D正确;
故选C。
5.(2022·浙江卷)X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。X的核外电子数等于其
周期数,YX 分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。M与X同主族,Q是同周期
3
中非金属性最强的元素。下列说法正确的是
3
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限公司A.X与Z形成的10电子微粒有2种
B.Z与Q形成的一种化合物可用于饮用水的消毒
C.M Z与MQ的晶体类型不同
2
D.由X、Y、Z三种元素组成的化合物的水溶液均显酸性
【答案】B
【解析】X的核外电子数等于其周期数,X为H,YX 分子呈三角锥形,Y为N,Z的核外电子数等于X、
3
Y核外电子数之和,则Z为O,M与X同主族,则M为Na,Q是同周期中非金属性最强的元素,则Q为
Cl,综合分析,X为H,Y为N,Z为O,M为Na,Q为Cl,以此解题。
A.由分析可知X为H,Z为O,则其形成的10电子微粒有HO、OH-、HO+,A错误;
2 3
B.由分析可知Z为O,Q为Cl,可形成ClO ,有氧化性,可用于自来水消毒,B正确;
2
C.由分析可知Z为O,M为Na,Q为Cl,则MZ为NaO,为离子晶体,MQ为NaCl,为离子晶体,晶
2 2
体类型相同,C错误;
D.由分析可知X为H,Y为N,Z为O,这三种元素可以形成NH₃·H₂O,其溶液显碱性,D错误;
故选B。
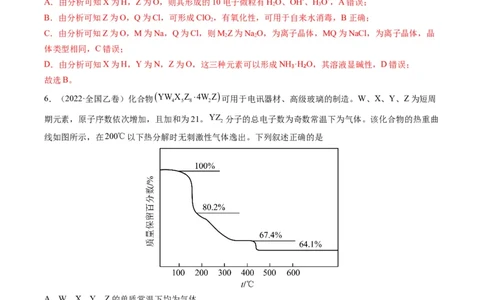
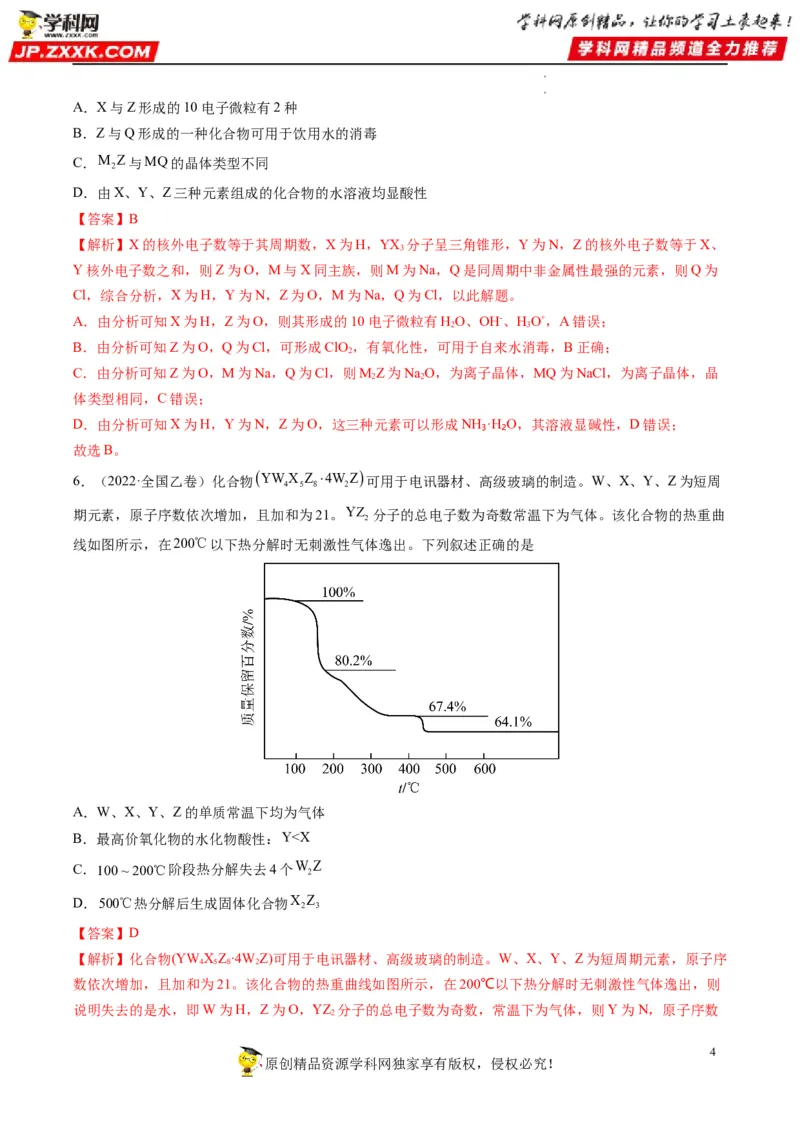
6.(2022·全国乙卷)化合物 YWX Z 4W Z 可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周
4 5 8 2
期元素,原子序数依次增加,且加和为21。YZ 分子的总电子数为奇数常温下为气体。该化合物的热重曲
2
线如图所示,在200℃以下热分解时无刺激性气体逸出。下列叙述正确的是
A.W、X、Y、Z的单质常温下均为气体
B.最高价氧化物的水化物酸性:YY>Z>W,A错误;
B.化合物XW即MgO为离子化合物,其中的化学键为离子键,B正确;
C.Y单质为铝单质,铝属于导体,导电性很强,Z单质为硅,为半导体,半导体导电性介于导体和绝缘体
之间,故Y单质的导电性能强于Z单质的,C错误;
D.Z的氧化物的水化物为硅酸,硅酸酸性弱于碳酸,D错误;
故选B。
8.(2021·全国甲)W、X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层电子数是W和X的
最外层电子数之和,也是Y的最外层电子数的2倍。W和X的单质常温下均为气体。下列叙述正确的是
5
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限公司A.原子半径:Z>Y>X>W
B.W与X只能形成一种化合物
C.Y的氧化物为碱性氧化物,不与强碱反应
D.W、X和Z可形成既含有离子键又含有共价键的化合物
【答案】D
【分析】
W.X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层电子数是W和X的最外层电子数之和,
也是Y的最外层电子数的2倍,则分析知,Z的最外层电子数为偶数,W和X的单质常温下均为气体,则
推知W和X为非金属元素,所以可判断W为H元素,X为N元素,Z的最外层电子数为1+5=6,Y的最
6
外层电子数为 =3,则Y为Al元素,Z为S元素,据此结合元素及其化合物的结构与性质分析解答。
2
【详解】
根据上述分析可知,W为H元素,X为N元素,Y为Al元素,Z为S元素,则
A.电子层数越多的元素原子半径越大,同周期元素原子半径依次减弱,则原子半径:Y(Al)>Z(S)>X(N)
>W(H),A错误;
B.W为H元素,X为N元素,两者可形成NH 和NH,B错误;
3 2 4
C.Y为Al元素,其氧化物为两性氧化物,可与强酸、强碱反应,C错误;
D.W、X和Z可形成(NH )S、NH HS,两者既含有离子键又含有共价键,D正确。
4 2 4
故选D。
9.(2021·广东)一种麻醉剂的分子结构式如图所示。其中,X的原子核只有1个质子;元素Y、Z、
W原子序数依次增大,且均位于X的下一周期;元素E的原子比W原子多8个电子。下列说法不正确的
是
XEZ
A. 是一种强酸
4
B.非金属性:W ZY
C.原子半径:Y W E
ZW
D. 中,Z的化合价为+2价
2
【答案】C
【分析】
题给化合物结构中X、W、E均形成1个共价键、Y形成4个共价键、Z形成2个共价键。
X的原子核只有1个质子,则X为H元素;元素Y、Z、W原子序数依次增大,且均位于X的下一周
期,即第二周期元素,则Y为C元素,Z为O元素,W为F元素;元素E的原子比W原子多8个电子,
6
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限公司则E为Cl元素,综合以上分析可知,X、Y、Z、W、E分别为H、C、O、F、Cl元素。
据此分析解答。
【详解】
A.氯元素非金属性较强,其最高价氧化物的水化物HClO 是一种强酸,故A正确;
4
B.同一周期元素从左到右非金属性逐渐增强,所以非金属性:F>O>C,故B正确;
C.同一周期从左到右原子半径逐渐减小,同一主族从上到下原子半径逐渐增大,电子层越多半径越大,
所以原子半径:Cl>C>F,故C错误;
D.OF 中,F为-1价,则O的化合价为+2价,故D正确;
2
答案选C。
10.(2021·湖南)W、X、Y、Z为原子序数依次增大的短周期主族元素,Y的原子序数等于W与X的原
子序数之和,Z的最外层电子数为K层的一半,W与X可形成原子个数比为2:1的18e分子。下列说法
正确的是
A.简单离子半径:ZXY
B.W与Y能形成含有非极性键的化合物
C.X和Y的最简单氢化物的沸点:XY
D.由W、X、Y三种元素所组成化合物的水溶液均显酸性
【答案】B
【分析】
Z的最外层电子数为K层的一半,则Z的核外有3个电子层,最外层电子数为1,即为Na,W与X能形成
原子个数比为2:1的18电子的分子,则形成的化合物为NH,所以W为H,X为N,Y的原子序数是W
2 4
和X的原子序数之和,则Y为O。据此分析解答。
【详解】
由分析可知,W为H,X为N,Y为O,Z为Na。
A.离子的电子层数相同时,原子序数越小,半径越大,即离子半径大小为:N3->O2->Na+,即简单离子
半径为:X>Y>Z,故A错误;
B.W为H,Y为O,能形成HO,含有极性共价键和非极性共价键,故B正确;
2 2
C.X的最简单氢化物为氨气,Y的最简单氢化物为水,水的沸点高于氨气,即最简单氢化物的沸点为Y
>X,故C错误;
D.由W、X、Y三种元素形成的化合物有硝酸,硝酸铵,氨水等,硝酸,硝酸铵显酸性,氨水显碱性,
故由W、X、Y三种元素形成的化合物不一定都是酸性,故D错误;
故选B。
【优选特训】
1.(2022·广东韶关·二模)常温下,W、X、Y、Z四种短周期元索的最高价氧化物对应的水化物溶液(浓
度均为0.01mol/L)的pH和原子半径、原子序数的关系如下图所示。下列说法不正确的是
7
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限公司A.X与Y形成的化合物的水溶液呈酸性 B.单质的沸点:Y>Z
C.简单离子半径:Y>Z>W>X D.ZO 可作为自来水的消毒剂
2
【答案】A
【解析】浓度均为0.01mol•L-1的溶液,W、Y、Z的最高价氧化物对应的水化物的pH都小于7,W、Y、Z
的最高价氧化物对应的水化物是酸,说明W、Y、Z都是非金属元素,W、Z最高价氧化物对应的水化物
的pH=2,为一元强酸,原子序数Z>W,则Z是Cl、W是N;Y的最高价氧化物对应的水化物的pH<2,
应该为二元强酸硫酸,则Y是S;X的最高价氧化物对应的水化物的pH=12,应该为一元强碱氢氧化钠,
则X是Na。
由以上分析可知,W、X、Y、Z分别为N、Na、S、Cl元素,
A. X与Y形成的化合物NaS 为强碱弱酸盐,水解后水溶液呈碱性,故A错误;
2
B. 硫常温下是固体,氯气为气体,单质的沸点:Y>Z,故B正确;
C. 电子层数越多,原子或离子的半径越大,电子层数相同时,核电荷数越大,对核外电子的吸引能力越
强,离子半径越小,则N3-、Na+、S2-、Cl-的半径大小为:S2->Cl->N3->Na+,即Y>Z>W>X,故C正确;
D. ClO 具有强氧化性,能使蛋白质变性,可作为自来水的消毒剂,故D正确;
2
故选A。
2.(2022·四川德阳·二模)短周期主族元素X、Y、Z、W的原子序数依次增大。X单质可用作保护气,Y
为短周期中原子半径最大的元素,Z原子的最外层电子数等于X与Y的最外层电子数之和。下列叙述正确
的是
A.简单氢化物的沸点:X<Z
B.ZW 分子中各原子最外层均达到8电子结构
2 2
C.简单离子的半径:X<Y
D.Y和Z的简单离子均能破坏水的电离平衡
【答案】B
【解析】X单质可用作保护气,则X为N元素,Y为短周期中原子半径最大的元素,则Y为Na元素,Z
原子的最外层电子数等于X与Y的最外层电子数之和,则Z为S元素,W为Cl元素。
A.NH 分子间能形成氢键,沸点大于HS,因此简单氢化物的沸点:Z>X,故A错误;
3 2
B.SCl 分子中S原子和Cl原子最外层电子均到达8电子结构,故B正确;
2 2
C.简单离子半径:Na+Z>W,B错误;
C.Z、X、Y、R分别为O、H、C、S,O都可以与其它三种元素形成两种化合物,分别是HO、HO、
2 2 2
CO、CO、SO 、SO ,C正确;
2 2 3
D. 常见的最简单的氢化物分别为CH、HO、HF、HS,其中水和HF分子间存在氢键,其他两种氢化物
4 2 2
中,相对分子质量最小的为CH,其沸点最低,D错误;
4
故选C。
4.(2022·浙江杭州·二模)有一种化合物是很多表面涂层的重要成分,其结构如图所示.其中
W、X、Y、Z为原子序数依次增大的短周期元素,只有X、Y在同一周期,Z的单质是黄绿色气体;下列
有关说法不正确的是
9
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限公司A.非金属性强弱比较:YX B.XW
4
的沸点高于W
2
Y的沸点
C.X的含氧酸有一元弱酸、二元弱酸等 D.Z Y中所有原子最外层都满足8电子结构
2
【答案】B
【解析】W、X、Y、Z为原子序数依次增大的短周期元素,Z的单质是黄绿色气体,Z为氯;只有X、Y
在同一周期, 则W为氢,位于第一周期,XY位于第二周期;由结构可知,XY形成共价键数分别为4、
2,则XY分别为碳、氧;
A.同周期从左到右,金属性减弱,非金属性变强,非金属性强弱比较:YX,A正确;
B.氧电负性较强,水分子中可以形成氢键,故CH 的沸点低于HO的沸点,B错误;
4 2
C.碳的含氧酸有一元弱酸醋酸、二元弱酸碳酸等,C正确;
D.ClO 中氯、氧原子的最外层都满足8电子结构,D正确;
2
故选B。
5.(2022·福建·莆田一中高三阶段练习)2022年9月9日,中国科学家首次在月球上发现一种磷酸盐矿物,
命名为“嫦娥石”。该物质除了含钙( Ca)、铁( Fe)、钇( Y)三种长周期元素外,还含有X、R、Z、W
20 28 39
四种原子序数依次增大的短周期主族元素。仅X、W为非金属元素,R、Z相邻,且R是短周期原子半径
最大的主族元素。下列叙述正确的是
A.钇( Y)是第四周期IIIB族元素 B.原子半径:R WZX
39
C.元素的金属性:CaR ZFe D.简单氢化物沸点:XW
【答案】C
【分析】矿物为磷酸盐,其中含有的X、R、Z、W原子序数依次增大,是短周期主族元素,仅X、W为非
金属,即X为氧,W为磷;R是短周期原子半径最大的主族元素,即R为钠;R、Z相邻,即Z是镁。
【详解】A.钇是第39号元素,原子结构示意图为: ,是周期表中第五周期第ⅢB族
元素,A错误;
B.根据同周期原子半径从左到右减小,同主族原子半径从上到下增大得原子半径大小关系为:
R>Z>W>X,B错误;
C.根据金属活动性顺序表得元素的金属性强弱关系为:Ca>R>Z>Fe,C正确;
D.X简单氢化物为H O,分子间存在氢键,W简单氢化物为PH ,分子间没有氢键,因此简单氢化物沸
2 3
点大小顺序为:X>W,D错误;
故选C。
6.(2022·吉林·东北师大附中模拟预测)某种电化学的电解液的组成如图所示,X、Y、Z、Q、W为原子
序数依次增大的短周期元素,下列说法正确的是
1
原创精品资源学科网独家享有版权,侵权必究! 0
学学科科网网((北北京京))股股份份有有限公司A.电解熔融QW 可获得Q的单质
3
B.原子半径:Z>Y
C.W的含氧酸均为强酸
D.Y、Z、W均能和X形成18电子的分子
【答案】D
【解析】由图可知X为H原子,Y为C原子,Z为N原子,Q为Al原子,W为Cl原子。
A.AlCl 为共价化合物,电解熔融的AlCl 无法获得Al单质,A项错误;
3 3
B.同周期主族元素原子半径从左往右依次减小,原子半径:C>N,B项错误;
C.W的含氧酸有HClO为弱酸、HClO 为强酸,则W的最高价氧化物形成的含氧酸为强酸,C项错误;
4
D.C、N、Cl均能与H原子形成C H 、N H 、HCl都为18电子的分子,D项正确;
2 6 2 4
答案选D。
7.(2022·贵州·模拟预测)前20号主族元素W、X、Y、Z的原子序数依次增大。已知X的单质既可与强
碱反应,又可与强酸反应,W与Y位于同一主族,Z的K层电子数与N层相等, W、X、Y、Z四种元素
的最外层电子数之和为13.下列说法正确的是
A.原子半径由小到大的顺序: X< Y
B.Y的最高价氧化物不能与酸溶液反应
C.X的单质不能从CuSO 溶液中置换出Cu
4
D.ZW 既含非极性共价键又含离子键
2
【答案】D
【解析】W、X、Y、Z为原子序数依次增大的前20号主族元素,X的单质既可与强碱反应,又可与强酸
反应,则X为Al,Z的K层电子数与N层相等,则Z原子核外电子层为2,8,8,2结构,Z为Ca,又
W、X、Y、Z四种元素的最外层电子数之和为13,W与Y位于同一主族,则W、Y的最外层电子数均为
4,则W为C,Y为Si,据此分析解答。
A.同周期元素从左至右原子半径依次减小,故原子半径:Al>Si,A错误;
B.Y为Si,其最高价氧化物为SiO,可与氢氟酸(HF)发生反应,B错误;
2
C.X为Al,Al的金属性强于Cu,可以从CuSO 溶液中置换出Cu,C错误;
4
D.Z为Ca,W为C,CaC 中Ca2+和C2形成离子键,C2中C和C形成非极性共价键,D正确;
2 2 2
答案选D。
8.(2022·陕西·西安中学模拟预测)X、Y、Z、W、T均为短周期主族元素,原子序数依次增大,X的电
1
原创精品资源学科网独家享有版权,侵权必究! 1
学学科科网网((北北京京))股股份份有有限公司子数与W的最外层电子数相等,W、Y形成的化合物能使品红溶液褪色,常温下,元素Z、W、T的原子
序数及其最高价氧化物对应的水化物的溶液(浓度均为0.1mol·L-1)的pH有如表所示关系。下列说法错误的
是
元素 Z W T
原子序数 小→大
0.1mol·L-1溶液的pH 13 0.7 1
A.简单离子半径:W>T>Y>Z
B.最高价氧化物对应的水化物的酸性:W>T
C.Z、T形成的简单离子均不能促进水的电离
D.X、Y形成的化合物与X、W形成的化合物均存在直线形分子
【答案】B
【解析】由题目可知,W、Y形成的化合物能使品红溶液褪色,则该化合物为SO ,则Y为O元素,W为
2
S元素;X的电子数与W的最外层电子数相等,W的最外层电子数为6,则X的电子数为6,X为C元素;
由T元素的最高价氧化物对应水化物的pH知,T元素的最高价氧化物对应水化物为一元强酸,因此T为
Cl元素,同理Z元素的最高价氧化物对应水化物为一元强碱,Z为Na元素。综上所述,X为C元素,Y
为O元素,Z为Na元素,W为S元素,T为Cl元素,据此答题。
A.电子层数越大,原子或离子半径越大,相同电子数的离子,原子序数越大,半径越小,因此W、T、
Y、Z四种元素的离子半径从大到小依次为S2-(W)>Cl-(T)>O2-(Y)>Na+(Z),A选项正确;
B.W元素的最高价氧化物对应水化物为HSO ,T元素的最高价氧化物对应水化物为HClO,二者酸性强
2 4 4
弱为HClO>H SO ,B选项错误;
4 2 4
C.Z和T形成的简单化合物为NaCl,为强酸和强碱反应生成的盐,在水溶液中不水解,不会影响水的电
离,C选项正确;
D.X和Y形成的化合物为CO或CO,在结构上为直线型分子,X和W形成的化合物为CS,在结构式为
2 2
直线型分子,因此,X、Y形成的化合物与X、W形成的化合物均存在直线形分子,D选项正确;
故答案选B。
9.X、Y、Z、W是原子半径依次增大的短周期主族元素,其中X元素与其他元素不在同一周期,Y的一
种核素常用于测定文物年代,基态Z原子中s能级与p能级上的电子总数相等。下列说法错误的是
A.W单质可以与水反应生成气体
B.Z、W所在周期内,Z、W元素第一电离能大小相邻
C.X与Y组成的化合物沸点可能比水的高
D.X、Y、Z、W的单质均可以在空气中燃烧
【答案】B
【分析】X元素与其他元素不在同一周期,则X为H元素,Y的一种核素常用于测定文物年代,则Y为C
元素,基态Z原子中s能级与p能级上的电子总数相等,则Z为Mg元素, X、Y、Z、W是原子半径依次
增大的短周期主族元素,则W为Na元素。
1
原创精品资源学科网独家享有版权,侵权必究! 2
学学科科网网((北北京京))股股份份有有限公司【详解】A.钠与水反应生成H ,故A正确;
2
B .Z、W所在周期是第三周期,同周期元素从左到右第一电离能呈增大趋势,但IIA>IIIA,VA>VIA,
所以 Mg第一电离能大于Al,Na、Mg元素第一电离能大小不相邻,故B错误;
C.C与H可以形成高分子化合物,沸点可能高于水,故C正确;
D.H 、C、Na、Mg均可以在空气中燃烧,故D正确;
2
故答案为:B。
10.(2022·安徽·芜湖一中高三阶段练习)化合物RZWY 12X Y常用作净水剂。X、Y、Z、W为短周
4 2 2
期主族元素,原子序数依次增加,且加和为38.元素Y和W可形成WY 化合物且位于同一主族,Z离子半
2
径为同周期中离子半径最小的,R离子与W离子的电子层结构相同。下列叙述正确的是
A.RZWY 12X Y为纯净物,其水溶液显酸性
4 2 2
B.Y与R形成的化合物中只存在离子键
C.简单氢化物的沸点高低顺序为Y>R>W
D.离子半径大小顺序为R>W>Z>Y
【答案】A
【分析】X、Y、Z、W为短周期主族元素,原子序数依次增加,且加和为38。元素Y和W可形成WY 化
2
合物且位于同一主族,则Y为O,W为S,两者形成的化合物为SO ,Z离子半径为同周期中离子半径最
2
小的,原子序数大于O小于S,则Z为Al,R离子与W离子电子层结构相同,结合化合物
RZWY 12X Y可知,R为K,X为H。RZWY 12X Y为KAl(SO )·12H O。
4 2 2 4 2 2 4 2 2
【详解】A.KAl(SO )·12H O为纯净物,其水溶液中铝离子水解使溶液显酸性,A正确;
4 2 2
B.O和K形成的KO 中含有共价键,B错误;
2 2
C.KH是离子晶体,其沸点大于HO,C错误;
2
D.离子半径大小顺序为S2->K+>O2->Al3+,D错误;
故答案选A。
11.(2022·江西九江·一模)X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大,Z、M同主族,
M与Z组成的化合物的排放是形成酸雨的主要原因之一,X是元素周期表中原子半径最小的元素,Y与Z
相邻,下列说法正确的是
A.原子半径:M>Q>Z> Y
B.气态氢化物稳定性:Y>Z>Q>M
C.X、Y、Z、M四种元素至少能形成三种离子化合物
D.Q的氧化物对应水化物的酸性强于M的氧化物对应水化物
【答案】C
【解析】
【分析】
X、Y、Z、M、Q是五种原子序数依次增大的短周期主族元素,X是元素周期表中原子半径最小的元素,
1
原创精品资源学科网独家享有版权,侵权必究! 3
学学科科网网((北北京京))股股份份有有限公司则X为H元素;Z、M同主族,M与Z组成的化合物的排放是形成酸雨的主要原因之一,则Z为O元素、
M为S元素;Y与Z相邻,则Y为N元素;Q的原子序数大于M,则Q为Cl元素。
【详解】
A.同周期元素,从左到右原子半径依次减小,则氧原子的原子半径小于氮原子,故A错误;
B.元素的非金属性越强,气态氢化物稳定性的稳定性越强,氧元素的非金属性强于氮元素,则水的稳定
性强于氨气,故B错误;
C.氢、氮、氧、硫四种元素形成的硫酸铵、硫酸氢铵、亚硫酸铵、亚硫酸氢铵都是离子化合物,故C正
确;
D.次氯酸是弱酸,酸性弱于硫酸,故D错误;
故选C。
12.某化合物的结构为 ,其中X、Y、W、Z四种短周期元素原子半径依次增大,X
和Z同主族,W和Z同周期,Y和Z的简单离子具有相同的电子层结构。下列叙述正确的是
A.简单离子半径:W>Z>Y
B.工业上可通过电解WCl 制取单质W
3
C.该化合物的水溶液显酸性
D.X与Y形成的化合物可与X与Z形成的化合物发生反应
【答案】D
【解析】
【分析】
X、Y、W、Z四种短周期元素原子半径依次增大,X和Z同主族,W和Z同周期,Z可形成带一个单位正
电荷的阳离子,为钠;Y和Z的简单离子具有相同的电子层结构,结合结构中成键情况可推断X为氢、Y
为氧。W与氢、氧可形成带1个单位负电荷的阴离子,W为铝;
【详解】
A.一般而言,电子层数越多半径越大;电子层数相同时,核电荷数越大,半径越小;则简单离子半径:
O2->Na+>Al3+,A错误;
B.氯化铝为共价化合物,熔融状态不导电,不能通过电解WCl 制取单质W,B错误;
3
C.该化合物为Na[Al(OH)],水溶液显碱性,C错误;
4
D.水和氢化钠可以反应生成氢氧化钠和氢气,D正确;
故选D。
1
原创精品资源学科网独家享有版权,侵权必究! 4
学学科科网网((北北京京))股股份份有有限公司1
原创精品资源学科网独家享有版权,侵权必究! 5
学学科科网网((北北京京))股股份份有有限公司