文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(湖南专用)
黄金卷02
(考试时间:75分钟;试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Al-27 I-127
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.化学科学与技术在宇宙探索、改进生活、改善环境与促进发展方面均发挥着关键性的作用。下列说法
正确的是
A.指南针是我国古代的四大发明之一,制造指南针的磁性物质是FeO
B.湖南苗族银饰和江西景德镇彩瓷是我国特有的文化产品,其主要成分均为金属材料
C.人工合成淀粉不仅有利于解决人类的温饱问题,也有利于实现“碳中和”
D.北斗导航专用ASIC硬件结合国产处理器打造出的一颗真正意义的“中国芯”,其主要成分为SiO
2
2.素质教育包括多个方面,如音乐、体育、美术等,受到高度关注。下列情况对应的化学知识或原理正
确的是
选
素质教育 化学知识或原理
项
A 音乐:“音乐焰火”创造出光和色的火树烟花不夜天 焰色反应属于化学变化
高性能树脂与碳纤维融合而
体育:北京冬奥会火炬“飞扬”一经亮相就吸睛无数,火炬外壳材
B 成的复合材料具有耐高温、
料是由高性能树脂与碳纤维融合而成的复合材料
耐腐蚀等优良的特性
美术:宋代《千里江山图》描绘了山清水秀的美丽景色,其中绿色
孔雀石、蓝铜矿颜料不易被
C 来自孔雀石颜料[主要成分为Cu(OH) ·CuCO],青色来自蓝铜矿颜料
2 3 空气氧化且耐酸、耐碱
[主要成分为Cu(OH) ·2CuCO]
2 3
传统爆炸粉为黑火药,其主
D 文学:爆竹声中一岁除,春风送暖入屠苏
要成分为木炭、硫磺、KClO
3
3.中国科学院兰州化物所阎兴斌研究员研究双层电容器中储能行为时,运用到某种离子化学物结构如图
所示。其中X、Y、Z、M、L、Q均为短周期主族元素,且原子序数依次增大。M、Q同族且两种元素组
成的某种阴离子在强酸性溶液环境下可以产生淡黄色沉淀;Y是有机物的基本骨架元素。下列结论正确的
是
A.Z的氢化物沸点一定高于Y的氢化物
B.Q的含氧酸不一定属于强酸
C.简单离子半径大小的顺序为:Q>X>M>LD.L的铵盐溶液能存放在玻璃试剂瓶中
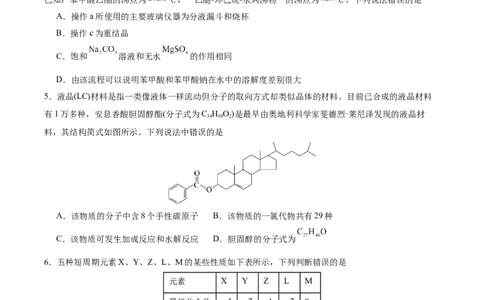
4.实验室初步分离苯甲酸乙酯、苯甲酸和环己烷的流程如下:
已知:苯甲酸乙酯的沸点为 ℃,“乙醚-环己烷-水共沸物”的沸点为 ℃。下列说法错误的是
A.操作a所使用的主要玻璃仪器为分液漏斗和烧杯
B.操作c为重结晶
C.饱和 溶液和无水 的作用相同
D.由该流程可以说明苯甲酸和苯甲酸钠在水中的溶解度差别很大
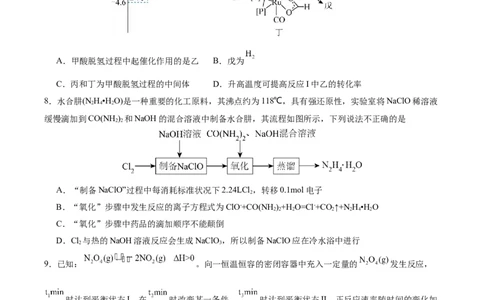
5.液晶(LC)材料是指一类像液体一样流动但分子的取向方式却类似晶体的材料。目前已合成的液晶材料
有1万多种,安息香酸胆固醇酯(分子式为C H O)是最早由奥地利科学家斐德烈·莱尼泽发现的液晶材
34 50 2
料,其结构简式如图所示。下列说法中错误的是
A.该物质的分子中含8个手性碳原子 B.该物质的一氯代物共有29种
C.该物质可发生加成反应和水解反应 D.胆固醇的分子式为
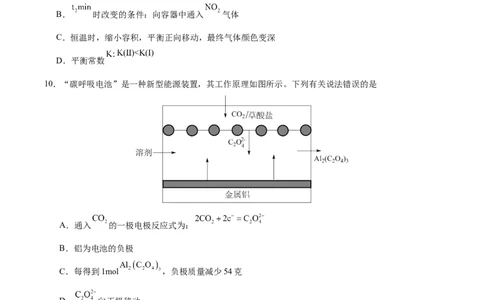
6.五种短周期元素X、Y、Z、L、M的某些性质如下表所示,下列判断错误的是
元素 X Y Z L M
最低化合价 0
电负性 2.5 2.5 3.0 3.5 1.0
A.元素L、M可形成离子化合物
B.Z在周期表中的位置为第3周期第ⅦA族
C.借助电负性数值预测:YLZ 加入水中可生成YL
2 2
D.基态X原子的核外电子共占据3个原子轨道
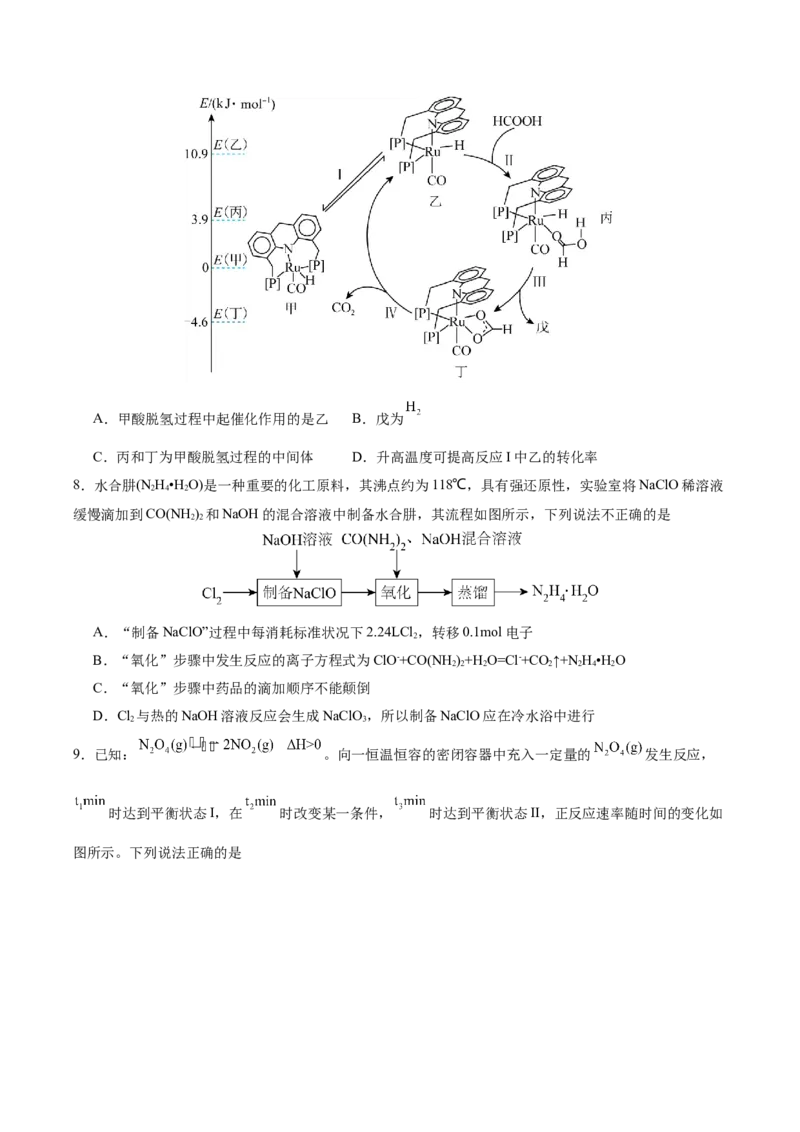
7.某课题组研究发现,甲酸脱氢的反应历程如图(图中E为相对能量)所示。下列说法错误的是A.甲酸脱氢过程中起催化作用的是乙 B.戊为
C.丙和丁为甲酸脱氢过程的中间体 D.升高温度可提高反应I中乙的转化率
8.水合肼(N H•H O)是一种重要的化工原料,其沸点约为118℃,具有强还原性,实验室将NaClO稀溶液
2 4 2
缓慢滴加到CO(NH) 和NaOH的混合溶液中制备水合肼,其流程如图所示,下列说法不正确的是
2 2
A.“制备NaClO”过程中每消耗标准状况下2.24LCl ,转移0.1mol电子
2
B.“氧化”步骤中发生反应的离子方程式为ClO-+CO(NH )+H O=Cl-+CO ↑+N H•H O
2 2 2 2 2 4 2
C.“氧化”步骤中药品的滴加顺序不能颠倒
D.Cl 与热的NaOH溶液反应会生成NaClO,所以制备NaClO应在冷水浴中进行
2 3
9.已知: 。向一恒温恒容的密闭容器中充入一定量的 发生反应,
时达到平衡状态I,在 时改变某一条件, 时达到平衡状态II,正反应速率随时间的变化如
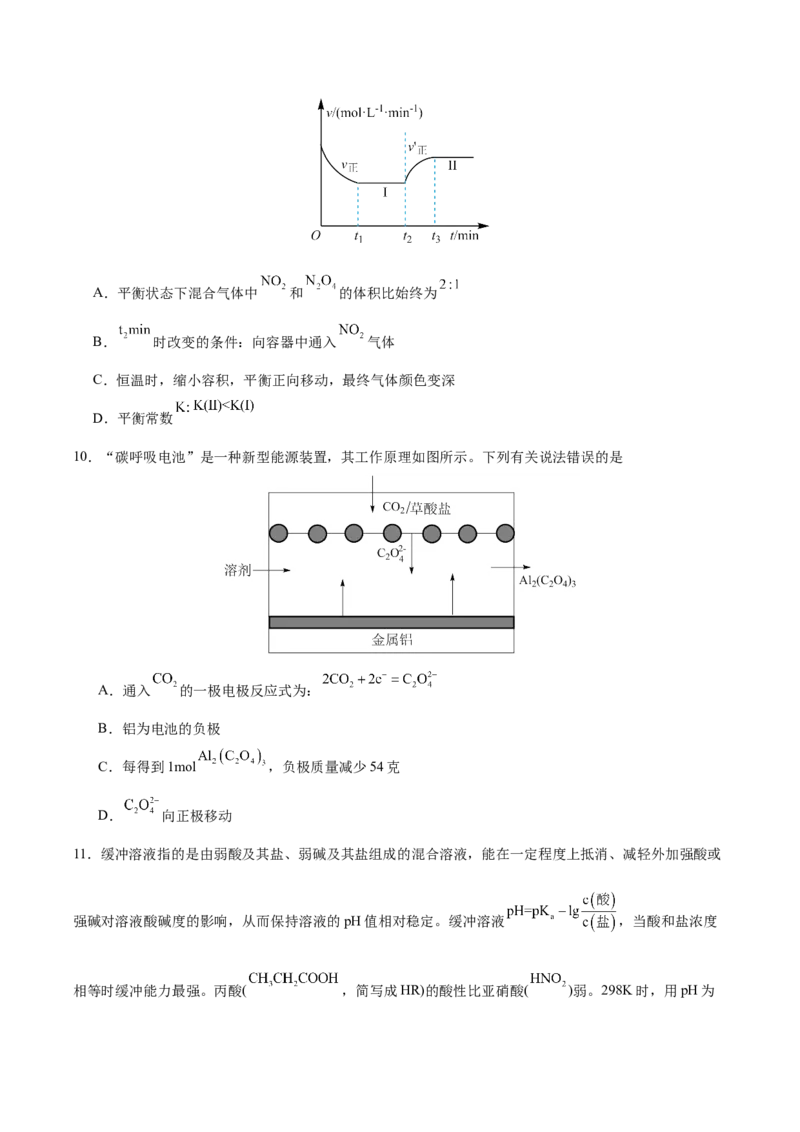
图所示。下列说法正确的是A.平衡状态下混合气体中 和 的体积比始终为
B. 时改变的条件:向容器中通入 气体
C.恒温时,缩小容积,平衡正向移动,最终气体颜色变深
D.平衡常数
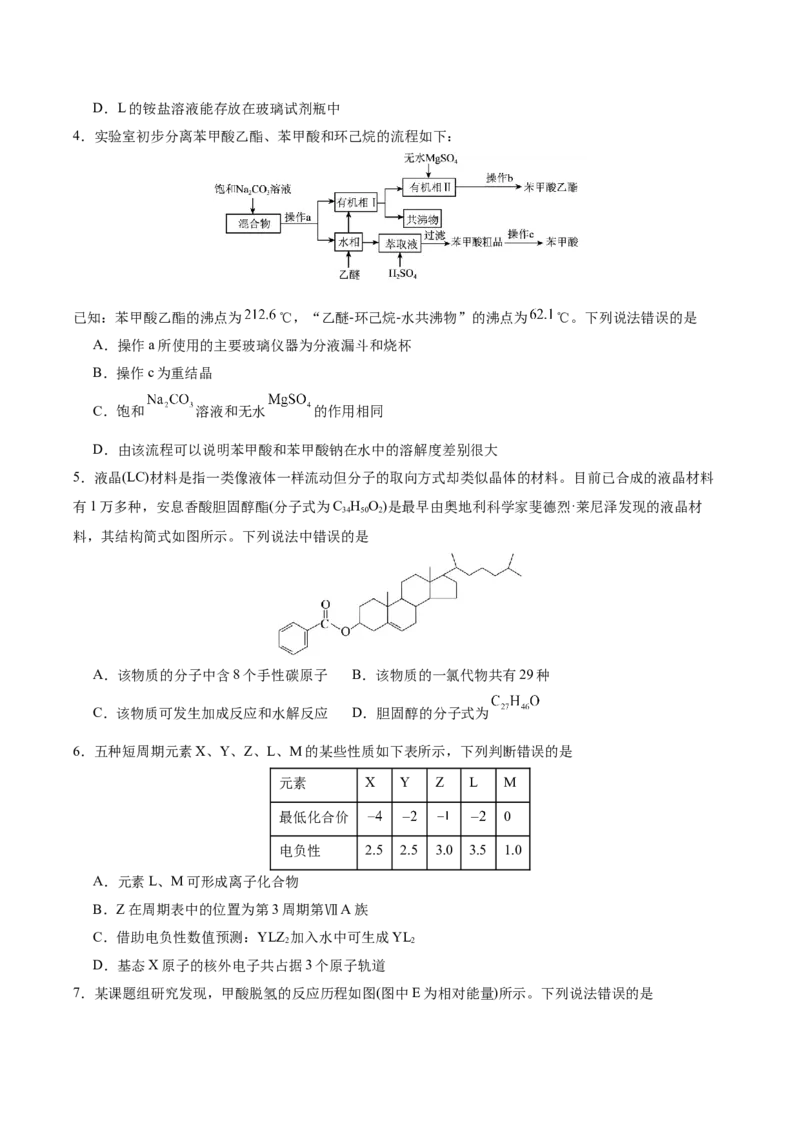
10.“碳呼吸电池”是一种新型能源装置,其工作原理如图所示。下列有关说法错误的是
A.通入 的一极电极反应式为:
B.铝为电池的负极
C.每得到1mol ,负极质量减少54克
D. 向正极移动
11.缓冲溶液指的是由弱酸及其盐、弱碱及其盐组成的混合溶液,能在一定程度上抵消、减轻外加强酸或
强碱对溶液酸碱度的影响,从而保持溶液的pH值相对稳定。缓冲溶液 ,当酸和盐浓度
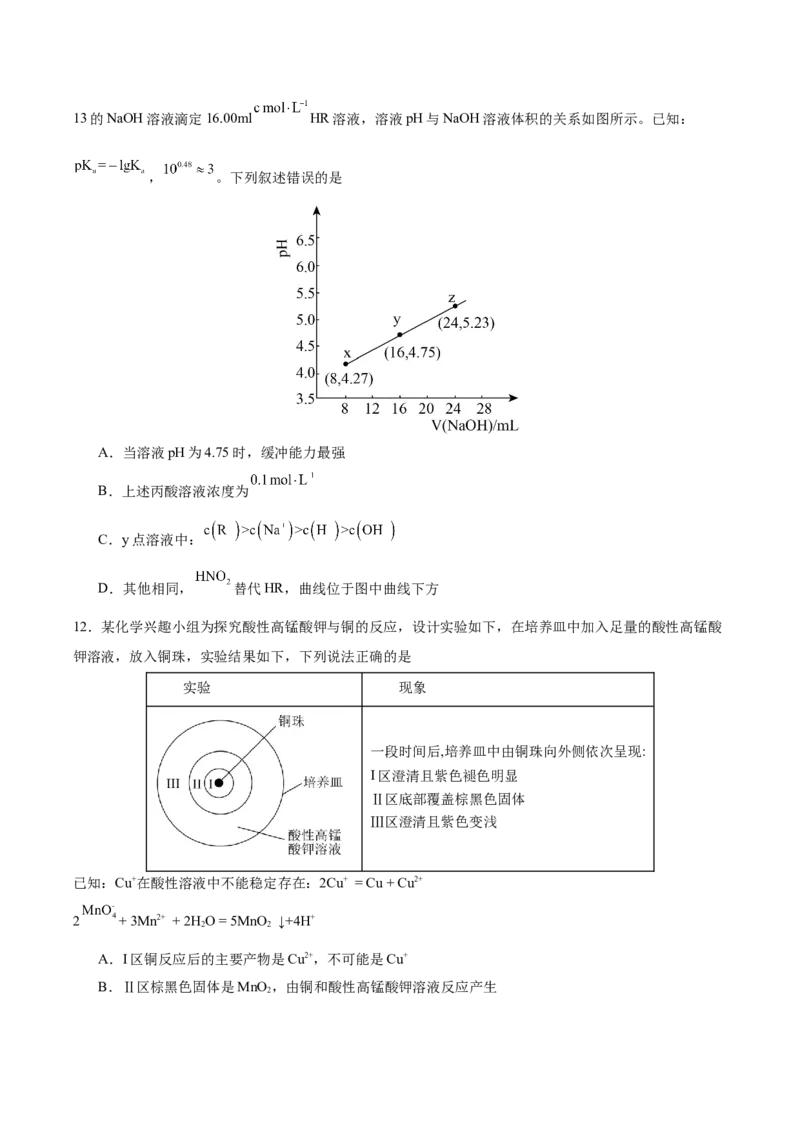
相等时缓冲能力最强。丙酸( ,简写成HR)的酸性比亚硝酸( )弱。298K时,用pH为13的NaOH溶液滴定16.00ml HR溶液,溶液pH与NaOH溶液体积的关系如图所示。已知:
, 。下列叙述错误的是
A.当溶液pH为4.75时,缓冲能力最强
B.上述丙酸溶液浓度为
C.y点溶液中:
D.其他相同, 替代HR,曲线位于图中曲线下方
12.某化学兴趣小组为探究酸性高锰酸钾与铜的反应,设计实验如下,在培养皿中加入足量的酸性高锰酸
钾溶液,放入铜珠,实验结果如下,下列说法正确的是
实验 现象
一段时间后,培养皿中由铜珠向外侧依次呈现:
I区澄清且紫色褪色明显
Ⅱ区底部覆盖棕黑色固体
Ⅲ区澄清且紫色变浅
已知:Cu+在酸性溶液中不能稳定存在:2Cu+ = Cu + Cu2+
2 + 3Mn2+ + 2H O = 5MnO ↓+4H+
2 2
A.I区铜反应后的主要产物是Cu2+,不可能是Cu+
B.Ⅱ区棕黑色固体是MnO ,由铜和酸性高锰酸钾溶液反应产生
2C.Ⅲ区紫色变浅说明在Ⅲ区 也发生了氧化还原反应
D.如果酸性高锰酸钾溶液量少,所有反应完全后,产物中没有Mn2+
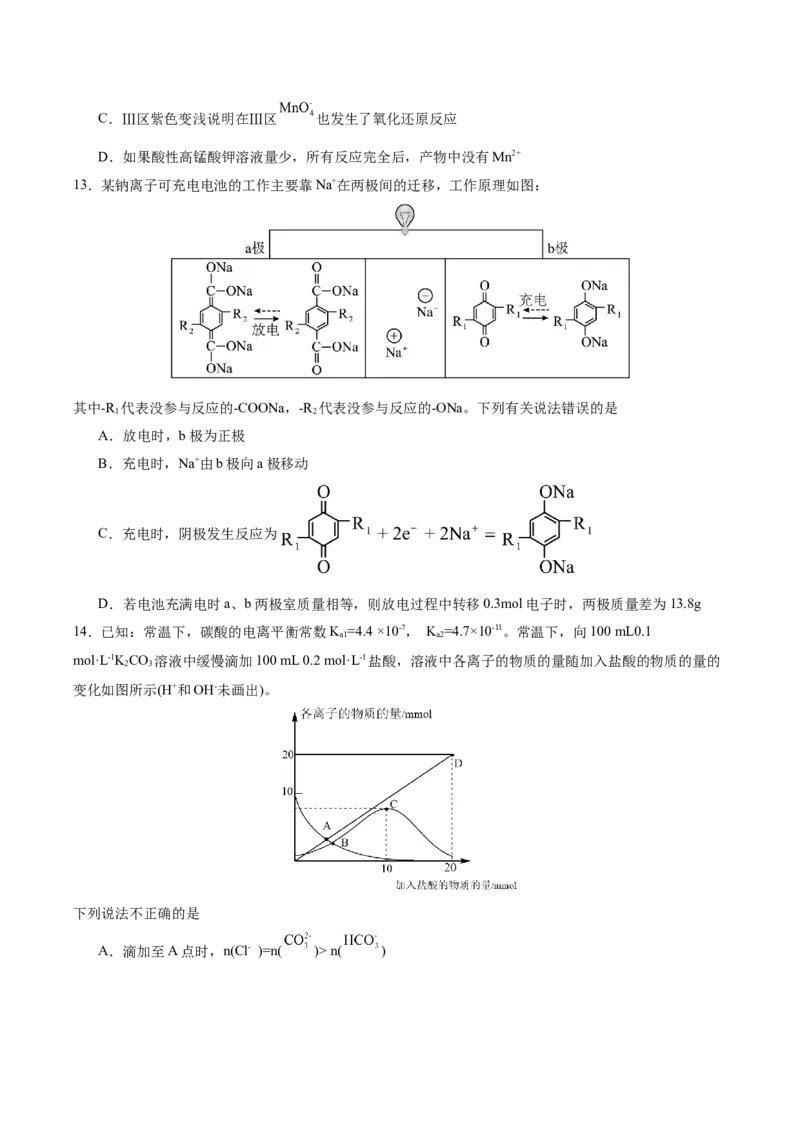
13.某钠离子可充电电池的工作主要靠Na+在两极间的迁移,工作原理如图:
其中-R 代表没参与反应的-COONa,-R 代表没参与反应的-ONa。下列有关说法错误的是
1 2
A.放电时,b极为正极
B.充电时,Na+由b极向a极移动
C.充电时,阴极发生反应为
D.若电池充满电时a、b两极室质量相等,则放电过程中转移0.3mol电子时,两极质量差为13.8g
14.已知:常温下,碳酸的电离平衡常数K =4.4 ×10-7, K =4.7×10-11。常温下,向100 mL0.1
a1 a2
mol·L-1KCO 溶液中缓慢滴加100 mL 0.2 mol·L-1盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的
2 3
变化如图所示(H+和OH-未画出)。
下列说法不正确的是
A.滴加至A点时,n(Cl- )=n( )> n( )B.滴加至B点时, ≈9.4× 103
C.滴加至C点时,c(Cl-)< c( )+ 2c( )
D.滴加至D点时,溶液的pH<7
二、非选择题:本题共4小题,共58分。
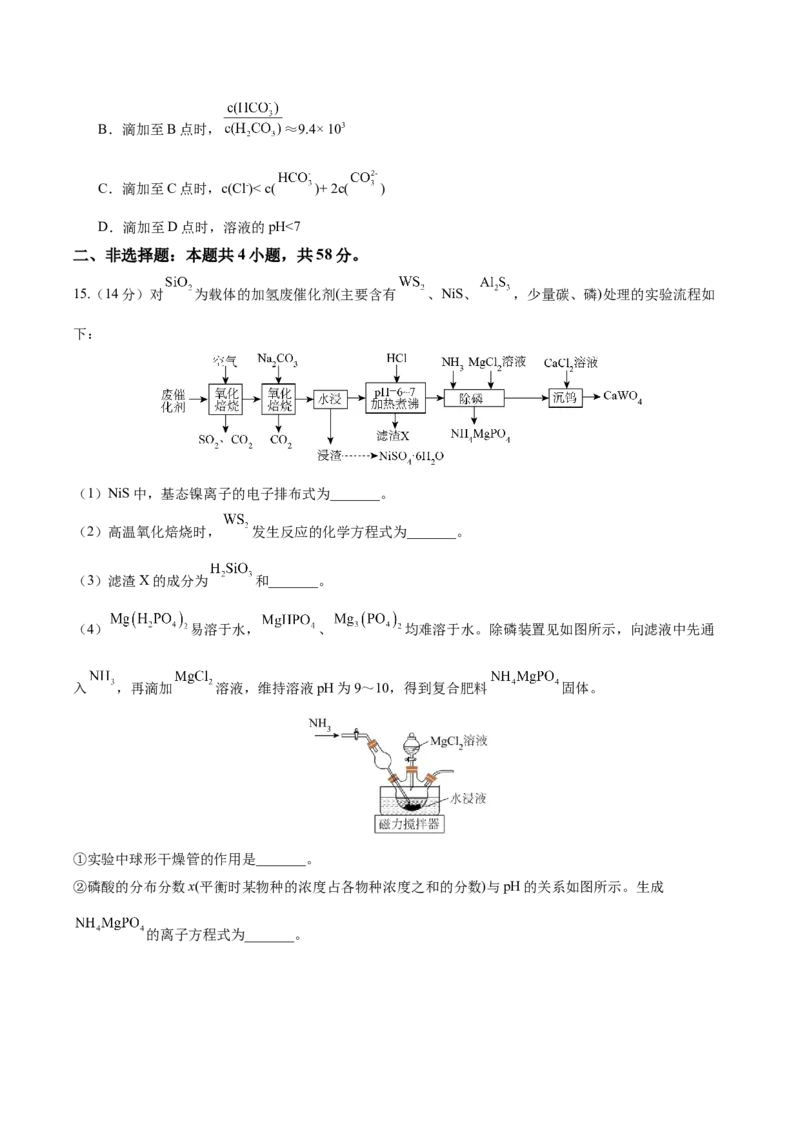
15.(14分)对 为载体的加氢废催化剂(主要含有 、NiS、 ,少量碳、磷)处理的实验流程如
下:
(1)NiS中,基态镍离子的电子排布式为_______。
(2)高温氧化焙烧时, 发生反应的化学方程式为_______。
(3)滤渣X的成分为 和_______。
(4) 易溶于水, 、 均难溶于水。除磷装置见如图所示,向滤液中先通
入 ,再滴加 溶液,维持溶液pH为9~10,得到复合肥料 固体。
①实验中球形干燥管的作用是_______。
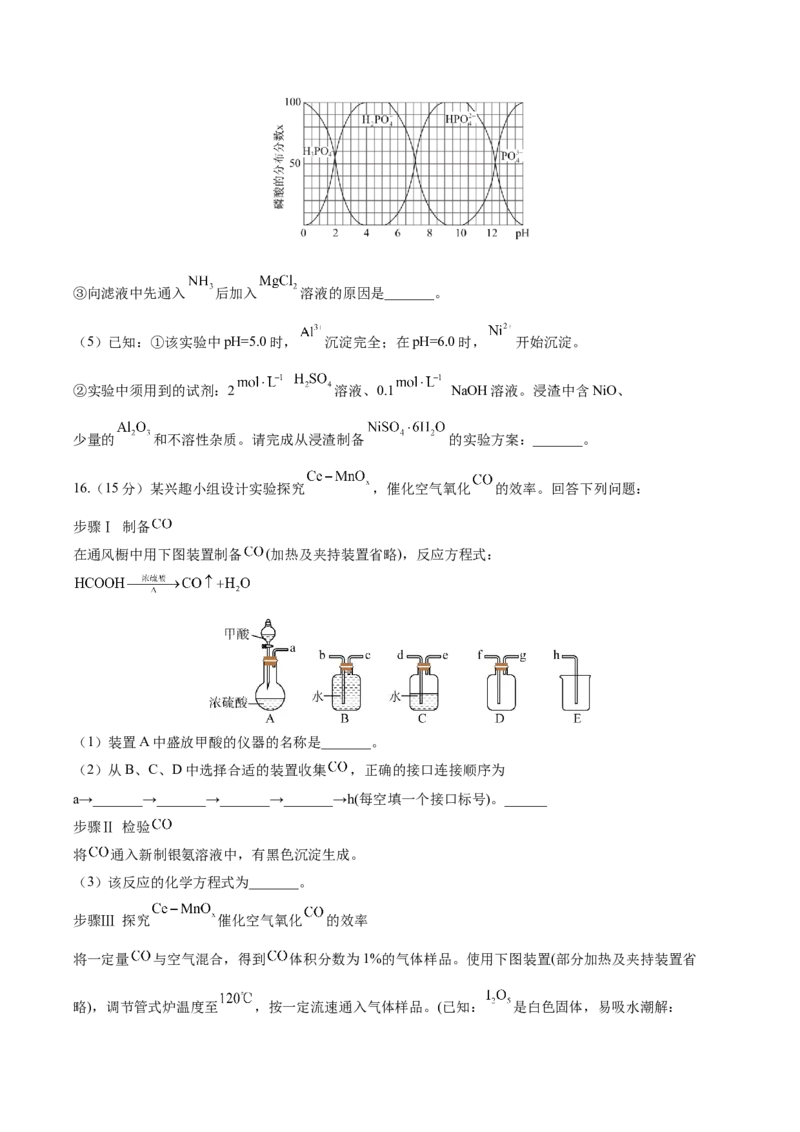
②磷酸的分布分数x(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图所示。生成
的离子方程式为_______。③向滤液中先通入 后加入 溶液的原因是_______。
(5)已知:①该实验中pH=5.0时, 沉淀完全;在pH=6.0时, 开始沉淀。
②实验中须用到的试剂:2 溶液、0.1 NaOH溶液。浸渣中含NiO、
少量的 和不溶性杂质。请完成从浸渣制备 的实验方案:_______。
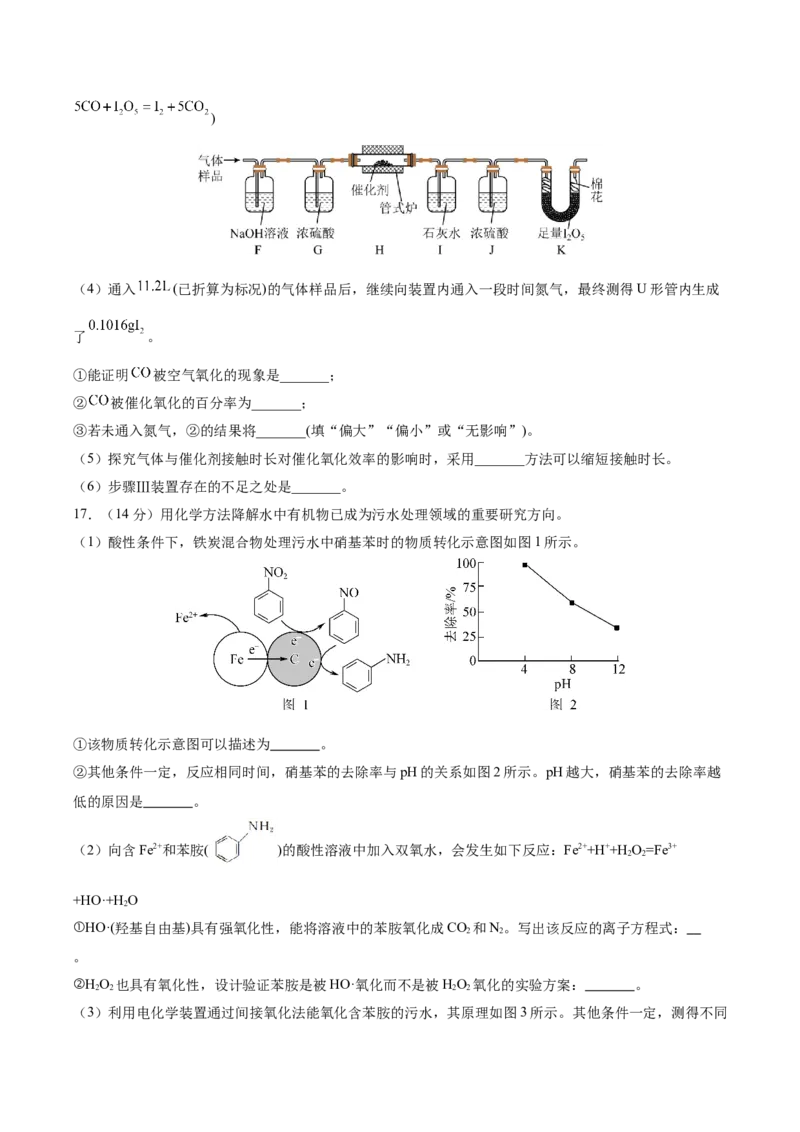
16.(15分)某兴趣小组设计实验探究 ,催化空气氧化 的效率。回答下列问题:
步骤Ⅰ 制备
在通风橱中用下图装置制备 (加热及夹持装置省略),反应方程式:
(1)装置A中盛放甲酸的仪器的名称是_______。
(2)从B、C、D中选择合适的装置收集 ,正确的接口连接顺序为
a→_______→_______→_______→_______→h(每空填一个接口标号)。______
步骤Ⅱ 检验
将 通入新制银氨溶液中,有黑色沉淀生成。
(3)该反应的化学方程式为_______。
步骤Ⅲ 探究 催化空气氧化 的效率
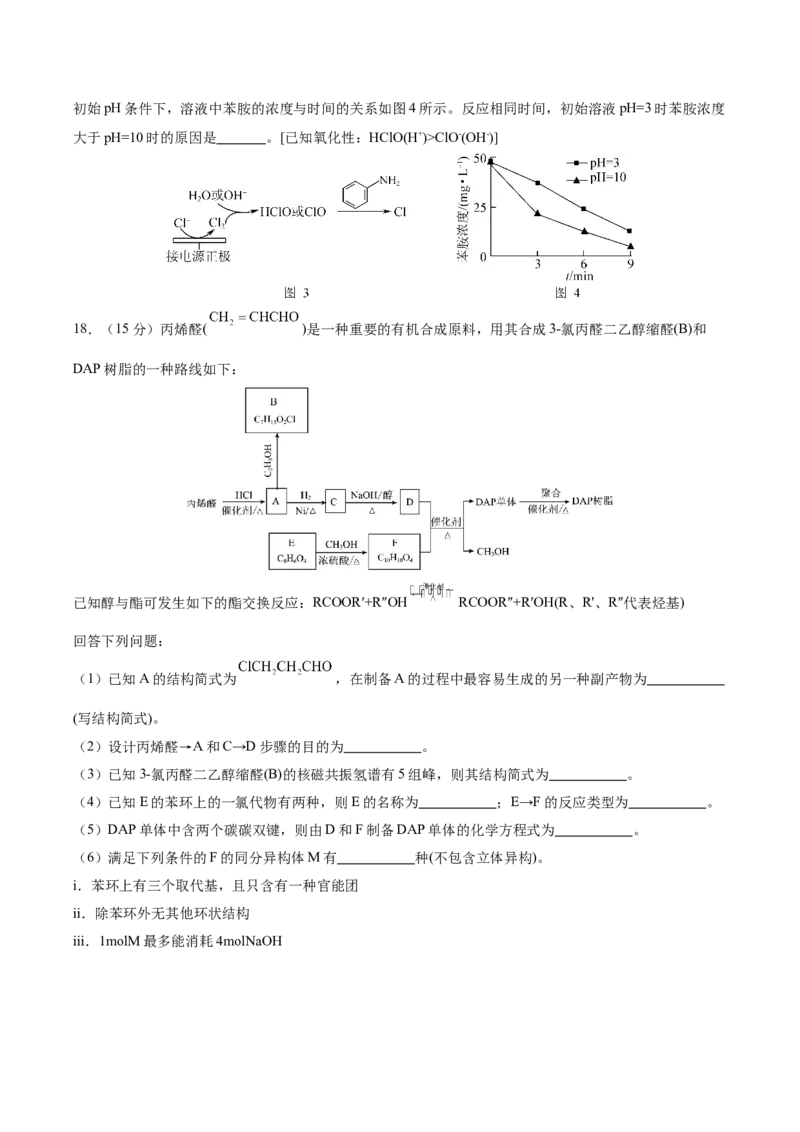
将一定量 与空气混合,得到 体积分数为1%的气体样品。使用下图装置(部分加热及夹持装置省
略),调节管式炉温度至 ,按一定流速通入气体样品。(已知: 是白色固体,易吸水潮解:)
(4)通入 (已折算为标况)的气体样品后,继续向装置内通入一段时间氮气,最终测得U形管内生成
了 。
①能证明 被空气氧化的现象是_______;
② 被催化氧化的百分率为_______;
③若未通入氮气,②的结果将_______(填“偏大”“偏小”或“无影响”)。
(5)探究气体与催化剂接触时长对催化氧化效率的影响时,采用_______方法可以缩短接触时长。
(6)步骤Ⅲ装置存在的不足之处是_______。
17.(14分)用化学方法降解水中有机物已成为污水处理领域的重要研究方向。
(1)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图1所示。
①该物质转化示意图可以描述为 。
②其他条件一定,反应相同时间,硝基苯的去除率与pH的关系如图2所示。pH越大,硝基苯的去除率越
低的原因是 。
(2)向含Fe2+和苯胺( )的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H O=Fe3+
2 2
+HO·+HO
2
①HO·(羟基自由基)具有强氧化性,能将溶液中的苯胺氧化成CO 和N。写出该反应的离子方程式:
2 2
。
②H O 也具有氧化性,设计验证苯胺是被HO·氧化而不是被HO 氧化的实验方案: 。
2 2 2 2
(3)利用电化学装置通过间接氧化法能氧化含苯胺的污水,其原理如图3所示。其他条件一定,测得不同初始pH条件下,溶液中苯胺的浓度与时间的关系如图4所示。反应相同时间,初始溶液pH=3时苯胺浓度
大于pH=10时的原因是 。[已知氧化性:HClO(H+)>ClO-(OH-)]
18.(15分)丙烯醛( )是一种重要的有机合成原料,用其合成3-氯丙醛二乙醇缩醛(B)和
DAP树脂的一种路线如下:
已知醇与酯可发生如下的酯交换反应:RCOOR′+R″OH RCOOR″+R′OH(R、R'、R″代表烃基)
回答下列问题:
(1)已知A的结构简式为 ,在制备A的过程中最容易生成的另一种副产物为
(写结构简式)。
(2)设计丙烯醛→A和C→D步骤的目的为 。
(3)已知3-氯丙醛二乙醇缩醛(B)的核磁共振氢谱有5组峰,则其结构简式为 。
(4)已知E的苯环上的一氯代物有两种,则E的名称为 ;E→F的反应类型为 。
(5)DAP单体中含两个碳碳双键,则由D和F制备DAP单体的化学方程式为 。
(6)满足下列条件的F的同分异构体M有 种(不包含立体异构)。
i.苯环上有三个取代基,且只含有一种官能团
ii.除苯环外无其他环状结构
iii.1molM最多能消耗4molNaOH(7)结合上述流程,以乙烯为原料制备 的合成路线为(无机试剂任选) 。