文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(广东专用)
黄金卷05
(考试时间:75分钟 试卷满分:100分)
第Ⅰ卷
一、选择题:本题共16个小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在
每小题给出的四个选项中,只有一项是符合题目要求的。
1.我国的航空航天事业取得巨大成就,下列所述物质为金属材料的是
航空航
天成果
宇航服中的聚酯 北斗卫星使用的氮化铝芯 长征火箭使用的
物质 C919外壳中的铝锂合金
纤维 片 液氢燃料
选项 A B C D
【答案】B
【解析】A.聚酯纤维为有机高分子材料,A项不符合题意;
B.铝锂合金为金属材料,B项符合题意;
C.氮化铝为新型无机非金属材料,C不符合题意;
D.液氢燃料为无机非金属材料,D不符合题意;
故选B。
2.关于下列诗句或谚语隐含的化学知识,说法错误的是
A.“爆竹声中一岁除”,爆竹中的火药含有硫黄
B.“木棉花落絮飞初”,“絮”的主要成分是纤维素
C.“谷雨种甘蔗”,甘蔗中的蔗糖是多糖
D.“雷雨发庄稼”,该过程有硝酸生成
【答案】C
【解析】A.爆竹中的火药含有硫黄,A项正确;B.柳絮含有植物纤维,其主要成分为纤维素,B项正确;
C.蔗糖是双糖,不是多糖,C项错误;
D.“雷雨发庄稼”,在雷雨天,氮气与氧气反应生成一氧化氮,一氧化氮和氧气生成二氧化氮,二氧化
氮与水生成硝酸,在土壤中形成硝酸盐,该过程有硝酸生成,D项正确;
答案选C。
3.“天问一号”探测器成功着陆火星,“祝融号”火星车执行探测任务。下列说法不正确的是
A.火星陨石中的20Ne质子数为20
B.火星大气中的40Ar和36Ar互为同位素
C.“天问一号”使用的新型镁锂合金是金属材料
D.“祝融号”使用的太阳能电池能将光能转化为电能
【答案】A
【解析】A.Ne是10号元素,原子核内有10个质子,火星陨石中的20Ne是质子数为10,质量数为20的
一种核素,A错误;
B.火星大气中的40Ar和36Ar质子数相同,而中子数不同,因此二者互为同位素,B正确;
C.镁锂合金属于合金,合金是金属材料,C正确;
D.“祝融号”使用的太阳能电池是将光能转化为电能的装置,D正确;
故合理选项是A。
4.实验室进行粗盐提纯时,完成该实验所需的装置或操作错误的是
A B C D
溶解 滴加试剂除杂 过滤 蒸发结晶
【答案】C
【解析】A.粗盐需在烧杯中溶解,A正确;
B.粗盐溶液加入相应试剂除去可溶性杂质,B正确;
C.过滤时漏斗下端要紧贴烧杯内壁,C错误;
D.蒸发结晶得到氯化钠晶体,D正确;
故选C。5.一种合成玫瑰香油的主要原料的结构简式如图所示,关于该有机物说法正确的是
A.分子式为C H O,属于烯烃 B.不能使酸性高锰酸钾溶液褪色
10 18
C.能发生水解反应 D.能发生加成反应和取代反应
【答案】D
【解析】A.根据结构简式知,分子式为C H O,含有O原子,不属于烃类,故A错误;
10 18
B.含有碳碳双键,能发生氧化反应,则可使酸性高锰酸钾溶液褪色,故B错误;
C.含有羟基,不能发生水解反应,故C错误;
D.含有碳碳双键和醇羟基,所以能发生加成反应、取代反应,故D正确;
故选:D。
6.某金属-空气电池的工作原理如图所示。下列说法错误的是
A.金属M作电池负极,放电时发生氧化反应
B.放电时,空气中的氧气得到电子
C.电池总反应为
D.放电时,外电路电子由碳材料电极流向金属M电极
【答案】D
【分析】由示意图中离子的移动方向可知,金属M电极为原电池的负极,M失去电子发生氧化反应生成
M2+,碳材料电极为正极,氧气在正极得到电子发生还原反应生成氢氧根离子,电池的总反应方程式为
。
【解析】A.由分析可知,金属M电极为原电池的负极,M失去电子发生氧化反应生成M2+,故A正确;;
B.由分析可知,碳材料电极为正极,氧气在正极得到电子发生还原反应生成氢氧根离子,故B正确;C.由分析可知,电池的总反应方程式为 ,故C正确;
D.原电池工作时,外电路电子由负极流向正极,则放电时,外电路电子由M电极流向金属碳材料电极,
故D错误;
故选D。
7.劳动开创未来。下列劳动项目与所述的化学知识没有关联的是
选项 劳动项目 化学知识
A 工人用明矾处理废水 是两性氢氧化物
B 工人用 消毒自来水 具有强氧化性
C 雕刻师用氢氟酸刻蚀石英制作艺术品 可与 反应
酿酒师在葡萄酒中添加适量的二氧化
D 可以杀菌和抗氧化
硫
【答案】A
【解析】A.明矾处理废水,利用 胶体的吸附性,与Al(OH) 是两性氢氧化物无关,A错误;
3
B. 具有强氧化性,可用 消毒自来水,B正确;
C. 可与 反应,可用氢氟酸刻蚀玻璃,C正确;
D. 可以杀菌和抗氧化,可在葡萄酒中添加适量的二氧化硫,D正确;
故选A。
8.下列离子方程式书写正确的是
A.将金属钠投入水中:
B.将铜丝插入稀硝酸中:
C.向硫酸铝溶液中加入过量氨水:
D.向氯化铁溶液中滴加碳酸钠溶液:
【答案】C【解析】A. 将金属钠投入水中: ,故A错误;
B. 将铜丝插入稀硝酸中生成NO: ,故B错误;
C. 向硫酸铝溶液中加入过量氨水生成氢氧化铝沉淀和硫酸铵,沉淀不溶于氨水:
,故C正确;
D. 向氯化铁溶液中滴加碳酸钠溶液双水解生成氢氧化铁和二氧化碳:
,故D错误;
故选C。
9.我国科学家利用高效固体催化剂LDH,实现了在常温常压、可见光下人工固氮,其原理如图所示。下
列有关该反应说法不正确的是
A.存在极性键、非极性键的断裂与形成
B.反应过程中存在太阳能转化为化学能
C.使用LDH,可同时提高反应速率和 的转化率
D.反应生成1.7g 时转移电子数目为0.3mol
【答案】C
【分析】该反应的化学方程式为2N+6H O 4NH +3O 。
2 2 3 2
【解析】A. 存在极性键、非极性键的断裂(H-O极性键、N-N非极性键)与形成(H-N极性键、O-O非极性
键),故A正确;B. 2N+6H O 4NH +3O 为吸热反应,反应过程中存在太阳能转化为化学能,故B正确;
2 2 3 2
C. 催化剂不能使平衡发生移动,使用LDH,可同时提高反应速率,但不能提高 的转化率,故C错误;
D. 该反应的化学方程式为2N+6H O 4NH +3O ,由于氮元素从0价降为-3价,所以每生成1 mol
2 2 3 2
NH 转移电子数为3mol,反应生成1.7g (即0.1mol) 时转移电子数目为0.3mol,故D正确;
3
故选C。
10.以Fe O/Al O 为氧载体,化学链制氢联合甲烷干重整制备合成气(CO、H)的原理如下图所示。下列有
2 3 2 3 2
关叙述错误的是
A.“还原”时,CH 为还原剂
4
B.“干重整”时,装置中可能出现积碳
C.“氧化II”中主要反应是2Fe(OH) Fe O+3H O
3 2 3 2
D.该过程能有效实现温室气体(CH、CO)的回收利用
4 2
【答案】C
【解析】A.“还原”时,CH 被氧化为二氧化碳,为还原剂,A正确;
4
B.甲烷中碳元素是-4价,二氧化碳中碳元素化合价是+4价,因此“干重整”时有可能生成单质碳,所
以装置中可能出现积碳,B正确;
C.铁和水蒸气反应生成四氧化三铁,则“氧化II”中主要反应是O+4Fe O 6Fe O,C错误;
2 3 4 2 3
D.根据示意图和已知信息可判断该过程能有效实现温室气体(CH、CO)的回收利用,D正确;
4 2答案选C。
11.X、Y、Z、W、R 是原子序数依次增大的短周期主族元素,Y 的同位素常用于判定古文物的年代,R
与 Y 位于同一主族,W 的电子层数与主族序数相同,X、Y、Z 组成的化合物甲的球棍模型如图所示,
甲在疫情期间可用做消毒剂。下列说法正确的是
A.X 与 Y 只能形成两种二元化合物
B.最高价氧化物对应水化物的酸性:R>Y
C.原子半径的大小关系:W>R>Z>Y>X
D.化合物甲中存在极性共价键、非极性共价键,具有强氧化性
【答案】D
【分析】判定文物年代可用14C,故Y为C,则R为Si,由球棍模型知,黑球为C,空心球半径比C小,
且周围形成1根共价键,推测为H,阴影球周围可形成2根键,推测为O,结合原子序数确定X为H,Z
为O,W原子序数介于O与Si之间,且电子层数与最外层电子数(主族序数)相等,故W为Al。
【解析】A.X:H与Y:C可形成多种烃类有机物,如烷烃、烯烃、炔烃、芳香烃等,A错误;
B.由于非金属性Y:C>R:Si,故最高价氧化物对应水化物的酸性Y>R,B错误;
C.一般电子层数多,原子半径大,电子层数相同时,核电荷数越大,原子半径越小,故四种原子半径大
小顺序为:W>R>Y>Z>X,C错误;
D.化合价甲中存在极性共价键C—H、C=O、C—O、O—H,非极性共价键C—C、O—O,其中过氧键—
O—O—结构具有强氧化性,D正确;
故答案选D。
12.化学实验源于生活。下列实验方案设计、现象与结论均正确的是
选项 目的 方案设计 现象与结论
检验食盐中是 溶液颜色不变,说明该食
A 向某食盐溶液中滴加淀粉溶液
否含碘元素 盐属于无碘盐
检验火柴头中
将几根未燃过的火柴头浸入水中,稍后取少量溶液 若有白色沉淀产生,|说明
B 是否含有氯元
于试管中,加入稀 、 溶液 火柴头中含有氯元素
素
C
检验菠菜中的 取少量菠菜叶剪碎研磨后加水搅拌,取上层清液于 若溶液变红,说明菠菜中铁元素 试管中,加入稀硝酸后再加入 溶液 含有铁元素
检验鸡皮中是 取一小块鸡皮于表面皿上,将几滴浓硝酸滴到鸡皮 一段时间后鸡皮变黄,说
D
否含有脂肪 上 明鸡皮中含有脂肪
【答案】C
【解析】A.食盐中所加碘一般为碘酸钾,碘酸钾遇淀粉不变蓝色,因此实验设计不合理,故A错误;
B.火柴头中的氯元素在氯酸钾中存在,氯酸钾溶于水不能直接电离出氯离子,加硝酸酸化的硝酸银不能
生成氯化银白色沉淀,故B错误;
C.加硝酸后再加KSCN溶液变红,说明溶液中存在 ,从而可说明菠菜中含有铁元素,故C正确;
D.加浓硝酸鸡皮变黄,是蛋白质的性质,不能证明脂肪存在,故D错误;
故选:C。
13.X、Y、Z、W、Q为原子序数依次递增的短周期主族元素。基态X原子价电子层有3个单电子,Z与
Y可形成原子个数比为1∶1的含非极性共价键的离子化合物。W、Q的最外层电子数之和等于Z的原子序
数。下列说法正确的是
A.简单离子半径:Z>Y B.X、W单质的晶体类型一定相同
C.简单气态氢化物的稳定性:X>Y D.Q的最高价含氧酸根的空间结构为正四面体形
【答案】D
【分析】X、Y、Z、W、Q为原子序数依次递增的短周期主族元素,基态X原子价电子层有3个单电子,
电子排布式应为1s22s22p3,所以X为N,Z与Y可形成原子个数比为1∶1的含非极性共价键的离子化合物
应为NaO,所以Y为O,Z为Na,W、Q的最外层电子数之和等于Z的原子序数11,所以W、Q分别为
2 2
P、S或Si、Cl。
【解析】A.简单离子半径:Na+<O2-,故A错误;
B.X单质为N 分子晶体,W单质可能为Si或P,可能是共价晶体,也可能是分子晶体,晶体类型不一定
2
相同,故B错误;
C.非金属性O比N强,故简单气态氢化物的稳定性:NH <HO,故C错误;
3 2
D.Q的最高价含氧酸根可能为 或者 ,两种离子中心原子价层电子对数均为4,均没有孤电子对,
空间结构均为正四面体形,故D正确;
所以答案为D。
14.工业上制备硫酸的流程: ,设 为阿伏伽德罗常数,
下列有关说法正确的是A. 中 的未成对电子数目为6
B. 的中心原子孤对电子数为1,其空间构型为V型
C.标准状况下,22.4L 中含有氧原子数目为
D. 作催化剂,能降低该反应的活化能,提高 的平衡转化率
【答案】B
【解析】A. 的电子排布式为1s22s22p63s23p63d6,未成对电子数目为4,故A错误;
B.SO2的中心原子价层电子对数为 ,孤对电子数为1,其空间构型为V型;故B正确;
C.标准状况下SO 为液态,所以22.4LSO 的物质的量大于1mol,所以含有氧原子数目大于为3N ,故C
3 3 A
错误;
D. 作催化剂,能降低该反应的活化能,但不能提高 的平衡转化率;故D错误;
故答案选B。
15.我国科学家报道了机理如下图所示的电化学过程。下列相关说法错误的是
A.Ni电极为阴极
B.Ni-YSZ电极上发生的反应为CH+2O2-—4e-=CO +2H
4 2 2
C.该电化学过程的总反应为CH C+2H
4 2
D.理论上,每有1mol CO 与1mol O2-结合,电路中转移2mole-
2
【答案】D
【分析】由图可知,该装置为电解池,Ni-YSZ电极物为电解池的阳极,Ni电极为阴极,在氧离子作用下,甲烷在阳极失去电子发生氧化反应生成二氧化碳和氢气,电极反应式为CH+2O2--4e-=CO +2H ,放电生成
4 2 2
的二氧化碳在熔融盐中与氧离子结合生成碳酸根离子,碳酸根离子在阴极得到电子发生还原反应生成碳和
氧离子,电极反应式为CO +4e-=C+3O2-,电解的总反应方程式为CH C+2H 。
4 2
【解析】A.由分析可知,Ni电极为阴极,碳酸根离子在阴极得到电子发生还原反应生成碳和氧离子,故
A正确;
B.由分析可知,Ni-YSZ电极物为电解池的阳极,电极反应式为CH+2O2--4e-=CO +2H ,故B正确;
4 2 2
C.由分析可知,电解的总反应方程式为CH C+2H ,故C正确;
4 2
D.由分析可知,每有1molCO 与1molO2-结合成1mol ,电路中转移4mole-,故D错误;
2
故选D。
16.在容积为VL的恒温密闭容器中模拟工业合成氨。充入N 和H 的总物质的量为1mol,容器内各组分
2 2
的物质的量分数与反应时间t的关系如图所示。下列说法不正确的是
A.a表示N 物质的量分数的变化情况物质的量分数
2
B.0~tmin,v(H )= mol·L-1·min-1
1 2
C.tmin时,NH 的分解速率小于其生成速率
2 3
D.tmin时改变的条件可能为减小容器容积
3
【答案】B
【分析】由题中图示可知,开始时N 和H 各占50%,总物质的量是1mol,则N 和H 各为0.5mol,由
2 2 2 2可得,某时刻总物质的量为n(总)=(0.5-
x)mol+(0.5-3x)mol+2xmol=(1-2x)mol,某时刻N 的物质的量分数为
2
=50%,所以,N 的物质的量分数一直保持不变,是50%,则a
2
代表N 的物质的量分数,随反应进行减小的是c代表H 的物质的量分数,b代表NH 的物质的量分数;据
2 2 3
此解答。
【解析】A.由上述分析可知,N 的物质的量分数一直保持不变,是50%,则a代表N 的物质的量分数,
2 2
故A正确;
B.由上述分析可知,a代表N 的物质的量分数,c代表H 的物质的量分数,b代表NH 的物质的量分数,
2 2 3
t 时H、NH 的物质的量分数相等,即 ,解之x=0.1mol,则0~tmin,v(H )=
1 2 3 1 2
mol·L-1·min-1,故B错误;
C.由上述分析可知,b代表NH 的物质的量分数,t 时刻及以后,NH 的物质的量分数增大,说明反应向
3 2 3
右进行,则NH 的分解速率小于其生成速率,故C正确;
3
D.由N(g)+3H(g) 2NH (g)可知,t 时刻,减小容积,压强增大,平衡正向移动,NH 的物质的量分数
2 2 3 3 3
增大,H 的物质的量分数减小,故D正确;
2
答案为B。
第Ⅱ卷
二、非选择题:本题共4个小题,共56分。
17.(14分)为证明AgCl溶于水存在溶解平衡,取1 mo/LKCl溶液10 mL,向其中加入0.2 mol/LAgNO
3
溶液1 mL,充分反应后将浊液过滤进行如下实验:序 实验
实验操作 实验现象
号 装置
ⅰ.滤液澄清透明,用激光照射有丁达尔现象。
向滤液中
ⅱ.放入Mg条后,立即有无色气泡产生,气体可燃,滤液中出现白色浑浊,
A 放入Mg
条
ⅲ.一段时间后开始出现棕褐色浑浊物。Mg条表面也逐渐变为棕褐色。产生
气泡的速率变缓慢
已知:①AgOH不稳定,立即分解为Ag O (棕褐色或棕黑色),Ag粉为黑色;
2
②AgCl、Ag O可溶于浓氨水生成 [Ag(NH)]+(银氨溶液),Mg、Ag不溶于浓氨水。
2 3 2
(1)实验A中的滤液所属分散系为 。现象ii中无色气泡是 (填化学式)。
(2)现象iii中,导致产生气泡的速率下降的主要原因是 。
(3)判断Mg条表面的棕褐色物质中含有Ag和Ag O。
2
①设计实验检验Ag:取实验A中表面变为棕褐色的Mg条于试管中,向其中加入足量稀盐酸,反应结束后,
继续加入浓硝酸,产生棕色气体和白色不溶物。用离子方程式表示棕褐色固体中产生Ag的原因:
。实验中加入稀盐酸的目的: 。
②设计检验棕褐色物质中有Ag O,实验方案是:取实验A中表面变为棕褐色的Mg条用蒸馏水洗净后,加
2
入 (填化学式)中浸泡,取上层清液于葡萄糖溶液中,水浴加热,若有 (填实验现象),
则证明Ag O存在。
2
(4)探究AgI转化为AgCl,设计实验如下:
装置 步骤 电压表读数
ⅰ.如图连接装置并加入试剂,闭合K a
ⅱ.向B中滴入AgNO(aq),至沉淀完全 b
3
ⅲ.再向B中投入一定量NaCl(s) c
ⅳ.重复ⅰ,再向B中加入与iii等量NaCl(s) d
已知:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大;
离子的氧化性(或还原性)强弱与其浓度有关。
①电压表读数a>b,其原因是 。
②综合实验现象能说明AgI转化为AgCl,则a、b、c三者的大小关系为 。
【答案】(1) 胶体 H
2(2)生成的固体覆盖在Mg表面,阻碍后续反应进行
(3) Mg+2Ag+=2Ag+Mg2+ 将镁除去,避免硝酸与镁反应,干扰检验Ag NH ·H O 银镜生
3 2
成
(4) 加入AgNO 后,生成AgI沉淀使B的溶液中c(I-)减小,I-还原性减弱,导致电压b<a a>c>b
3
【解析】(1)产生丁达尔现象是胶体的性质,因此滤液所属分散系为胶体;
放入Mg条后,立即有无色气泡产生,气体可燃,滤液中出现白色浑浊,Mg属于活泼金属,可以与水反应,
Mg+2HO=Mg (OH) ↓+H ↑,故气泡为H;
2 2 2 2
(2)Mg条表面也逐渐覆盖了棕褐色的Ag O和Ag,减小了镁条与水的接触面积,产生气泡的速率变缓慢;
2
答案为生成的固体覆盖在Mg表面,阻碍后续反应进行;
(3)①活泼金属置换不活泼金属原理,生成Ag的离子方程式为Mg+2Ag+ =Mg2+ +2Ag;
利用Mg属于活泼金属可以与非氧化性酸反应,而银属于不活泼金属不能与非氧化性酸反应,除掉Mg,防
止干扰实验,再选择氧化性酸验证Ag的存在,实验中加入稀盐酸的目的是将镁除去,避免硝酸与镁反应,
干扰检验Ag;
②根据Ag O可溶于浓氨水生成[Ag(NH)]+,利用银镜反应验证;答案为取实验A中表面变为棕褐色的Mg
2 3 2
条用蒸馏水洗净后,加入NH ·H O中浸泡,取上层清液于葡萄糖溶液中,水浴加热,若有银镜生成,则证
3 2
明Ag O存在;
2
(4)加入AgNO 后,生成AgI沉淀使B的溶液中c(I-)减小,I-还原性减弱,导致电压b<a;
3
②实验表明Cl-本身对该原电池电压无影响,说明加入Cl-使c(I-)增大,证明发生了反应AgI+Cl-=AgCl+I-,部分
AgI转化为AgCl, 则c > b,综合实验现象能说明AgI转化为AgCl,则a、b、c三者的大小关系为a>c>b。
18.(14分)工业上可由菱锌矿(主要成分为ZnCO ,还含有Ni、Cd、Fe、Mn等元素)制备ZnO。工艺如
3
图所示:
相关金属离子[c(Mn+)=0.1 mol/L]形成氢氧化物沉淀的pH范围如下:
金属离子 Fe3+ Fe2+ Zn2+ Cd2+ Mn2+ Ni2+
开始沉淀的pH 1.5 6.3 6.0 7.4 8.1 6.9
沉淀完全的pH 2.8 8.3 8.0 9.4 10.1 8.9
已知:①“溶浸”后的溶液pH=1,所含金属离子主要有:Zn2+、Fe3+、Cd2+、Mn2+、Ni2+。②弱酸性溶液中KMnO 氧化Mn2+时,产物中含Mn元素物质只有MnO 。
4 2
③氧化性强弱顺序:Ni2+>Cd2+>Zn2+
(1)基态Zn原子的简化电子排布式为[Ar]_______,ZnO溶于氨水生成[Zn(NH )]2+,1 mol [Zn(NH )]2+共有
3 4 3 4
_______mol的σ键。
(2)①“溶浸”过程中,为了提高浸出率,可采取的措施是_______。(写一条即可)
②“调pH”时,可替代ZnO的一种含锌化合物是_______。(用化学式表示)
③“调pH”时,若pH=5.5,此时溶液中Zn2+的最大浓度c=_______mol/L。
(3)写出“氧化除杂”时KMnO 溶液与Mn2+反应的离子方程式_______。
4
(4)“还原除杂”除去的离子是_______;加入的还原剂是_______。
(5)“沉锌”时生成ZnCO ·2Zn(OH) ·2H O (碱式碳酸锌)沉淀,该沉淀“高温灼烧”后获得ZnO。氧化锌的
3 2 2
一种晶体的晶胞是立方晶胞(如图所示),其中与锌原子距离最近的O原子数有_______个,请在图中画出该
晶胞沿z轴方向的平面投影图_______。
【答案】(1) 3d104s2 16
(2) 加热或搅拌或适当提高硫酸的浓度或将矿石粉碎 ZnCO 或Zn(OH) 或
3 2
ZnCO ·2Zn(OH) ·2H O 1
3 2 2
(3)
(4) Ni2+、Cd2+ Zn
(5) 4
【分析】由菱锌矿(主要成分为ZnCO ,还含有Ni、Cd、 Fe、 Mn等元素)制备ZnO,加入稀硫酸溶浸后
3
得到含Zn2+、Ni2+、Cd2+、Fe2+、Mn2+的滤液,滤液调节pH后加入KMnO 氧化除杂使铁离子、锰离子转化
4
为Fe(OH) 、MnO ,除去Fe3+、Mn2+;接着还原除杂除去Ni2+、Ca2+;最后向含ZnSO 的溶液中加入
3 2 4
NaCO 溶液生成碱式碳酸锌[ZnCO·2Zn(OH) ·2H O]沉淀,碱式碳酸锌高温灼烧得到ZnO。
2 3 3 2 2
【解析】(1)Zn是30号元素,根据构造原理,可知基态Zn原子核外电子排布式是1s22s22p63s23p63d104s2,则其简化的电子排布式是[Ar] 3d104s2;
在络离子[Zn(NH )]2+中含有4个配位体NH ,配位体与中心Zn2+形成4个配位键;每个配位体中含有3个
3 4 3
N-H共价键,配位键及N-H共价键都是σ键,故在1个络离子中含有σ键数目是4+3×4=16个,则在1
mol[Zn(NH )]2+中含有16 molσ键;
3 4
(2)①“溶浸”过程中,为了提高浸出率,可采取的措施是加热或搅拌或适当提高硫酸的浓度或将矿石
粉碎等;
②在调整溶液pH时,除降低溶液pH,不能引入新的杂质离子,可替代ZnO的一种含锌化合物可以是
ZnCO 或Zn(OH) 或ZnCO ·2Zn(OH) ·2H O;
3 2 3 2 2
③根据表格信息可知当Zn2+浓度为0.1 mol/L时,其形成Zn(OH) 沉淀需要溶液pH=6.0,则Zn(OH) 的溶度
2 2
积产生K [Zn(OH) ]=0.1×(10-8)2=1.0×-17。若调整溶液pH=5.5,c(H+)=10-5.5 mol/L,则c(OH-)=
sp 2
,则此时溶液中Zn2+最大浓度c= ;
(3)在氧化除杂时,KMnO 与Mn2+发生氧化还原反应产生MnO ,根据电子守恒、电荷守恒及原子守恒,
4 2
可得反应的离子方程式为 ;
(4)根据流程图可知:在还原除杂之前,已经除去了杂质离子Fe3+、Mn2+,要使还原除杂后溶液中仅含有
金属阳离子Zn2+,需除去溶液中的杂质离子Ni2+、Cd2+;由于离子的氧化性顺序为:Ni2+>Cd2+>Zn2+,故
加入的还原剂可以是金属Zn;
(5)以上底面心Zn原子为研究对象,在一个晶胞中与该Zn原子距离最近的O原子数有2个,通过该平
面可以形成2个晶胞,故在晶胞中与Zn原子距离且最近的O原子数共有4个;
关键晶胞结构可知:晶胞在Z轴的投影情况是:Zn原子位于正方形的四个顶点上,四条棱边中心上和面心
上,4个O原子分别位于面内对角线离顶点 处,可用图示可表示为 。
19.(14分)氮及其化合物是科学家们一直在探究的问题,它们在工农业生产和生命活动中起着重要的作
用。回答下列问题:
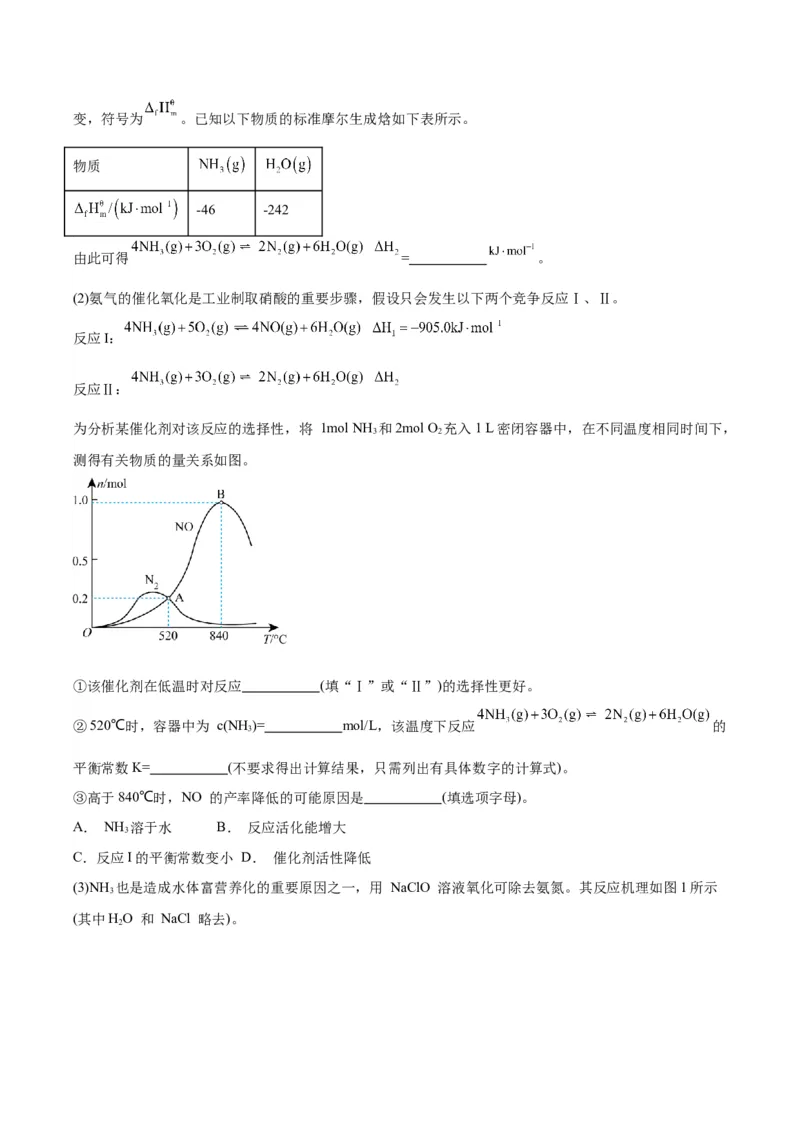
(1)查阅资料:标准摩尔生成焓是指在 25℃和101kPa时,由元素最稳定的单质生成 1mol纯化合物时的焓变,符号为 。已知以下物质的标准摩尔生成焓如下表所示。
物质
-46 -242
由此可得 = 。
(2)氨气的催化氧化是工业制取硝酸的重要步骤,假设只会发生以下两个竞争反应Ⅰ、Ⅱ。
反应I:
反应Ⅱ:
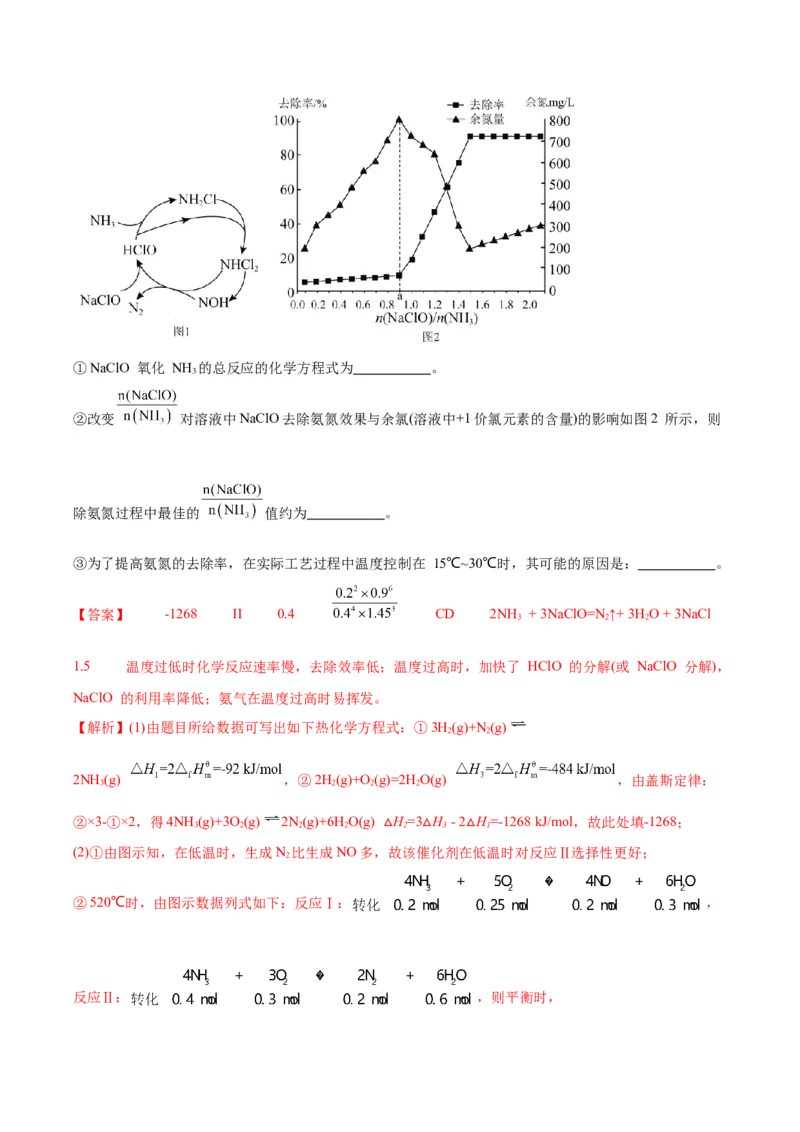
为分析某催化剂对该反应的选择性,将 1mol NH 和2mol O 充入1 L密闭容器中,在不同温度相同时间下,
3 2
测得有关物质的量关系如图。
①该催化剂在低温时对反应 (填“Ⅰ”或“Ⅱ”)的选择性更好。
②520℃时,容器中为 c(NH )= mol/L,该温度下反应 的
3
平衡常数K= (不要求得出计算结果,只需列出有具体数字的计算式)。
③高于840℃时,NO 的产率降低的可能原因是 (填选项字母)。
A. NH 溶于水 B. 反应活化能增大
3
C.反应I的平衡常数变小 D. 催化剂活性降低
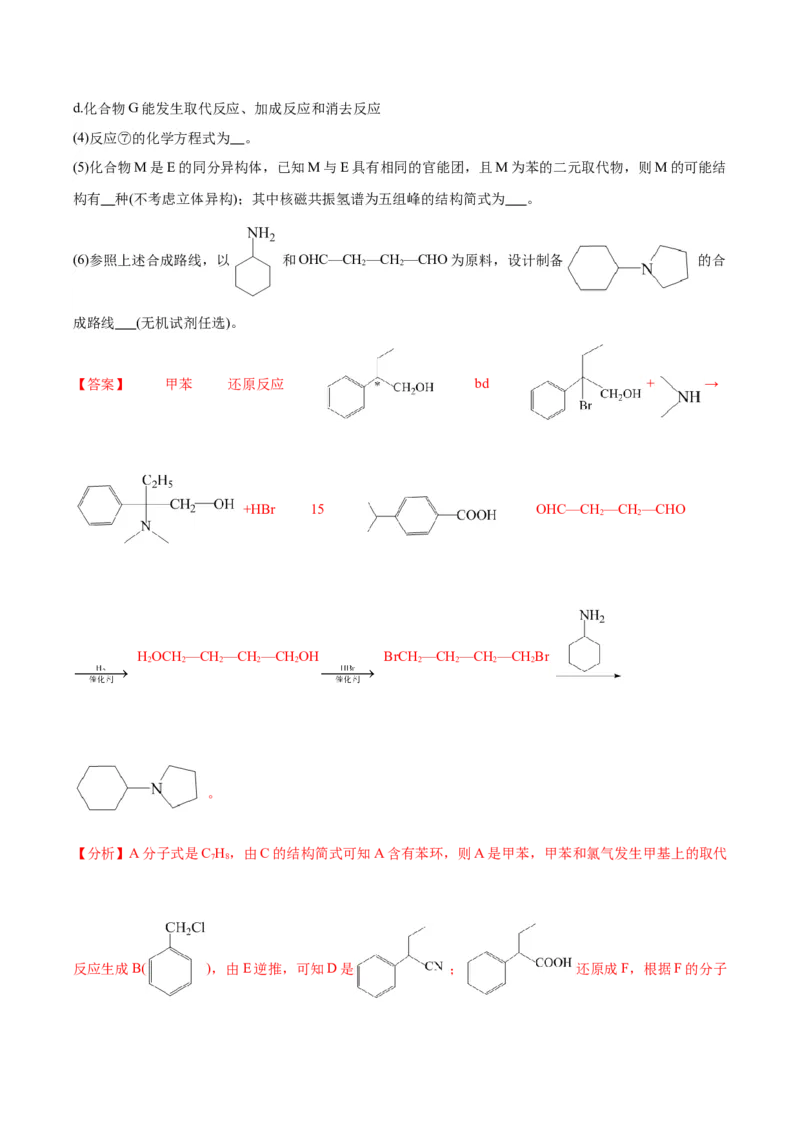
(3)NH 也是造成水体富营养化的重要原因之一,用 NaClO 溶液氧化可除去氨氮。其反应机理如图1所示
3
(其中HO 和 NaCl 略去)。
2①NaClO 氧化 NH 的总反应的化学方程式为 。
3
②改变 对溶液中NaClO去除氨氮效果与余氯(溶液中+1价氯元素的含量)的影响如图2 所示,则
除氨氮过程中最佳的 值约为 。
③为了提高氨氮的去除率,在实际工艺过程中温度控制在 15℃~30℃时,其可能的原因是: 。
【答案】 -1268 II 0.4 CD 2NH + 3NaClO=N ↑+ 3H O + 3NaCl
3 2 2
1.5 温度过低时化学反应速率慢,去除效率低;温度过高时,加快了 HClO 的分解(或 NaClO 分解),
NaClO 的利用率降低;氨气在温度过高时易挥发。
【解析】(1)由题目所给数据可写出如下热化学方程式:①3H(g)+N(g)
2 2
2NH (g) ,②2H(g)+O(g)=2HO(g) ,由盖斯定律:
3 2 2 2
②×3-①×2,得4NH (g)+3O(g) 2N(g)+6HO(g) H=3 H - 2 H=-1268 kJ/mol,故此处填-1268;
3 2 2 2 2 3 1
(2)①由图示知,在低温时,生成N 比生成NO多,△故该催△化剂在△低温时对反应Ⅱ选择性更好;
2
②520℃时,由图示数据列式如下:反应Ⅰ: ,
反应Ⅱ: ,则平衡时,、 、 、
,则反应Ⅱ的平衡常数 ;
③由于反应用到了催化剂,故此时NO产率降低有可能是因为温度过高导致催化剂活性下降,另外此反应
正向为放热反应,升高温度,平衡逆向移动,也会导致NO产率下降,故此处选CD;
(3)①由图1知,初步确定总反应的反应物为NaClO、NH ,生成物为N,根据元素守恒结合题干信息,确
3 2
定生成物中还有HO、NaCl,结合得失电子守恒和元素守恒配平得总反应为:2NH + 3NaClO=N ↑+ 3H O
2 3 2 2
+ 3NaCl;
②去除率较高,余氯量较低,说明去除效果最佳,符合要求的最佳值约为1.5;
③控温15~30℃,可从温度过低和过高两个角度回答,即温度过低时化学反应速率慢,去除效率低;温度
过高时,加快了 HClO 的分解(或 NaClO 分解),NaClO 的利用率降低且氨气在温度过高时易挥发。
20.(14分)曲美布汀是一种消化系统药物的有效成分,能缓解各种原因引起的胃肠痉挛,可通过以下路
线合成。
已知:R—CN R—COOH
回答下列问题:
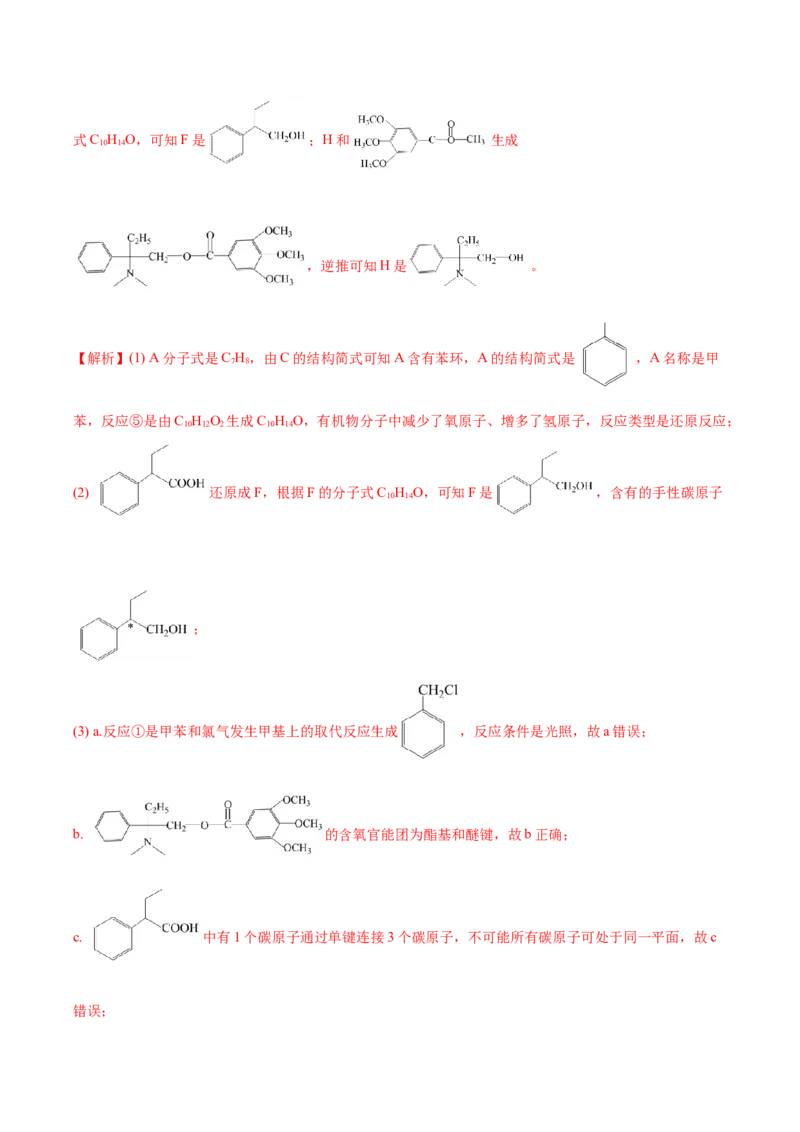
(1)A的名称是 ,反应⑤的反应类型是 。
(2)写出F的结构简式并用星号(*)标出手性碳原子 。
(3)下列有关说法正确的是 (填标号)。
a.反应①需用铁粉作催化剂
b.曲美布汀的含氧官能团为酯基和醚键
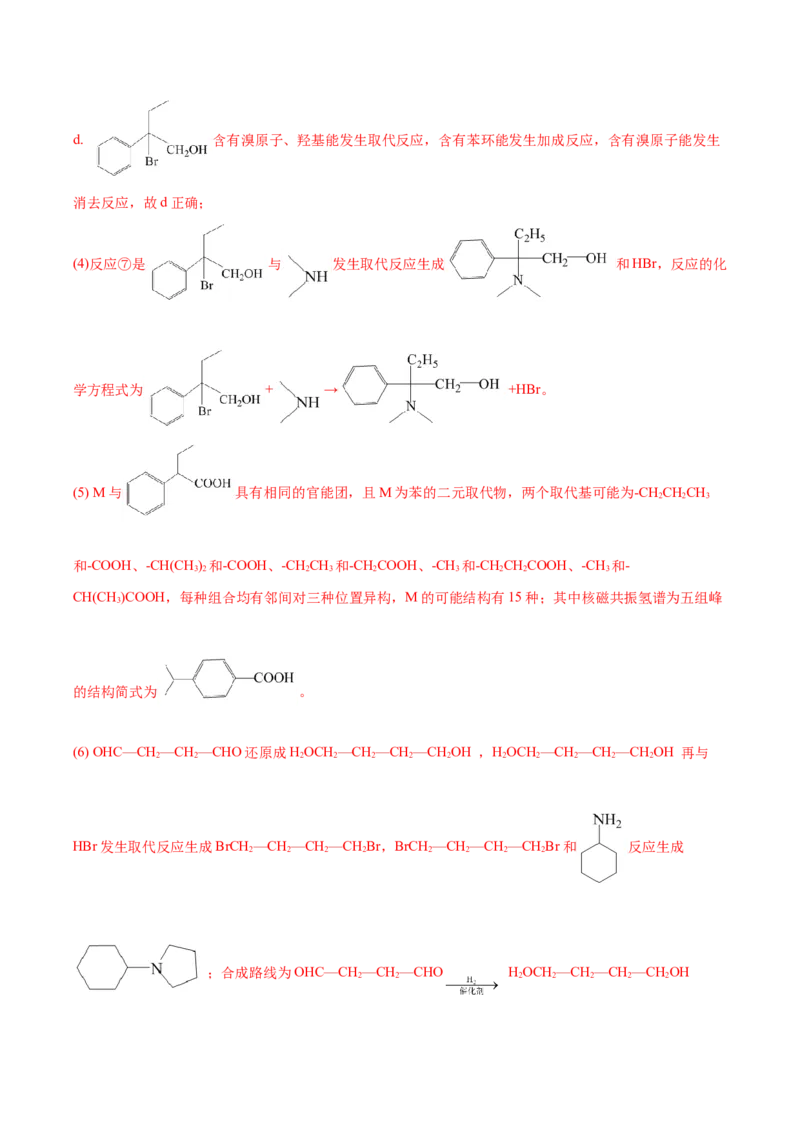
c.E中所有碳原子可处于同一平面d.化合物G能发生取代反应、加成反应和消去反应
(4)反应⑦的化学方程式为 。
(5)化合物M是E的同分异构体,已知M与E具有相同的官能团,且M为苯的二元取代物,则M的可能结
构有 种(不考虑立体异构);其中核磁共振氢谱为五组峰的结构简式为 。
(6)参照上述合成路线,以 和OHC—CH —CH—CHO为原料,设计制备 的合
2 2
成路线 (无机试剂任选)。
【答案】 甲苯 还原反应 bd + →
+HBr 15 OHC—CH —CH—CHO
2 2
HOCH —CH—CH—CHOH BrCH—CH—CH—CHBr
2 2 2 2 2 2 2 2 2
。
【分析】A分子式是C H,由C的结构简式可知A含有苯环,则A是甲苯,甲苯和氯气发生甲基上的取代
7 8
反应生成B( ),由E逆推,可知D是 ; 还原成F,根据F的分子式C H O,可知F是 ;H和 生成
10 14
,逆推可知H是 。
【解析】(1) A分子式是C H,由C的结构简式可知A含有苯环,A的结构简式是 ,A名称是甲
7 8
苯,反应⑤是由C H O 生成C H O,有机物分子中减少了氧原子、增多了氢原子,反应类型是还原反应;
10 12 2 10 14
(2) 还原成F,根据F的分子式C H O,可知F是 ,含有的手性碳原子
10 14
;
(3) a.反应①是甲苯和氯气发生甲基上的取代反应生成 ,反应条件是光照,故a错误;
b. 的含氧官能团为酯基和醚键,故b正确;
c. 中有1个碳原子通过单键连接3个碳原子,不可能所有碳原子可处于同一平面,故c
错误;d. 含有溴原子、羟基能发生取代反应,含有苯环能发生加成反应,含有溴原子能发生
消去反应,故d正确;
(4)反应⑦是 与 发生取代反应生成 和HBr,反应的化
学方程式为 + → +HBr。
(5) M与 具有相同的官能团,且M为苯的二元取代物,两个取代基可能为-CHCHCH
2 2 3
和-COOH、-CH(CH ) 和-COOH、-CHCH 和-CHCOOH、-CH 和-CHCHCOOH、-CH 和-
3 2 2 3 2 3 2 2 3
CH(CH )COOH,每种组合均有邻间对三种位置异构,M的可能结构有15种;其中核磁共振氢谱为五组峰
3
的结构简式为 。
(6) OHC—CH —CH—CHO还原成HOCH —CH—CH—CHOH ,HOCH —CH—CH—CHOH 再与
2 2 2 2 2 2 2 2 2 2 2 2
HBr发生取代反应生成BrCH—CH—CH—CHBr,BrCH—CH—CH—CHBr和 反应生成
2 2 2 2 2 2 2 2
;合成路线为OHC—CH —CH—CHO HOCH —CH—CH—CHOH
2 2 2 2 2 2 2BrCH—CH—CH—CHBr 。
2 2 2 2