文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(湖南专用)
黄金卷05
(考试时间:75分钟;试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Cl-35.5 Si-28 Na-23 Ag-108
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.中国传统文化中包含大量化学知识,下列说法错误的是
A.“石硫磺(S)能化……银、铜、铁,奇物”,这句话体现了石硫磺的氧化性
B.“春蚕到死丝方尽,蜡炬成灰泪始干”,其中的“蜡炬成灰”属于化学变化
C.《本草纲目》中多次提到“烧酒”,用高粱酿酒中的“馏酒”是指蒸馏操作
D.“至于矾现五色之形,硫为群石之将,皆变化于烈火”,其中的“矾”指的是金属硫化物
【答案】D
【详解】A.硫黄与金属反应生成金属硫化物,硫元素化合价降低,硫作氧化剂,表现氧化性,故A正确;
B.石蜡燃烧生成二氧化碳、水,属于化学变化,故B正确;
C.“馏酒”是指用蒸馏方法将乙醇蒸出,故C正确;
D.“矾”指的是金属(如钠、锌、铁、铜等)的硫酸盐,故D错误;
选D。
2.实验室中使用盐酸、硫酸和硝酸时,对应关系错误的是
A.稀盐酸:配制 溶液
B.稀硫酸:蔗糖和淀粉的水解
C.稀硝酸:清洗附有银镜的试管
D.浓硝酸:苯的硝化
【答案】D
【详解】A.实验室配制AlCl 溶液时向其中加入少量的稀盐酸以抑制Al3+水解,A不合题意;
3
B.蔗糖和淀粉的水解时常采用稀硫酸作催化剂,B不合题意;
C.清洗附有银镜的试管用稀硝酸,反应原理为:3Ag+4HNO (稀)=3AgNO +NO↑+2HO,C不合题意;
3 3 2
D.苯的硝化是苯和浓硫酸共热,反应生成硝基苯的反应,故需要用到浓硫酸和浓硝酸的混合溶液,D符
合题意;
故答案为:D。
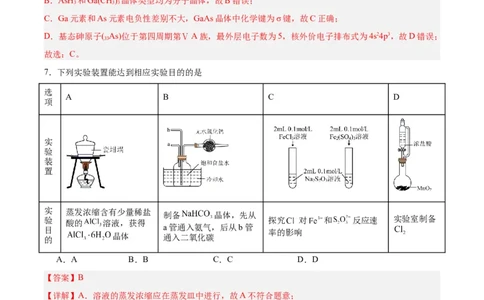
3.完成下述实验,装置或试剂错误的是A.实验室制Cl B.实验室收集NO
2
C.验证NH 易溶于水且溶液呈碱性 D.除去CO 中混有的少量HCl
3 2
【答案】D
【详解】A.在加热条件下,浓盐酸和MnO 反应生成Cl,图中装置能制取氯气,故A正确;
2 2
B.NO难溶于水,所以可以采用排水法收集,故B正确;
C.打开活塞,将胶头滴管中的水挤入烧瓶中,氨气溶于导致烧瓶内压强急剧减小,外界大气压不变,大
气压将水通过导管进入烧瓶中而形成喷泉,氨气和水反应生成的一水合氨电离出OH-而使其水溶液呈碱性,
酚酞遇碱溶液变红色,所以该装置能 验证NH 易溶于水且溶液呈碱性,故C正确;
3
D.CO、HCl都能和NaCO 溶液反应,应该用饱和NaHCO 溶液除去CO 中的HCl,故D错误;
2 2 3 3 2
故选:D。
4.下列有关电极方程式或离子方程式错误的是
A.碱性锌锰电池的正极反应:MnO +H O+e-=MnO(OH)+OH-
2 2
B.铅酸蓄电池充电时的阳极反应:Pb2++2H O-2e-=PbO+4H+
2 2
C.K[Fe(CN) ]溶液滴入FeCl 溶液中:K++Fe2++[Fe(CN)]3-=KFe[Fe(CN) ]↓
3 6 2 6 6
D.TiCl 加入水中:TiCl +(x+2)H O=TiO·xHO↓+4H++4Cl-
4 4 2 2 2
【答案】B
【详解】A.碱性锌锰电池放电时正极得到电子生成MnO(OH),电极方程式为MnO +H O+e-=MnO(OH)
2 2
+OH-,A正确;
B.铅酸电池在充电时阳极失电子,其电极式为:PbSO -2e-+2H O=PbO +4H++SO ,B错误;
4 2 2
C.K[Fe(CN) ]用来鉴别Fe2+生成滕氏蓝沉淀,反应的离子方程式为K++Fe2++[Fe(CN)]3-=KFe[Fe(CN) ]↓,C
3 6 6 6
正确;
D.TiCl 容易与水反应发生水解,反应的离子方程式为TiCl +(x+2)H O=TiO·xHO↓+4H++4Cl-,D正确;
4 4 2 2 2
故答案选B。
5.石墨与F 在450℃反应,石墨层间插入F得到层状结构化合物(CF) ,该物质仍具润滑性,其单层局部
2 x结构如图所示。下列关于该化合物的说法正确的是
A.与石墨相比,(CF) 导电性增强
x
B.与石墨相比,(CF) 抗氧化性增强
x
C.(CF) 中 的键长比 短
x
D.1mol(CF) 中含有2xmol共价单键
x
【答案】B
【详解】A.石墨晶体中每个碳原子上未参与杂化的1个2p轨道上电子在层内离域运动,故石墨晶体能导
电,而(CF) 中没有未参与杂化的2p轨道上的电子,故与石墨相比,(CF) 导电性减弱,A错误;
x x
B.(CF) 中C原子的所有价键均参与成键,未有未参与成键的孤电子或者不饱和键,故与石墨相比,(CF)
x x
抗氧化性增强,B正确;
C.已知C的原子半径比F的大,故可知(CF) 中 的键长比 长,C错误;
x
D.由题干结构示意图可知,在(CF) 中C与周围的3个碳原子形成共价键,每个C-C键被2个碳原子共用,
x
和1个F原子形成共价键,即1mol(CF) 中含有2.5xmol共价单键,D错误;
x
故答案为:B。
6.周期表中ⅤA族元素及其化合物作用广泛。氨是重要的化工原料;肼( )的燃烧热为 ,
是常用的火箭燃料;由磷酸钙、石英砂和碳粉在电弧炉中熔烧可生成白磷( )和CO;在一定条件下白磷可
转化为黑鳞,在700~900℃条件下, 与 可制得半导体材料砷化镓晶体;铋酸钠( )不
溶于冷水,在酸性条件下与 反应生成 、 ,在钢铁工业中可用于锰元素的分析测定。下
列说法正确的是
A. 和 中的键角相等B. 和 晶体类型均为共价晶体
C.砷化镓晶体中化学键为σ键
D.基态砷原子( )核外价电子排布式为
【答案】C
【详解】A. 中只含有N-H键, 含有N-H和N-N,二者键角不相等,故A错误;
B.AsH 和Ga(CH ) 晶体类型均为分子晶体,故B错误;
3 3 3
C.Ga元素和As元素电负性差别不大,GaAs晶体中化学键为σ键,故C正确;
D.基态砷原子( As)位于第四周期第ⅤA族,最外层电子数为5,核外价电子排布式为4s24p3,故D错误;
33
故选:C。
7.下列实验装置能达到相应实验目的的是
选
A B C D
项
实
验
装
置
实 蒸发浓缩含有少量稀盐
制备 晶体,先从
验 探究 对 和 反应速 实验室制备
酸的 溶液,获得
a管通入氨气,后从b管
目 率的影响
的 晶体 通入二氧化碳
A.A B.B C.C D.D
【答案】B
【详解】A.溶液的蒸发浓缩应在蒸发皿中进行,故A不符合题意;
B.氨气极易溶于水,二氧化碳在水中溶解度较小,制备 晶体,先从a管通入氨气,形成碱性溶
液后,再从b管通入二氧化碳,以增加二氧化碳的溶解量,能达到相应实验目的,故B符合题意;
C.图中向两支试管中加入的 的浓度不同,且 离子也可能影响 和 反应速率,不能达到相
应实验目的,故C不符合题意;
D. 和浓盐酸反应制备氯气,需要加热,不能达到相应实验目的,故D不符合题意;故选B。
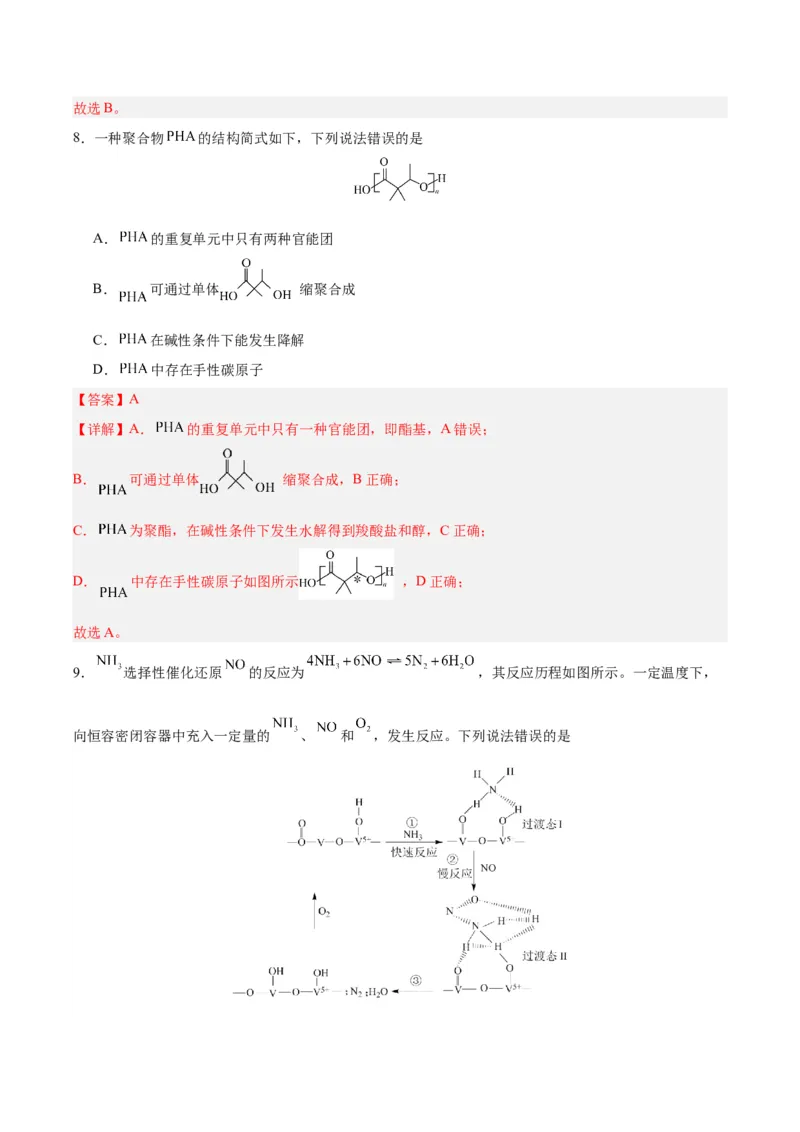
8.一种聚合物 的结构简式如下,下列说法错误的是
A. 的重复单元中只有两种官能团
B. 可通过单体 缩聚合成
C. 在碱性条件下能发生降解
D. 中存在手性碳原子
【答案】A
【详解】A. 的重复单元中只有一种官能团,即酯基,A错误;
B. 可通过单体 缩聚合成,B正确;
C. 为聚酯,在碱性条件下发生水解得到羧酸盐和醇,C正确;
D. 中存在手性碳原子如图所示 ,D正确;
故选A。
9. 选择性催化还原 的反应为 ,其反应历程如图所示。一定温度下,
向恒容密闭容器中充入一定量的 、 和 ,发生反应。下列说法错误的是A.使用催化剂, 、 的活化分子数增多,还原 的速率加快
B.①的反应速率快,说明反应①的活化能大,是整个反应的决速步
C. 与催化剂发生强的化学吸附,而 在此过程中几乎不被催化剂吸附
D.其他条件不变时,增大 的浓度,能使更多的 转化为
【答案】B
【详解】A.使用催化剂能降低反应的活化能,活化分子数增多,反应速率加快,A正确;
B.反应①的反应速率快,说明反应①的活化能小,反应的决速步是反应速率最慢的反应②,B错误;
C.由反应历程图可知,在反应过程中, 与催化剂发生强的化学吸附,而 与NH 结合, 几乎
3
不被催化剂吸附,C正确;
D.其他条件不变时,增大 的浓度,平衡正向移动,能使更多的 转化为 ,D正确;
故选B。
10.高氯酸铵( )受热或撞击可分解成 、 、 和 ,可用作火箭推进剂。一种以工业
(含少量的 和 )溶液制取高氯酸铵的流程如下,电解时使用惰性电极,电解后溶
液中有 生成。
关于制取高氯酸铵的反应,下列说法正确的是
A.沉铬时加入 有利于 转化为
B.电解时阴极电极方程式为:
C.加入饱和 溶液反应时可能有 生成D. 、 、 三种物质中, 溶解度最大
【答案】C
【分析】 ,氯酸钠溶液加入氢氧化钡,可以促使 转化为
,进而和钡离子生成硫酸钡沉淀;过滤滤液电解阳极上发生氧化反应五价氯转化为七价氯得到高氯
酸钠,阴极生成氢气和氢氧根离子,浓缩加入饱和氯化铵将高氯酸钠转化为溶解度较小的高氯酸铵晶体结
晶析出;
【详解】A.由分析可知,加入可以增加溶液的碱性,促使 转化为 ,A错误;
B.电解阳极上发生氧化反应五价氯转化为七价氯得到高氯酸钠,阴极生成氢气和氢氧根离子,阴极电极
方程式为: ,B错误;
C.电解生成氢氧化钠,加入饱和氯化铵溶液,铵根离子和氢氧根离子反应会生成氨气,C正确;
D.三种物质中, 首先结晶析出,故其溶解度最小,D错误;
故选C。
11.新型储氢材料是开发利用氢能的重要研究方向。某种新型储氢材料的晶胞如图,八面体中心为金属离
子铁,顶点均为 配体;四面体中心为硼原子,顶点均为氢原子。下列说法错误的是
A.材料中硼原子采用sp3杂化方式
B.化学式为
C.金属离子的价电子排布式为
D.该化合物中存在离子键、极性键和配位键
【答案】B【详解】A.从图中可知,B原子的价层电子对数为4+0=4,杂化方式为sp3杂化,A正确;
B.八面体中心为亚铁离子,顶点为NH 配体,则一个八面体表示为Fe(NH ),根据均摊法,黑球位于顶
3 3 6
点和面心,则黑球个数为 =4,白球位于晶胞内,其个数为8,白球表示为BH,则该物质的化
4
学式为 ,B错误;
C.Fe的电子排布式为[Ar]3d64s2,+2价的铁价电子排布式为3d6,C正确;
D.该化合物中Fe(NH ) 与BH 之间形成离子键,NH 内部存在极性键,亚铁离子和NH 形成配位键,D
3 6 4 3 3
正确;
故答案选B。
12.科研人员发现利用低温固体质子导体作电解质,催化合成NH ,与传统的热催化合成氨相比,催化效
3
率较高。其合成原理如图甲所示,电源电压改变与生成NH 速率的关系如图乙所示。下列说法正确的是
3
A.Pt-C是该合成氨装置的阴极
B.Pt-C N 电极上发生的反应为
3 4
C.当电压高于1.2V时,混合气体中N 和NH 的体积分数之和小于100%
2 3
D.若H 的进出口流量差为22.4 L/min,则固体质子导体中H+的流速为2 mol/min
2
【答案】C
【详解】A.Pt-C极发生氧化反应,H-2e-=2H+,故为阳极,A错误;
2
B.Pt-C N 为阴极,发生还原反应,N+6H++6e-=2NH,B错误;
3 4 2 3
C.当电压高于1.2V时,氨气反应速率变慢,原因是H+ +2e-= H ,混合气体中有N、NH 和H,混合
2 2 3 2
气体中N 和NH 的体积分数之和小于100%,故C正确;
2 3
D.若H 的进出口流量差为22.4 L/min,未知是否为标况,氢气的物质的量不一定为1mol,故质子导体中
2
H+的流速不一定为2 mol/min,D错误;
故答案为:C。13.在某催化剂作用下,乙炔选择性加成反应C H(g)+ H (g) C H(g) ΔH <0速率方程为v =k
2 2 2 2 4 正 正
c(C H)·c(H),v =k c(C H)(k 、k 为速率常数,只与温度、催化剂有关)。一定温度下,在2 L恒容密
2 2 2 逆 逆 2 4 正 逆
闭容器中充入1 mol C H(g)和1 mol H (g),只发生上述反应。测得C H 的物质的量如表所示。
2 2 2 2 4
t/ min 0 5 10 15 20
n/ mol 0 0.3 0.5 0.6 0.6
下列叙述正确的是
A.0~10 min内,v(H )=0.05 mol·L-1·min- 1
2
B.升高温度,k 增大的倍数大于k 增大的倍数
正 逆
C.净反应速率(v -v )由大到小最终等于0
正 逆
D.在上述条件下,15min时2k =15k
逆 正
【答案】C
【详解】A.0~10 min内v(H )=0.025 mol·L-1·min-1,选项A错误;
2
B.根据平衡状态的特点,平衡时正、逆反应速率相等,则K= 。上述反应的正反应是放热反应,升高
温度,平衡常数减小,而升高温度,速率常数增大,由此推知,k 增大的倍数 小于k 增大的倍数,选项
正 逆
B错误;
C.根据表格数据可知,开始正反应速率最大,逆反应速率为0,随着反应进行,净反应速率由大到小,最
终等于0(平衡),选项C正确;
D.15 min时达到平衡,c(C H)=0.2 mol/L ,c(H)=0.2 mol/L ,c(C H)=0.3 mol/ L,故K= =7.5,15k
2 2 2 2 4 逆
=2k ,选项D错误;
正
答案选C。
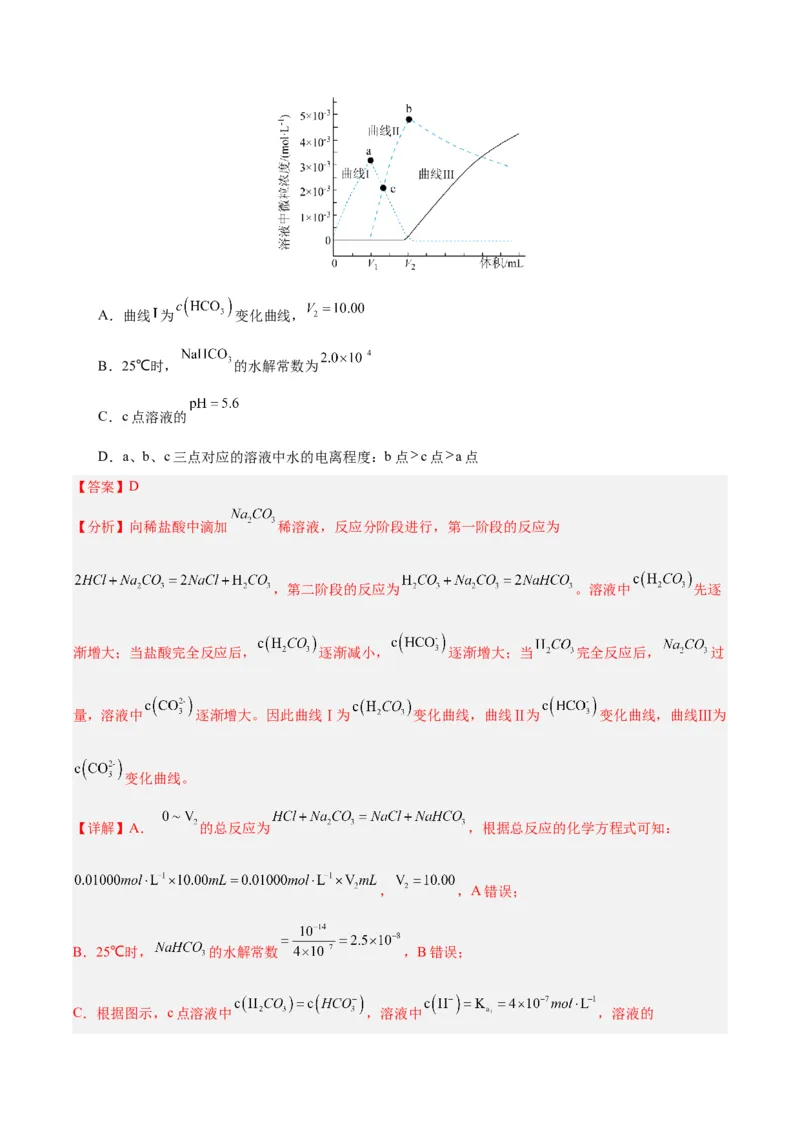
14.25℃时,用 溶液滴定 溶液,溶液中 、
、 随滴加 溶液体积的变化关系如图所示(忽略滴定过程中 的逸出)。已知:
25℃时, 的 , , 。下列说法正确的是A.曲线 为 变化曲线,
B.25℃时, 的水解常数为
C.c点溶液的
D.a、b、c三点对应的溶液中水的电离程度:b点 c点 a点
【答案】D
【分析】向稀盐酸中滴加 稀溶液,反应分阶段进行,第一阶段的反应为
,第二阶段的反应为 。溶液中 先逐
渐增大;当盐酸完全反应后, 逐渐减小, 逐渐增大;当 完全反应后, 过
量,溶液中 逐渐增大。因此曲线Ⅰ为 变化曲线,曲线Ⅱ为 变化曲线,曲线Ⅲ为
变化曲线。
【详解】A. 的总反应为 ,根据总反应的化学方程式可知:
, ,A错误;
B.25℃时, 的水解常数 ,B错误;
C.根据图示,c点溶液中 ,溶液中 ,溶液的,C错误;
D.a点溶液中的溶质为 和 ,b点溶液中的溶质为 和 ,c点溶液中的溶质为
、 和 , 使水的电离程度减小, 水解使水的电离程度增大,故a、b、c
三点对应的溶液中水的电离程度:b点>c点>a点,D正确。
故选D。
二、非选择题:本题共4小题,共58分。
15.(15分)二氯异氰尿酸钠 是一种常用高效含氯杀菌消毒剂,常温下为白色固体,难
溶于冷水。实验室利用高浓度的 溶液和氰尿酸 固体在 10℃时反应制备
,反应原理为 ,实验装置如
图所示(夹持装置略)。已知:40℃时, 。
回答下列问题:
(1)二氯异氰尿酸钠中,氯元素的化合价为______,其水解产物中的氧化性物质可消毒杀菌,该氧化性
物质的电子式为______
(2)装置A中发生反应的化学方程式为__________________。
(3)将装置B换为装置E,装置E的作用除吸收 外,还可以______.
(4)实验中应控制冷水浴的温度在5℃左右,温度不能太高,其原因是______。
(5)待装置C中液面上方出现黄绿色气体时,再由三颈烧瓶的上口加入氰尿酸固体,发生反应制得二氯
异氰尿酸钠。该反应过程中仍需不断通入 ,目的是______。
(6)“有效氯”含量指从 中氧化出相同量的 所需 的质量与指定化合物的质量之比,常以百分数
表示。为测定二氯异氰尿酸钠的“有效氯”含量,现称取某二氯异氰尿酸钠样品 ,依次加人水、足量 固体和少量稀硫酸,配制成 待测液;准确量取 待测液于锥形瓶中,用
标准溶液滴定至溶液呈微黄色时,加入指示剂,继续滴定至终点
,消耗 标准溶液 。
①滴定至溶液呈微黄色时,加入的指示剂是______。
②到达滴定终点时,观察到的现象是__________________。
③样品的“有效氯”含量为______。
【答案】(1)+1(1分) (2分)
(2) (2分)
(3)防堵塞(或防倒吸或暂时储存多余的氯气)(1分)
(4)温度太高,氯气与 反应会生成 (2分)
(5)将反应生成的氢氧化钠再次生成次氯酸钠,提高原料的利用率(2分)
(6)淀粉溶液(1分) 滴入最后半滴 标准溶液时,溶液颜色从蓝色刚好变为无色,且半分钟内
不变色(2分) 50%(或50.0%)(2分)
【分析】由于浓盐酸易挥发,制取的氯气中含有杂质 气体,可用饱和食盐水除去,装置C内氯气和
溶液反应生成 ,装置D为尾气处理。
【解析】(1) 中 的化合价为 。二氯异氰尿酸钠水解产物中的 具有氧化性,可消
毒杀菌, 的电子式为 ;
故答案为:+1; ;
(2)装置A中制备 的化学方程式为 ;
故答案为: ;
(3)装置B换为装置E后,装置E的作用除吸收 外,还可以防堵塞(或防倒吸或暂时储存多余的氯气)。
故答案为:防堵塞(或防倒吸或暂时储存多余的氯气);
(4)根据信息,温度太高,氯气与 反应会生成 ,得不到 ,而使实验失败。故答案为:温度太高,氯气与NaOH反应会生成 NaClO;
3
(5)反应过程中仍需不断通入 ,目的是将反应生成的氢氧化钠再次生成次氯酸钠,提高原料的利用率;
故答案为:将反应生成的氢氧化钠再次生成次氯酸钠,提高原料的利用率;
(6)① 标准溶液滴定至溶液呈微黄色时,溶液中还剩余少量的 ,加入指示剂淀粉溶液,溶液变
蓝色,继续滴定至终点。
②到达滴定终点时,观察到的现象是滴入最后半滴 标准溶液时,溶液颜色从蓝色刚好变为无色,
且半分钟内不变色。
③根据关系式 ,可计算出
,
,样品的“有效氯”含量为 。
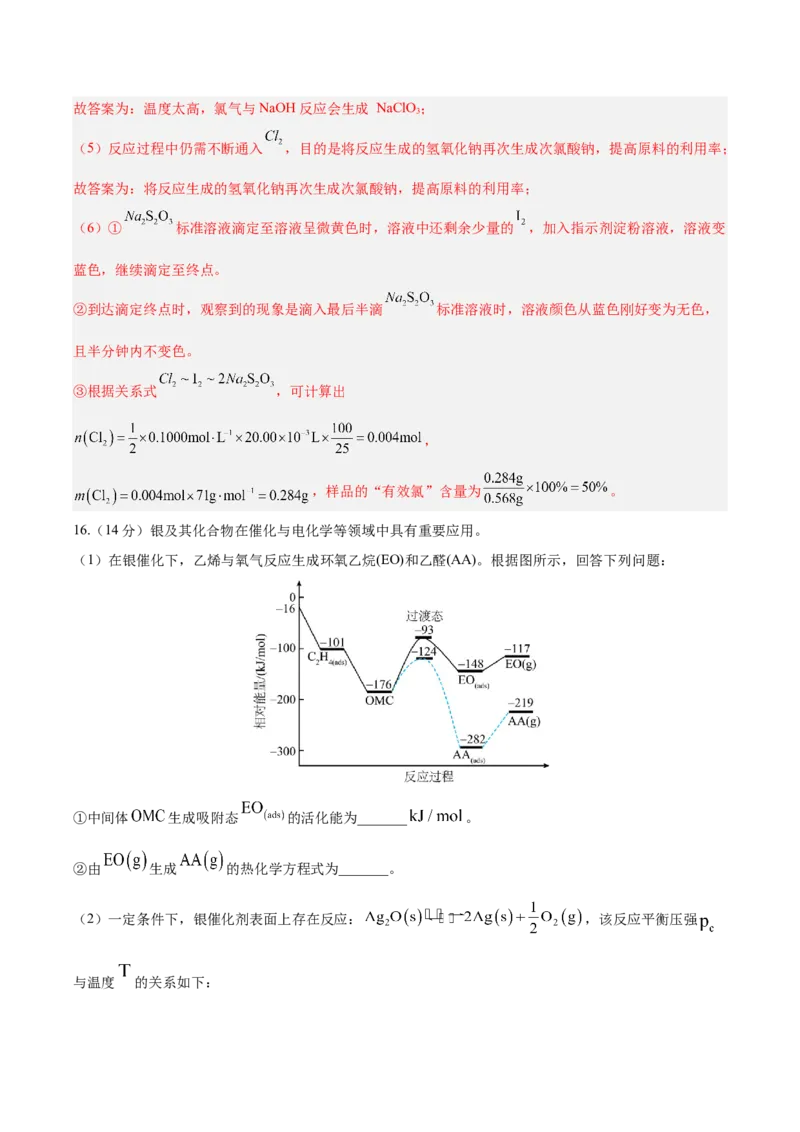
16.(14分)银及其化合物在催化与电化学等领域中具有重要应用。
(1)在银催化下,乙烯与氧气反应生成环氧乙烷(EO)和乙醛(AA)。根据图所示,回答下列问题:
①中间体 生成吸附态 的活化能为_______ 。
②由 生成 的热化学方程式为_______。
(2)一定条件下,银催化剂表面上存在反应: ,该反应平衡压强
与温度 的关系如下:401 443 463
10 51 100
① 时的平衡常数 _______ 。
②起始状态Ⅰ中有 和 ,经下列过程达到各平衡状态:
已知状态Ⅰ和Ⅲ的固体质量相等,下列叙述正确的是_______(填字母)。
A.从Ⅰ到Ⅱ的过程
B.
C.平衡常数:
D.若体积 ,则
E.逆反应的速率:
③某温度下,向恒容容器中加入 ,分解过程中反应速率 与压强 的关系为
,k为速率常数(定温下为常数)。当固体质量减少 时,逆反应速率最大。若转化率
为 ,则 _______(用 表示)。
(3) 可用作固体离子导体,能通过加热 制得。上述两种晶体的晶胞示意图如图所示(为了
简化,只画出了碘离子在晶胞中的位置)。①测定晶体结构最常用的仪器是_______ (填字母)。
A.质谱仪 B.红外光谱仪 C.核磁共振仪 D. 射线衍射仪
② 与 晶胞的体积之比为_______。
③测定 中导电离子类型的实验装置如图所示。实验测得支管a中 质量不变,可判定导电离子
是 而不是 ,依据是_______。
【答案】(1)①83(1分) ②EO(g) = AA(g)ΔH=-102kJ/mol(2分)
(2)①10(2分) ②CDE(2分) ③ (2分)
(3)①D(1分) ②12:7 (2分) ③a中银电极质量减小,b中银电极质量增大(2分)
【解析】(1)①过渡态物质的总能量与反应物总能量的差值为活化能,中间体OMC生成吸附态 的
活化能为(-93kJ/mol)-(-176kJ/mol)=83 kJ/mol;
②由图可知,EO(g)生成AA(g)放出热量(-117 kJ/mol)-(-219 kJ/mol)=102 kJ/mol,放热焓变为负值,故热化
学方程式为EO(g) AA(g) ;
(2)①反应中只有氧气为气体,结合表格数据可知,463K时的平衡常数 ;
②结合表格数据可知,升高温度,压强变大,平衡正向移动,则反应为吸热反应;
A.从Ⅱ到Ⅲ为体积增大,反应正向移动的过程,导致固体质量减小,已知状态Ⅰ和Ⅲ的固体质量相等,则从Ⅰ到Ⅱ的过程为固体质量增大的过程,平衡逆向移动,为熵减过程,故从Ⅰ到Ⅱ的过程, ,A
错误;
B.平衡常数 只受温度的影响,则 ,B错误;
C.反应为吸热反应,降低温度,平衡逆向移动,平衡常数减小,故平衡常数: K(II)>K(IV),C正确;
D.已知状态Ⅰ和Ⅲ的固体质量相等,则氧气的物质的量相等,若体积 ,根据阿
伏伽德罗定律可知 , = ,K(Ⅲ)= ,则 ,
D正确;
E.结合A分析可知,逆反应的速率: ;固体不影响反应速率,温度越低反应速率越低,逆反
应的速率: ,故有逆反应的速率: , E正确;
故选CDE;
③某温度下,设向恒容容器中加入mg ,当固体质量减少4%时,逆反应速率最大,此时达到平衡状
态,减小质量为生成氧气的质量,则生成 ,若转化率为14.5%,则此时生成
,根据阿伏伽德罗定律,此时 ,则 ;
(3)①晶体与非晶体的最可靠的科学方法是X射线衍射法;故测定晶体结构最常用的仪器是D.X射线
衍射仪;
②据“均摊法”, 晶胞中含 个I,则晶体密度为 ,则则 与 晶胞的体积之比为12:7;
③由图可知,a为阳极、b为阴极,实验测得支管a中质量不变,则碘离子没有迁移到a中与银离子产生
AgI沉淀,银离子在阴极得到电子发生还原反应生成银单质,导致b中银电极质量增大,a中银电极银单质
失去电子发生氧化反应生成银离子,导致a中银电极质量质量减小,可判定导电离子是 而不是 。
17.(14分)金属铼(Re)是重要的新兴金属,应用于国防、石油化工以及电子制造等领域,通过还原高铼酸
铵(NH ReO)可制取金属铼。以钼精矿(主要成分为钼的硫化物和少量铼的硫化物)制取高铼酸铵的流程如下
4 4
图所示。回答下列问题:
(1)“焙烧”过程加入生石灰的目的___________。
(2)“焙烧”常采用高压空气、逆流操作(空气从培烧炉下部通入,矿粉从中上部加入),这样操作的目的是
___________,请再举出一项提高“焙烧”效率的合理措施:___________。
(3)“浸出”中,浸出率与温度的关系如下左图所示,浸出率与硫酸浓度的关系如下右图所示。工业生产应
选择的适宜条件是___________。(4)“萃取”机理为: ,则“反萃取”对应的离子方程式为___________。
(5)硫酸铼(IV)铵[(NH )Re (SO )·mHO]是制备高纯铼的基础产品,为测定其组成进行如下实验:
4 a b 4 c 2
①称取3.300g样品配成100mL溶液M。
②取10.00mL溶液M,用0.05mol/L的BaCl 标准溶液滴定,恰好完全沉淀,进行三次平行实验,平均消耗
2
40.00 mL BaCl 标准溶液。
2
③另取10.00mL溶液M,加足量浓NaOH溶液并加热,生成标准状况下气体44.80mL。
通过计算可知铼的物质的量为___________,确定硫酸铼铵的化学式为___________。
【答案】(1)吸收二氧化硫,避免污染环境(2分)
(2)①增大接触面积,提高反应速率,使焙烧充分,提高原料的利用率(2分) ②适当升温或将矿石粉
碎(2分)
(3)95℃和c(HSO )=3.0mol/L(2分)
2 4
(4) 或 (2分)
(5)①0.005mol(2分) ②(NH )Re(SO)·H O(2分)
4 4 4 4 2
【分析】钼精矿在空气中焙烧硫元素转化成二氧化硫,二氧化硫与生石灰、氧气反应生成硫酸钙,铼元素
转化成Ca(ReO ),钼元素转化成CaMoO,加入硫酸、软锰矿,硫酸钙属于微溶物,过滤,得到浸渣
4 2 4
CaSO,加入氨水和生石灰,得到NH ReO,然后过滤,通过萃取和反萃取、蒸发浓缩、冷却结晶、过滤、
4 4 4
洗涤、干燥得到产品,据此分析;
【解析】(1)由上述分析可知二氧化硫与生石灰、氧气反应生成硫酸钙,可避免二氧化硫污染环境;
(2)“焙烧”常采用高压空气、逆流操作可增大接触面积,提高反应速率,使焙烧充分,提高原料的利
用率;适当升高温度,加快反应速率,也可提高“焙烧”效率;
(3)由图可知95℃和c(HSO )=3.0mol/L时,浸出较高,因此选择的条件为:95℃和c(HSO )=3.0mol/L;
2 4 2 4
(4)反萃取时 与氨气反应生成 ,反应离子方程式为:
或 ;
(5)由②可知,10.00mL溶液M中含SO 的物质的量为0.05mol/L×0.04L=0.002mol;由③可知10.00mL
溶液M中含铵根离子的物质的量等于生成氨气的物质的量,为 ,可知SO 和铵根
离子的物质的量相等,结合化合物中各元素的代数和为0可得该物质中a=c=4,b=1,除水外的组成为:(NH )Re(SO),该物质的物质的量为0.0005mol;摩尔质量为 ,则化学式为:
4 4 4 4
(NH )Re(SO)·H O,含铼的物质的量为0.0005mol。
4 4 4 4 2
18.(15分)苯甲醛是一种重要的化工原料,可发生如下转化。
已知: (R、 代表烃基)
回答下列问题:
(1)B所含官能团的名称为 。
(2)苯甲醛→A的反应类型是 。
(3)D、G的结构简式分别为 、 。
(4)苯甲醛与新制 反应的化学方程式为
。
(5)F→M的化学方程式为 。
(6)B有多种同分异构体,属于甲酸酯且含酚羟基的同分异构体共有 。种,写出一种其中含亚
甲基( )的同分异构体的结构简式: 。
(7)写出用苯甲醛为原料(其他无机试剂任选)制备 的合成路线:
。
【答案】(1)(1)羟基、羧基(2分) (2)加成反应(1分)
(3) (2分)
(4) (2分)(5) (2分)
(6)13(2分) (2分)
(7) (2分)
【解析】(1)B所含官能团的名称为羧基、羟基;
(2)苯甲醛 C HCHO.→A的反应类型是加成反应;
6 5
(3)B和芳香醇C发生酯化反应生成酯D,由D的分子式可知,芳香醇C为C HCHOH,则D的结
6 5 2
构简式为 ;F和甲醛发生缩聚反应生成高分子树脂M,由 M的结构简式可知F
为对甲基苯酚,由已知条件可知,C HCOCl 和F生成G的结构简式为
6 5
(4)苯甲醛与新制Cu(OH),反应的化学方程式为:
(5) F → M的化学方程式为:
(6)B有多种同分异构体,属于甲酸酯且含酚羟基的同分异构体若苯环上有3个支链,3个支链分别为酚
羟基、甲基、甲酸酯基(-OOCH)时,有10种,若苯环上有2个支链,2个支链分别为酚羟基、-CH20OCH
时,有3种,共有13种,其中含亚甲基的一种同分异构体的结构简式为:
(7) 用苯甲醛为原料制备合成路线为: