文档内容
课堂检测·素养达标
1.碱金属是典型的活泼金属,其根本原因是 ( )
A.碱金属单质的密度小,熔点和沸点低
B.碱金属在常温下易被氧化
C.碱金属原子最外电子层上都只有1个电子,容易失去
D.碱金属原子的核电荷数比较小
2.(2019·聊城高一检测)锂(Li)是一种银白色的金属元素,质软,是密度最小的
金属。用于原子反应堆、制轻合金及电池等,锂电池或锂离子电池备受人们推
崇。
锂(Li)不可能具有的性质是 ( )
A.锂在空气中燃烧只会生成氧化锂
B.锂很软,用小刀可以切割
C.锂的熔点比金属铯高
D.金属锂可以保存在煤油或液体石蜡中3.(2019·德州高一检测)下列关于卤素(从F→I)的说法正确的是 ( )
A.单质的颜色逐渐加深
B.气态氢化物的稳定性逐渐增强
C.从F到I,原子核对最外层电子的吸引能力依次减弱,原子的得电子能力依次
增强
D.卤素单质与水反应,均发生自身氧化还原反应
4.(教材改编)F、Cl和Br都是第ⅦA族元素,关于这三种元素原子的说法正确
的是 ( )
A.原子半径:F>Cl>Br
B.最外层电子数都相同
C.核外电子层数都相同
D.最外层电子数都不相同
【补偿训练】
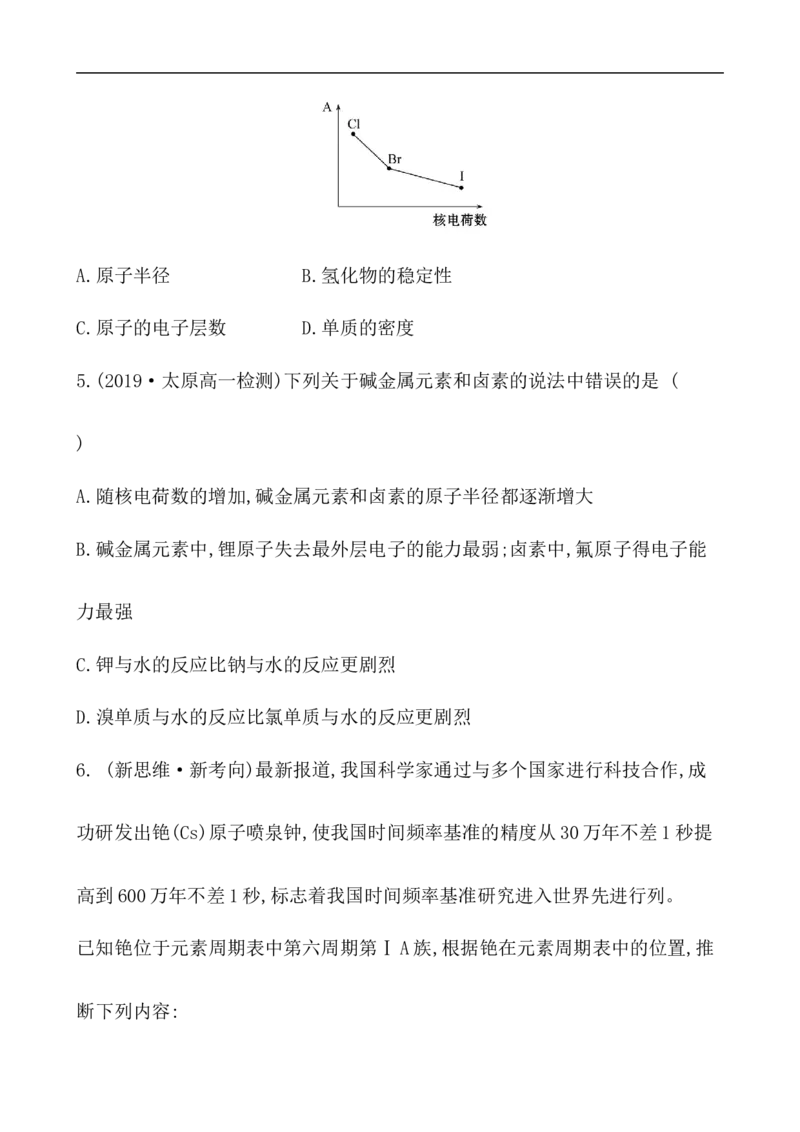
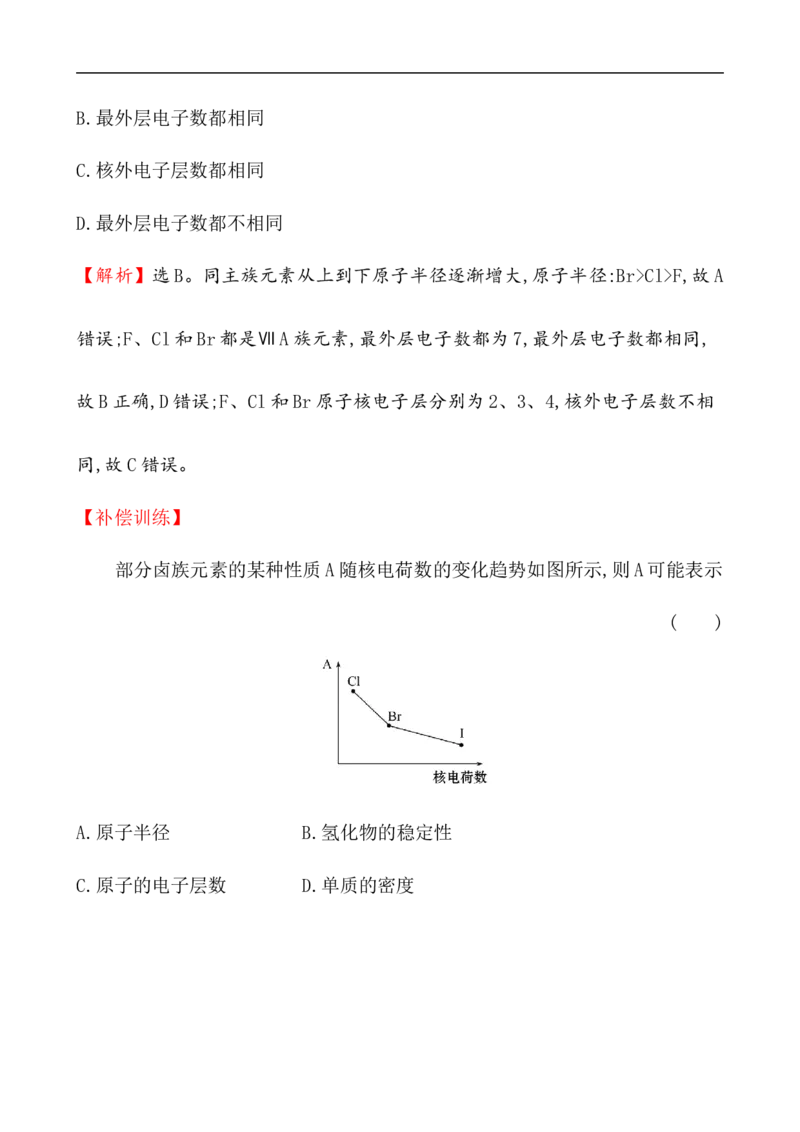
部分卤族元素的某种性质A随核电荷数的变化趋势如图所示,则A可能表示
( )A.原子半径 B.氢化物的稳定性
C.原子的电子层数 D.单质的密度
5.(2019·太原高一检测)下列关于碱金属元素和卤素的说法中错误的是 (
)
A.随核电荷数的增加,碱金属元素和卤素的原子半径都逐渐增大
B.碱金属元素中,锂原子失去最外层电子的能力最弱;卤素中,氟原子得电子能
力最强
C.钾与水的反应比钠与水的反应更剧烈
D.溴单质与水的反应比氯单质与水的反应更剧烈
6. (新思维·新考向)最新报道,我国科学家通过与多个国家进行科技合作,成
功研发出铯(Cs)原子喷泉钟,使我国时间频率基准的精度从30万年不差1秒提
高到600万年不差1秒,标志着我国时间频率基准研究进入世界先进行列。
已知铯位于元素周期表中第六周期第ⅠA族,根据铯在元素周期表中的位置,推
断下列内容:(1)铯的原子核外共有________层电子,最外层电子数为________,铯的原子序
数为________。
(2)铯单质与水剧烈反应,放出________色气体,同时使紫色石蕊试液显
________色,因为__________________________________(写出化学方程式)。
(3)预测铯单质的还原性比钠单质的还原性________(填“弱”或“强”)。课堂检测·素养达标
1.碱金属是典型的活泼金属,其根本原因是 ( )
A.碱金属单质的密度小,熔点和沸点低
B.碱金属在常温下易被氧化
C.碱金属原子最外电子层上都只有1个电子,容易失去
D.碱金属原子的核电荷数比较小
【解析】选C。结构决定性质,碱金属原子最外电子层上都只有1个电子,容易
失去,故碱金属是典型的活泼金属。
2.(2019·聊城高一检测)锂(Li)是一种银白色的金属元素,质软,是密度最小的
金属。用于原子反应堆、制轻合金及电池等,锂电池或锂离子电池备受人们推
崇。
锂(Li)不可能具有的性质是 ( )
A.锂在空气中燃烧只会生成氧化锂
B.锂很软,用小刀可以切割C.锂的熔点比金属铯高
D.金属锂可以保存在煤油或液体石蜡中
【解析】选D。锂较其他碱金属活泼性差,燃烧不生成过氧化物,生成氧化锂,A
正确;碱金属都很软,可用小刀切割,B正确;碱金属Li→Cs熔点逐渐降低,C正确;
金属锂的密度比煤油小,所以不能保存在煤油中,D不正确。
3.(2019·德州高一检测)下列关于卤素(从F→I)的说法正确的是 ( )
A.单质的颜色逐渐加深
B.气态氢化物的稳定性逐渐增强
C.从F到I,原子核对最外层电子的吸引能力依次减弱,原子的得电子能力依次
增强
D.卤素单质与水反应,均发生自身氧化还原反应
【解析】选A。从F→I,单质的颜色逐渐加深,A正确;气态氢化物的稳定性逐渐
减弱,B错误;从F到I,原子半径增大,原子核对最外层电子的吸引能力依次减弱,
原子的得电子能力依次减弱,C错误;F 与水反应,F 只作氧化剂,D错误。
2 2
4.(教材改编)F、Cl和Br都是第ⅦA族元素,关于这三种元素原子的说法正确
的是 ( )
A.原子半径:F>Cl>BrB.最外层电子数都相同
C.核外电子层数都相同
D.最外层电子数都不相同
【解析】选B。同主族元素从上到下原子半径逐渐增大,原子半径:Br>Cl>F,故A
错误;F、Cl和Br都是ⅦA族元素,最外层电子数都为7,最外层电子数都相同,
故B正确,D错误;F、Cl和Br原子核电子层分别为2、3、4,核外电子层数不相
同,故C错误。
【补偿训练】
部分卤族元素的某种性质A随核电荷数的变化趋势如图所示,则A可能表示
( )
A.原子半径 B.氢化物的稳定性
C.原子的电子层数 D.单质的密度【解析】选B。A项,从氯到碘,原子半径逐渐增大,A项不符合题意;B项,从HCl
到HI,稳定性逐渐减弱,B项符合题意;C项,从Cl到I,原子的电子层数逐渐增多,
C项不符合题意;D项,从Cl 到I ,单质的密度逐渐增大,D项不符合题意。
2 2
5.(2019·太原高一检测)下列关于碱金属元素和卤素的说法中错误的是 (
)
A.随核电荷数的增加,碱金属元素和卤素的原子半径都逐渐增大
B.碱金属元素中,锂原子失去最外层电子的能力最弱;卤素中,氟原子得电子能
力最强
C.钾与水的反应比钠与水的反应更剧烈
D.溴单质与水的反应比氯单质与水的反应更剧烈
【解析】选D。同主族元素原子的半径随核电荷数的增加而增大,A正确;同主族
元素随核电荷数的增加,金属性增强,非金属性减弱,故碱金属元素中,锂原子失
去最外层电子的能力最弱;卤素中,氟原子得电子能力最强,B正确;钾的金属性
比钠强,钾与水的反应比钠与水的反应更剧烈,C正确;氯气化学性质比溴强,氯
单质与水的反应比溴单质与水的反应剧烈,D错误。6. (新思维·新考向)最新报道,我国科学家通过与多个国家进行科技合作,成
功研发出铯(Cs)原子喷泉钟,使我国时间频率基准的精度从30万年不差1秒提
高到600万年不差1秒,标志着我国时间频率基准研究进入世界先进行列。
已知铯位于元素周期表中第六周期第ⅠA族,根据铯在元素周期表中的位置,推
断下列内容:
(1)铯的原子核外共有________层电子,最外层电子数为________,铯的原子序
数为________。
(2)铯单质与水剧烈反应,放出________色气体,同时使紫色石蕊试液显
________色,因为__________________________________(写出化学方程式)。
(3)预测铯单质的还原性比钠单质的还原性________(填“弱”或“强”)。
【解析】根据原子核外电子排布规律,结合铯在元素周期表中的位置知:铯原子
核外电子分六层排布,分别是2、8、18、18、8、1,原子序数是55,最外层只有1个电子。铯与钠同主族,具有极强的金属性。与水反应生成氢气和氢氧化
铯:2Cs+2H O 2CsOH+H ↑,氢氧化铯是强碱,使紫色石蕊试液变蓝色。
2 2
答案:(1)6 1 55 (2)无 蓝
2Cs+2H O 2CsOH+H ↑ (3)强
2 2