文档内容
2023 年 1 月浙江省普通高校招生选考化学试题
化学试题
可能用到的相对原子质量:H1 Li7 C12 N14 O16 Na23 Mg24 Al27 Si28 S32
C135.5 K39 Ca40 Fe56 Cu64 Br80 Ag108 I127 Ba137
一、选择题(本大题共16小题,每小题3分,共48分。每小题列出的四个备选项中只有一个
是符合题目要求的,不选、多选、错选均不得分)
1. 下列物质中属于耐高温酸性氧化物的是
.
A B. C. D.
2. 硫酸铜应用广泛,下列说法不正确的是
A. 元素位于周期表p区 B. 硫酸铜属于强电解质
C. 硫酸铜溶液呈酸性 D. 硫酸铜能使蛋白质变性
3. 下列化学用语表示正确的是
A. 中子数为18的氯原子:
B. 碳的基态原子轨道表示式:
C. 的空间结构: (平面三角形)
D. 的形成过程:
4. 物质的性质决定用途,下列两者对应关系不正确的是
A. 能使某些色素褪色,可用作漂白剂 B. 金属钠导热性好,可用作传热介质
C. 溶液呈碱性,可用作消毒剂 D. 呈红色,可用作颜料
5. 下列关于元素及其化合物的性质说法不正确的是
A. 和乙醇反应可生成 B. 工业上煅烧黄铁矿 生产
第1页 | 共12页C. 工业上用氨的催化氧化制备 D. 常温下铁与浓硝酸反应可制备
6. 关于反应 ,下列说法正确的是
A. 生成 ,转移 电子 B. 是还原产物
C. 既是氧化剂又是还原剂 D. 若设计成原电池, 为负极产物
7. 下列反应的离子方程式不正确的是
A. 通入氢氧化钠溶液:
B. 氧化铝溶于氢氧化钠溶液:
C. 过量 通入饱和碳酸钠溶液:
.
D 溶液中滴入氯化钙溶液:
8. 下列说法不正确的是
A. 从分子结构上看糖类都是多羟基醛及其缩合产物
B. 蛋白质溶液与浓硝酸作用产生白色沉淀,加热后沉淀变黄色
C. 水果中因含有低级酯类物质而具有特殊香味
D. 聚乙烯、聚氯乙烯是热塑性塑料
9. 七叶亭是一种植物抗菌素,适用于细菌性痢疾,其结构如图,下列说法正确的是
A. 分子中存在2种官能团
B. 分子中所有碳原子共平面
C. 该物质与足量溴水反应,最多可消耗
D. 该物质与足量 溶液反应,最多可消耗
10. X、Y、Z、M、Q五种短周期元素,原子序数依次增大。X的 轨道全充满,Y的s能级电子数量是p
能级的两倍,M是地壳中含量最多的元素,Q是纯碱中的一种元素。下列说法不正确的是
A. 电负性:
第2页 | 共12页B. 最高正价:
C. Q与M的化合物中可能含有非极性共价键
D. 最高价氧化物对应水化物的酸性:
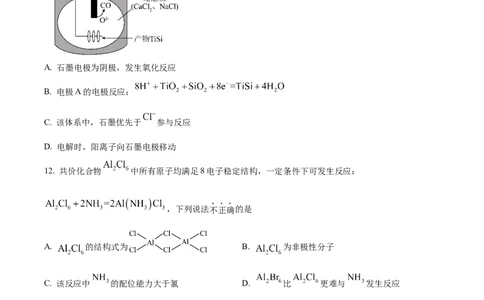
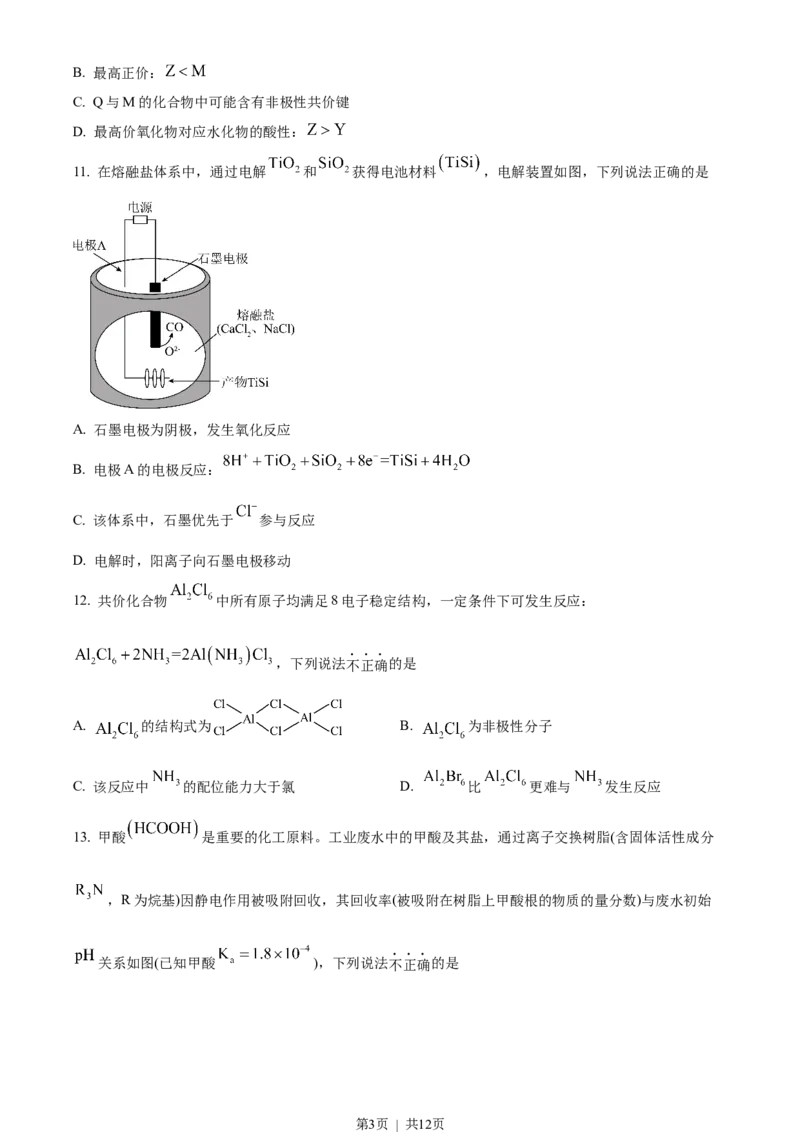
11. 在熔融盐体系中,通过电解 和 获得电池材料 ,电解装置如图,下列说法正确的是
A. 石墨电极为阴极,发生氧化反应
B. 电极A的电极反应:
C. 该体系中,石墨优先于 参与反应
D. 电解时,阳离子向石墨电极移动
12. 共价化合物 中所有原子均满足8电子稳定结构,一定条件下可发生反应:
,下列说法不正确的是
A. 的结构式为 B. 为非极性分子
C. 该反应中 的配位能力大于氯 D. 比 更难与 发生反应
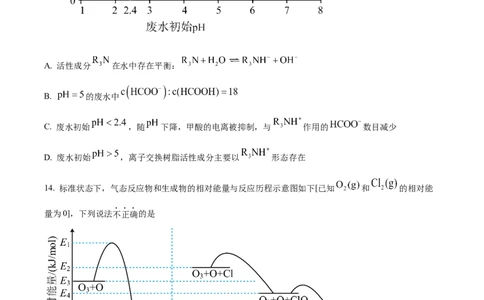
13. 甲酸 是重要的化工原料。工业废水中的甲酸及其盐,通过离子交换树脂(含固体活性成分
,R为烷基)因静电作用被吸附回收,其回收率(被吸附在树脂上甲酸根的物质的量分数)与废水初始
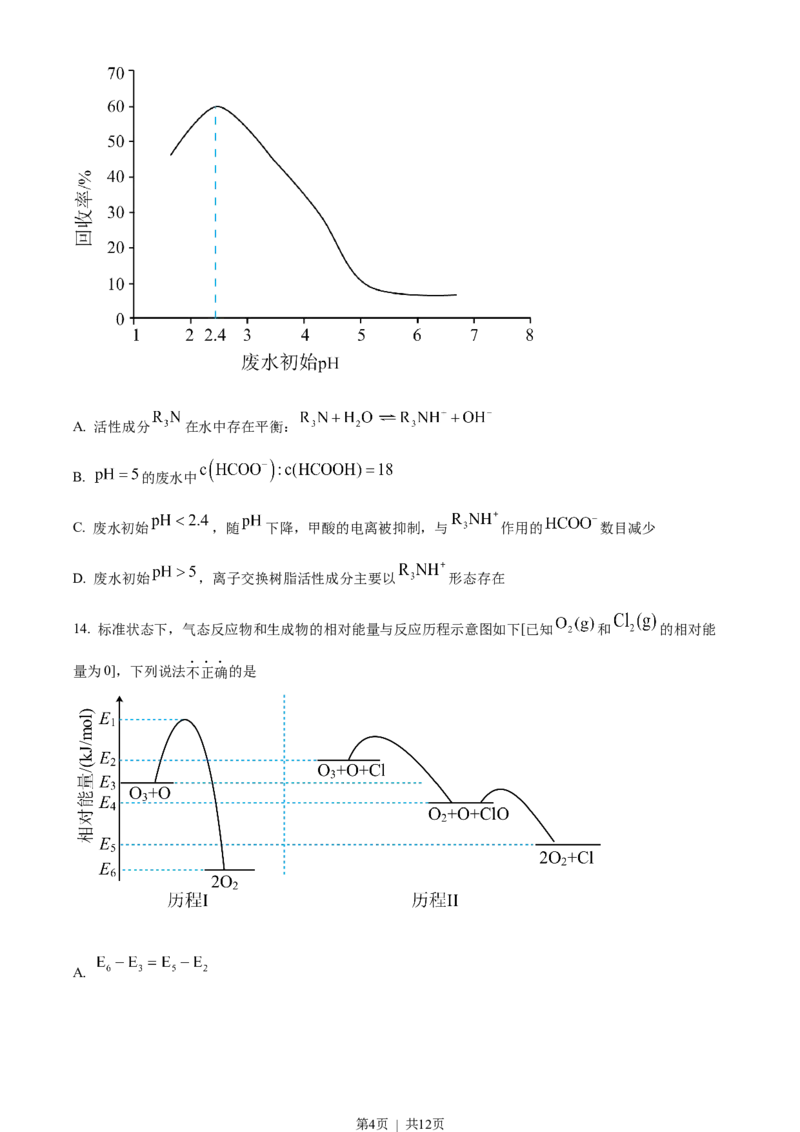
关系如图(已知甲酸 ),下列说法不正确的是
第3页 | 共12页A. 活性成分 在水中存在平衡:
B. 的废水中
C. 废水初始 ,随 下降,甲酸的电离被抑制,与 作用的 数目减少
D. 废水初始 ,离子交换树脂活性成分主要以 形态存在
14. 标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下[已知 和 的相对能
量为0],下列说法不正确的是
A.
第4页 | 共12页B. 可计算 键能为
C. 相同条件下, 的平衡转化率:历程Ⅱ>历程Ⅰ
D. 历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:
15. 碳酸钙是常见难溶物,将过量碳酸钙粉末置于水中达到溶解平衡:
[已知 , ,
的电离常数 ],下列有关说法正确的是
A. 上层清液中存 在
B. 上层清液中含碳微粒最主要以 形式存在
C. 向体系中通入 气体,溶液中 保持不变
D. 通过加 溶液可实现 向 的有效转化
16. 探究铁及其化合物的性质,下列方案设计、现象和结论都正确的是
实验方案 现象 结论
短时间内无明显现
A 往 溶液中加入 片 的氧化能力比 弱
象
往 溶液中滴加 溶液,
溶液先变成血红色
B 与 的反应不可逆
后无明显变化
再加入少量 固体
将食品脱氧剂样品中的还原铁粉溶于盐
C 溶液呈浅绿色 食品脱氧剂样品中没有 价铁
酸,滴加 溶液
先水解得 再聚集
向沸水中逐滴加5~6滴饱和 溶液, 溶液先变成红褐色
D
再析出沉淀
持续煮沸 成 沉淀
A. A B. B C. C D. D
二、非选择题(本大题共5小题,共52分)
17. 硅材料在生活中占有重要地位。请回答:
第5页 | 共12页(1) 分子的空间结构(以 为中心)名称为________,分子中氮原子的杂化轨道类型是_______。
受热分解生成 和 ,其受热不稳定的原因是________。
(2)由硅原子核形成的三种微粒,电子排布式分别为:① 、② 、③
,有关这些微粒的叙述,正确的是___________。
A. 微粒半径:③>①>②
B. 电子排布属于基态原子(或离子)的是:①②
C. 电离一个电子所需最低能量:①>②>③
D. 得电子能力:①>②
(3)Si与P形成的某化合物晶体的晶胞如图。该晶体类型是___________,该化合物的化学式为
___________。
18. 化合物X由三种元素组成,某学习小组按如下流程进行实验:
已知:白色固体A用 溶解后,多余的酸用 恰好中和,请回答:
(1)X的组成元素是___________,X的化学式是___________。
(2)写出 溶液呈棕黄色所发生的化学反应方程式___________。
(3)写出生成白色固体H的离子方程式___________。
(4)设计实验检验溶液Ⅰ中的阳离子___________。
19. “碳达峰·碳中和”是我国社会发展重大战略之一, 还原 是实现“双碳”经济的有效途径之一,
第6页 | 共12页相关的主要反应有:
Ⅰ:
Ⅱ:
请回答:
(1)有利于提高 平衡转化率的条件是___________。
A. 低温低压 B. 低温高压 C. 高温低压 D. 高温高压
(2)反应 的 ___________ ,
___________(用 表示)。
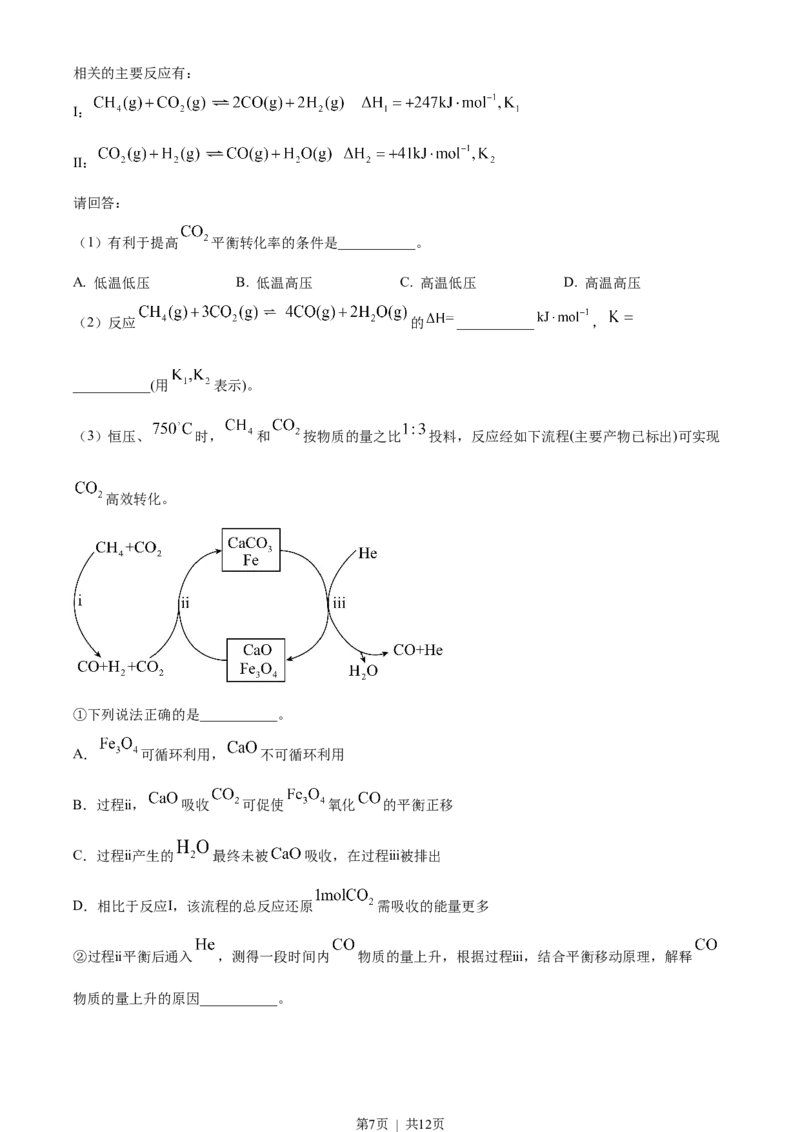
(3)恒压、 时, 和 按物质的量之比 投料,反应经如下流程(主要产物已标出)可实现
高效转化。
①下列说法正确的是___________。
A. 可循环利用, 不可循环利用
B.过程ⅱ, 吸收 可促使 氧化 的平衡正移
C.过程ⅱ产生的 最终未被 吸收,在过程ⅲ被排出
D.相比于反应Ⅰ,该流程的总反应还原 需吸收的能量更多
②过程ⅱ平衡后通入 ,测得一段时间内 物质的量上升,根据过程ⅲ,结合平衡移动原理,解释
物质的量上升的原因___________。
第7页 | 共12页(4) 还原能力 可衡量 转化效率, (同一时段内 与 的物
质的量变化量之比)。
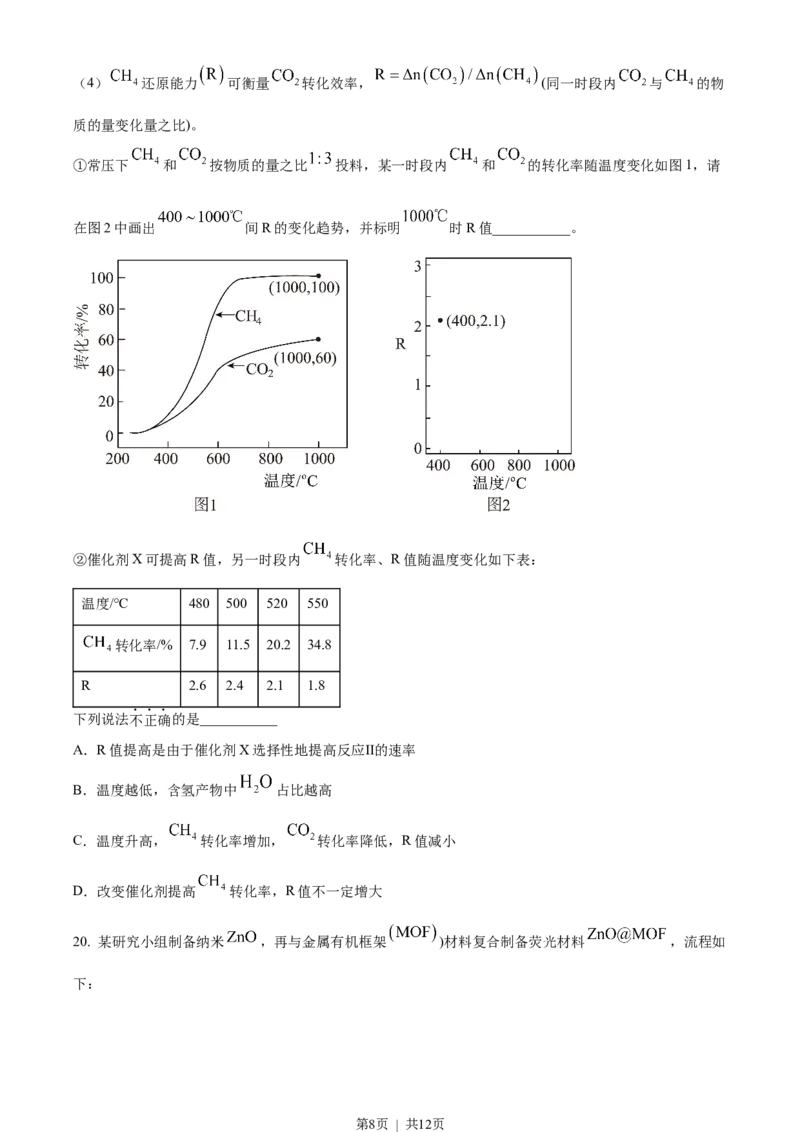
①常压下 和 按物质的量之比 投料,某一时段内 和 的转化率随温度变化如图1,请
在图2中画出 间R的变化趋势,并标明 时R值___________。
②催化剂X可提高R值,另一时段内 转化率、R值随温度变化如下表:
温度/℃ 480 500 520 550
转化率/% 7.9 11.5 20.2 34.8
R 2.6 2.4 2.1 1.8
下列说法不正确的是___________
A.R值提高是由于催化剂X选择性地提高反应Ⅱ的速率
B.温度越低,含氢产物中 占比越高
C.温度升高, 转化率增加, 转化率降低,R值减小
D.改变催化剂提高 转化率,R值不一定增大
20. 某研究小组制备纳米 ,再与金属有机框架 )材料复合制备荧光材料 ,流程如
下:
第8页 | 共12页已知:①含锌组分间的转化关系:
② 是 的一种晶型, 以下稳定。
请回答:
(1)步骤Ⅰ,初始滴入 溶液时,体系中主要含锌组分的化学式是___________。
(2)下列有关说法不正确的是___________。
A. 步骤Ⅰ,搅拌的作用是避免反应物浓度局部过高,使反应充分
的
B. 步骤Ⅰ,若将过量 溶液滴入 溶液制备 ,可提高 利用率
C. 步骤Ⅱ,为了更好地除去杂质,可用 的热水洗涤
D. 步骤Ⅲ,控温煅烧的目的是为了控制 的颗粒大小
(3)步骤Ⅲ,盛放样品的容器名称是___________。
(4)用 和过量 反应,得到的沉淀可直接控温煅烧得纳米 ,沉淀无需
洗涤的原因是___________。
(5)为测定纳米 产品的纯度,可用已知浓度的 标准溶液滴定 。从下列选项中选择合理
的仪器和操作,补全如下步骤[“___________”上填写一件最关键仪器,“(___________)”内填写一种操作,
均用字母表示]。___________
用___________(称量 样品 )→用烧杯(___________)→用___________(___________)→用移液管
(___________)→用滴定管(盛装 标准溶液,滴定 )
仪器:a、烧杯;b、托盘天平;c、容量瓶;d、分析天平;e、试剂瓶
操作:f、配制一定体积的Zn2+溶液;g、酸溶样品;h、量取一定体积的 溶液;i、装瓶贴标签
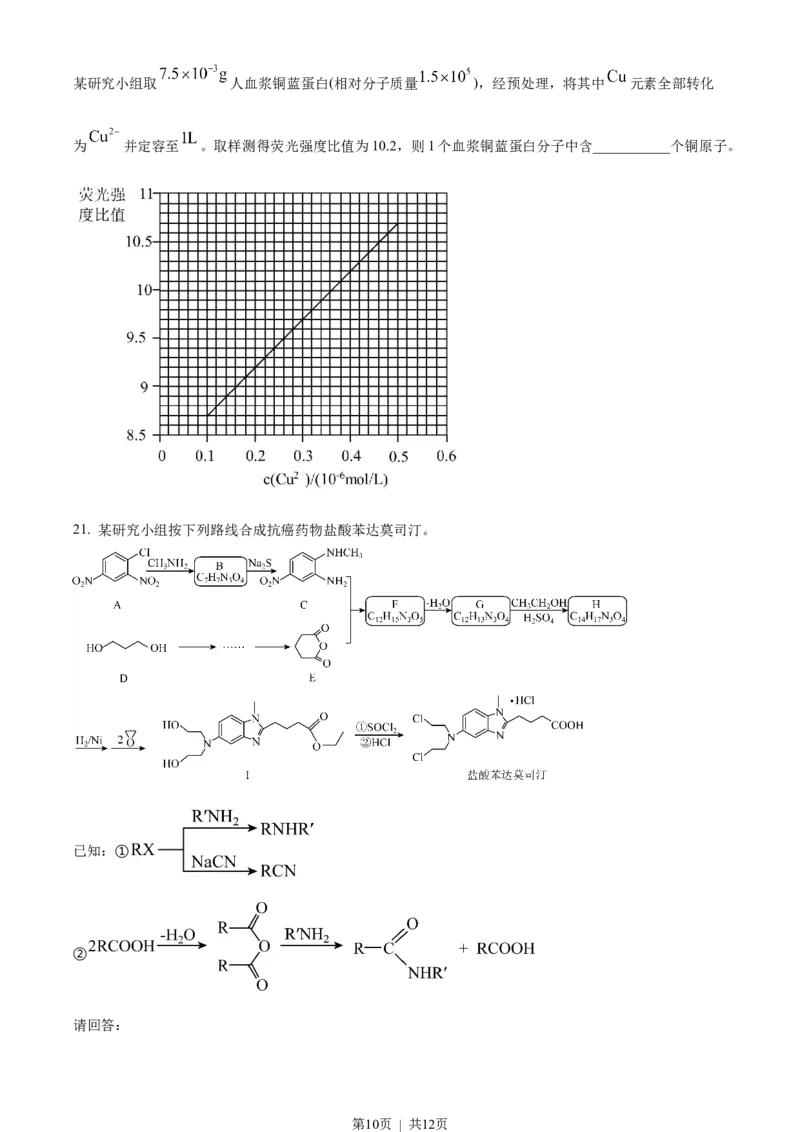
(6)制备的 荧光材料可测 浓度。已知 的荧光强度比值与 在一定浓
度范围内的关系如图。
第9页 | 共12页某研究小组取 人血浆铜蓝蛋白(相对分子质量 ),经预处理,将其中 元素全部转化
为 并定容至 。取样测得荧光强度比值为10.2,则1个血浆铜蓝蛋白分子中含___________个铜原子。
21. 某研究小组按下列路线合成抗癌药物盐酸苯达莫司汀。
已知:①
②
请回答:
第10页 | 共12页(1)化合物A的官能团名称是___________。
(2)化合物B的结构简式是___________。
(3)下列说法正确的是___________。
A. 的反应类型为取代反应
B. 化合物D与乙醇互为同系物
C. 化合物I的分子式是
D. 将苯达莫司汀制成盐酸盐有助于增加其水溶性
(4)写出 的化学方程式______。
(5)设计以D为原料合成E的路线(用流程图表示,无机试剂任选)___。
(6)写出3种同时符合下列条件的化合物C的同分异构体的结构简式_______。
的
①分子中只含一个环,且为六元环;② 谱和 谱检测表明:分子中共有2种不同化学环境
氢原子,无氮氮键,有乙酰基 。
第11页 | 共12页第12页 | 共12页