辛格迪丨GMP良好文档规范(GDocP)核心要义与行业合规要求

01
GDocP基础定义与行业定位
良好文档规范(GDocP,亦称GDP/GRK)是药品、医疗器械、化妆品等生命健康行业GMP合规的核心组成部分,更是数据完整性管控的核心抓手。在行业术语体系中,GDocP、GDP、GRK(良好记录管理规范)本质指向同一合规目标,即通过标准化、规范化的文档全生命周期管理,保障数据真实可靠、全程可追溯,满足NMPA、FDA、EMA、TGA、PIC/S等全球主流监管机构的强制合规要求。 行业审计格言“如果没有被记录下来,那就从未发生过”,精准道出GDocP的核心价值:文档不仅是流程记录,更是合规举证、质量追溯、风险防控的唯一凭证。GDocP并非单纯的“记录填写”,而是贯穿产品全生命周期的合规管控体系,直接关联药品质量体系(PQS)、质量风险管理(QRM)、批次放行等关键业务环节,是企业履行行业法律职责、规避监管处罚的底线要求。

辛格迪的文档管理系统(DMS)深度契合GDocP的行业定位与核心价值,以一体化的文档与数据管控体系为核心,将GDocP合规要求嵌入生命健康企业全业务流程,通过技术手段实现文档管理的标准化、自动化与智能化,让GDocP从“合规底线要求”转化为企业质量管控与全球化布局的核心能力,为企业应对全球监管审计、筑牢质量体系提供全流程技术支撑。
02
GDocP与数据完整性:ALCOA++核心原则
GDocP的核心管控目标是实现数据完整性,ALCOA++原则是衡量文档与数据合规性的黄金标准,也是全球监管审计的核心核查依据,企业需深度理解并落地每一项原则内涵。
ALCOA基础五原则:可归因性(Attributable)、清晰性(Legible)、同步性(Contemporaneous)、原始性(Original)、准确性(Accurate);
ALCOA + 补充原则:完整性(Complete)、一致性(Consistent)、持久性(Enduring);
ALCOA++进阶原则:新增可用性(Available)。
监管机构对ALCOA++原则的执行力度持续收紧,任何一项原则的缺失,都会直接导致审计缺陷、警告信、产品召回甚至市场禁入,这也是生命健康行业文档管控零容错的核心原因。
辛格迪的文档管理系统(DMS)以ALCOA++原则为设计核心,打造全维度数据完整性防护体系,针对每一项原则提供专属技术支撑:通过身份唯一认证实现可归因性,通过标准化文档模板与智能校验实现清晰性与准确性,通过实时数据采集与自动时间戳实现同步性,通过原始数据加密存储与不可篡改机制实现原始性,通过全流程数据闭环管理实现完整性与一致性,通过多节点备份与长期存储架构实现持久性,通过智能检索与跨端调取功能实现可用性,让ALCOA++原则的落地从 “人工管控” 升级为 “技术硬约束”,从根源上规避数据完整性合规风险。
03
GDocP强制适用范围与合规责任主体
GDocP/GRK的合规要求覆盖企业全组织、全供应链,所有参与产品研发、生产、检验、仓储、分销、售后的人员均需严格遵守,责任主体包含企业内部生产、质检、研发等岗位员工,承包商、原材料供应商等外部合作方,以及偏差处理、批次放行等关键岗位授权人员;从业务场景来看,覆盖产品研发设计、临床试验、原辅料验收、生产制造、上市后监测直至废弃处置的全生命周期,其中批发放行、偏差调查、CAPA落地、产品召回等环节是监管核查的重中之重。
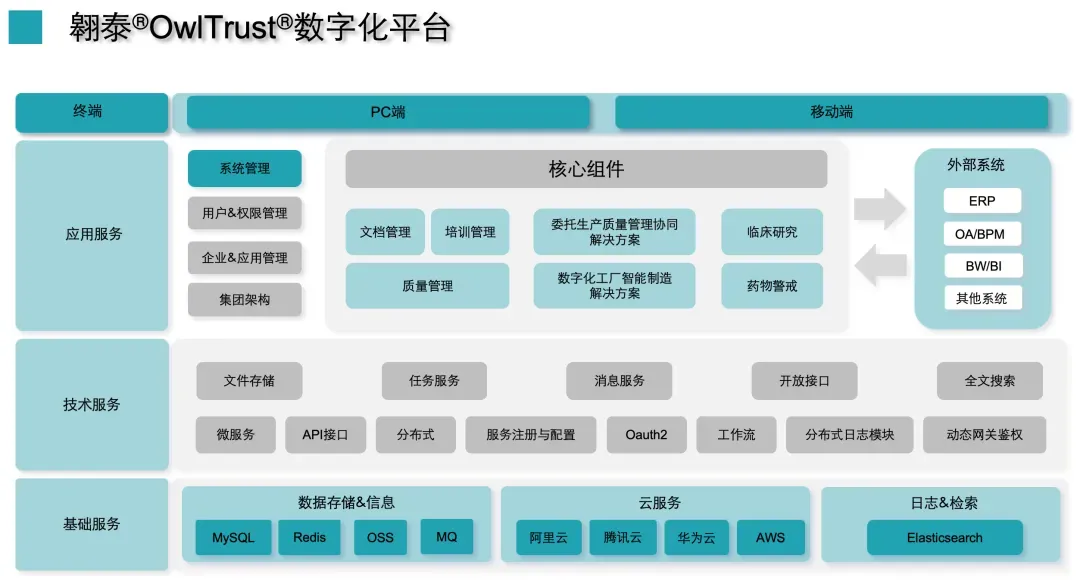
翱泰 质量合规数字化平台
辛格迪翱泰®OwlTrust®质量及合规平台针对GDocP全适用范围与多责任主体特点,打造全供应链、全生命周期、全角色的一体化管控平台:一方面,平台支持企业内部各岗位的权限精细化配置,实现不同角色的操作留痕与责任追溯;另一方面,搭建外部合作方协同管理模块,打通企业与供应商、检测机构、物流企业等的文档数据链路,实现外部合作环节的GDocP合规管控;同时,针对研发、生产、审计、召回等核心业务场景,开发专属功能模块,将合规要求嵌入场景化操作流程,确保全场景、全主体的GDocP合规落地无死角。
04
传统文档管理的合规痛点与文档管理系统(DMS)的破局思路
当前多数企业仍采用纸质 + 零散电子文档的传统管理模式,成为NMPA、FDA、TGA、EMA等机构审计缺陷的重灾区,核心痛点集中在记录管控不规范、数据追溯性差、人员合规意识薄弱、全生命周期管理缺失、监管应对能力不足等方面。这些痛点不仅会导致企业面临巨额罚款、生产线停产等直接损失,还会破坏品牌信誉、阻碍全球化布局,甚至引发公共卫生风险,同时也会影响企业ISO 9001、ISO 13485等核心认证的获取。
辛格迪文件管理系统(DMS)直击传统文档管理的核心合规痛点,通过技术创新实现全维度破局,具体解决思路如下:
解决记录管控不规范:替代纸质记录与零散电子记录,实现文档全电子化管理,设置操作权限硬约束、修改留痕强制规则,杜绝共享账号、涂改伪造、无理由修改等违规行为;
解决数据追溯性差:搭建统一的文档数据中台,打破跨部门、跨系统的数据孤岛,实现所有文档的集中存储、全链路追溯,原始记录永久保存且可快速调取;
解决人员合意识薄弱:翱泰平台内置GDocP与ALCOA++原则培训模块、操作端实时合规提醒功能,将合规培训与实际操作深度结合,让员工在操作中强化合规认知,形成 “操作即合规” 的行为习惯;
解决全生命周期管理缺失:打造文档从起草、审批、分发、修订、作废到归档的全生命周期自动化管控流程,实现过期文档自动回收、无效文件实时屏蔽,杜绝因文件流转混乱导致的操作失误;
解决监管应对能力不足:内置审计追踪、自检预警功能,自动记录所有操作行为,支持自定义自检频次与缺陷排查,生成标准化审计举证报告,让企业面对监管审计时从容应对,大幅降低警告信、处罚单风险。
05
GDocP核心合规要求与辛格迪文档管理系统(DMS)的落地适配
结合PIC/S、NMPA GMP、EU GMP、FDA CGMP等国际指南,GDocP的基础合规要求可归纳为数据准确性与完整性、实时同步记录、身份可追溯、文档安全存储、修改合规管控、快速可及性、全流程管控七大核心维度,辛格迪文档管理系统(DMS)围绕七大核心维度,打造全流程、高适配的合规管控体系,实现GDocP合规要求的技术化、自动化落地,具体适配如下:
数据准确性与完整性:辛格迪翱泰平台内置智能数据校验引擎,支持录入数据实时校验、逻辑核对,设置必填项强制约束,杜绝虚假条目、缺失数据,同时实现数据全程可追溯、可复核,确保数据从录入到归档的准确完整;
实时同步记录:对接企业生产、检验等现场设备,实现数据自动采集、实时录入,电子记录自动生成不可篡改的时间戳,从技术上杜绝事后补录、延迟记录等违规行为;
身份可追溯:采用一人一账号的唯一身份认证体系,支持指纹、人脸识别等多因子验证,签名与身份永久绑定,操作行为全程关联操作人员身份,严禁共享密码、代签伪造,实现每一项操作的责任可追溯;
文档安全存储:采用银行级数据加密技术,对文档数据进行传输、存储全链路加密,搭建多地域、多节点的备份架构,纸质文档可实现电子化扫描后加密归档,满足防潮防火要求,电子文档定期自动归档,防止数据篡改、丢失、泄露;
修改合规管控:设置标准化的文档修改流程,强制要求修改操作采用单线划改模式、保留原始信息,同时自动标注修改人、修改时间、修改原因,从系统层面杜绝涂白、覆盖等违规修改行为,所有修改记录永久留痕可查;
快速可及性:打造智能化的文档分类归档与检索系统,支持关键词、时间、批次、操作人员等多维度检索,毫秒级调取结果,同时支持电脑、平板、移动终端等跨端访问,审计时可快速调取全链路记录,满足监管核查的快速访问需求;
全流程管控:实现文档起草、勘误、审核、批准、分发、培训、修订、作废、销毁的全生命周期线上化、自动化管控,每一个环节都设置标准化审批流程,操作行为自动留痕,确保文档全流程的管控可追溯、可核查,从根源上规避流程混乱导致的合规风险。
辛格迪翱泰®OwlTrust®质量及合规平台以GDocP核心理论与GMP合规底层逻辑为基础,通过技术创新将合规要求从 “人工要求” 转化为 “系统硬约束”,为生命健康企业搭建覆盖全组织、全供应链、全生命周期的GDocP合规管控体系,不仅帮助企业满足全球监管机构的合规要求,更能通过文档与数据的标准化管理,提升企业质量管控效率、降低运营风险,为企业的高质量发展与全球化布局提供坚实的技术支撑。
|内容策划|
PRESENTED
▽
本文编辑|Cathy
主编|Tony 责编|Jenny
www.hiheit.com
欢迎访问辛格迪官网,了解详细解决方案

|产品体验专区|
REQUEST A DEMO
▽
翱泰®OwlTrust®—质量合规专家
申请体验账号请拨打:400-886-2808

[长按二维码咨询]

[长按登记试用]
|客户案例|
CUSTOMER CASE
▽











|翺泰|
OWLTRUST
▽
● 质量套件 解决方案 咨询服务 ●
质量套件
解决方案
咨询服务
|推荐阅读|
RECOMMEND
▽
● 精彩文章,点击阅读 ●
质量管理数字化
中国申请加入PIC/S,关于“PIC/S GMP”你的了解有多少?
数据完整性
获奖信息
签约快讯
客户成功
【丽珠医药】斩获三项重磅大奖
【迈威生物】产品首次获得海外上市许可
【杰视医疗】国产首个眼科专用气体获批上市



 夜雨聆风
夜雨聆风




