AI时代的药学研发:革命已至,药学研发者该何去何从?
当AlphaFold3在2024年预测了几乎所有已知蛋白质结构,当生成式AI在72小时内设计出全新分子骨架,当AI辅助的候选分子首次进入临床——一个不可回避的问题摆在每一位药学人面前:在这个算法重塑一切的时代,药学家究竟是会被AI替代,还是会借AI完成一次伟大的进化?
引言:时代的断点
2026年,全球制药行业正站在一个历史性的断点上。
如果说过去十年是”大数据+高通量筛选”对传统药物研发的第一次冲击,那么2024–2026这三年,以大语言模型、生成式AI、蛋白质结构预测为代表的第二代人工智能技术,正在以前所未有的速度重构整个药学研发的底层逻辑。
一组数据值得我们深思:
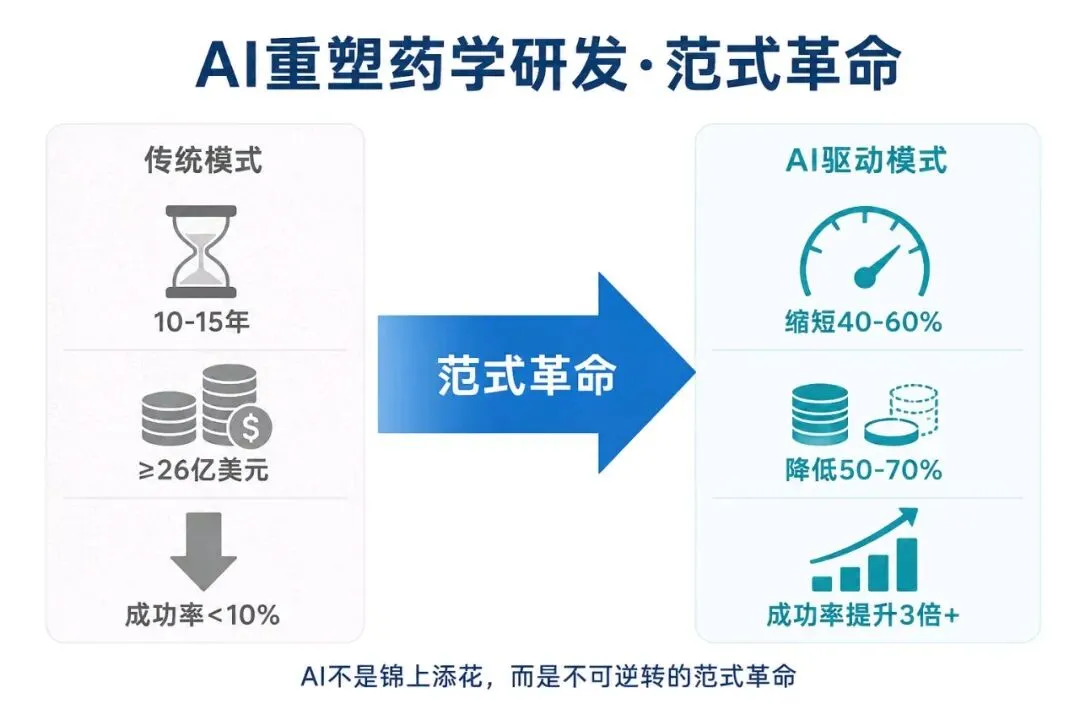
传统新药研发平均成本已突破26亿美元,耗时10–15年;临床I期到上市的成功率不足10%。而AI辅助的临床前研发数据显示,靶点发现到PCC(候选化合物)确定时间可缩短40–60%,成本可降低 50–70%。
我们可以清晰地看到一个事实:AI不是药学研发的”锦上添花”,而是一场不可逆转的范式革命。
一、浪潮之巅:AI正在如何重塑药学研发?
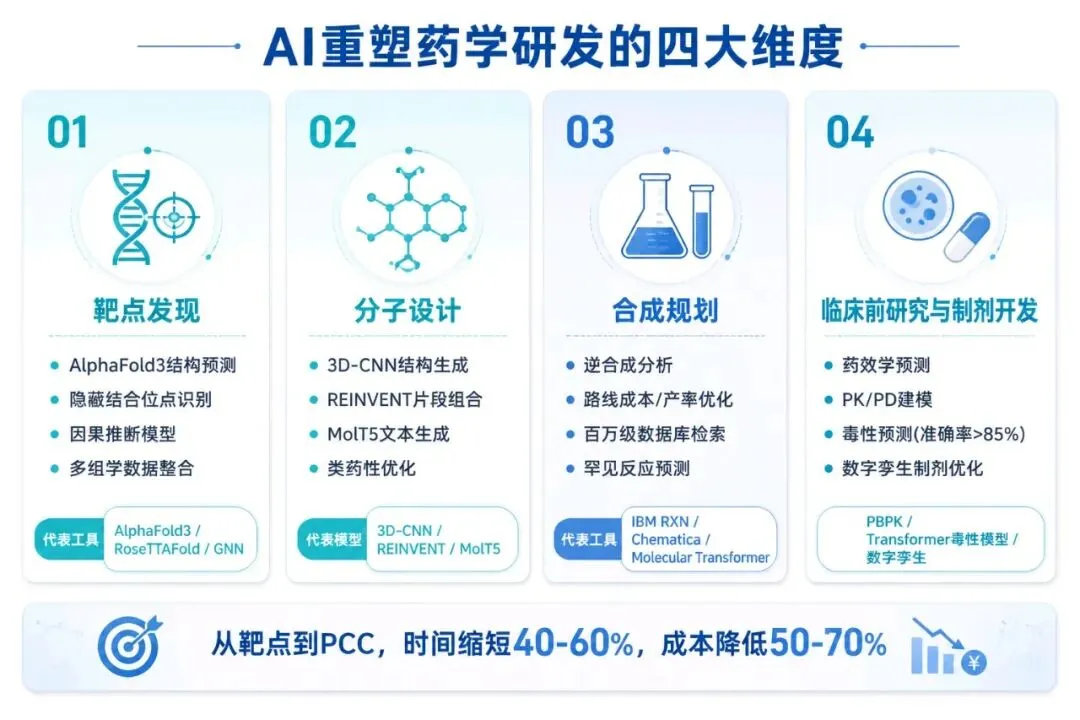
1.1 靶点发现:从”盲人摸象”到”上帝视角”
在传统的靶点发现中,药学家像在黑暗中摸索——通过文献综述、基因敲除实验、表型筛选等耗时数年才能锁定一个候选靶点。
而今天,以 AlphaFold3、RoseTTAFold 为代表的蛋白质结构预测工具,以及图神经网络(GNN)在生物网络分析中的应用,让研究人员可以在几周内完成以下工作:
• 预测数千个蛋白质-蛋白质相互作用界面
• 识别疾病相关的隐蔽结合位点(cryptic pockets)
• 通过因果推断模型从多组学数据中锁定关键致病靶点
📍典型案例:2024年,Isomorphic Labs利用AlphaFold3在短短4个月内完成了对一个难成药靶点(GPCR家族)的解析和候选分子筛选,而传统方法需要2–3年。
1.2 分子设计与生成:AI化身”分子建筑师”
如果说传统药物化学家是”修补匠”,那么生成式AI就是”建筑师”。
生成式AI在分子设计领域的三大核心能力:
• 基于结构的生成(代表模型:3D-CNN、Equiformer):能在靶点结合腔内直接生成分子。
•基于片段的生成(代表模型:REINVENT、MoleculeSTM):能从分子片段库中组合全新骨架。
• 基于文本的生成(代表模型:ChemBERTa、MolT5):能通过文字描述直接生成分子结构。
📍关键突破:2025年,英矽智能的ISM001-055成为全球首款完全由AI发现并进入II期临床的抗纤维化药物。从靶点发现到临床前候选化合物确定仅用了18个月,而传统模式需要4–6年。
1.3 合成路线规划:从”炒菜试错”到”最优路径”
逆合成分析一直是药物化学家的核心技能。面对日益复杂的分子骨架,即使是经验丰富的化学家,也可能需要数周才能规划出合理路线。
如今,AI逆合成规划工具(如IBM RXN、Chematica)已经实现了:
• 百万级反应数据库的毫秒级检索
• 多步合成路径的成本、产率、安全性综合优化
• 罕见反应类型的预测与实验验证
📍 数据震撼:在《自然·化学》发表的研究中,AI规划的合成路线在80%的案例中优于人工方案,平均步骤数减少 30%,总产率提升45%。
1.4 临床前研究与制剂开发:从”经验试错”到”理性设计”
这是药学研发中AI价值常被低估,但潜力巨大的领域。
• 药效学预测:基于多模态深度学习的模型,可在细胞实验前筛选出最可能有效的分子。
• 药代动力学(PK)预测:利用PBPK模型+机器学习,无需大量动物实验即可预测人体暴露量。
• 制剂开发:通过数字孪生模拟IVIVC,AI基于分子特性、适应症、动物体内行为,推荐制剂形式和规格,辅助处方和工艺优化,显著提高制剂开发效率。
二、冷静的审视:AI不是神话,但也绝非泡沫
在经历了生成式AI狂欢之后,我们需要清醒地认识到AI在药学研发中的真实边界:
2.1 数据质量是最大的瓶颈
“Garbage in, garbage out”。尽管公共数据库体量巨大,但仍面临挑战:
数据不一致:不同实验室的IC50值可能相差一个数量级。
负结果缺失:90%以上的失败实验从未被公开发表。
多模态整合难:将基因组、蛋白质组、临床数据整合为统一训练集仍是痛点。
2.2 可解释性——药学家最后的”护城河”
AI模型可以告诉我们”某个分子有活性”,但往往无法解释”为什么”。毒性预测模型的假阳性/假阴性率依然偏高。AI设计的分子可能体外活性出色,但体内代谢稳定性极差。监管机构(FDA/EMA)对AI驱动药物持审慎态度,要求提供清晰的机制验证证据。
2.3 可合成性与可专利性
这是AI分子设计的”阿喀琉斯之踵”。AI生成的分子中,有 15–30%存在合成不可行问题;且AI可能会”无意识地”侵犯已有专利空间。转化为可商业化的生产工艺,仍需人工深度介入。
三、人机共生:药学家在AI时代的新角色
我们可以得出一个重要结论:AI不会取代药学家,但会用AI的药学家一定会取代不会用AI的药学家。
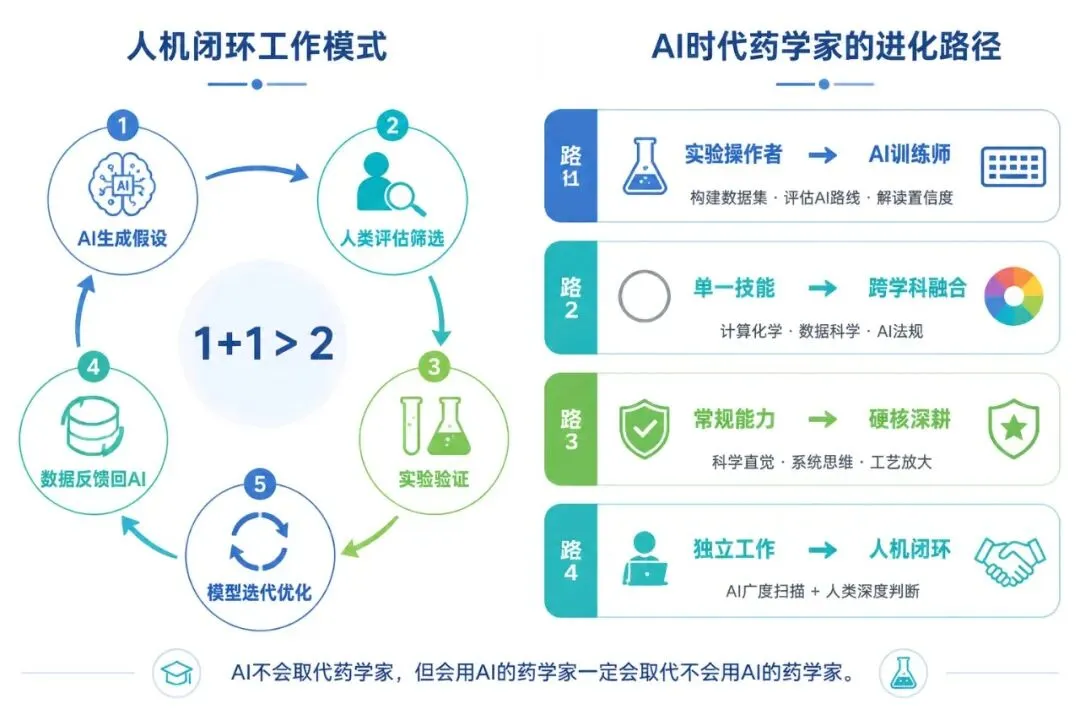
未来药学人有四条清晰的进化路径:
路径一:从”实验操作者”进化为”AI训练师”
未来的药学家,手要快,脑要灵,更要会用数据说话。合成化学家需构建高质量训练集;药理学家需解读AI预测的置信度;制剂学家需掌握数字孪生进行虚拟预测。
路径二:从”单一技能”走向”跨学科融合”
AI时代最稀缺的是跨界人才。掌握分子动力学模拟、数据清洗与特征工程的”计算型/数据型药学家”,薪资正在成倍增长。
路径三:深耕AI无法替代的”硬核能力”
包括对分子”类药性”的直觉与创造力、处理ADMET复杂系统的全局思维,以及从实验室到GMP商业化生产的工艺放大工程经验。
路径四:拥抱”人机闭环”工作模式
这是最优解:AI负责广度扫描(在数百万分子空间中快速筛选) → 人类负责深度判断(机制验证、安全性评估) → 实验数据反馈AI → 模型迭代优化。
四、展望2027–2030:药学研发的五大趋势
站在现在看未来,药学研发即将迎来以下关键节点:
🚩 2027年:AI驱动的临床前候选分子首次大规模验证(资本将加速涌入)
🚩 2028年:干湿闭环实验室(Dry-Wet Lab)普及(实验自动化+AI决策一体化,研发效率再提3倍)
🚩 2029年:首个AI全程辅助发现的新药获批上市(AI地位得到最终确认)
🚩 2030年:AI+自动化合成成为行业标配(传统药物化学岗位面临深度转型)
结语:AI赋能药学人的时代
AI时代,药学研发该何去何从?
答案不是悲观的”被替代论”,也不是盲目的”AI万能论”。
真正的答案是:这是药学家从”重复性劳动”走向”创造性思维”、从”经验驱动”走向”数据+经验双驱动”的历史性转折点。
如果你是一名药学生,请拥抱算法、学会编程、理解数据——这是未来药学家的标配。
如果你是一名从业者,请保持开放、持续学习——AI不是来抢饭碗的,而是来帮你换个更大的碗。
如果你是一家药企决策者,请立即布局AI——这不是”要不要做”的选择题,而是”做多深”的必答题。
2026年,变革的窗口已经打开。犹豫的人还在观望,而行动的人已经在路上。
谨以此文与每一位药学人共勉
 夜雨聆风
夜雨聆风




