文档内容
【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
物理和化学试题
化学试题(共60分)
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 K-39 Ca-40 Zn-65
四、选择题(本题包括12小题,每小题2分,共24分。每小题只有一个选项符合题意)
1. 人类的日常生活和工农业生产离不开水。下列过程中水发生化学变化的是
A. 水降温结冰 B. 溶解蔗糖
C. 电解水制取H 和O D. 蒸馏自来水获得蒸馏水
2 2
2. 黑火药是中国古代四大发明之一,由C、S和KNO 等混合而成。下列说法正确的是
3
A. C、S均具有可燃性 B. 黑火药可存放于高温处
C. 黑火药爆炸时吸热 D. KNO 属于氧化物
3
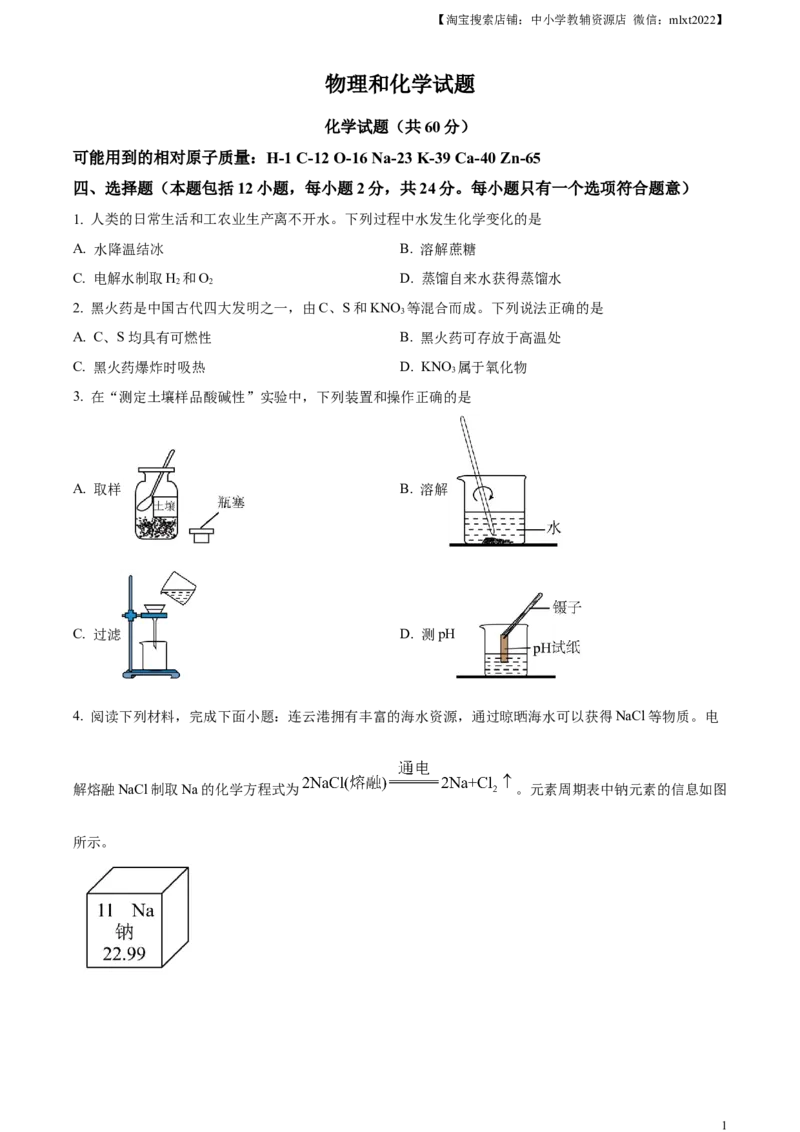
3. 在“测定土壤样品酸碱性”实验中,下列装置和操作正确的是
A. 取样 B. 溶解
C. 过滤 D. 测pH
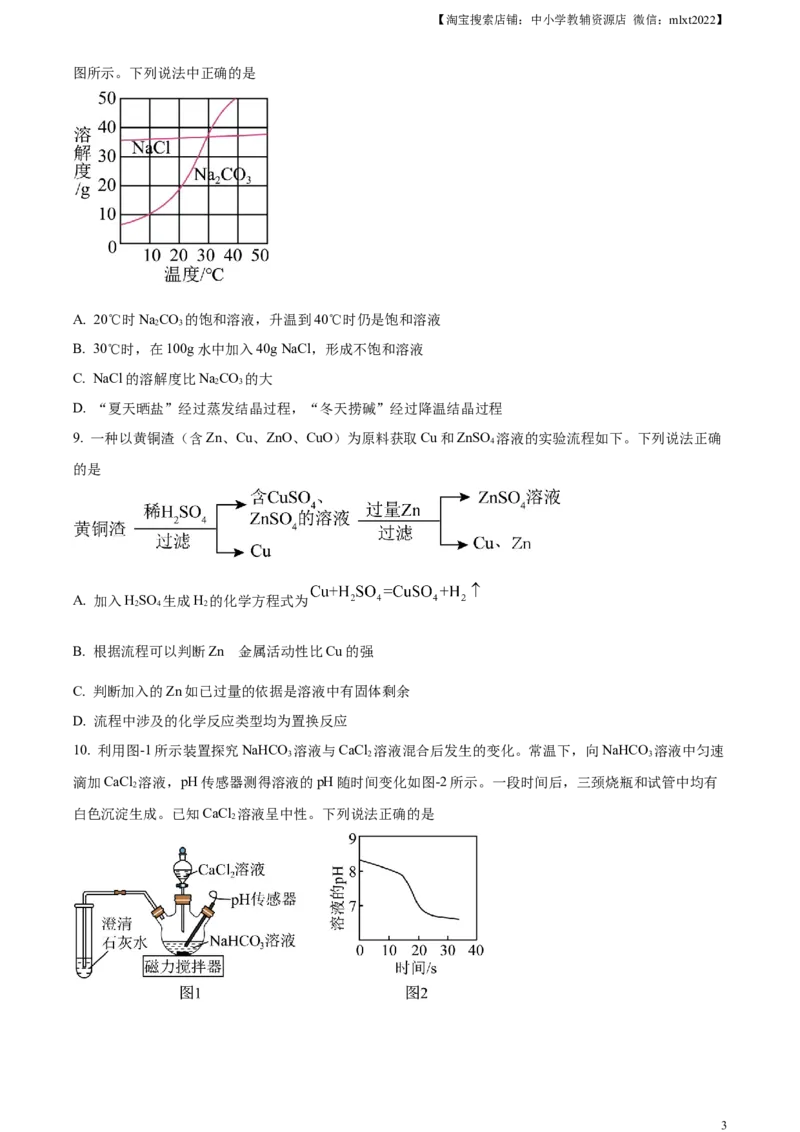
4. 阅读下列材料,完成下面小题:连云港拥有丰富的海水资源,通过晾晒海水可以获得NaCl等物质。电
解熔融NaCl制取Na的化学方程式为 。元素周期表中钠元素的信息如图
所示。
1【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
的
(1)下列化学用语表示正确 是
A. 氯元素:Cl B. 两个钠原子:Na
2 2
C. 构成NaCl的离子:Na+、Cl- D. HO中氢元素的化合价:
2
(2)下列有关钠元素的说法中正确的是
A. 属于非金属元素 B. 原子序数为11
C. 相对原子质量为22.99g D. Na+中有11个电子
(3)电解熔融NaCl制取Na的化学反应属于
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
5. 下列有关碳及其化合物的性质与用途具有对应关系的是
A. 石墨很软有滑腻感,可制造石墨电极
B. CO 能与NaOH反应,可用于人工降雨
2
C. 具有还原性,可用于炼铁
D. NaHCO 呈白色,可用于治疗胃酸过多症
3
6. 服用葡萄糖酸锌(C H O Zn)可以给人体补锌。已知人体内水的质量分数为 ,下列关于
12 22 14
C H O Zn的说法正确的是
12 22 14
A. 由四种元素组成
B. H、O元素的质量比为
C. C元素的质量分数最大
D. O、Zn元素均为人体必需的微量元素
7. 下列实验方案能达到实验目的的是
选
实验目的 实验方案
项
A 防止自行车链条生锈 在链条表面涂油
B 除去CO 中少量的CO 点燃
2
C 鉴别NH Cl和(NH )SO 取样,加Ca(OH) 固体研磨,闻气味
4 4 2 4 2
D 稀释浓硫酸 取水倒入浓硫酸中,并用玻璃棒不断搅拌
A. A B. B C. C D. D
8. 我国盐湖地区有“夏天晒盐(NaCl),冬天捞碱(NaCO)”的做法。NaCl、NaCO 的溶解度曲线如
2 3 2 3
2【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
图所示。下列说法中正确的是
A. 20℃时NaCO 的饱和溶液,升温到40℃时仍是饱和溶液
2 3
B. 30℃时,在100g水中加入40g NaCl,形成不饱和溶液
C. NaCl的溶解度比NaCO 的大
2 3
D. “夏天晒盐”经过蒸发结晶过程,“冬天捞碱”经过降温结晶过程
9. 一种以黄铜渣(含Zn、Cu、ZnO、CuO)为原料获取Cu和ZnSO 溶液的实验流程如下。下列说法正确
4
的是
A. 加入HSO 生成H 的化学方程式为
2 4 2
的
B. 根据流程可以判断Zn 金属活动性比Cu的强
C. 判断加入的Zn如已过量的依据是溶液中有固体剩余
D. 流程中涉及的化学反应类型均为置换反应
10. 利用图-1所示装置探究NaHCO 溶液与CaCl 溶液混合后发生的变化。常温下,向NaHCO 溶液中匀速
3 2 3
滴加CaCl 溶液,pH传感器测得溶液的pH随时间变化如图-2所示。一段时间后,三颈烧瓶和试管中均有
2
白色沉淀生成。已知CaCl 溶液呈中性。下列说法正确的是
2
3【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
A. NaHCO 溶液显酸性
3
的
B. 时溶液显酸性 原因是CaCl 过量
2
C. 三颈烧瓶中生成的白色沉淀为Ca(HCO )
3 2
.
D 实验表明:
五、非选择题(本题包括4小题,共36分)
11. 科技是第一生产力,近年来我国在科技领域取得了一系列辉煌成就。
(1)“福建号”航母在建造过程中大量使用特种钢。该特种钢的耐腐蚀性能比纯铁的_____(填“好”或
“差”)。
(2)“天舟号”货运飞船换装了以LiFePO 作正极材料的新型锂电池。已知LiFePO 中Li为+1价,
4 4
为-3价,则其中Fe的化合价为_____。
(3)“嫦娥号”月球登陆器表面覆盖了由聚酰亚胺和铝箔构成的多层保温材料。
①聚酰亚胺属于有机合成材料。聚酰亚胺中一定含有的元素是______(填元素符号)、H、O、N等。
②铝块可以制成铝箔是利用了铝的______(填“导电”或“延展”)性。
(4)“长征五号”大推力运载火箭助力我国天宫空间站建设。该火箭助推器使用煤油(含C 、C 、
11 24
C H 、C H 等分子)作燃料,液氧作助燃剂。
12 26 13 28
①煤油属于_____(填“纯净物”或“混合物”)。
的
②煤油在氧气中充分燃烧,产物 化学式为____。
12. O 是人类生存必需的物质,认识和获取O 具有重要意义。
2 2
(1)工业生产的O 可加压贮存在蓝色钢瓶中,在此过程中发生的变化是______(填字母)。
2
a.O 分子质量变小 b.O 分子间间隔减小 c.O 分子转变为其他分子
2 2 2
(2)实验室里现有MnO 固体、HO,溶液以及下列装置(A~D):
2 2 2
①仪器M的名称是_____(填字母)。
a.长颈漏斗 b.锥形瓶 c.集气瓶
②利用上述药品制取O,应选择的两个装置是______(填字母)。
2
4【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
③检验一瓶无色气体是氧气的简单方法是______(包括操作和现象)。
(3)气焊的化学原理为 ,X的化学式为______。
(4)氧循环对维持自然界中的物质、能量及生态平衡具有重要意义。
①能向自然界中释放O 的是______(填字母)。
2
a.动植物的呼吸 b.可燃物的燃烧 c.植物的光合作用
②氧气和臭氧(O)可以相互转化。在紫外线的作用下,O 转化为O 的化学方程式为______。
3 2 3
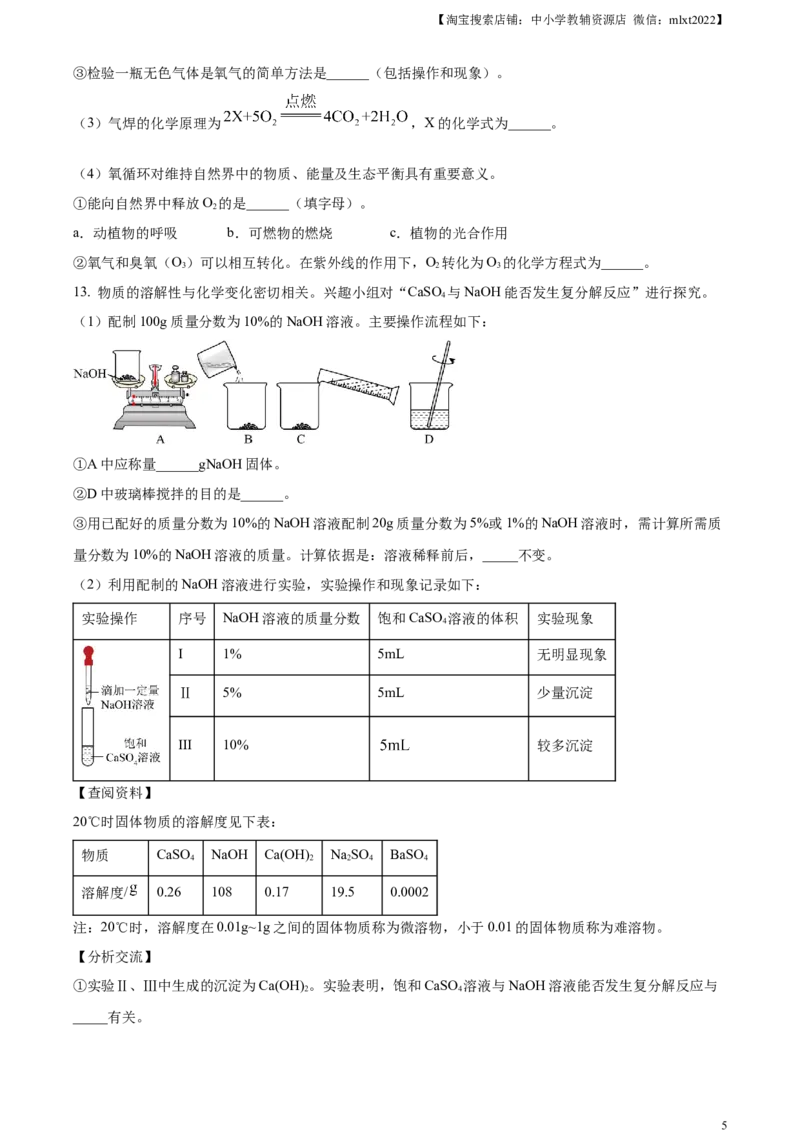
13. 物质的溶解性与化学变化密切相关。兴趣小组对“CaSO 与NaOH能否发生复分解反应”进行探究。
4
(1)配制100g质量分数为10%的NaOH溶液。主要操作流程如下:
①A中应称量______gNaOH固体。
②D中玻璃棒搅拌的目的是______。
③用已配好的质量分数为10%的NaOH溶液配制20g质量分数为5%或1%的NaOH溶液时,需计算所需质
量分数为10%的NaOH溶液的质量。计算依据是:溶液稀释前后,_____不变。
(2)利用配制的NaOH溶液进行实验,实验操作和现象记录如下:
实验操作 序号 NaOH溶液的质量分数 饱和CaSO 溶液的体积 实验现象
4
I 1% 5mL 无明显现象
Ⅱ 5% 5mL 少量沉淀
III 10% 较多沉淀
【查阅资料】
20℃时固体物质的溶解度见下表:
物质 CaSO NaOH Ca(OH) NaSO BaSO
4 2 2 4 4
溶解度/ 0.26 108 0.17 19.5 0.0002
注:20℃时,溶解度在0.01g~1g之间的固体物质称为微溶物,小于0.01的固体物质称为难溶物。
【分析交流】
①实验Ⅱ、Ⅲ中生成的沉淀为Ca(OH) 。实验表明,饱和CaSO 溶液与NaOH溶液能否发生复分解反应与
2 4
_____有关。
5【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
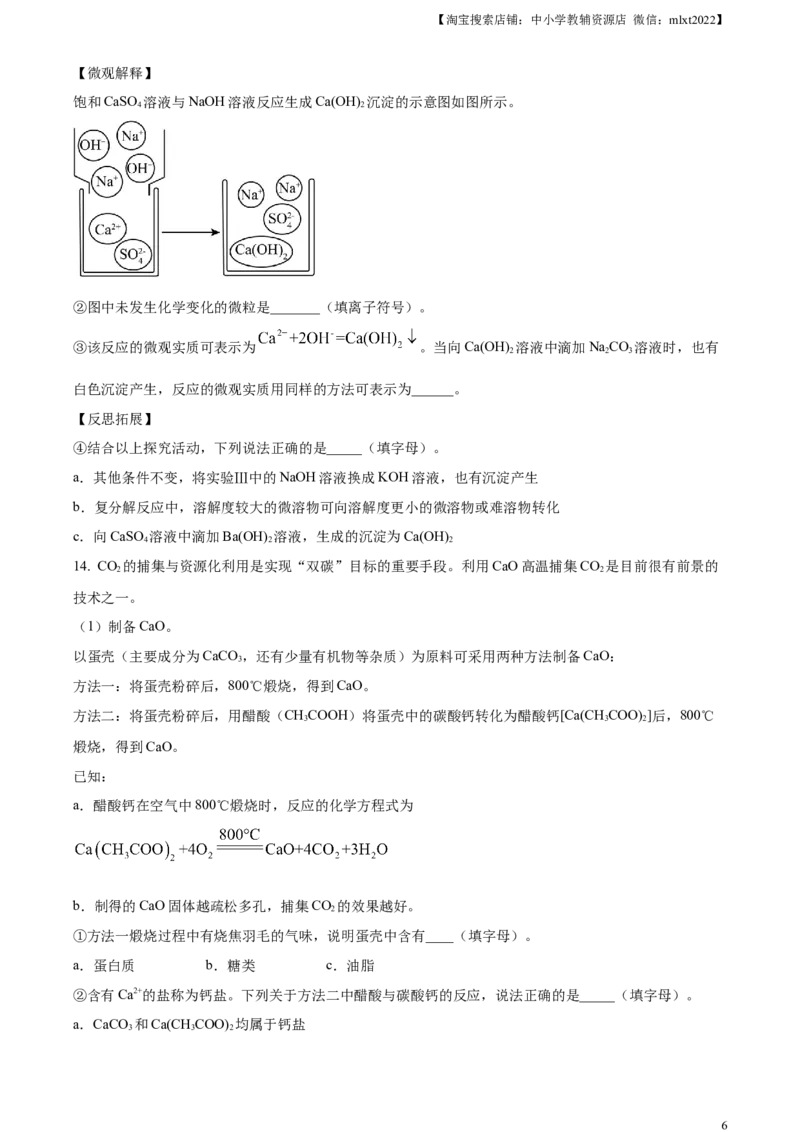
【微观解释】
饱和CaSO 溶液与NaOH溶液反应生成Ca(OH) 沉淀的示意图如图所示。
4 2
②图中未发生化学变化的微粒是_______(填离子符号)。
③该反应的微观实质可表示为 。当向Ca(OH) 溶液中滴加NaCO 溶液时,也有
2 2 3
白色沉淀产生,反应的微观实质用同样的方法可表示为______。
【反思拓展】
④结合以上探究活动,下列说法正确的是_____(填字母)。
a.其他条件不变,将实验Ⅲ中的NaOH溶液换成KOH溶液,也有沉淀产生
b.复分解反应中,溶解度较大的微溶物可向溶解度更小的微溶物或难溶物转化
c.向CaSO 溶液中滴加Ba(OH) 溶液,生成的沉淀为Ca(OH)
4 2 2
14. CO 的捕集与资源化利用是实现“双碳”目标的重要手段。利用CaO高温捕集CO 是目前很有前景的
2 2
技术之一。
(1)制备CaO。
以蛋壳(主要成分为CaCO ,还有少量有机物等杂质)为原料可采用两种方法制备CaO:
3
方法一:将蛋壳粉碎后,800℃煅烧,得到CaO。
方法二:将蛋壳粉碎后,用醋酸(CHCOOH)将蛋壳中的碳酸钙转化为醋酸钙[Ca(CHCOO) ]后,800℃
3 3 2
煅烧,得到CaO。
已知:
a.醋酸钙在空气中800℃煅烧时,反应的化学方程式为
b.制得的CaO固体越疏松多孔,捕集CO 的效果越好。
2
①方法一煅烧过程中有烧焦羽毛的气味,说明蛋壳中含有____(填字母)。
a.蛋白质 b.糖类 c.油脂
②含有Ca2+的盐称为钙盐。下列关于方法二中醋酸与碳酸钙的反应,说法正确的是_____(填字母)。
a.CaCO 和Ca(CHCOO) 均属于钙盐
3 3 2
6【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
b.无色酚酞溶液遇醋酸溶液显红色
c.醋酸与碳酸钙反应生成醋酸钙的同时,有CO 气体生成
2
③研究表明:方法二制得的CaO捕集CO 的效果比方法一的更好,原因是_____。
2
(2)捕集CO。640℃时CaO能与CO 反应生成CaCO ,固定封存CO。28gCaO最多能捕集CO 的质量
2 2 3 2 2
是多少?(写出计算过程,否则不得分)
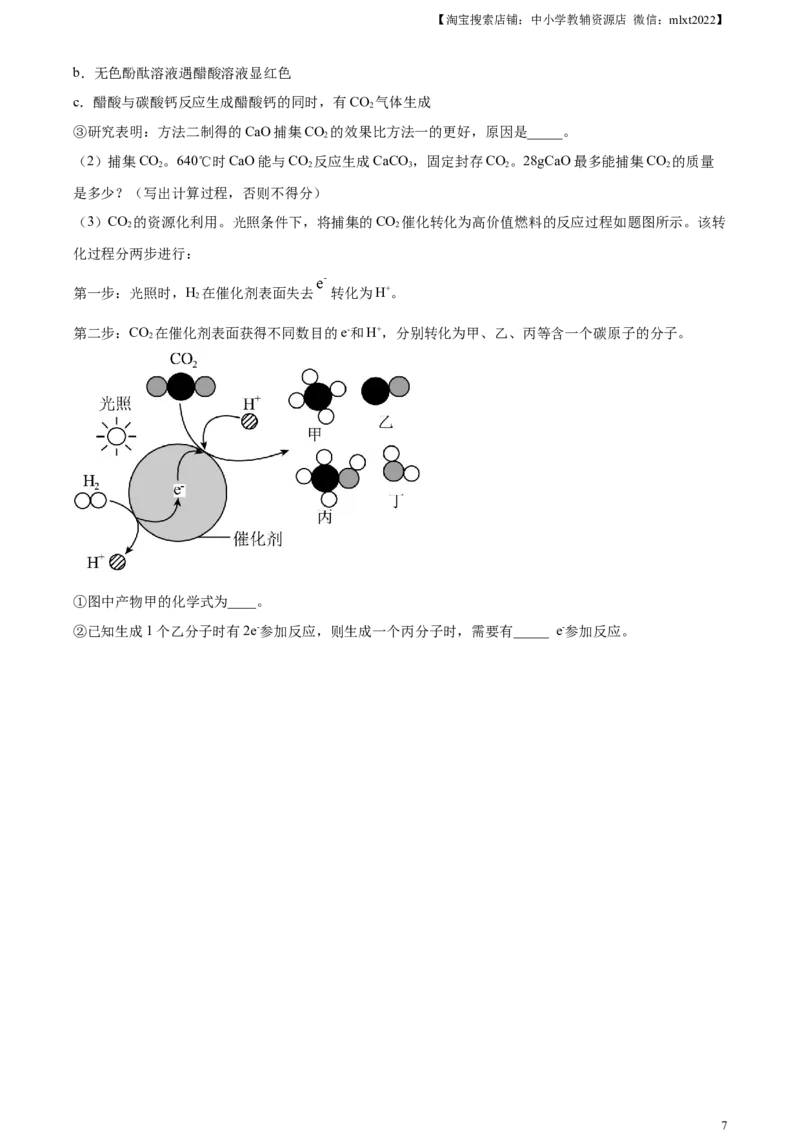
(3)CO 的资源化利用。光照条件下,将捕集的CO 催化转化为高价值燃料的反应过程如题图所示。该转
2 2
化过程分两步进行:
第一步:光照时,H 在催化剂表面失去 转化为H+。
2
第二步:CO 在催化剂表面获得不同数目的e-和H+,分别转化为甲、乙、丙等含一个碳原子的分子。
2
①图中产物甲的化学式为____。
②已知生成1个乙分子时有2e-参加反应,则生成一个丙分子时,需要有_____ e-参加反应。
7