文档内容
2023 级高三学年上学期九月份月考
D. 铁经过发蓝处理形成致密氧化膜:
化 学 试 题
4.在铋基催化剂表面上,一定波长的光可使废气中的 CO 与 NOx(以 NO 为例)发生氧化还原反应:
2
考试时间:75 分钟 分值:100 分
。设 N 为阿伏加德罗常数的值,下列说法正确的是
可能用到的相对原子质量:H 1 O 16 A
A.常温下,氧化性:NO>O
一、选择题(每题 3 分,共 45 分) 2
B.该反应中氧化产物与还原产物的个数之比为
C.消耗 30gNO 时转移电子数目为 2N
1. 化学与生产、生活密切相关,下列说法错误的是 A D.可以利用浓氢氧化钠溶液来吸收 NO
A. 制作豆腐时加入硫酸钙等凝固剂,可使豆浆中的蛋白质聚沉 5. 仅用下表提供的试剂和用品,能实现相应实验目的的是
B. 石灰硫黄合剂是一种无机硫制剂,具有杀菌杀虫和保护植物的功能
选项 实验目的 试剂 用品
C. 苯甲酸钠是一种常用的增味剂,能增加食品的鲜味
D. 华为公司自主研发 麒麟芯片是业界领先的手机芯片,其基本材料是单晶硅
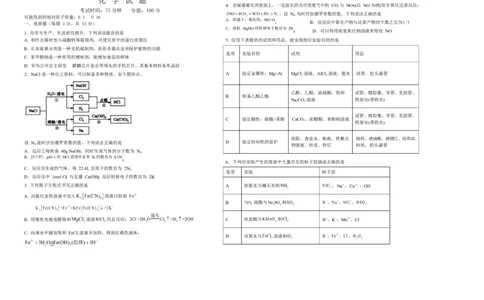
2.NaCl 是一种化工原料,可以制备多种物质,如下图所示。 A 验证金属性:Mg>Al MgCl
2
溶液、AlCl
3
溶液、氨水 试管、胶头滴管
乙醇、乙酸、浓硫酸、饱和 试管、橡胶塞、导管、乳胶管、
B 制备乙酸乙酯
Na CO 溶液 铁架台(带铁夹)
2 3
试管、橡胶塞、导管、乳胶管、
C 验证酸性:碳酸>苯酚 CaCO 、浓醋酸、苯酚钠溶液
3 铁架台(带铁夹)
琼脂、食盐水、酚酞、铁氰化 烧杯、玻璃棒、酒精灯、培养皿、
设 N 是阿伏加德罗常数的值,下列说法正确的是 D 验证锌对铁的保护
A 钾溶液、锌皮、铁钉 砂纸、胶头滴管
A.反应①每制备 40g NaOH,同时生成气体的分子数为 N
A
B.25℃时,pH=1 的 HCl 溶液中含有 H 的数目为 0.1N
+
A 6.下列对实验产生的废液中大量存在的粒子组描述正确的是
C.反应③生成的气体,每 22.4L 含原子的数目为 2N
A
选项 实验 粒子组
D.反应④中 1mol Cl 与足量 Ca(OH) 反应转移电子的数目为 2N
2 2 A
3. 下列离子方程式书写正确的是 A 浓氨水与碱石灰制 、 、 、
A. 向氯化亚铁溶液中加入 溶液以检验 Fe2+
B 硫酸与 制
B. 用惰性电极电解饱和 溶液制 的总反应: C 浓盐酸与 制
C. 向沸水中滴加饱和 FeCl 溶液并加热,得到红褐色液体:
3 D 双氧水与 溶液制7.金属铝冶炼过程如图所示。以下说法错误的是
A. 若 a 在沸水中可生成 e,则 a→f 的反应一定是化合反应
A.已知铝土矿主要成分为 (杂质为 、 等),可以利用以下方案提纯 ,
B. 在 g→f→e→d 转化过程中,一定存在物质颜色的变化
C. 若可用 f 一步转化为 a,则 a 在 Cl 中燃烧一定生成+2 价氯化物
2
D. 若 b 和 d 均能与同一物质反应生成 c,则 a 一定是铝
B. A 选项流程中若将 NaOH 溶液和盐酸两种试剂的加入顺序进行调换,则通入的过量气体成分是 10.能满足下列物质间直接转化关系(部分条件省略),且推理错误的是
CO
2
C. 冰晶石在冶炼铝的过程中的主要作用是降低 的熔点
D. 制备沥青焦的过程中,煤的干馏一步属于化学变化。 A.若 Y 可使品红溶液褪色,则 X 可能为硫或 FeS
2
B.若 W 是乙酸乙酯,Y 可能与新制的银氨溶液反应产生银镜现象
8.最近有科学家发现正丁烷( )脱氢或不完全氧化也可制得 1,3-丁二烯( ),已知
C.若 X 是 ,该转化可用于工业制硝酸
热化学方程式如下: D.若 W 是 Na CO ,则 X 一定 C
2 3
① = ∆H = +123kJ·mol-1 11. 以银锰精矿(主要含 )和氧化锰矿(主要含 )为原料联合提取银
1
和锰的一种流程示意图如下。
② = ∆H = -119 kJ·mol-1
2
③ = ∆H = -57.3kJ·mol-1
3
下列说法正确的是( )
A.由②可知,正丁烷( )的燃烧热为 119 kJ·mol-1
已知:酸性条件下,氧化性: > ;“浸锰”时,主要反应为 ,
B.由①和②可推知: = ∆H
4
= -242 kJ·mol-1
-
同时去除 ;“浸银”时,使用含高浓度 Cl溶液作为浸出剂, 中的 Ag+以 形
将
C. = ∆H = -57.3kJ·mol-1
式浸出。下列说法错误的是
A. 由上述流程可推断:硫化锰的溶解程度大于硫化银
D.同质量的正丁烷( )经过不同反应历程转变为 1,3-丁二烯( )所需要的能量相同
B. 浸锰液中主要金属阳离子有
9. 部分含 或 或 物质的分类与相应化合价关系如图。下列推断合理的是
C. “浸银”所用浸出剂中 与 电离出的 结合,使平衡正向移动,提高 浸出率
D. “沉银”时可加入过量的铁粉作为还原剂,发生反应的离子方程式为
y 化学 试题 第 2页 共 6
页12.丙烯与 HCl 加成生成 CH CHClCH 或 CH CH CH Cl 的能量与反应历程如图所示,下列说法正
3 3 3 2 2
确的是
A.中间体稳定性:A0
2
(反应速率 v=kx,k 为反应速率常数)。 C.Q 点处与 P 点处反应①的平衡常数 K 相等
D.H 的平衡产率由 M 点转变为曲线 a 上任意一点时,要提高水醇比
2
y 化学 试题 第 3页 共 6
页二、非选择题(共 55 分)
16. 钛( Ti)被称为“航空金属”。工业上常利用钛铁矿[主要成分FeTiO (钛酸亚铁),含少量Fe O 、
22 3 2 3
CaO、
SiO 等杂质]为原料生产金属钛和绿矾(FeSO ·7H O)等产品的一种工艺流程如下:
2 4 2
回答下列问题:
(1)仪器 A 的名称为______,实验装置连接顺序为 a→ ef→bc←d,气体 X 为______。
已知:TiO2+易水解生成不溶于水的 H TiO 。
2 3 (2)开始实验时,应最先打开 (填“K ”“K ”或“K ”)。
1 2 3
(1)请写出硫酸浸取过程中发生主要反应的化学方程式: 。
(3)步骤Ⅰ中发生反应的化学方程式为_______。
(2)“滤渣Ⅰ”的主要成分为 (填化学式)。 (4)为分离(NH OH) SO 和(NH ) SO ,向二者混合溶液中加入氨水,生成 NH OH·H O,说明碱性:
3 2 4 4 2 4 2 2
(3)步骤②加入铁粉的目的是 。 NH OH·H O NH ·H O(填“>”、“<”或“=”);再加入甲醇,析出 (填化
2 2 3 2
(4)步骤⑤除生成 TiCl 外,还生成一种可燃性气体,请写出其化学反应方程式 。 学式)晶体,过滤,滤液经减压蒸馏后,向馏出液中加入硫酸,得到硫酸羟胺产品。
4
(5)步骤⑥中镁与 TiCl 高温下反应制备钛时需加保护气,下列不能作为保护气的是______(填字母)。 (5)本实验选择进行减压蒸馏的原因是 。
4
A.Ar B.CO C.N D.He 18. 我国“碳中和”研究领域取得了很大的成效,CO 2 转化为甲醇是实现“碳中和”的重要手段,该
2 2 过
(6)从滤液 X 获得绿矾(FeSO ·7H O)的一系列操作是 过滤,洗涤,干燥。
4 2 程主要发生下列反应:
17. 硫酸羟胺在工业和分析领域有广泛应用。已知硫酸羟胺具有还原性,易溶于水,羟胺 Ⅰ. kJ/mo1
为白色晶体,沸点为 70℃,易溶于水、甲醇,受热易分解。实验室制备硫酸羟胺
Ⅱ. kJ/mol
的流程及装置如图(加热及夹持装置略)。
Ⅲ. kJ/mol
(1)若反应Ⅲ逆反应的活化能为 kJ·mol-1,则正反应的活化能为___________kJ·mol-1(用含 的
式子表示);反应Ⅱ的正、逆反应速率分别表示为: ;
,其中 、 分别为正、逆反应速率常数。升高温度时, ___________
(填“增大”、“减小”或“不变”)。
(2)刚性绝热密闭容器中只发生反应Ⅰ,下列一定能说明反应达到平衡状态的是________(填标
号)。
y 化学 试题 第 4页 共 6
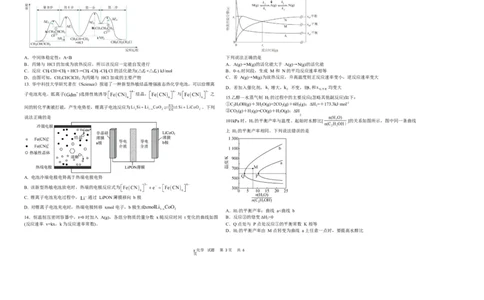
页A.气体混合物的密度不再变化 B. 消耗速率和 CO 生成速率相等 ①图中代表 随温度变化的曲线是___________,CO 转化率以 270℃为分界线呈现先减
2
小后增大趋势的原因是___________。
C.CO 和 的物质的量之比不再变化 D.气体平均相对分子质量不再变化
②达平衡时, , ,则反应Ⅲ的 ___________MPa-2.(结果保留
E.体系的压强不再变化 F.体系的温度不再变化
两位有效数字)
(3)反应Ⅲ在催化剂作用下的反应历程如图所示,一个 分子首先在“ ”表
(5)在“碳达峰”与“碳中和”可持续发展的目标下,作为清洁能源的天然气受到了广泛的关
注。目
面解离成 2 个 (该过程未在历程中标出),随后参与到 的转化过程。 前正在开发用甲烷和氧气合成甲醇: 。已知:
(C 为常数)。根据图中信息,该反应为__________反应(填“放热”或“吸
热”),
该反应在___________(填“高温”或“低温”)下可自发进行。
19.恩曲他滨(H)具有和天然核苷类似的结构,其抗病毒活性引起广泛关注。恩曲他滨的合成路线
如下:
实验发现,原料气中氢气比例较低时,反应速率较慢,结合反应历程分析,可能的原因是
___________。
(4)在某温度下,以 的进气比通入反应管中,维持压强为 3.8MPa 进行上
述三个反应,发生反应,平衡后测得 的转化率 , 的选择性
及 CO 的选择性 随温度(T)的变化关系如图:
已知:① 在制备过程中可以循环利用;
② 。
回答下列问题:
(1)A→B 的反应类型为 ,物质 D 中的官能团名称为 。
(2)在水中的溶解度: ,则设计 B→C→B 的目的为 。
(3)已知 D→E 过程无其他副产物生成,则 D→E 的化学方程式为 。
(4)物质 K 是物质 B 的同分异构体,满足下列条件的 K 的结构简式为 (写出一种即可)。
已知:S( 或 CO) (转化为 或 CO 的 ) (消耗的 ) Ⅰ.1mol 该物质最多能与 反应
y 化学 试题 第 5页 共 6
页Ⅱ.核磁共振氢谱峰面积之比为
(5)参照上述路线,设计如下转化。X 和 Y 的结构简式分别为 和 。
y 化学 试题 第 6页 共 6
页