文档内容
保密★启用前
2024
学年顺德区普通高中高三教学质量检测(二)
化学试题
2025.2
本试卷共8页,20小题,满分100分,考试用时75分钟.
注意事项:1.答卷前,考生务必将自己的姓名、考生号、考场号和座位号填写在答题卡
上.用2B铅笔将试卷类型(B)填涂在答题卡相应位置上.并在答题卡相
应位置上填涂考生号.
2.作答选择题时,选出每小题答案后,用2B铅笔把答题卡对应题目选项的
答案信息点涂黑;如需改动,用橡皮擦干净后,再选涂其他答案.答案不
能答在试卷上.
3,非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卡各题
目指定区域内相应位五上;如需改动,先划掉原来的答案,然后再写上新
答案;不准使用铅笔和涂改液.不按以上要求作答无效.
4.考生必须保持答题卡的整洁.考试结束后,将试卷和答题卡一并交回.
可能用到的相对原子质fib H 1 N 14 0 16 S32 Fe 56 Cu64 As 75 In 115
一、选择题:本大题共16小题,共44分。第I/O小题,每小题2分;第11/6小题,
每小题4分。在每小题列出的四个选项中,只有一项符合题目要求。
1 .佛山黄飞鸿纪念馆记录了一代宗师黄飞鸿的生平事迹。下列有关文物中,主要材质为
硅酸盐的是
A.醒狮狮头 B.中华陶《王者之风》 C.电影宣传单 D.钢铁双刀
2 .化学推动我国社会进步与科技发展,下列说法正确的是
A.次氯酸喷雾消毒机器人实现快速消毒,次氯酸的结构式为H-C1—O
B. N型TOPCon光伏电池工作时,存在电能转换为光能
C. “天舟八号”为空间站送去液氧推进剂,死02与1802互为同位素
D.深海勘探使用的无人潜水器采用的新型镁锂合金比纯镁硬度大、强度高
3 .熊熊火焰,铁韵悠长。冶铁术贯穿历史长河,推动人类发展。下列说法不正确的是
A.修筑冶铁竖炉的耐火材料黏土等,属于有机高分子材料
B.古代冶铁使用的铁矿石,如赤铁矿主要成分是Fe2O3
C.生铁的含碳量比钢高,炼钢过程中发生了化学反应
D.现代炼钢中常用的脱氧剂含单质硅,硅位于元素周期表p区
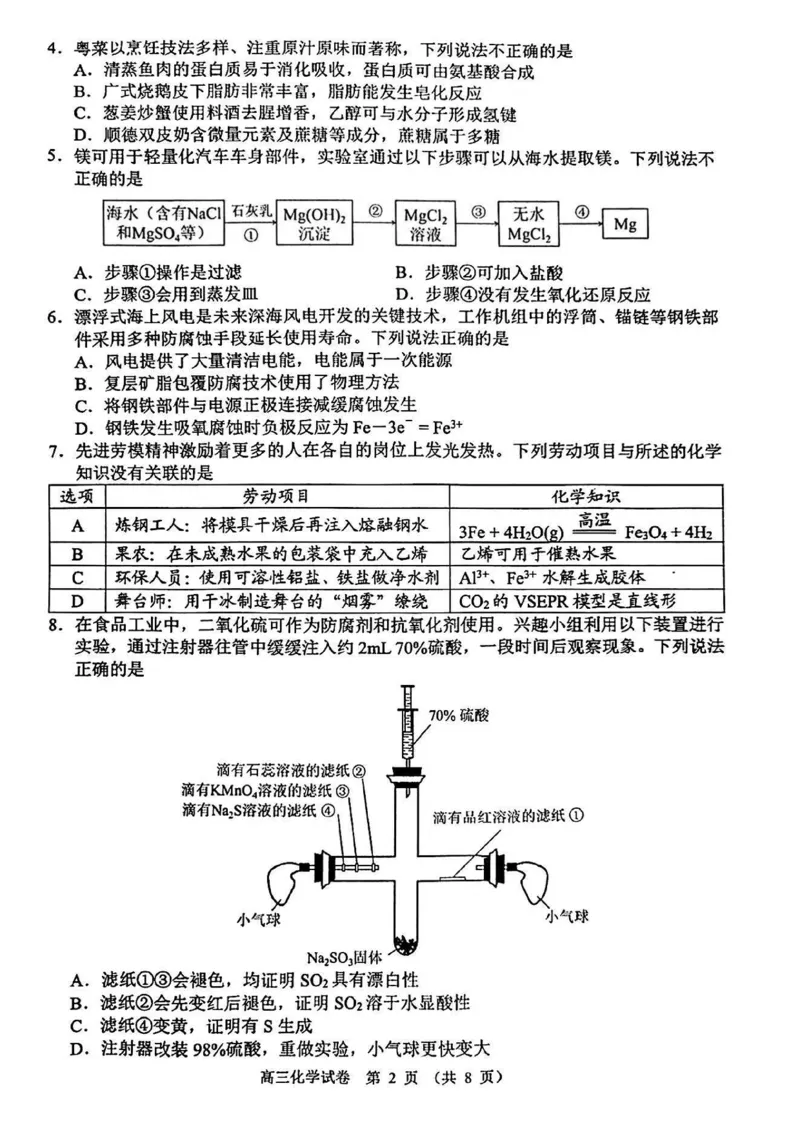
高三化学试卷第1页(共8页)4 .粤菜以烹饪技法多样、注重原汁原味而著称,下列说法不正确的是
A.清蒸鱼肉的蛋白质易于消化吸收,蛋白质可由氨基酸合成
B.广式烧鹅皮下脂肪非常丰富,脂肪能发生皂化反应
C.葱姜炒蟹使用料酒去腥增香,乙醉可与水分子形成氢键
D.顺德双皮奶含微量元索及蔗糖等成分,蔗糖属于多糖
5 .镁可用于轻量化汽车车身部件,实验室通过以下步骤可以从海水提取镁。下列说法不
正确的是
A.步骤①操作是过滤 B.步骤②可加入盐酸
C.步骤③会用到蒸发皿 D.步骤④没有发生氧化还原反应
6 .漂浮式海上风电是未来深海风电开发的关键技术,工作机组中的浮筒、锚链等钢铁部
件采用多种防腐蚀手段延长使用寿命。下列说法正确的是
A.风电提供了大量清洁电能,电能属于一次能源
B.复层矿脂包覆防腐技术使用了物理方法
C.将钢铁部件与电源正极连接减缓腐蚀发生
D.钢铁发生吸氧腐蚀时负极反应为Fe-3e- = Fe3+
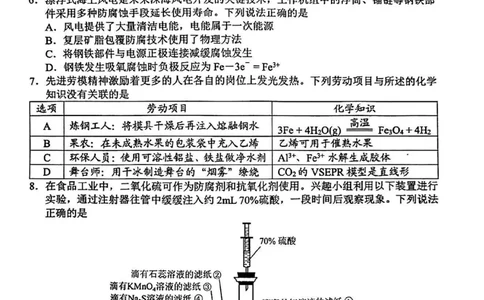
7.先进劳模精神激励着更多的人在各自的岗位上发光发热。下列劳动项目与所述的化学
知识没有关联的是
选项 劳动项目 化学知识
高温
A 炼钢工人:将模具干燥后再注入熔融钢水
3Fe +4H20(g) —— Fe3O4 + 4H2
B 果农:在未成熟水果的包装袋中充入乙烯 乙烯可用于催熟水果
C 环保人员:使用可溶性铝盐、铁盐做净水剂 AF+、Fe3+水解生成胶体 一
D 舞台师:用干冰制造舞台的“烟雾”缭绕 CO2的VSEPR模型是直线形
8.在食品工业中,二氧化硫可作为防腐剂和抗氧化剂使用。兴趣小组利用以下装置进行
实验,通过注射器往管中缓缓注入约2mL 70%硫酸,一段时间后观察现象。下列说法
正确的是
*1^70%硫酸
滴有石芨溶液的滤纸② {邑
滴有KMnC>4溶液的滤纸③\ [T]
滴有Na2s溶液的滤纸④]\ 滴有用红溶液的滤纸①
小气球 小气球
Na2s固体加
A.滤纸①③会褪色,均证明SO2具有漂白性
B.滤纸②会先变红后褪色,证明SCh溶于水显酸性
C.滤纸④变黄,证明有S生成
D.注射器改装98%硫酸,重做实验,小气球更快变大
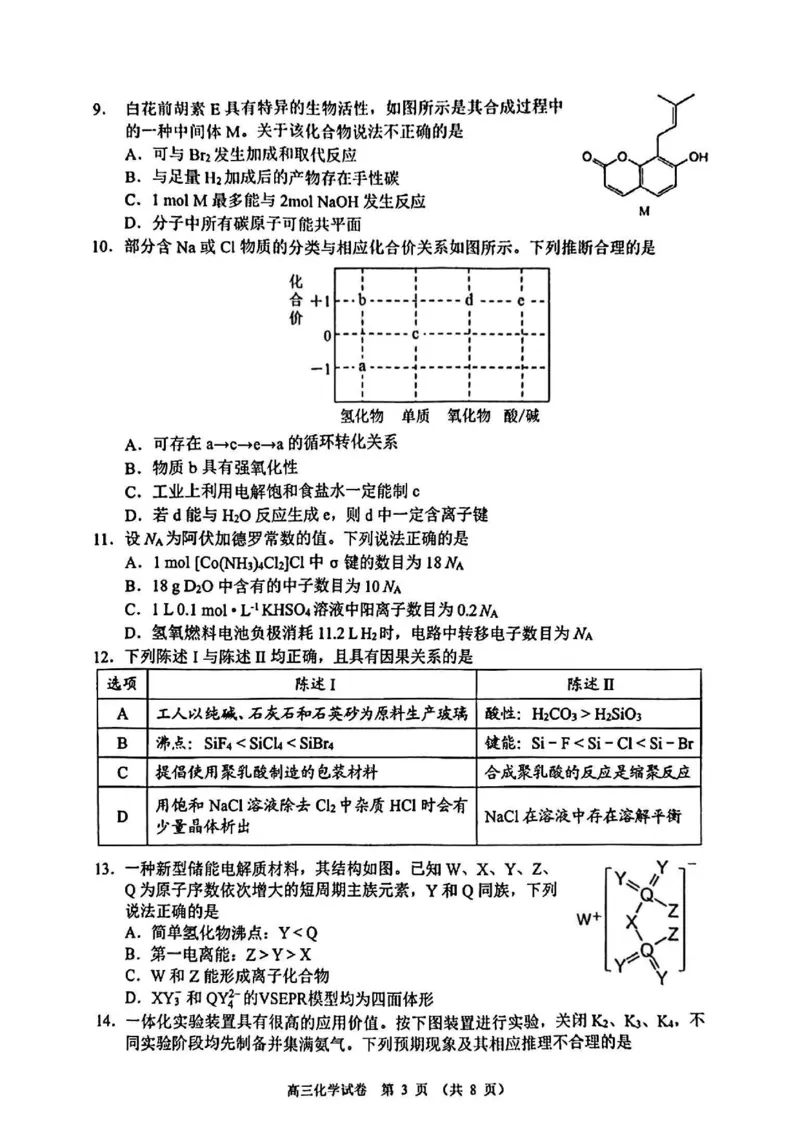
高三化学试卷 第2页(共8页)9.白花前胡素E具有特异的生物活性,如图所示是其合成过程中 J
的一种中间体M.关于该化合物说法不正确的是 /
A.可与B、发生加成和取代反应
B.与足量出加成后的产物存在手性碳 T T T
C. ImolM最多能与2moi NaOH发生反应
D・分子中所有碳原子可能共平面 “
10.部分含Na或CI物质的分类与相应化合价关系如图所示。下列推断合理的是
氢化物 单质 氧化物酸/碱
A.可存在a->c->e-*a的循环转化关系
B.物质b具有强氧化性
C.工业上利用电解饱和食盐水一定能制c
D.若d能与H2O反应生成e,则d中一定含离子键
11.设
Na
为阿伏加德罗常数的值。下列说法正确的是
A. 1 mol [Co(NH3)4Ch]Cl 中。键的数目为 18 M
B. 18gD2O中含有的中子数目为10M
C. 1 L0.1 mol・I/KHSO4溶液中阳离子数目为0.2M
D.氢氧燃料电池负极消耗11.2L%时,电路中转移电子数目为必
12.下列陈述I与陈述II均正确,且具有因果关系的是
选项 陈述I 陈述n
A 工人以纯碱、石灰石和石英砂为原料生产玻璃 酸性:H2CO3>H2SiO3
B 沸点:SiF4Y>X
C. W和Z能形成离子化合物
D. XYi和QY|-的VSEPR模型均为四面体形
14. 一体化实验装置具有很高的应用价值。按下图装置进行实验,关闭R、Kj、K4.不
同实验阶段均先制备并集满氨气。下列预期现象及其相应推理不合理的是
高三化学试卷第3页(共8页)A.制氨时,打开R后滴有酚酰的蒸储水变红即集满氨气,产氨过程爆增
B.加入浓盐酸后产生白烟,说明有NH4cl生成
C.加入水后打开七产生喷泉,说明烧瓶内气压增大
D.打开心,挤压气唧鼓入空气,可使提前加热的的丝持续保持红热
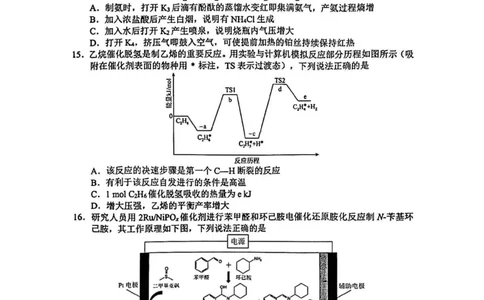
15.乙烷催化脱氢是制乙烯的重要反应。用实验与计算机模拟反应部分历程如图所示(吸
附在催化剂表面的物种用*标注,TS表示过渡态),下列说法正确的是
O TS2
E
/
2
因
送 \ / C2H>H,
O
反应历程
A.该反应的决速步骤是第一个C—H断裂的反应
B.有利于该反应自发进行的条件是高温
C. 1 mol C2H6催化脱氢吸收的热量为e kJ
D.增大压强,乙烯的平衡产率增大
16.研究人员用2RWNiPOx催化剂进行苯甲醛和环己胺电催化还原胺化反应制型苇基环
己股,其工作原理如下图,下列说法正确的是
A.辅助电极的电势高于Pt电极的电势
B.有机物M中C、N原子的杂化方式均相同
C.电催化过程中不断消耗H+
D.理论上每生成1 mol N-羊基环己胺,Pt电极上有1 mol《 被氧化
高三化学试卷 第4页(共8页)二、非选择题:本题共4小题,共56分。
17. (14分)硝酸铁具有较强的氧化性,可用于制备高性能电极材料。某学习小组对Fe(NCh)3
溶液与Cu的反应进行探究。
(1)配制一定浓度的Fe(NO3)3溶液。
实验室配制 480 mL 0.2 mol-L'1 Fe(NO3)3 溶液,需要称取 Fe(NOj)3*9H2O(M = 404
g/mol)晶体 g«需用到的玻璃仪器有玻璃棒、烧杯、量筒、胶头滴管、
(填仪器名称)。
(2)探究Fe(NO3)3溶液中与Cu反应的微粒。
查阅资料:Fe(NCh)3溶液呈酸性。常温下不同浓度Fe(NCh)3溶液中的H+浓度和pH
如下表:
c[Fe(NO3)3] / (mobL1) c(H+)/ (mobL4) PH
0.100 0.0315 1.50
2.000 0.235 0.63
①该学习小组的同学对Fe(NO3)3溶液中与Cu反应的微粒提出了如下假设:
假设 1 F/+ 将 Cu 氧化:2Fe3+ + Cu = Cu2++ 2Fd+
假设2酸性条件下NO;将Cu氧化: (填离子方程式)。
②初步实验
实验操作 实验现象
步骤 i.取 10mLO.lmobL1 的 Fe(NO3)3 溶•液子 溶液由粽黄色逐渐变为蓝绿色,
试管中,向其中加入1g Cu粉并不断振荡 未见气泡产生
甲
步骤ii.取反应后的上层清液于试管中,向其
中加入几滴___________ 溶液
取10 mL 2 mobL'1 Fe(NO3)3溶液于试管中,向
乙 溶液由棕黄色逐渐变为深棕色
其中加入IgCu粉,振荡,静受
③分析讨论甲同学根据实验现象判断,假设1成立。乙同学认为证据不足。
(3)探究Fe(NO3)3溶液中与Cu反应的过程。
①乙同学查阅相关资料:a.铜粉几乎不与WO.3moi・日稀硝酸反应;b. Fe»会与
NO结合生成深棕色的[Fe(NO)]2+ , [Fe(NO)]2+会缓慢分解得到Fe2+和NO。他认
为:在Fe(NCh)3溶液与Cu反应的过程中,FeJ\ NOi'均参与了反应,并对该过
程提出了猜想:
反应过程 I: 2Fe3++Cu = Cu2++ 2F/+
反应过程H: (填离子方程式)
反应过程 Ills [Fe(NO)]2+ = Fe2++ NOf
即认为Fe2+能促使铜粉与W0.3mol/L稀硝酸反应。
②验证猜想
实验操作 实验现象
在100mL0.235moi・LT稀硝酸中加入IgCu粉,振荡 无明显现象
在100mL0.235 mobL-1稀硝酸中加入Ig Cu粉和0.05g_______
得到深棕色溶液
固体,振荡
③实验小结该实验现象验证了乙同学的猜想。
④实验讨论 在Fe(NO3)3溶液与Cu反应的过程中,小组检测到了浓度不低的Fe3+,
请尝试从反应I和II的速率角度解释原因_。
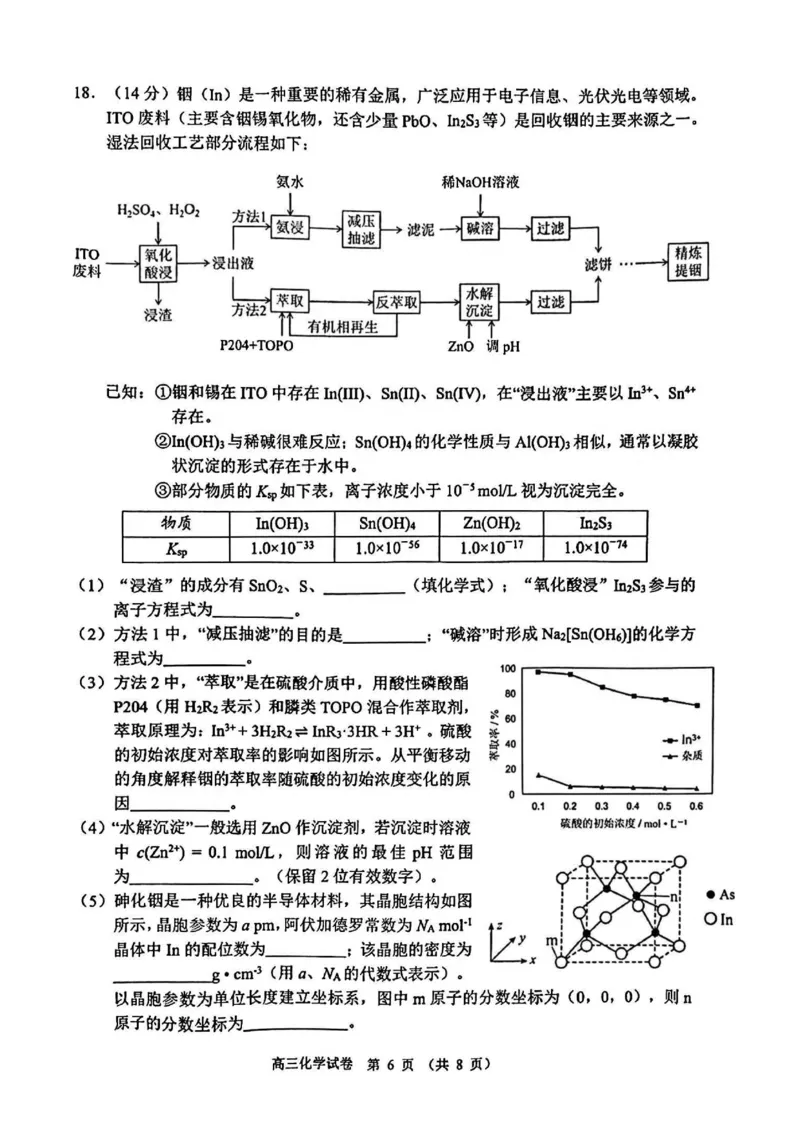
高三化学试卷 第5页(共8页)18. (14分)钿(In)是一种重要的稀有金属,广泛应用于电子信息、光伏光电等领域。
ITO废料(主要含锢锡氧化物,还含少量PbO、In2s3等)是回收钿的主要来源之一。
湿法回收工艺部分流程如下:
氨水 稀NaOH溶液
P204+TOPO ZnO 调 pH
已知:①锢和锡在ITO中存在In(in)、Sn(II)、Sn(IV),在“浸出液”主要以加升、Sn"
存在。
②In(0H)3与稀碱很难反应;Sn(OH)4的化学性质与Al(0H)3相似,通常以凝胶
状沉淀的形式存在于水中。
③部分物质的脑如下表,离子浓度小于lOrmoVL视为沉淀完全。
物质 In(OH)3 Sn(OH)4 Zn(OH)2 In2s3
Ksp 1610-33 1.0x10-56 l.OxlO-17 1610-74
(1) “浸渣”的成分有SMh、S、 (填化学式);“氧化酸浸” 1112s3参与的
离子方程式为
(2)方法1中,“减压抽滤”的目的是; “碱溶”时形成Na2[Sn(OH6)]的化学方
程式为 O
(3)方法2中,“萃取”是在硫酸介质中,用酸性磷酸酯
P204 (用H2R2表示)和麟类TOPO混合作萃取剂,
萃取原理为:In3++3H2R2=InRy3HR + 3H+。硫酸
的初始浓度对萃取率的影响如图所示。从平衡移动
的角度解释锢的萃取率随硫酸的初始浓度变化的原
因 0
(4) “水解沉淀”一般选用ZnO作沉淀剂,若沉淀时溶液
中c(Zn2+) = 0.1 mol/L,则溶液的最佳pH范围
为 o (保留2位有效数字)。
(5)碑化锢是一种优良的半导体材料,其晶胞结构如图
所示,晶胞参数为。pm,阿伏加德罗常数为 Na moN
晶体中In的配位数为;该晶胞的密度为
g・cnr3 (用〃、为的代数式表示).
以晶胞参数为单位长度建立坐标系,图中m原子的分数坐标为(0, 0, 0),则n
原子的分数坐标为
高三化学试卷 第6页(共8页)19. (14分)研究烟气的脱硫、脱硝对防治空气污染、促进社会可持续发展具有重要意义.
I.工业生产中可利用CO从燃煤烟气中脱硫.
已知:CO(g)和S⑸的燃烧热分别为283.0kJ/mol、296.8 kJ/mol
(1)则脱硫反应 SCh(g) +2CO(g) = S(s) +282(g)的反应热△,=。
II. NH3选择性催化还原脱硝(NH3-SCR)是去除NO,的有效方法,其主要反应有
i . 4NH3(g) + 6NO(g) = 5N2(g) + 6H2O(1)
ii. 8NH3(g) + 6NO2(g) = 7N2(g) + 12H2O(1)
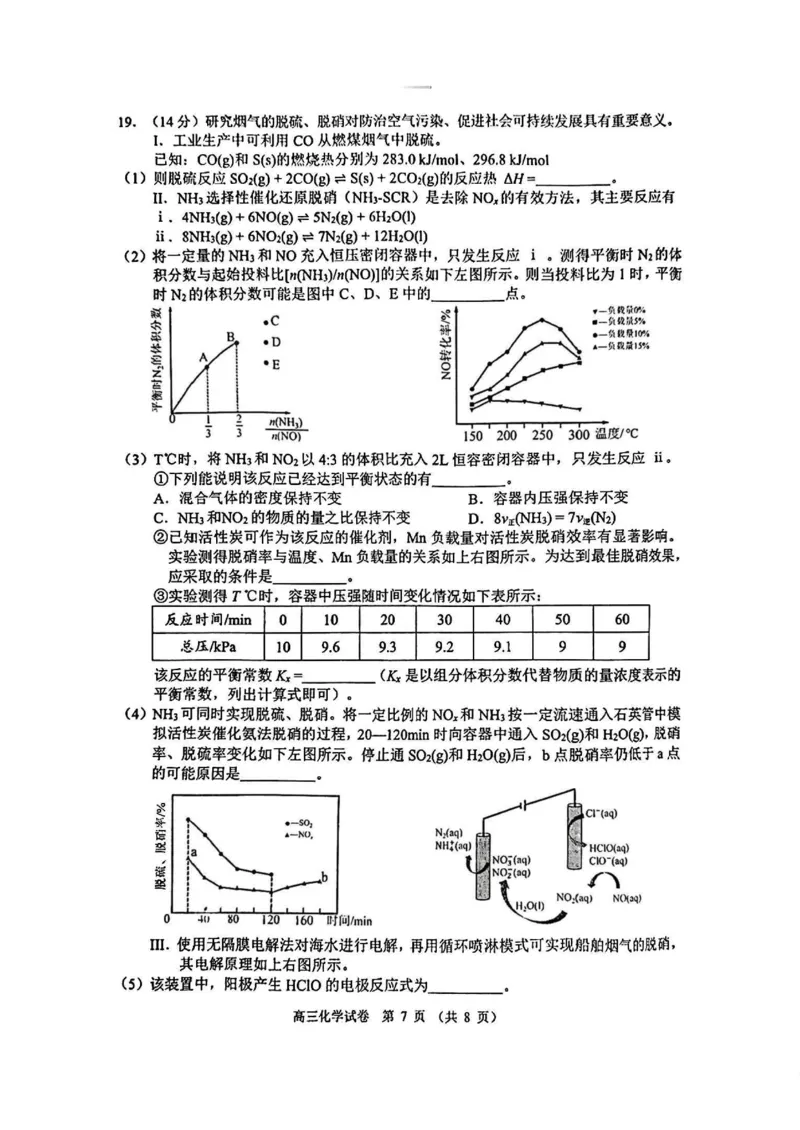
(2)将一定量的NH3和NO充入恒压密闭容器中,只发生反应i 0测得平衡时Nz的体
积分数与起始投料比S(NH3)/〃(NO)]的关系如下左图所示。则当投料比为1时,平衡
时N2的体积分数可能是图中C、D、E中的______ 点。
(3) TC时,将NH3和NO?以4:3的体积比充入2L恒容密闭容器中,只发生反应行。
①下列能说明该反应已经达到平衡状态的有°
A.混合气体的密度保持不变 B.容器内压强保持不变
C. NH3和NO2的物质的量之比保持不变 D. 8vI(NH3) = 7va>(N2)
②已知活性炭可作为该反应的催化剂,Mn负载量对活性炭脱硝效率有显著影响。
实验测得脱硝率与温度、Mn负载量的关系如上右图所示。为达到最佳脱硝效果,
应采取的条件是。
③实验测得TC时,容器中压强随时间变化情况如下表所示:
反应时间/min 0 10 20 30 40 50 60
总压/kPa 10 9.6 9.3 9.2 9.1 9 9
该反应的平衡常数及=___________(%是以组分体积分数代替物质的量浓度表示的
平衡常数,列出计算式即可)。
(4) NH3可同时实现脱硫、脱硝。将一定比例的NO*和NH3按一定流速通入石英管中模
拟活性炭催化氨法脱硝的过程,20-120min时向容器中通入SCh(g)和H2O(g),脱硝
率、脱硫率变化如下左图所示。停止通SCh(g)和H2O(g)后,b点脱硝率仍低于a点
的可能原因是。
%
/
史
在
窖
,
海
垩
III.使用无隔膜电解法对海水进行电解,再用循环喷淋模式可实现船舶烟气的脱硝,
其电解原理如上右图所示。
(5)该装置中,阳极产生HC1O的电极反应式为 。
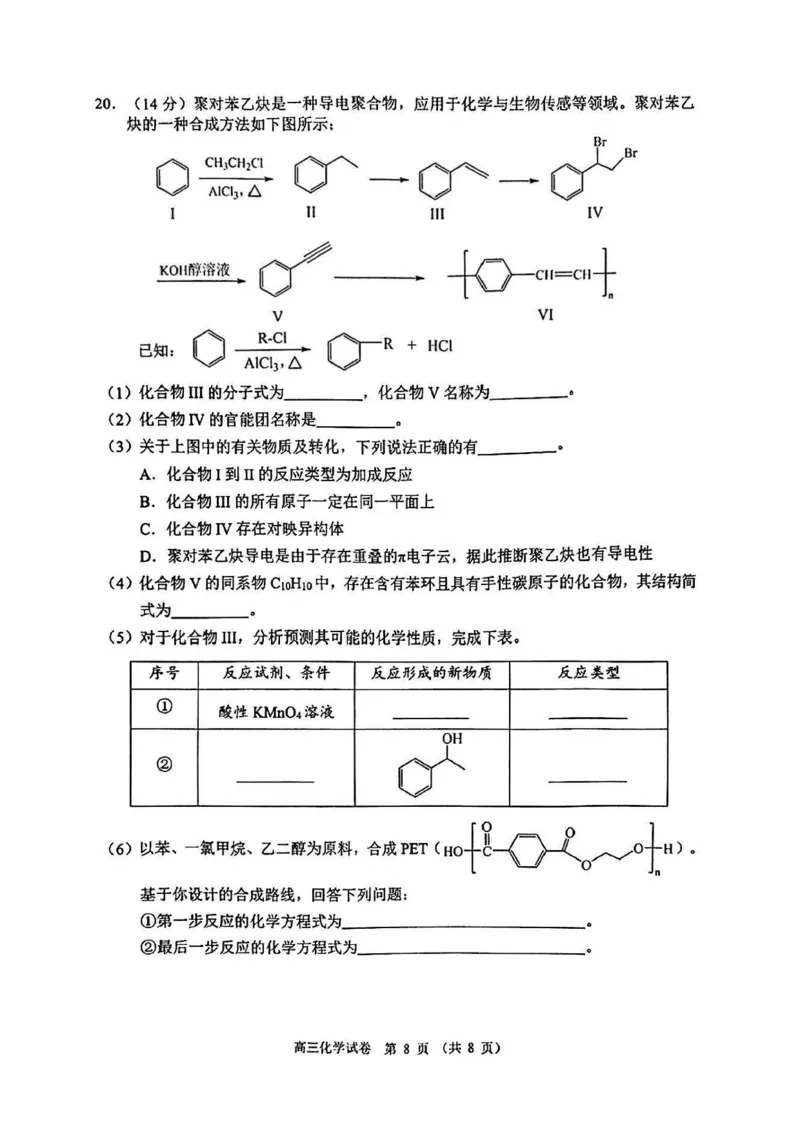
高三化学试卷第7页(共8页)20. (14分)聚对苯乙烘是一种导电聚合物,应用于化学与生物传感等领域。聚对苯乙
快的一种合成方法如下图所示:
(1)化合物III的分子式为,化合物V名称为__________。
(2)化合物IV的官能团名称是 o
(3)关于上图中的有关物质及转化,下列说法正确的有。
A.化合物I到n的反应类型为加成反应
B.化合物ni的所有原子一定在同一平面上
c,化合物IV存在对映异构体
D.聚对苯乙块导电是由于存在重叠的兀电子云,据此推断聚乙块也有导电性
(4)化合物V的同系物CioHio中,存在含有苯环且具有手性碳原子的化合物,其结构简
式为。
(5)对于化合物III,分析预测其可能的化学性质,完成下表。
序号 反应试剂、条件 反应形成的新物质 反应类型
①
酸性KMnO4溶液
— —
OH
②
(6)以苯、一氯甲烷、乙二醇为原料,合成PET o1h) o
基于你设计的合成路线,回答下列问题:
①第一步反应的化学方程式为______________________________。
②最后一步反应的化学方程式为•
海三化学试卷 第8页(共8页)2024学年顺德区普通高中高三教学质量检测(二)
化学参考答案
一、选择题:本大题共16小题,共44分。第170小题,每小题2分;第1176小题,每小题4分。
题号 1 2 3 4 5 6 7 8
答案 B D A D D B D C
题号 9 10 11 12 13 14 15 16
答案 C A A D C C B D
二、非选择题:本题共4小题,共56分。
17. (14 分)
(1) 40.4 (1 分) 500mL 容量瓶(1 分)
(2) 3Cu + 2NO3+ 8H+ = 3Cu2+ + 2NO t + 4H2O (2 分)
K3[Fe(CN)6] (2分) 有蓝色沉淀生成(2分)
(3) 4Fe2+ + NOr+ 4H+ = 3Fe3+ + [Fe(NO)]2+ + 2H2O (2 分)
FeSO4 (2 分)
反应过程U是快反应,反应过程I是慢反应,生成Fe升的速率大于消耗Fe3+的速率(2分)
18. (14 分)
(1) PbSO4 (1 分)1112s3 + 3H2O2+ 6H+ = In3-+ S + 6H2O (2 分)
(2)加快凝胶状沉淀Sn(OH)4的过滤速度(1分)
Sn(OH)4 + 2NaOH =Na2[Sn(OH)6] (2 分)
(3)当硫酸初始浓度较低时,随着硫酸浓度增大,溶液H-浓度增大,In3+ + 3H2R2 InR3-3HR + 3H+平
衡逆向移动,In3+的萃取率减小(2分)
(4) 4.7 < pH <6.0
4x190 分 春"分,
(5) 4 (1 分)
X Na X 10 - 30
19. (14 分)
(1) -269.2 kJ/mol(2分)
(2) E (2 分)
(3)① AB (2 分) ②250℃,负载量10% (2分) ③ (2分)
(4) SO2与H2O、NH3反应生成的钱盐附着在催化剂表面,使催化剂活性下降,脱硝率降低(2分)
(5) Cr-2e- + H2O= HC1O + H+ (2 分)
20. (14 分)
(1)C8H8 (1分)苯乙焕(1分)
(2)碳漠键 (1分)
(3) CD (2 分)
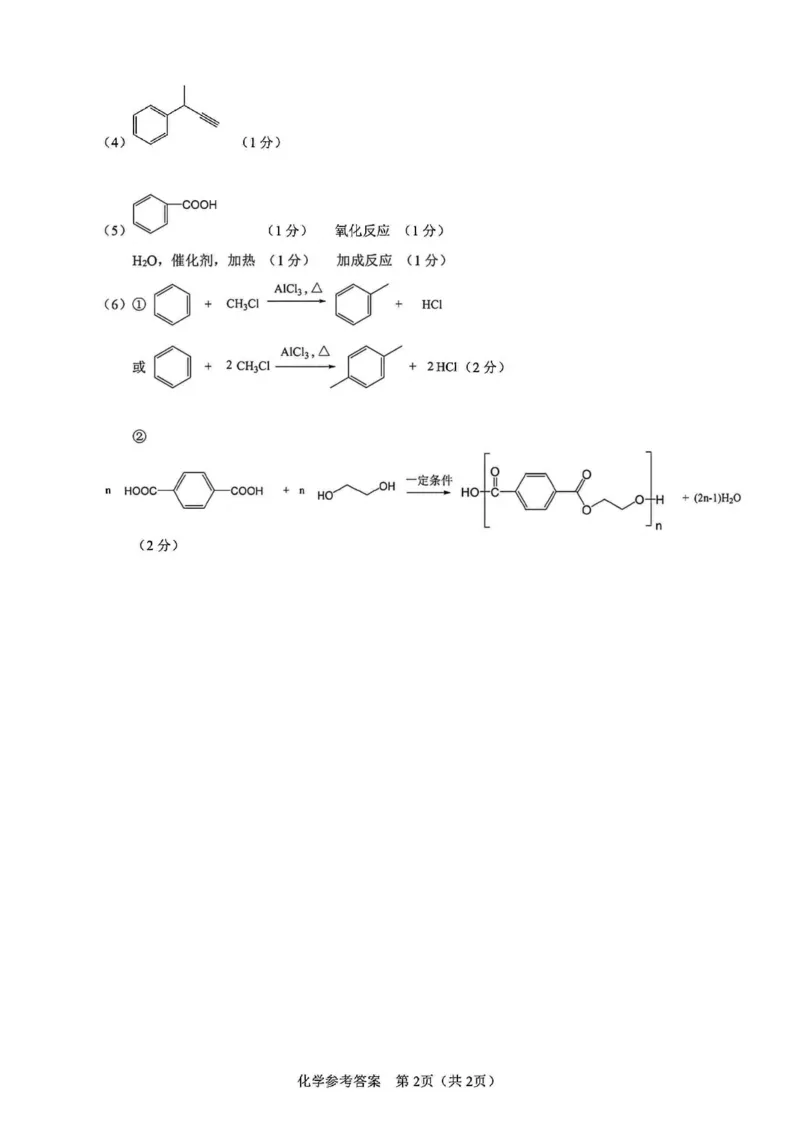
化学参考答案第1页(共2页)(4) (1分)
(1分)氧化反应(1分)
(2分)
(2分)
化学参考答案 第2页(共2页)