文档内容
德阳市高中2022级质量监测考试(二)
化 学 试 卷
说明:
1.本试卷分第Ⅰ卷和第Ⅱ卷,共8页。考生作答时,须将答案答在答题卡上,在本试卷、草稿
纸上答题无效。考试结束后,将答题卡交回。
2.本试卷满分100分,75分钟完卷。
可能用到的相对原子质量:H—1 N—14 O—16 Na—23 S—32 Fe—56 Ni—59
第Ⅰ卷(选择题 共45分)
一、选择题(本题包括15个小题,每小题3分,共45分,每小题只有一个选项符合题意)
1.材料是人类赖以生存和发展的物质基础,下列有关材料的描述错误的是
A.碳化硅是传统无机非金属材料
B.航天飞行材料硬铝属于合金
C.冠醚与碱金属离子形成的超分子材料是混合物
D.宇宙飞船外壳材料酚醛树脂是有机高分子化合物
2.下列有关生物有机分子说法错误的是
A.核糖和脱氧核糖都是戊糖
B.淀粉和纤维素均不能发生银镜反应
C.酶分子通过折叠、螺旋或缠绕形成活性空间
D.由2~10个单糖通过糖苷键连接而成的分子称为多糖
3.下列化学用语或图示表示错误的是
A.2-甲基-3-乙基戊烷的键线式:
B.NH
4
Cl的电子式:NH+[ ]-
4
C.乙炔的空间填充模型:
D.CO 分子的结构式:O=C=O
2
4.一定条件下,有机物X、Y的转化关系如右下图,下列说法正确的是
A.X分子中所有原子一定共平面
B.X不能使酸性高锰酸钾溶液褪色
C.X转化为Y经历了加成和消去两步反应
D.X和Y的核磁共振氢谱均有5组峰
化学试卷 第 页(共 页)
1 85.硫及其化合物的部分转化关系如图。设N 为阿伏加德罗常数的值,下列说法错误的是
A
A.标准状况下,11.2LHS中含有质子数目为9N
2 A
B.100mL0.1mol/LNaSO 溶液中,Na+数目为0.02N
2 3 A
C.反应 每消耗6.4gSO,生成物中硫原子数目为0.3N
① 2 A
D.反应 每生成1molSO2-,转移电子数目为2N
② 3 A
6.下列过程对应的方程式正确的是
A.炽热的铁水注入未干燥的模具: =高==温===
3Fe + 4H2O(g) Fe3O4 + 4H2
B.磁性氧化铁溶于稀硝酸:FeO+6H+=2Fe3++3HO
2 3 2
C.用稀盐酸清洗水垢中的Mg(OH):OH-+H+=HO
2 2
D.向亚硫酸钠溶液中通入少量氯气:SO2-+Cl+HO=HSO-+Cl-+HClO
3 2 2 3
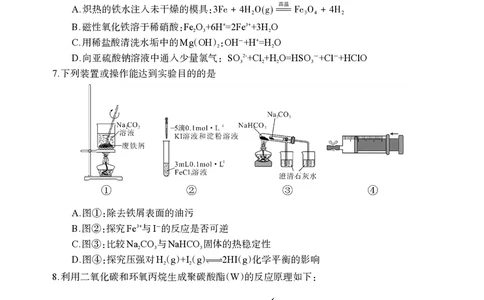
7.下列装置或操作能达到实验目的的是
A.图 :除去铁屑表面的油污
①
B.图 :探究Fe3+与I-的反应是否可逆
②
C.图 :比较NaCO 与NaHCO 固体的热稳定性
③ 2 3 3
D.图
④
:探究压强对H(
2
g)+I(
2
g)2H(I g)化学平衡的影响
8.利用二氧化碳和环氧丙烷生成聚碳酸酯(W)的反应原理如下:
下列说法错误的是
A.Y和环氧乙烷互为同系物
B.Z可以发生水解反应生成CO
2
C.X的一氯代物有五种(含顺反异构)
D.聚合物W属于可降解高分子材料
化学试卷 第 页(共 页)
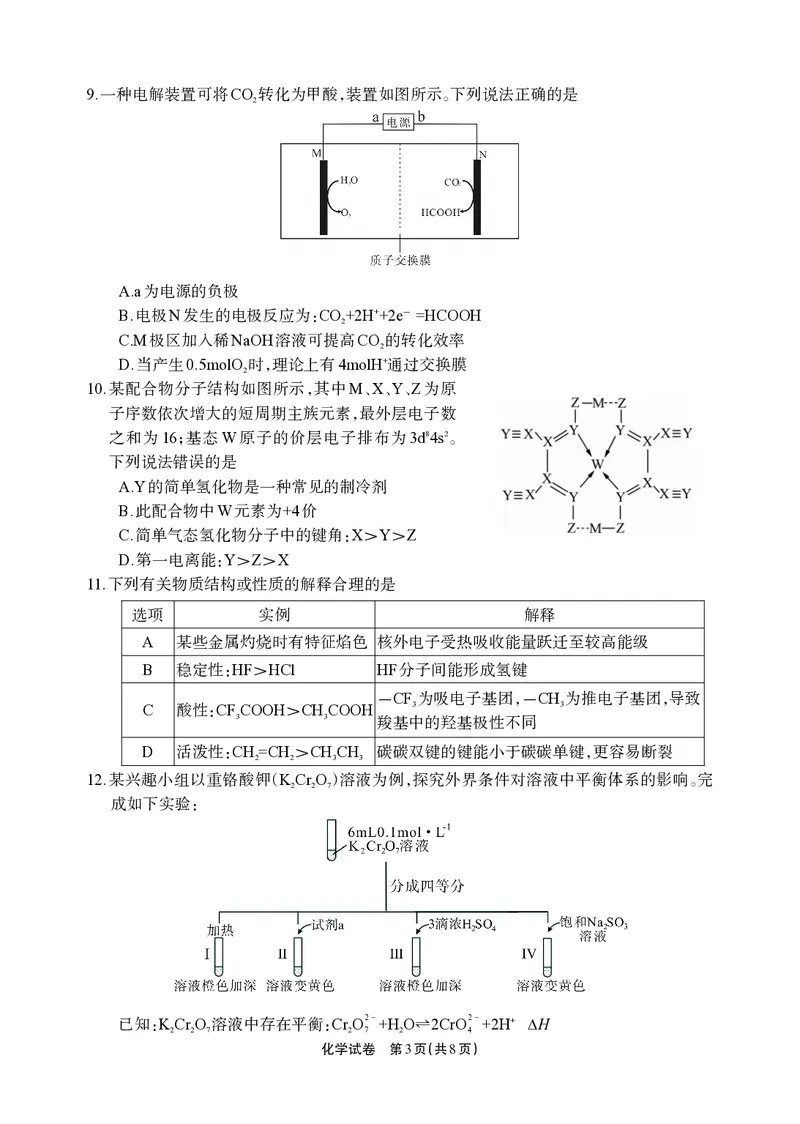
2 89.一种电解装置可将CO 转化为甲酸,装置如图所示。下列说法正确的是
2
A.a为电源的负极
B.电极N发生的电极反应为:CO+2H++2e-=HCOOH
2
C.M极区加入稀NaOH溶液可提高CO 的转化效率
2
D.当产生0.5molO 时,理论上有4molH+通过交换膜
2
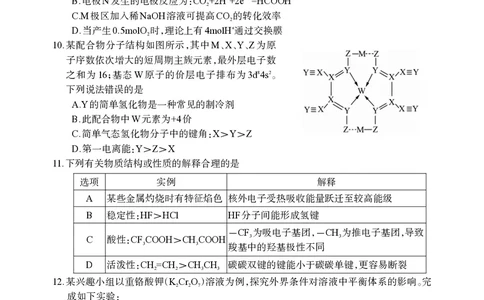
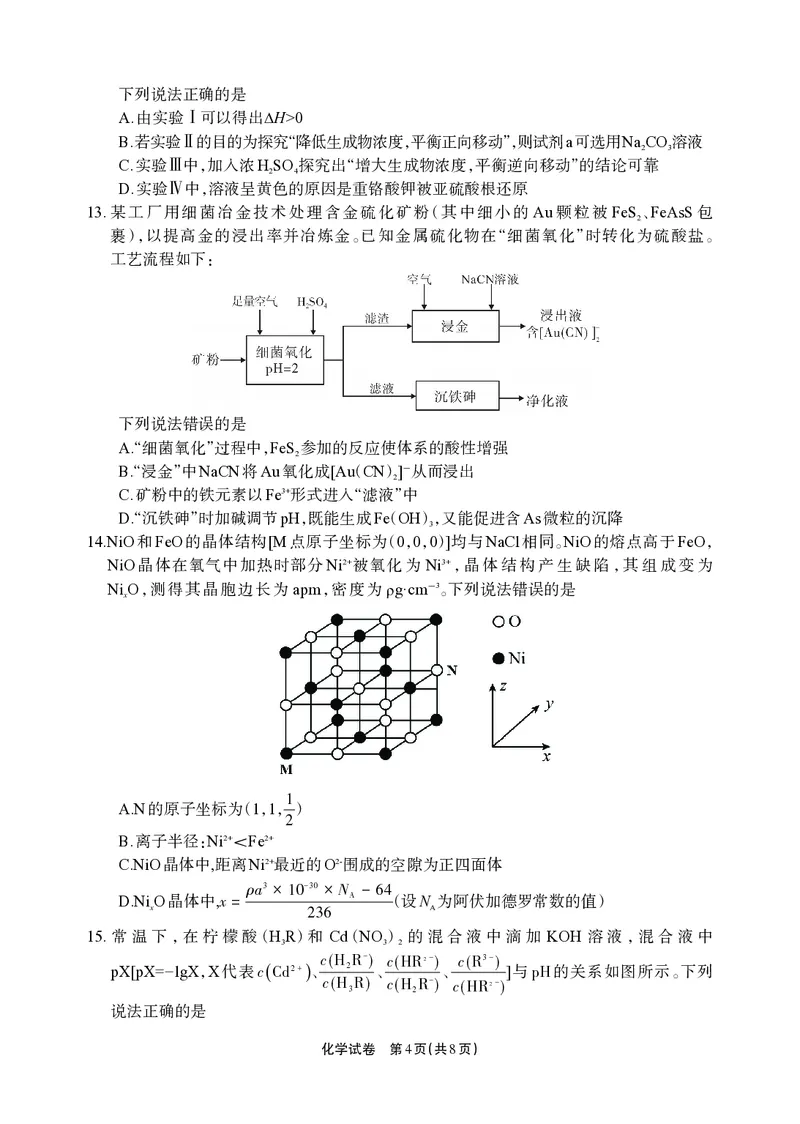
10.某配合物分子结构如图所示,其中M、X、Y、Z为原
子序数依次增大的短周期主族元素,最外层电子数
之和为16;基态W原子的价层电子排布为3d84s2。
下列说法错误的是
A.Y的简单氢化物是一种常见的制冷剂
B.此配合物中W元素为+4价
C.简单气态氢化物分子中的键角:X>Y>Z
D.第一电离能:Y>Z>X
11.下列有关物质结构或性质的解释合理的是
选项 实例 解释
A 某些金属灼烧时有特征焰色 核外电子受热吸收能量跃迁至较高能级
B 稳定性:HF>HCl HF分子间能形成氢键
-CF 为吸电子基团,-CH 为推电子基团,导致
C 酸性:CFCOOH>CHCOOH 3 3
3 3 羧基中的羟基极性不同
D 活泼性:CH=CH>CHCH 碳碳双键的键能小于碳碳单键,更容易断裂
2 2 3 3
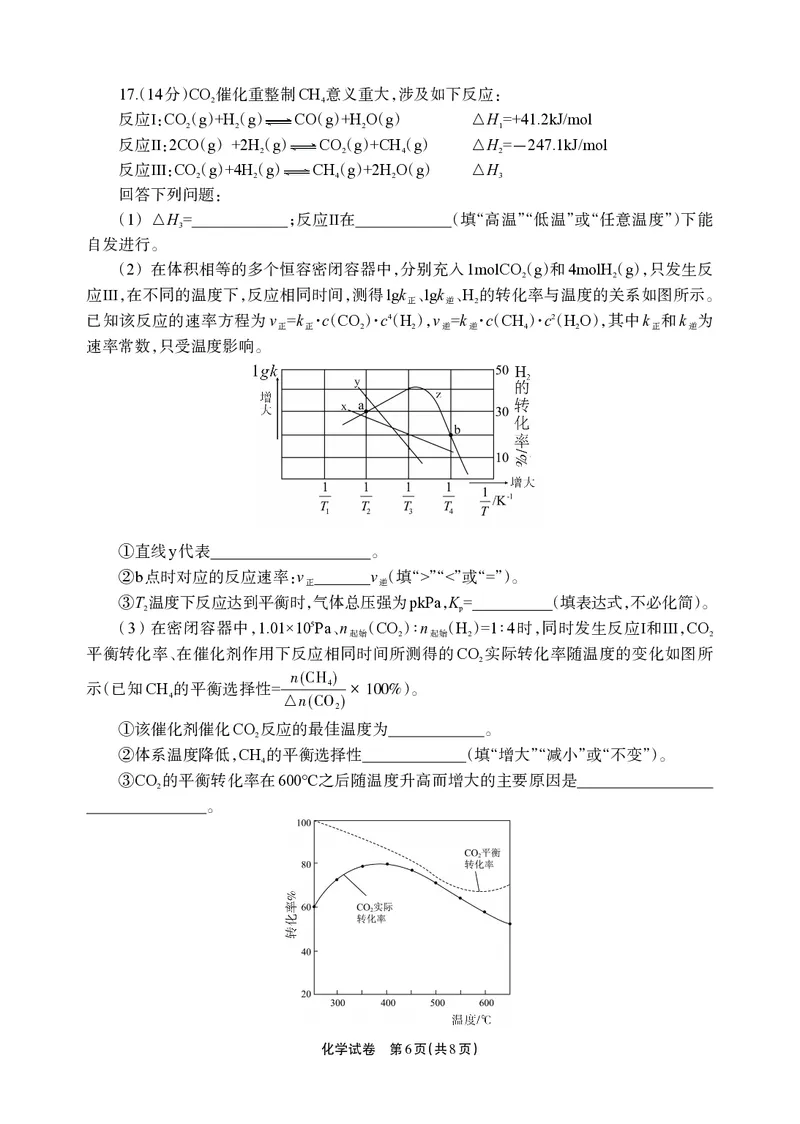
12.某兴趣小组以重铬酸钾(KCrO)溶液为例,探究外界条件对溶液中平衡体系的影响。完
2 2 7
成如下实验:
已知:KCrO 溶液中存在平衡:CrO2-+HO 2CrO2-+2H+ ∆H
2 2 7 2 7 2 ⇌ 4
化学试卷 第 页(共 页)
3 8下列说法正确的是
A.由实验 可以得出∆H>0
Ⅰ
B.若实验 的目的为探究“降低生成物浓度,平衡正向移动”,则试剂a可选用NaCO 溶液
Ⅱ 2 3
C.实验 中,加入浓HSO 探究出“增大生成物浓度,平衡逆向移动”的结论可靠
Ⅲ 2 4
D.实验 中,溶液呈黄色的原因是重铬酸钾被亚硫酸根还原
Ⅳ
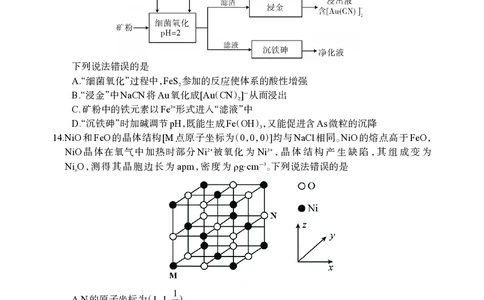
13.某工厂用细菌冶金技术处理含金硫化矿粉(其中细小的Au颗粒被FeS、FeAsS包
2
裹),以提高金的浸出率并冶炼金。已知金属硫化物在“细菌氧化”时转化为硫酸盐。
工艺流程如下:
下列说法错误的是
A“. 细菌氧化”过程中,FeS 参加的反应使体系的酸性增强
2
B“. 浸金”中NaCN将Au氧化成[Au(CN)]-从而浸出
2
C.矿粉中的铁元素以Fe3+形式进入“滤液”中
D“. 沉铁砷”时加碱调节pH,既能生成Fe(OH),又能促进含As微粒的沉降
3
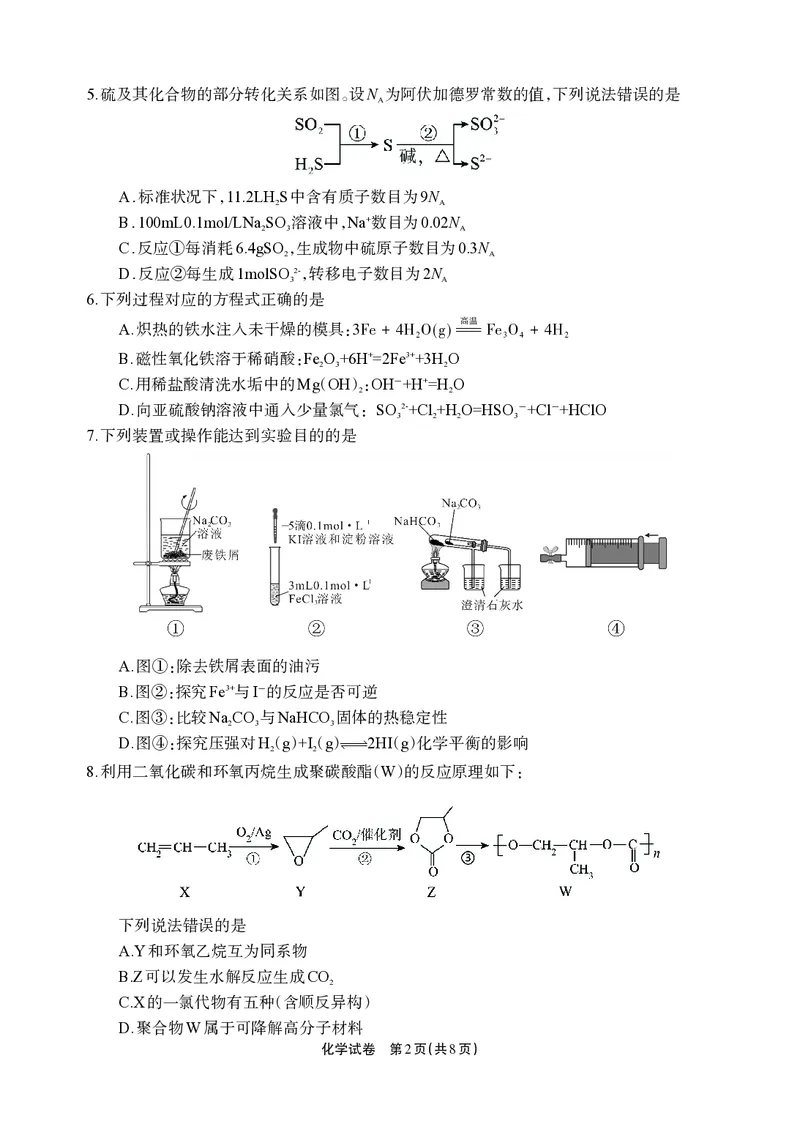
14.NiO和FeO的晶体结构[M点原子坐标为(0,0,0)]均与NaCl相同。NiO的熔点高于FeO,
NiO晶体在氧气中加热时部分Ni2+被氧化为 Ni3+,晶体结构产生缺陷,其组成变为
NiO,测得其晶胞边长为apm,密度为ρg·cm-3。下列说法错误的是
x
A.N的原子坐标为(1,1,1)
2
B.离子半径:Ni2+<Fe2+
C.NiO晶体中,距离Ni2+最近的O2-围成的空隙为正四面体
ρa N
3 -30
D.NiO晶体中,x × 10 × A - 64(设N 为阿伏加德罗常数的值)
x = A
236
15. 常温下,在柠檬酸(HR)和 Cd(NO) 的混合液中滴加 KOH 溶液,混合液中
3 3 2
pX[pX=-lgX,X代表c( 2+ )、 c (H2R - )、 c (HR 2- )、 c (R 3- ) ]与 的关系如图所示。下列
Cd c (H3R) c (H2R - ) c (HR 2- ) pH
说法正确的是
化学试卷 第 页(共 页)
4 8c( )
3-
A.L 代表p[ R ]与pH的关系 B.c点溶液中有Cd(OH)沉淀
1 c( ) 2
2-
HR
C.d点的坐标为(4.5,2) D.0.1mol/LNaHR溶液呈酸性
2
第Ⅱ卷(非选择题 共55分)
二、填空题(共58分)
16(. 14分)蔗糖铁是一种快速有效的补铁剂,某小组设计如下实验步骤制备蔗糖铁并测
定其中铁含量。
步骤1:向FeCl 溶液中缓慢滴加NaCO 溶液,边加边搅拌,控制温度在20℃左右,反应
3 2 3
1h后,过滤,得Fe(OH)原胶泥;
3
步骤2:用蒸馏水洗涤Fe(OH)原胶泥多次,得到Fe(OH) 胶泥;
3 3
步骤3:配制蔗糖溶液,并用NaOH溶液调节其pH(生成D-葡萄糖二酸根离子),再与
Fe(OH)胶泥混合加热,过滤,得到蔗糖铁原液;
3
步骤4:量取5.00mL蔗糖铁原液,加入物质X,加热至微沸,冷却后滴加KMnO 溶液,至
4
溶液恰好显粉红色并能持续5s(恰好除去溶液中的还原性物质)。再依次加入物质X与KI试
液(过量)各30mL,蒸馏水30mL和淀粉溶液2mL,用0.1mol/LNaSO 标准液滴定,消耗
2 2 3
NaSO 标准液体积为17.90mL(已知:I+2NaSO=2NaI+NaSO)。
2 2 3 2 2 2 3 2 4 6
回答下列问题:
(1)“步骤1”中控制反应温度的方法为 。
(2)“步骤1”中发生反应的离子方程式为 。
(3)“步骤2”中检验Fe(OH)原胶泥已洗涤干净的方法为
3
。
(4)“步骤4”中物质X为 。
(5)“步骤4”中滴定终点的现象为 。
(6)蔗糖铁样品中Fe元素的含量为 mg/mL(保留一位小数)。
(7)实验中出现下列情况,可能使蔗糖铁中铁含量测定结果偏大的是 (填标号)。
a.KI溶液因接触空气部分变质
b.用NaSO 标准液滴定至终点时俯视读数
2 2 3
c.滴加KMnO 溶液后,溶液呈粉红色并持续5s以上
4
化学试卷 第 页(共 页)
5 817(. 14分)CO 催化重整制CH 意义重大,涉及如下反应:
2 4
反应Ⅰ:CO(g)+H(g) CO(g)+HO(g) H=+41.2kJ/mol
2 2 2 △ 1
反应Ⅱ:2CO(g)+2H(g) CO(g)+CH(g) H=-247.1kJ/mol
2 2 4 △ 2
反应Ⅲ:CO(g)+4H(g) CH(g)+2HO(g) H
2 2 4 2 △ 3
回答下列问题:
(1) H= ;反应Ⅱ在 (填“高温”“低温”或“任意温度”)下能
△ 3
自发进行。
(2)在体积相等的多个恒容密闭容器中,分别充入1molCO(g)和4molH(g),只发生反
2 2
应Ⅲ,在不同的温度下,反应相同时间,测得lgk 、lgk 、H 的转化率与温度的关系如图所示。
正 逆 2
已知该反应的速率方程为v =k ·c(CO)·c(4 H),v =k ·c(CH)·c(2 HO),其中k 和k 为
正 正 2 2 逆 逆 4 2 正 逆
速率常数,只受温度影响。
直线y代表 。
①
b点时对应的反应速率:v v (填“>”“<”或“=”)。
② 正 逆
T 温度下反应达到平衡时,气体总压强为pkPa,K= (填表达式,不必化简)。
③ 2 p
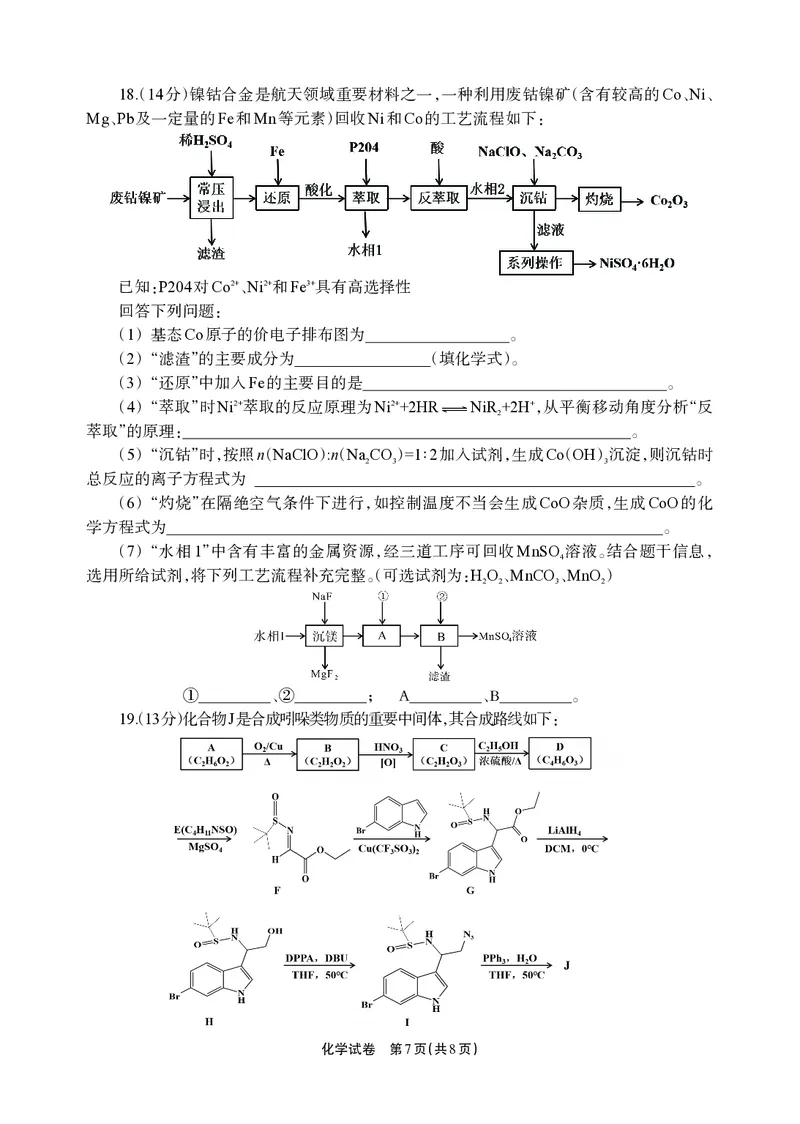
(3)在密闭容器中,1.01×105Pa、n (CO)∶n (H)=1∶4时,同时发生反应Ⅰ和Ⅲ,CO
起始 2 起始 2 2
平衡转化率、在催化剂作用下反应相同时间所测得的CO 实际转化率随温度的变化如图所
2
n
示(已知CH 的平衡选择性= (CH4) )。
4 n × 100%
△ (CO2)
该催化剂催化CO 反应的最佳温度为 。
① 2
体系温度降低,CH 的平衡选择性 (填“增大”“减小”或“不变”)。
② 4
CO 的平衡转化率在600℃之后随温度升高而增大的主要原因是
③ 2
。
化学试卷 第 页(共 页)
6 818(. 14分)镍钴合金是航天领域重要材料之一,一种利用废钴镍矿(含有较高的Co、Ni、
Mg、Pb及一定量的Fe和Mn等元素)回收Ni和Co的工艺流程如下:
已知:P204对Co2+、Ni2+和Fe3+具有高选择性
回答下列问题:
(1)基态Co原子的价电子排布图为 。
(2)“滤渣”的主要成分为 (填化学式)。
(3)“还原”中加入Fe的主要目的是 。
(4)“萃取”时Ni2+萃取的反应原理为Ni2++2HR NiR+2H+,从平衡移动角度分析“反
2
萃取”的原理: 。
(5)“沉钴”时,按照n(NaClO):n(NaCO)=1∶2加入试剂,生成Co(OH)沉淀,则沉钴时
2 3 3
总反应的离子方程式为 。
(6)“灼烧”在隔绝空气条件下进行,如控制温度不当会生成CoO杂质,生成CoO的化
学方程式为 。
(7)“水相1”中含有丰富的金属资源,经三道工序可回收MnSO 溶液。结合题干信息,
4
选用所给试剂,将下列工艺流程补充完整。(可选试剂为:HO、MnCO、MnO)
2 2 3 2
、 ; A 、B 。
① ②
19(. 13分)化合物J是合成吲哚类物质的重要中间体,其合成路线如下:
化学试卷 第 页(共 页)
7 8已知:
回答下列问题:
(1)A的化学名称为 ;C中含氧官能团的名称为
。
(2)D+E→F的化学方程式为
。
(3)由F生成G的反应类型为 ;化合物J的结构简式为
。
(4)在D的同分异构体中,满足下列条件的结构简式为 。
能发生银镜反应; 能发生水解反应; 含有一个手性碳
① ② ③
核磁共振氢谱有5组峰,峰面积之比为2:1:1:1:1
④
(5)某同学结合J的合成路线,设计了化合物K的一种合成路线。该路线中L和M的结
构简式分别为 、 。
O
S
N (K)
O
O
化学试卷 第 页(共 页)
8 8