文档内容
安庆示范高中 2024 届高三联考
化学试题 2024.4
命题单位:安庆一中 审稿单位:望江二中、岳西中学、石化一中
考生注意:
1.满分100分,考试时间75分钟。
2.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用 2B铅笔把答题卡上
对应题目的答案标号涂黑;非选择题请用直径 0.5毫米黑色墨水签字笔在答题卡上各题的答
题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
可能用到的相对原子质量:H—1 O—16 Na—23 Fe—56 Se—79
第Ⅰ卷(选择题共42分)
一、选择题:本题共 14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.含银卤化物胶片是摄影中常用的感光材料。下列叙述的变化过程,发生非氧化还原反应的是( )
A.拍摄:卤化银AgX( 、Br)曝光后会产生Ag(黑色粉末)和
B.显影:加入显影剂(如 等),使潜影银核中的AgX进一步转化为Ag
C.定影:用 溶解胶片上多余的AgX,形成可溶的配离子 ,从而定影
D.回收:溶解在定影液中的银可利用电解法回收,生成单质银
2.化学与生产、生活、科技密切相关。下列说法错误的是( )
A.“鲲龙”水陆两栖飞机实现海上首飞,其所用燃料航空煤油是石油分馏产品
B.“墨子号”卫星成功发射,实现了光纤量子通信,生产光纤的主要原料是二氧化硅
C.电阻率低、热导率高的石墨烯可用于制作超级导电材料
D. 是制造智能磁性材料的原料之一, 属于合金
3.碳材料家族又添2位新成员:通过对两种分子实施“麻醉”和“手术”,我国科学家首次成功合成了分
别由10个或14个碳原子组成的芳香性环形纯碳分子材料(结构如图所示),下列叙述错误的是( )
A. 分子中存在极性键和非极性键
学科网(北京)股份有限公司B.环形碳( )和环形碳( )互为同素异形体
C.1 mol的 含 个σ键
D. 转化为环形碳( )的过程, 发生了还原反应
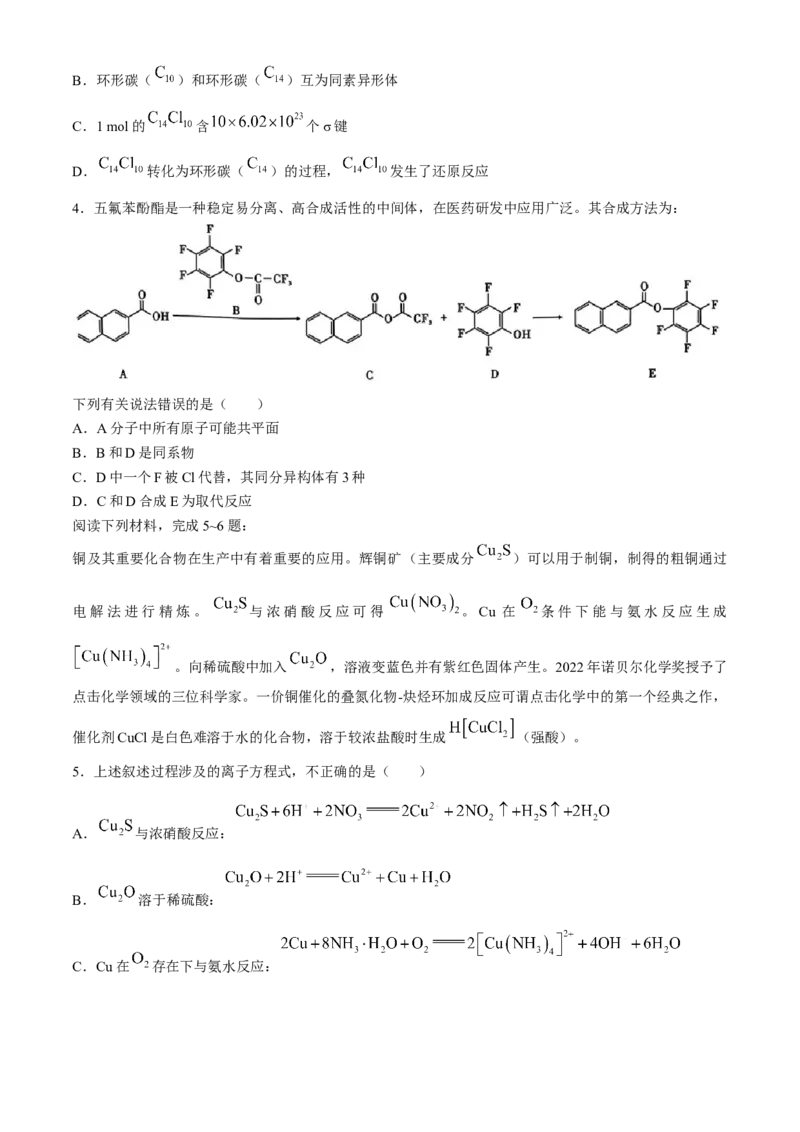
4.五氟苯酚酯是一种稳定易分离、高合成活性的中间体,在医药研发中应用广泛。其合成方法为:
下列有关说法错误的是( )
A.A分子中所有原子可能共平面
B.B和D是同系物
C.D中一个F被Cl代替,其同分异构体有3种
D.C和D合成E为取代反应
阅读下列材料,完成5~6题:
铜及其重要化合物在生产中有着重要的应用。辉铜矿(主要成分 )可以用于制铜,制得的粗铜通过
电解法进行精炼。 与浓硝酸反应可得 。Cu 在 条件下能与氨水反应生成
。向稀硫酸中加入 ,溶液变蓝色并有紫红色固体产生。2022年诺贝尔化学奖授予了
点击化学领域的三位科学家。一价铜催化的叠氮化物-炔烃环加成反应可谓点击化学中的第一个经典之作,
催化剂CuCl是白色难溶于水的化合物,溶于较浓盐酸时生成 (强酸)。
5.上述叙述过程涉及的离子方程式,不正确的是( )
A. 与浓硝酸反应:
B. 溶于稀硫酸:
C.Cu在 存在下与氨水反应:
学科网(北京)股份有限公司D.CuCl溶于较浓盐酸:
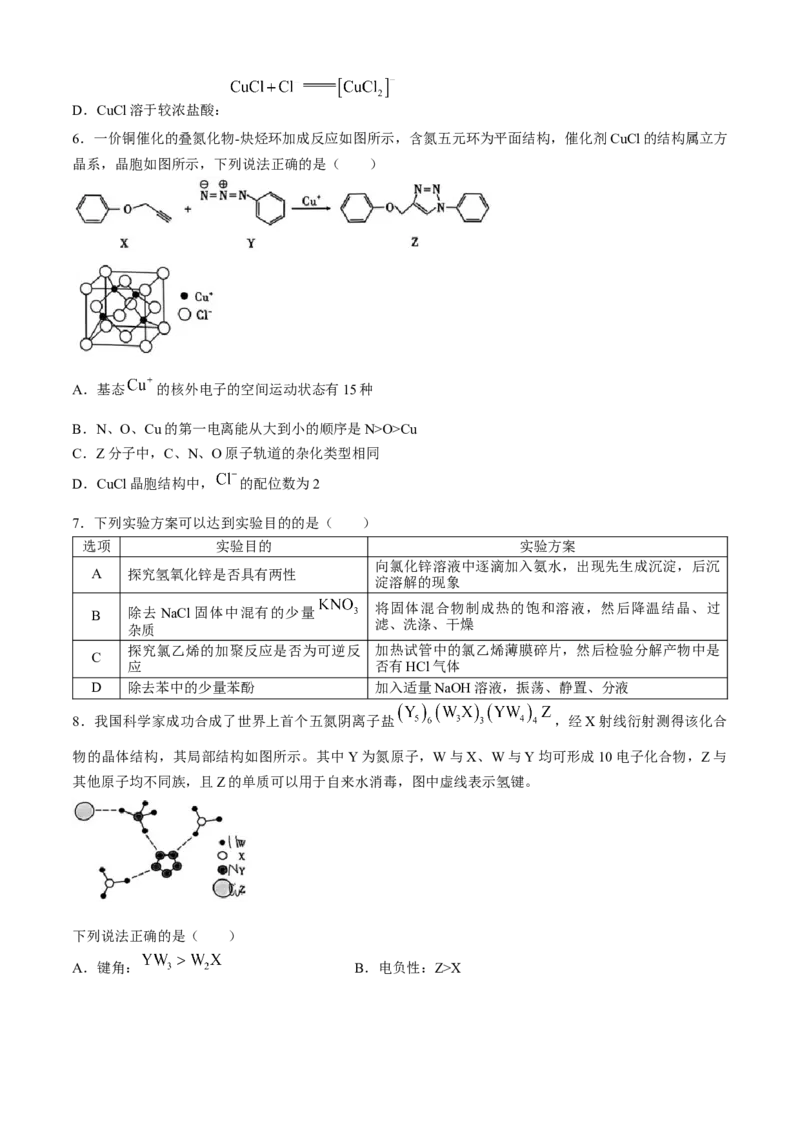
6.一价铜催化的叠氮化物-炔烃环加成反应如图所示,含氮五元环为平面结构,催化剂CuCl的结构属立方
晶系,晶胞如图所示,下列说法正确的是( )
A.基态 的核外电子的空间运动状态有15种
B.N、O、Cu的第一电离能从大到小的顺序是N>O>Cu
C.Z分子中,C、N、O原子轨道的杂化类型相同
D.CuCl晶胞结构中, 的配位数为2
7.下列实验方案可以达到实验目的的是( )
选项 实验目的 实验方案
向氯化锌溶液中逐滴加入氨水,出现先生成沉淀,后沉
A 探究氢氧化锌是否具有两性
淀溶解的现象
将固体混合物制成热的饱和溶液,然后降温结晶、过
B 除去NaCl固体中混有的少量
滤、洗涤、干燥
杂质
探究氯乙烯的加聚反应是否为可逆反 加热试管中的氯乙烯薄膜碎片,然后检验分解产物中是
C
应 否有HCl气体
D 除去苯中的少量苯酚 加入适量NaOH溶液,振荡、静置、分液
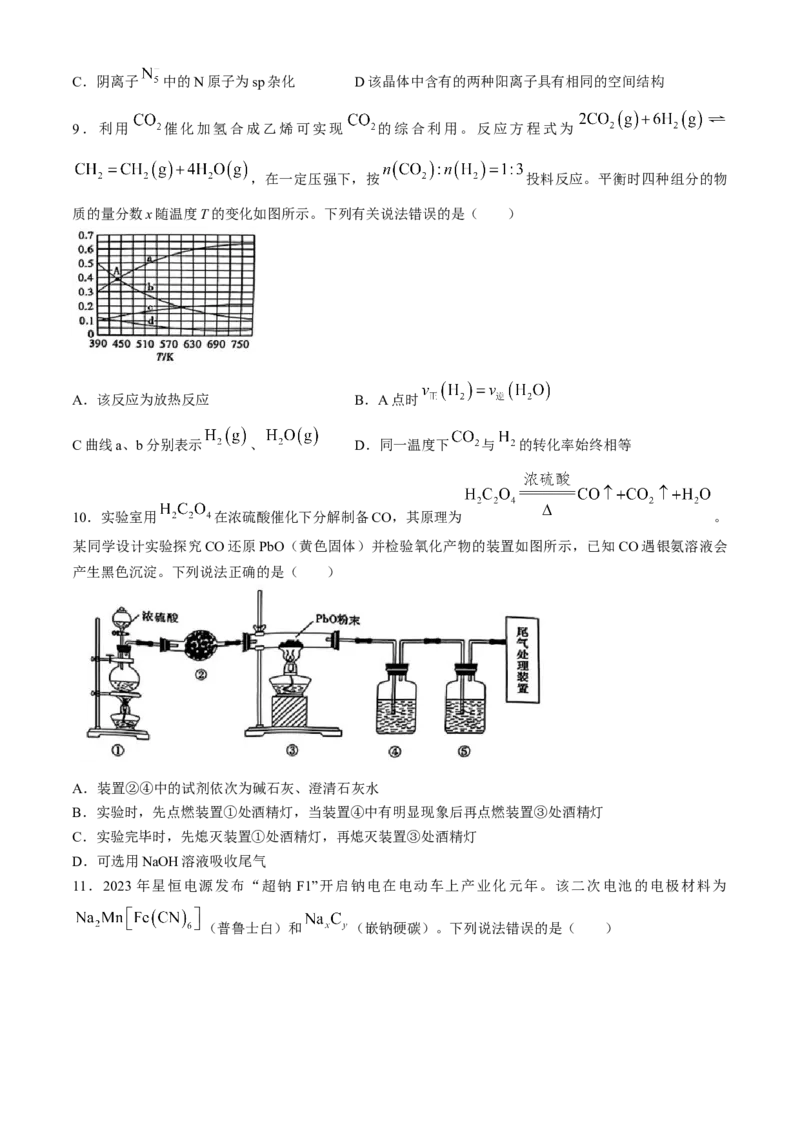
8.我国科学家成功合成了世界上首个五氮阴离子盐 ,经X射线衍射测得该化合
物的晶体结构,其局部结构如图所示。其中 Y为氮原子,W与X、W与Y均可形成10电子化合物,Z与
其他原子均不同族,且Z的单质可以用于自来水消毒,图中虚线表示氢键。
下列说法正确的是( )
A.键角: B.电负性:Z>X
学科网(北京)股份有限公司C.阴离子 中的N原子为sp杂化 D该晶体中含有的两种阳离子具有相同的空间结构
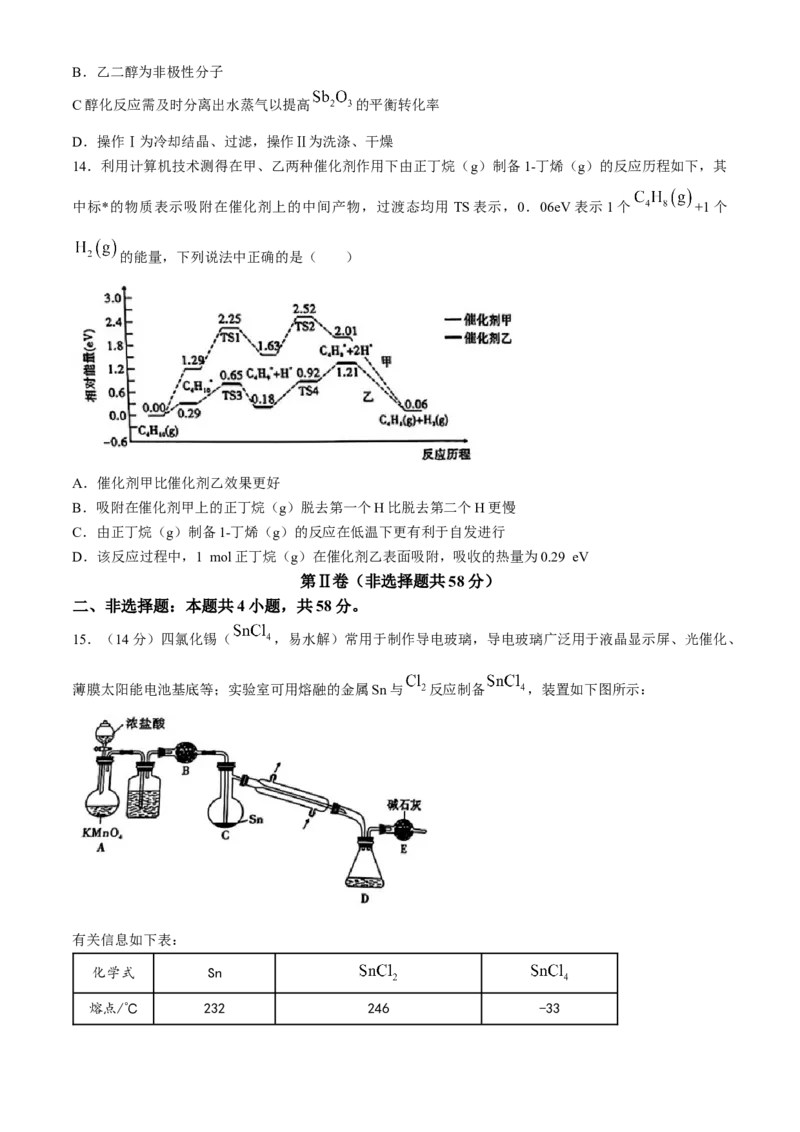
9.利用 催化加氢合成乙烯可实现 的综合利用。反应方程式为
,在一定压强下,按 投料反应。平衡时四种组分的物
质的量分数x随温度T的变化如图所示。下列有关说法错误的是( )
A.该反应为放热反应 B.A点时
C曲线a、b分别表示 、 D.同一温度下 与 的转化率始终相等
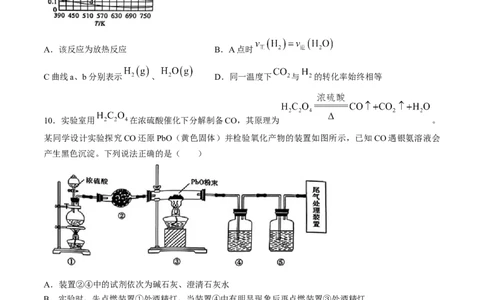
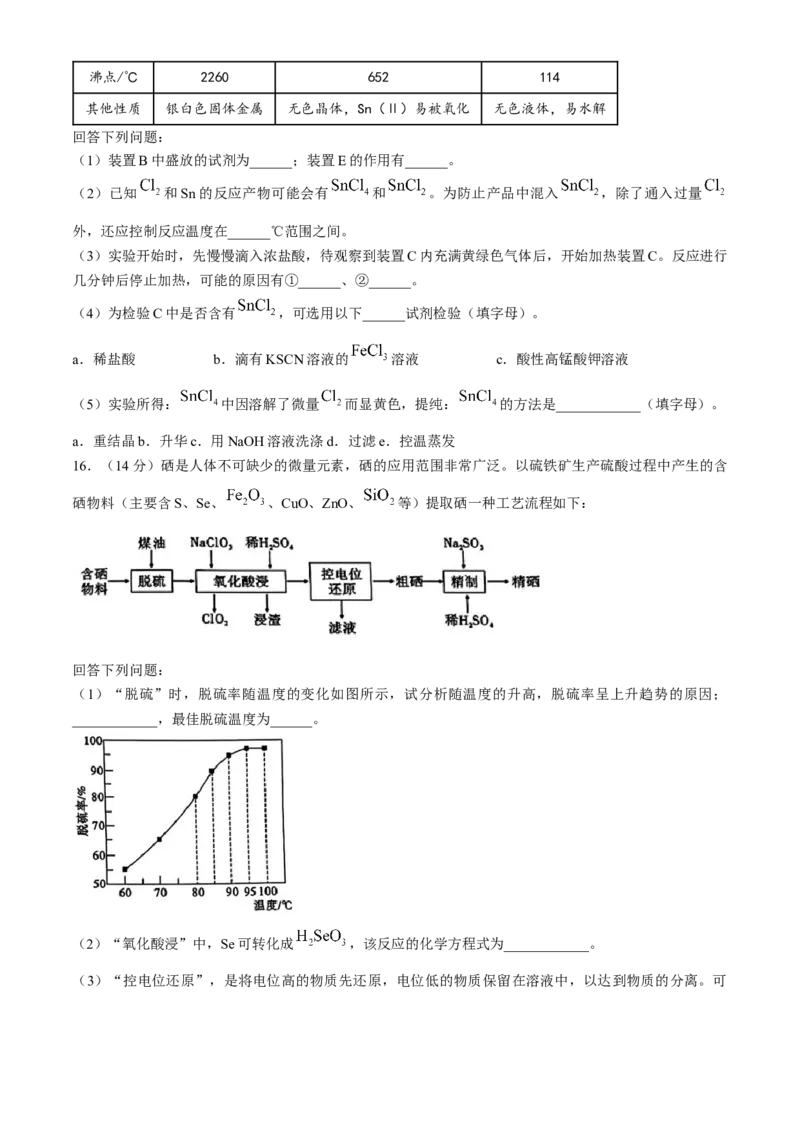
10.实验室用 在浓硫酸催化下分解制备CO,其原理为 。
某同学设计实验探究CO还原PbO(黄色固体)并检验氧化产物的装置如图所示,已知CO遇银氨溶液会
产生黑色沉淀。下列说法正确的是( )
A.装置②④中的试剂依次为碱石灰、澄清石灰水
B.实验时,先点燃装置①处酒精灯,当装置④中有明显现象后再点燃装置③处酒精灯
C.实验完毕时,先熄灭装置①处酒精灯,再熄灭装置③处酒精灯
D.可选用NaOH溶液吸收尾气
11.2023 年星恒电源发布“超钠 F1”开启钠电在电动车上产业化元年。该二次电池的电极材料为
(普鲁士白)和 (嵌钠硬碳)。下列说法错误的是( )
学科网(北京)股份有限公司A.充电时,用铅酸蓄电池作电源,需将铅蓄电池的Pb电极连接该电池的右边电极
B.充电时,电路中每转移1 mol电子,阴极电极质量增加23 g
e.放电时, 从正极脱嵌,在负极嵌入
D.钠离子电池比能量虽低于锂离子电池,但未使用稀缺锂元素,量产后成本低于锂离子电池
12.常温下,向1 L 0.05 mol/L 溶液(不考虑空气的影响)中缓慢通入0.05 mol ,充分混合,
完全,整个过程中无气体逸出,忽略溶液中体积和温度的变化,测得溶液的pH与通入 的物质的量之间
的变化曲线如图所示。已知:常温下, , 。下列说法错误的
是( )
A.a点溶液pH约为10
B.水的电离程度:b>d
C.c点溶液中,
D.若将 换成 ,其他不变,当通入 0.05 mol 时,溶液中的浓度大小有:
13.聚酯反应催化剂乙二醇锑 是一种无毒的白色晶状粉末,其制备流程如下:
下列说法错误的是( )
A.煅烧过程需注意防治污染
学科网(北京)股份有限公司B.乙二醇为非极性分子
C醇化反应需及时分离出水蒸气以提高 的平衡转化率
D.操作Ⅰ为冷却结晶、过滤,操作Ⅱ为洗涤、干燥
14.利用计算机技术测得在甲、乙两种催化剂作用下由正丁烷(g)制备1-丁烯(g)的反应历程如下,其
中标*的物质表示吸附在催化剂上的中间产物,过渡态均用TS表示,0.06eV表示1个 +1个
的能量,下列说法中正确的是( )
A.催化剂甲比催化剂乙效果更好
B.吸附在催化剂甲上的正丁烷(g)脱去第一个H比脱去第二个H更慢
C.由正丁烷(g)制备1-丁烯(g)的反应在低温下更有利于自发进行
D.该反应过程中,1 mol正丁烷(g)在催化剂乙表面吸附,吸收的热量为0.29 eV
第Ⅱ卷(非选择题共58分)
二、非选择题:本题共4小题,共58分。
15.(14分)四氯化锡( ,易水解)常用于制作导电玻璃,导电玻璃广泛用于液晶显示屏、光催化、
薄膜太阳能电池基底等;实验室可用熔融的金属Sn与 反应制备 ,装置如下图所示:
有关信息如下表:
化学式 Sn
熔点/℃ 232 246 -33
学科网(北京)股份有限公司沸点/℃ 2260 652 114
其他性质 银白色固体金属 无色晶体,Sn(Ⅱ)易被氧化 无色液体,易水解
回答下列问题:
(1)装置B中盛放的试剂为______;装置E的作用有______。
(2)已知 和Sn的反应产物可能会有 和 。为防止产品中混入 ,除了通入过量
外,还应控制反应温度在______℃范围之间。
(3)实验开始时,先慢慢滴入浓盐酸,待观察到装置C内充满黄绿色气体后,开始加热装置C。反应进行
几分钟后停止加热,可能的原因有①______、②______。
(4)为检验C中是否含有 ,可选用以下______试剂检验(填字母)。
a.稀盐酸 b.滴有KSCN溶液的 溶液 c.酸性高锰酸钾溶液
(5)实验所得: 中因溶解了微量 而显黄色,提纯: 的方法是____________(填字母)。
a.重结晶b.升华c.用NaOH溶液洗涤d.过滤e.控温蒸发
16.(14分)硒是人体不可缺少的微量元素,硒的应用范围非常广泛。以硫铁矿生产硫酸过程中产生的含
硒物料(主要含S、Se、 、CuO、ZnO、 等)提取硒一种工艺流程如下:
回答下列问题:
(1)“脱硫”时,脱硫率随温度的变化如图所示,试分析随温度的升高,脱硫率呈上升趋势的原因;
____________,最佳脱硫温度为______。
(2)“氧化酸浸”中,Se可转化成 ,该反应的化学方程式为____________。
(3)“控电位还原”,是将电位高的物质先还原,电位低的物质保留在溶液中,以达到物质的分离。可
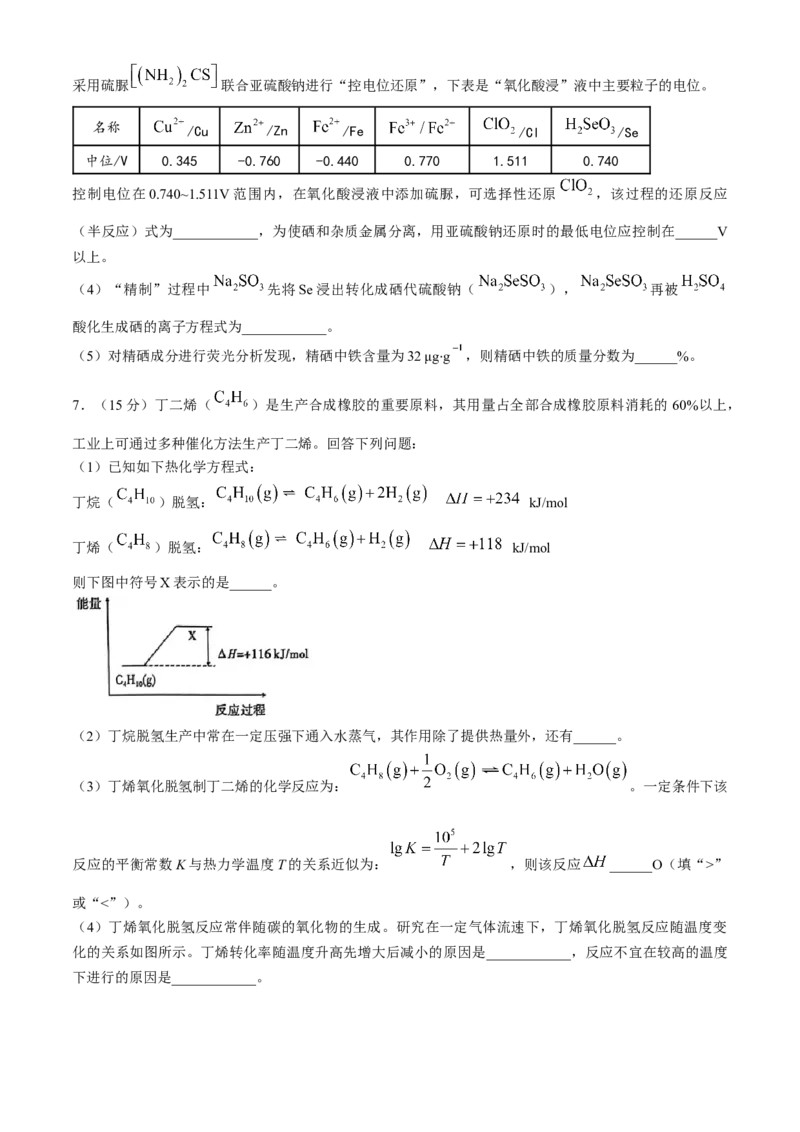
学科网(北京)股份有限公司采用硫脲 联合亚硫酸钠进行“控电位还原”,下表是“氧化酸浸”液中主要粒子的电位。
名称 /Cu /Zn /Fe /Cl /Se
中位/V 0.345 -0.760 -0.440 0.770 1.511 0.740
控制电位在0.740~1.511V范围内,在氧化酸浸液中添加硫脲,可选择性还原 ,该过程的还原反应
(半反应)式为____________,为使硒和杂质金属分离,用亚硫酸钠还原时的最低电位应控制在______V
以上。
(4)“精制”过程中 先将Se浸出转化成硒代硫酸钠( ), 再被
酸化生成硒的离子方程式为____________。
(5)对精硒成分进行荧光分析发现,精硒中铁含量为32 μgg ,则精硒中铁的质量分数为______%。
⋅
7.(15分)丁二烯( )是生产合成橡胶的重要原料,其用量占全部合成橡胶原料消耗的 60%以上,
工业上可通过多种催化方法生产丁二烯。回答下列问题:
(1)已知如下热化学方程式:
丁烷( )脱氢: kJ/mol
丁烯( )脱氢: kJ/mol
则下图中符号X表示的是______。
(2)丁烷脱氢生产中常在一定压强下通入水蒸气,其作用除了提供热量外,还有______。
(3)丁烯氧化脱氢制丁二烯的化学反应为: 。一定条件下该
反应的平衡常数K与热力学温度T的关系近似为: ,则该反应 ______O(填“>”
或“<”)。
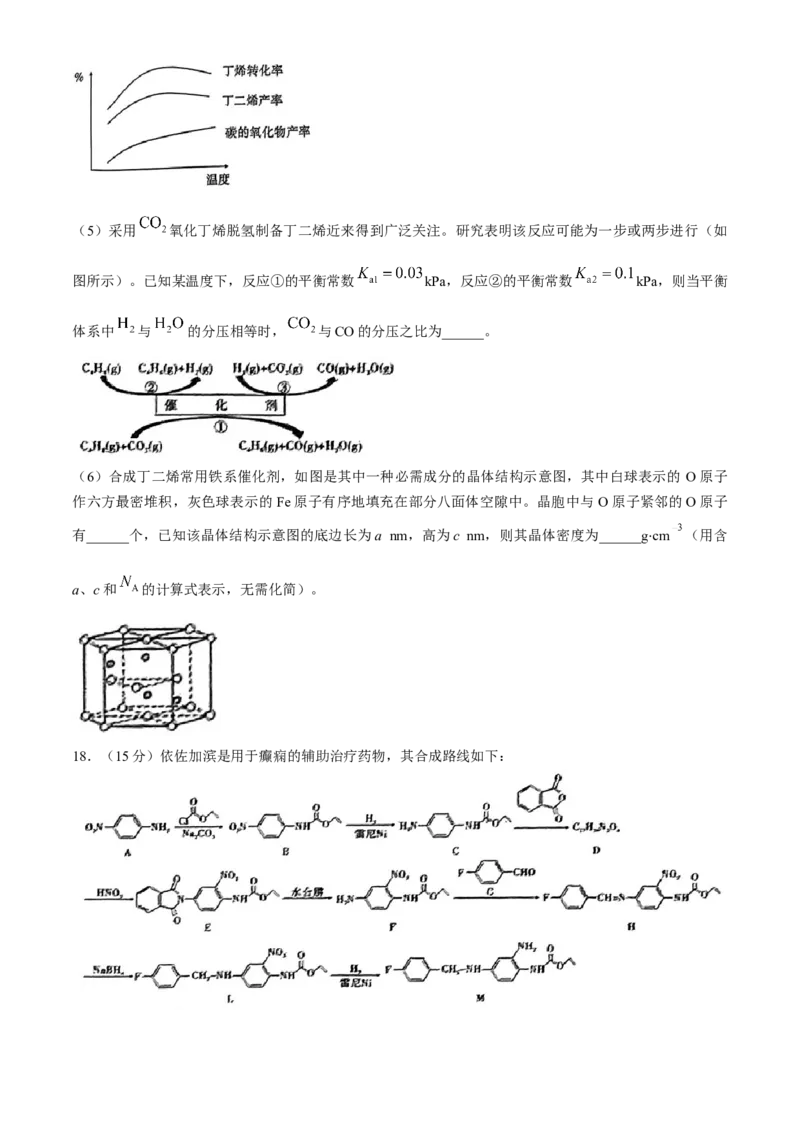
(4)丁烯氧化脱氢反应常伴随碳的氧化物的生成。研究在一定气体流速下,丁烯氧化脱氢反应随温度变
化的关系如图所示。丁烯转化率随温度升高先增大后减小的原因是____________,反应不宜在较高的温度
下进行的原因是____________。
学科网(北京)股份有限公司(5)采用 氧化丁烯脱氢制备丁二烯近来得到广泛关注。研究表明该反应可能为一步或两步进行(如
图所示)。已知某温度下,反应①的平衡常数 kPa,反应②的平衡常数 kPa,则当平衡
体系中 与 的分压相等时, 与CO的分压之比为______。
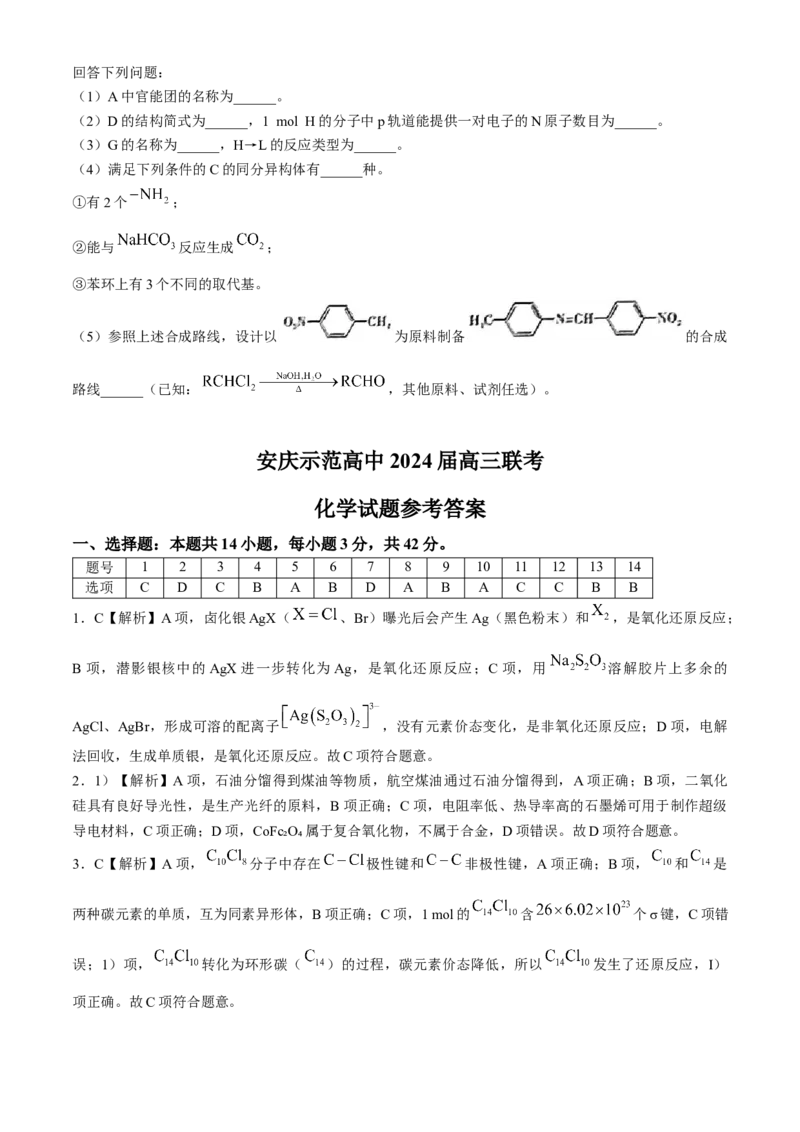
(6)合成丁二烯常用铁系催化剂,如图是其中一种必需成分的晶体结构示意图,其中白球表示的 O原子
作六方最密堆积,灰色球表示的Fe原子有序地填充在部分八面体空隙中。晶胞中与 O原子紧邻的O原子
有______个,已知该晶体结构示意图的底边长为a nm,高为c nm,则其晶体密度为______gcm (用含
⋅
a、c和 的计算式表示,无需化简)。
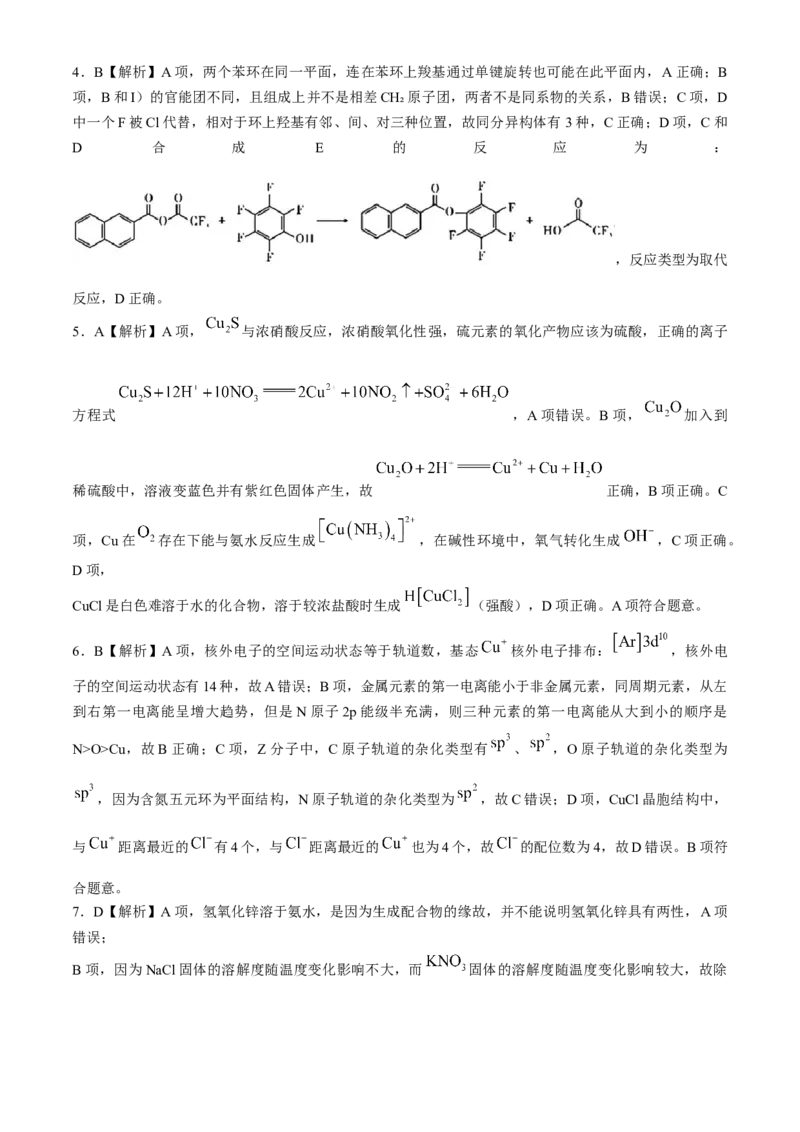
18.(15分)依佐加滨是用于癫痫的辅助治疗药物,其合成路线如下:
学科网(北京)股份有限公司回答下列问题:
(1)A中官能团的名称为______。
(2)D的结构简式为______,1 mol H的分子中p轨道能提供一对电子的N原子数目为______。
(3)G的名称为______,H→L的反应类型为______。
(4)满足下列条件的C的同分异构体有______种。
①有2个 ;
②能与 反应生成 ;
③苯环上有3个不同的取代基。
(5)参照上述合成路线,设计以 为原料制备 的合成
路线______(已知: ,其他原料、试剂任选)。
安庆示范高中 2024 届高三联考
化学试题参考答案
一、选择题:本题共14小题,每小题3分,共42分。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
选项 C D C B A B D A B A C C B B
1.C【解析】A项,卤化银AgX( 、Br)曝光后会产生Ag(黑色粉末)和 ,是氧化还原反应;
B项,潜影银核中的AgX进一步转化为Ag,是氧化还原反应;C项,用 溶解胶片上多余的
AgCl、AgBr,形成可溶的配离子 ,没有元素价态变化,是非氧化还原反应;D项,电解
法回收,生成单质银,是氧化还原反应。故C项符合题意。
2.1)【解析】A项,石油分馏得到煤油等物质,航空煤油通过石油分馏得到,A项正确;B项,二氧化
硅具有良好导光性,是生产光纤的原料,B项正确;C项,电阻率低、热导率高的石墨烯可用于制作超级
导电材料,C项正确;D项,CoFc₂O₄属于复合氧化物,不属于合金,D项错误。故D项符合题意。
3.C【解析】A项, 分子中存在 极性键和 非极性键,A项正确;B项, 和 是
两种碳元素的单质,互为同素异形体,B项正确;C项,1 mol的 含 个σ键,C项错
误;1)项, 转化为环形碳( )的过程,碳元素价态降低,所以 发生了还原反应,I)
项正确。故C项符合题意。
学科网(北京)股份有限公司4.B【解析】A项,两个苯环在同一平面,连在苯环上羧基通过单键旋转也可能在此平面内,A正确;B
项,B和I)的官能团不同,且组成上并不是相差CH₂原子团,两者不是同系物的关系,B错误;C项,D
中一个F被Cl代替,相对于环上羟基有邻、间、对三种位置,故同分异构体有 3种,C正确;D项,C和
D 合 成 E 的 反 应 为 :
,反应类型为取代
反应,D正确。
5.A【解析】A项, 与浓硝酸反应,浓硝酸氧化性强,硫元素的氧化产物应该为硫酸,正确的离子
方程式 ,A项错误。B项, 加入到
稀硫酸中,溶液变蓝色并有紫红色固体产生,故 正确,B项正确。C
项,Cu在 存在下能与氨水反应生成 ,在碱性环境中,氧气转化生成 ,C项正确。
D项,
CuCl是白色难溶于水的化合物,溶于较浓盐酸时生成 (强酸),D项正确。A项符合题意。
6.B【解析】A项,核外电子的空间运动状态等于轨道数,基态 核外电子排布: ,核外电
子的空间运动状态有14种,故A错误;B项,金属元素的第一电离能小于非金属元素,同周期元素,从左
到右第一电离能呈增大趋势,但是N原子2p能级半充满,则三种元素的第一电离能从大到小的顺序是
N>O>Cu,故B正确;C项,Z分子中,C原子轨道的杂化类型有 、 ,O原子轨道的杂化类型为
,因为含氮五元环为平面结构,N原子轨道的杂化类型为 ,故C错误;D项,CuCl晶胞结构中,
与 距离最近的 有4个,与 距离最近的 也为4个,故 的配位数为4,故D错误。B项符
合题意。
7.D【解析】A项,氢氧化锌溶于氨水,是因为生成配合物的缘故,并不能说明氢氧化锌具有两性,A项
错误;
B项,因为NaCl固体的溶解度随温度变化影响不大,而 固体的溶解度随温度变化影响较大,故除
学科网(北京)股份有限公司去NaCl固体中混有的少量 杂质,应是将固体混合物制成热的饱和溶液后,然后趁热过滤、洗涤、
干燥,B项错误;C项,可逆反应是指在同一个外界条件下,该反应可以向正逆两个方向同时进行,C项
错误;D项,苯酚与氢氧化钠反应生成可溶于水的苯酚钠,而苯不溶于氢氧化钠溶液,可用分液法分离,
D项正确。
8.A【解析】结合图示结构,W为氧,Y为氮原子,则X为氧,Z的单质可以用于自来水消毒,则Z为氯
据此分析。A项,键角: ,故A正确;B项,电负性: ,故B错误;C项,根据图示
阴离子 结构可知,N原子为 杂化,故C错误;D项,该化合物中的两种阳离子分别为 和
,空间构型分别为正四面体与三角锥形,故D错误。
9.B【解析】由 与 的物质的量之比为1∶3等于方程式计量系数比可知同一温度下 与 的转
化率始终相等,且二者物质的量分数之比等于1∶3,即a为 ,c为 ,由 与 的计
量系数比可知b为 ,d为 ,由图可知随温度升高,反正逆向移动,因此该反应放热,A
正确。
反应平衡时, 不等于 ,B错误。
10.A【解析】A项,②的作用是吸收 分解的 和 ,故选择碱石灰,④的作用是检验CO
还原PhO的氧化产物 ,故选择澄清石灰水,A项正确;B项,⑤中是银氨溶液,应是当装置⑤中有明
显现象后再点燃装置③处酒精灯,B项错误;C项,应是先熄灭装置③处酒精灯,再熄灭装置①处酒精灯,
C项错误;D项,NaOH溶液吸收不了CO尾气,D项错误。
11.C【解析】A项,充电时,铅酸蓄电池作电源,Pb电极为外界电源负极,应连接该电池的负极,A正
确;
B项,充电时,阴极发生反应: ,电路中每转移1 mol电子,阴极电极质量
增加23 g,B正确;C项,放电时,负极材料为 ,发生反应 ,正极材
料 为 , 放 电 时 正 极 反 应 为
学科网(北京)股份有限公司, 从负极脱嵌,在正极嵌入,C错误;D项,比能量就是参与电极反应的单位
质量的电极材料放出电能的大小,Li、Na原子正常状态下反应时均为失去1个电子,但Li的相对原子质量
小于Na的,故钠离子电池的比能量虽低于锂离子电池,但未使用稀缺锂元素,量产后成成本低于锂离子
电池,具有广泛应用前景,D正确。
12.C【解析】A项,求a处pH,需要求得 ,此处只有亚硫酸钠,以第一步水解为主,依据公式
, , 因 为 , 所 以 ,
,解得 ,故 , ,A 正确;B
项,依据反应 ,可知该反应生成氢离子抑制水的电离,故水的
电 离 程 度 : b>d , B 正 确 ; C 项 , 溶 液 中 存 在 电 荷 守 恒 :
, 物 料 守 恒 :
, 叠 加 得 质 子 守 恒 :
①,又由 得
, ,故 ,故
②,①②式联解,可知: ,C错误;D项,通入的 为0.05
mol 时,根据物料守恒有: ,根据得失电子守恒有:
,故 ,D正确。
13.B【解析】A项,辉锑矿煅烧会产生二氧化硫,需注意防治污染,A正确;B项,乙二醇为极性分子,
B错误;C项,该条件下醇化反应是可逆反应且会生成水,故及时分离出水蒸气可提高 Sb₂O₃的平衡转化
率,C正确;D项,根据制备流程可知操作1为冷却结晶、过滤,操作Ⅱ为洗涤、干燥,D正确。
14.B【解析】A项,由图可知,选用催化剂乙效果更好,故A错误;B项,由图可知,吸附在催化剂甲
上的正丁烷(g)脱去第一个 H 最高能垒为 2.25 eV-1.29 eV=0.96 eV,脱去第二个 H 最高能垒为
2.52eV-1.63eV=0.89eV,故 B 正确;C 项,由图可知, 的 和
学科网(北京)股份有限公司都大于0, 小于0可以自发,当T比较大时可以自发反应,所以该反应在高温条件下有利于
自发进行,故C错误;D项,由图可知,选用催化剂乙时,相对能量从0.00eV→0.29eV的过程为正丁烷在
催化剂表面的吸附过程,1 mol正丁烷(g)吸附所吸收的热量为 eV,故D错误;故选B。
二、非选择题:本题共4小题,共58分。
15.【答案】(每空2分,共14分)
(1)无水 (或 ) 防止空气中的水蒸气进入D中,并吸收多余的
(2)232~652
(3)①反应放热,能维持反应继续进行
②防止温度过高 变为气态,混入 中
(4)b
(5)e
16.【答案】(每空2分,共14分)
(1)温度升高,单质硫在煤油中的溶解度增加95℃(90℃-95℃之间任意温度皆可给分)
(2)
(3) 0.45
(4)
(5)
17.【答案】(除标注外,每空2分,共15分)
(1) (没有气体符号不得分)
(2)该反应为气体分子数增大的反应,减小体系分压,有利于反应正向进行,提高丁二烯的产率
(3)<
(4)温度升高速率加快,转化率增大;温度过高催化剂失活,速率减小,转化率下降(每点各1分,其他
合理表述也可得分)
丁二烯产率下降,碳的氧化物含量上升(每点1分)
(5)10∶3
(6)12(1分) (其他合理形式也得分)
学科网(北京)股份有限公司18.【答案】(除标注外,每空2分,共15分)
(1)硝基、氨基(2分)
(2)(2)(2分) (2分)
(3)对氟苯甲醛或4-氟苯甲醛(2分) 还原反应或加成反应(1分)
(4)50(2分)
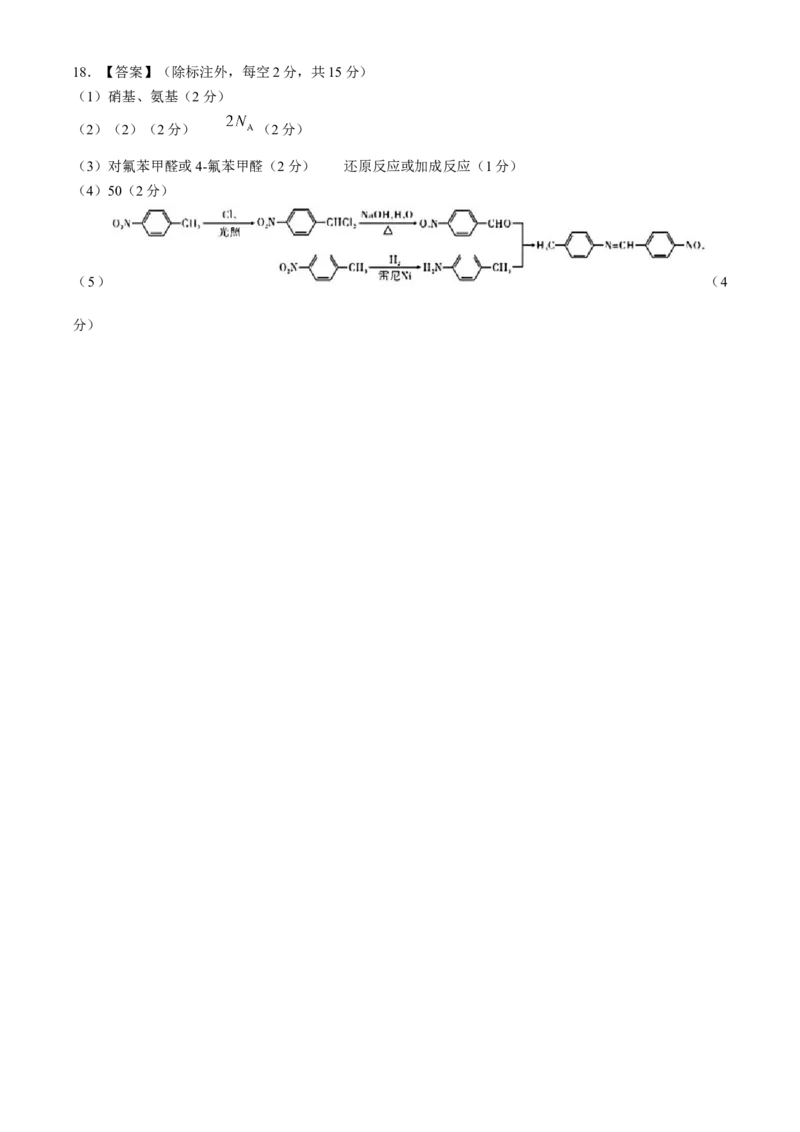
(5) (4
分)
学科网(北京)股份有限公司