文档内容
B.常温常压下,35.5gCl 与足量镁粉充分反应,转移的电子数为2N
三贤中学 2023-2024 学年度高三第二次教学质量检测 2 A
C.常温常压下,22.4LNO 和CO 的混合气体含有的氧原子数为2N
2 2 A
高三化学试卷
D.2.24LCO和CO 混合气体中含有的碳原子数目为0.1N
2 A
(卷面总分100分 答题时间 90 分钟) 5.下列离子方程式与所述事实相符且正确的是( )
命题人:刘瑞娟
A.用H O 从酸化的海带灰浸出液中提取碘:2I-+H O ===I +2OH-
2 2 2 2 2
可能用到的相对原子质量: H:1 Cl:35.5 O:16 Fe:56 Cu:64 Mg:24
B.向碳酸氢铵溶液中加入过量的NaOH溶液:NH +OH-===NH ·H O
3 2
一、单选题(18小题,每题3分,共54 分)
C.向明矾溶液中加入Ba(OH) 溶液至生成沉淀的物质的量最多:Al3++2SO +2Ba2++4OH-
2
1.中国丝绸有五千年的历史和文化。古代染坊常用某种“碱剂”来精炼丝绸,该“碱剂”的主要成 ===AlO +2BaSO
4
↓+2H
2
O
分是一种盐,能促进蚕丝表层的丝胶蛋白杂质水解而除去,使丝绸颜色洁白、质感柔软、色泽光
D.等体积、等物质的量浓度的NaHCO 溶液与Ba(OH) 溶液混合:HCO +Ba2++OH-
3 2
亮。这种“碱剂”可能是( )
===BaCO ↓+H O
3 2
A.草木灰 B.火碱 C.食盐 D.胆矾
6.在配制一定物质的量浓度的盐酸时,下列错误操作可使所配制溶液浓度偏高的是( )
2.雷雨天,空气中的N 会发生一系列反应,生成氮的化合物。雷雨时,一般不可能生成的氮的化
2 A.用量筒量取浓盐酸时仰视读数 B.稀释搅拌时有液体飞溅
合物是( )
C.定容时仰视容量瓶刻度线 D.定容摇匀后液面下降,再加水至刻度线
①NH ②NO ③NO ④N O ⑤N O ⑥HNO
3 2 2 3 2 5 3
7.以下是在实验室模拟“侯氏制碱法”生产流程的示意图:
A.②④⑥ B.②③⑤⑥ C.①④⑤ D.①③⑤
3.钠及其化合物与人们的生活密切相关,某同学对其认识不正确的是( )
A.碳酸氢钠常用于治疗胃酸过多症 则下列叙述错误的是( )
B.热的纯碱可去除油污 A.A气体是NH ,B气体是CO
3 2
C.发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔 B.侯氏制碱法的工艺过程中应用了物质溶解度的差异
D.金属钠着火时,使用泡沫灭火器来灭火 C.第III步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒
4.N A 为阿伏加德罗常数的值,下列说法正确的是( ) D.第IV步操作是将晶体溶于水后加热、蒸发、结晶
A.标准状况下,22.4L的SO 2 中含有的SO 2 分子数为N A 8.下列陈述Ⅰ、Ⅱ均正确并且有因果关系的是( )
化学 第 页 共7页
1
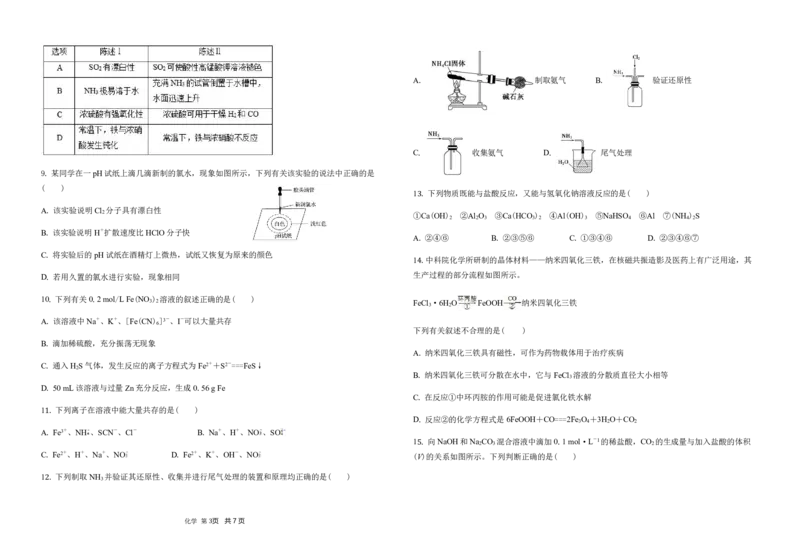
{#{QQABLQYQggggAAAAAAgCAwXACAMQkBACAIoOAEAIsAIAAQNABAA=}#}A. 制取氨气 B. 验证还原性
C. 收集氨气 D. 尾气处理
9.某同学在一pH试纸上滴几滴新制的氯水,现象如图所示,下列有关该实验的说法中正确的是
( )
1 .下列物质既能与盐酸反应,又能与氢氧化钠溶液反应的是( )
A.该实验说明Cl 分子具有漂白性 3
2 ①Ca(OH) ②Al O ③Ca(HCO ) ④Al(OH) ⑤NaHSO ⑥Al ⑦(NH ) S
2 2 3 3 2 3 4 4 2
B.该实验说明H+扩散速度比HClO分子快
A.②④⑥ B.②③⑤⑥ C.①③④⑥ D.②③④⑥⑦
C.将实验后的pH试纸在酒精灯上微热,试纸又恢复为原来的颜色
1 .中科院化学所研制的晶体材料——纳米四氧化三铁,在核磁共振造影及医药上有广泛用途,其
D.若用久置的氯水进行实验,现象相同 生 4 产过程的部分流程如图所示。
10.下列有关0.2mol/LFe(NO ) 溶液的叙述正确的是( )
3 2 FeCl ·6H O FeOOH 纳米四氧化三铁
3 2
A.该溶液中Na+、K+、[Fe(CN) ]3-、I-可以大量共存
6
下列有关叙述不合理的是( )
B.滴加稀硫酸,充分振荡无现象
A.纳米四氧化三铁具有磁性,可作为药物载体用于治疗疾病
C.通入H S气体,发生反应的离子方程式为Fe2++S2-===FeS↓
2
B.纳米四氧化三铁可分散在水中,它与FeCl 溶液的分散质直径大小相等
3
D.50mL该溶液与过量Zn充分反应,生成0.56gFe
C.在反应①中环丙胺的作用可能是促进氯化铁水解
1 .下列离子在溶液中能大量共存的是( )
D.反应②的化学方程式是6FeOOH+CO===2Fe O +3H O+CO
3 4 2 2
1
A.Fe3+、NH 、SCN-、Cl- B.Na+、H+、NO 、SO
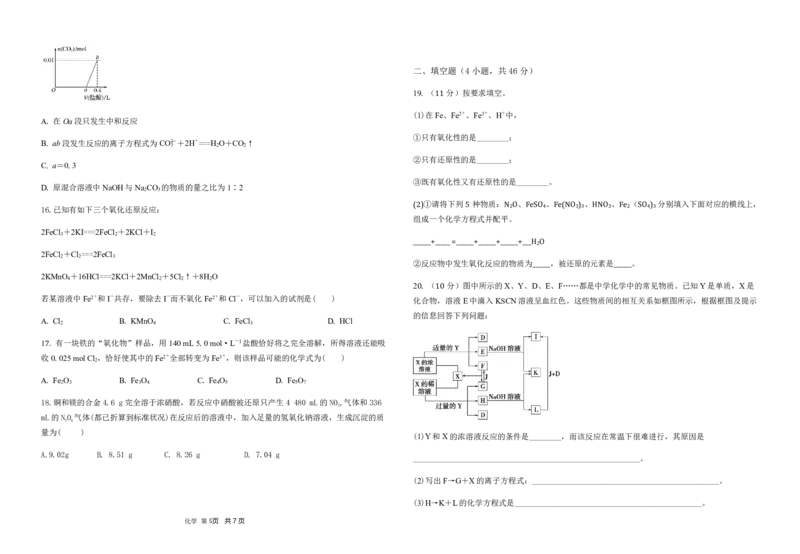
1 .向NaOH和Na CO 混合溶液中滴加0.1mol·L-1的稀盐酸,CO 的生成量与加入盐酸的体积
2 3 2
C.Fe2+、H+、Na+、NO D.Fe2+、K+、OH-、NO
(V)的关系如图所示。下列判断正确的是( )
5
1 .下列制取NH 并验证其还原性、收集并进行尾气处理的装置和原理均正确的是( )
3
2
化学 第 页 共7页
3
{#{QQABLQYQggggAAAAAAgCAwXACAMQkBACAIoOAEAIsAIAAQNABAA=}#}二、填空题(4小题,共46分)
19.( 分)按要求填空。
11
(1)在Fe、Fe2+、Fe3+、H+中,
A.在Oa段只发生中和反应
①只有氧化性的是________;
B.ab段发生反应的离子方程式为CO +2H+===H O+CO ↑
2 2
②只有还原性的是________;
C.a=0.3
③既有氧化性又有还原性的是________。
D.原混合溶液中NaOH与Na CO 的物质的量之比为1∶2
2 3
①请将下列 种物质: 、 、 、 、 ( 分别填入下面对应的横线上,
16.已知有如下三个氧化还原反应:
组成一个化学方程式并配平。2 4 3 3 3 2 4 3
(2) 5 N O FeSO Fe(NO ) HNO Fe SO )
2FeCl +2KI===2FeCl +2KCl+I
3 2 2
2FeCl 2 +Cl 2 ===2FeCl 3 ______+_____=______+______+______+___H 2 O
②反应物中发生氧化反应的物质为 ,被还原的元素是 。
2KMnO +16HCl===2KCl+2MnCl +5Cl ↑+8H O
4 2 2 2 ______ ______
2 .( 分)图中所示的X、Y、D、E、F……都是中学化学中的常见物质。已知Y是单质,X是
若某溶液中Fe2+和I-共存,要除去I-而不氧化Fe2+和Cl-,可以加入的试剂是( ) 化合物,溶液E中滴入KSCN溶液呈血红色。这些物质间的相互关系如框图所示,根据框图及提示
0 10
的信息回答下列问题:
A.Cl B.KMnO C.FeCl D.HCl
2 4 3
1 .有一块铁的“氧化物”样品,用140mL5.0mol·L-1盐酸恰好将之完全溶解,所得溶液还能吸
收0.025molCl ,恰好使其中的Fe2+全部转变为Fe3+,则该样品可能的化学式为( )
7 2
A.Fe O B.Fe O C.Fe O D.Fe O
2 3 3 4 4 5 5 7
18.铜和镁的合金4.6 g完全溶于浓硝酸,若反应中硝酸被还原只产生4 480 mL的NO,气体和336
2
mL的NO 气体(都已折算到标准状况)在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质
2 4
量为( )
(1)Y和X的浓溶液反应的条件是________,而该反应在常温下很难进行,其原因是
A.9.02g B. 8.51 g C. 8.26 g D. 7.04 g
_________________________________________________________。
(2)写出F→G+X的离子方程式:_______________________________________________。
(3)H→K+L的化学方程式是_______________________________________________。
化学 第 页 共7页
5
{#{QQABLQYQggggAAAAAAgCAwXACAMQkBACAIoOAEAIsAIAAQNABAA=}#}(4)在试管中制备L,为了能观察到L的颜色,需要进行特殊的操作,该特殊的操作是
②
_________________________________________________________。
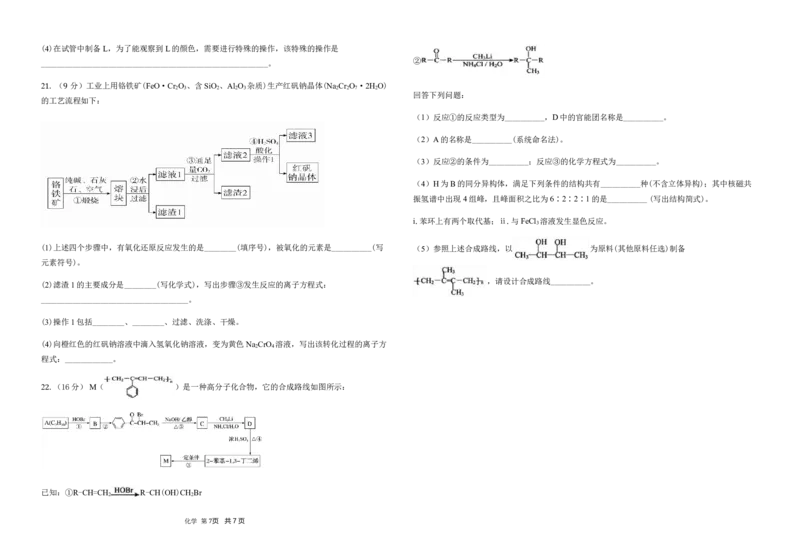
2 .( 分)工业上用铬铁矿(FeO·Cr O 、含SiO 、Al O 杂质)生产红矾钠晶体(Na Cr O ·2H O)
2 3 2 2 3 2 2 7 2
回答下列问题:
的工艺流程如下:
1 9
(1)反应①的反应类型为__________,D中的官能团名称是__________。
(2)A的名称是__________(系统命名法)。
(3)反应②的条件为__________;反应③的化学方程式为__________。
(4)H为B的同分异构体,满足下列条件的结构共有__________种(不含立体异构);其中核磁共
振氢谱中出现4组峰,且峰面积之比为6∶2∶2∶1的是__________(写出结构简式)。
i.苯环上有两个取代基;ⅱ.与FeCl 溶液发生显色反应。
3
(1)上述四个步骤中,有氧化还原反应发生的是________(填序号),被氧化的元素是__________(写 (5)参照上述合成路线,以 为原料(其他原料任选)制备
元素符号)。
,请设计合成路线__________。
(2)滤渣1的主要成分是________(写化学式),写出步骤③发生反应的离子方程式:
_____________________________________。
(3)操作1包括________、________、过滤、洗涤、干燥。
(4)向橙红色的红矾钠溶液中滴入氢氧化钠溶液,变为黄色Na CrO 溶液,写出该转化过程的离子方
2 4
程式:____________。
2 .(16分)M( )是一种高分子化合物,它的合成路线如图所示:
2
已知:①R-CH=CH R-CH(OH)CH Br
2 2
化学 第 页 共7页
7
{#{QQABLQYQggggAAAAAAgCAwXACAMQkBACAIoOAEAIsAIAAQNABAA=}#}