文档内容
3.1.2 电离平衡常数 练习(原卷版)
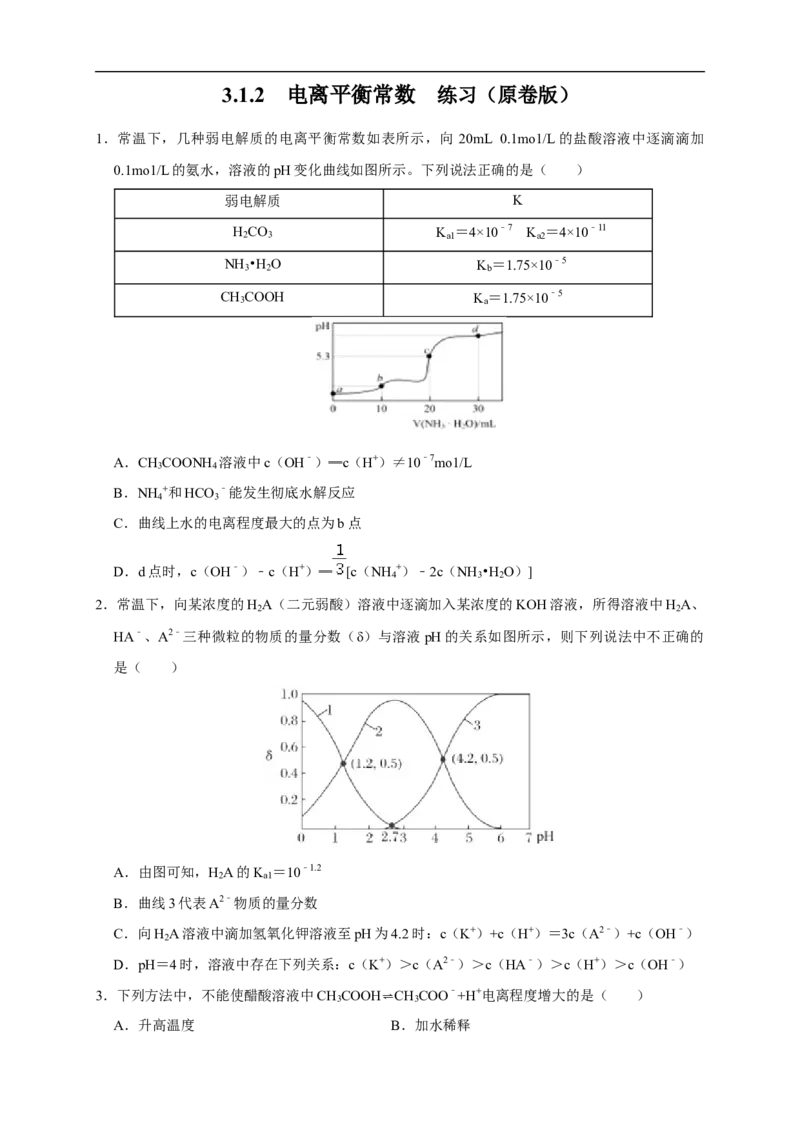
1.常温下,几种弱电解质的电离平衡常数如表所示,向 20mL 0.1mo1/L的盐酸溶液中逐滴滴加
0.1mo1/L的氨水,溶液的pH变化曲线如图所示。下列说法正确的是( )
弱电解质 K
H CO K =4×10﹣7 K =4×10﹣11
2 3 a1 a2
NH •H O K =1.75×10﹣5
3 2 b
CH COOH K =1.75×10﹣5
3 a
A.CH COONH 溶液中c(OH﹣)═c(H+)≠10﹣7mo1/L
3 4
B.NH +和HCO ﹣能发生彻底水解反应
4 3
C.曲线上水的电离程度最大的点为b点
D.d点时,c(OH﹣)﹣c(H+)═ [c(NH +)﹣2c(NH •H O)]
4 3 2
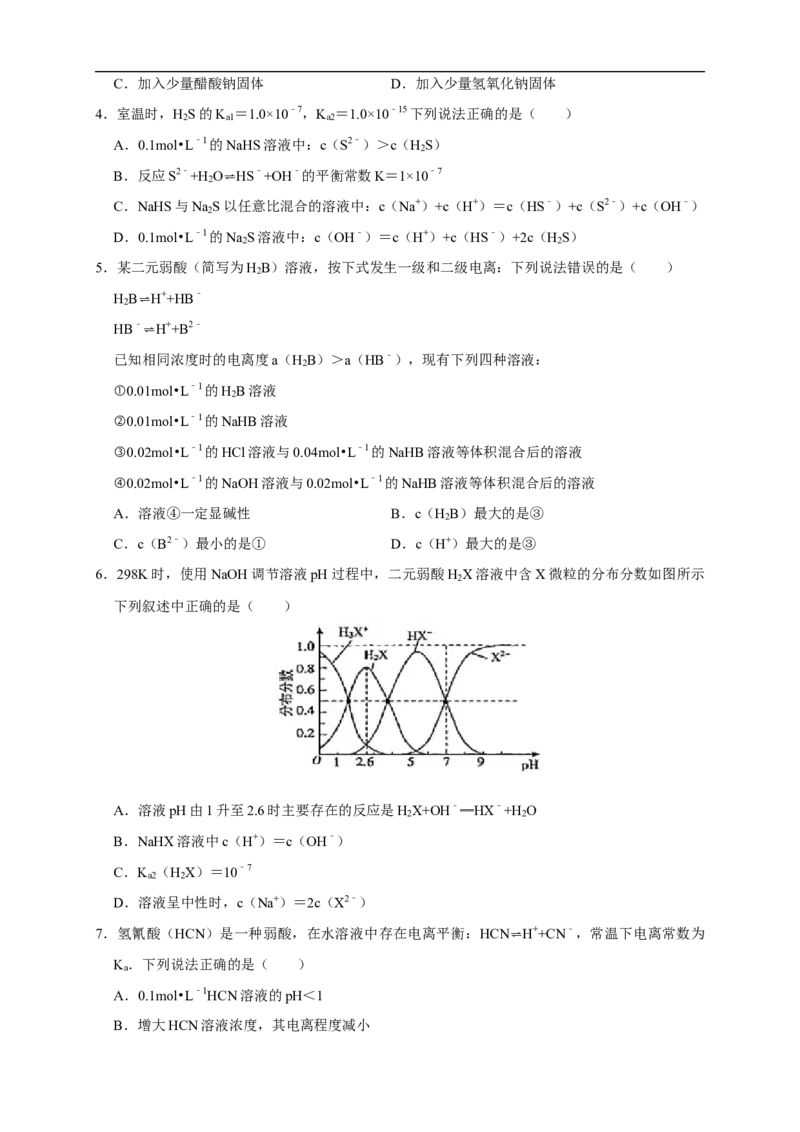
2.常温下,向某浓度的H A(二元弱酸)溶液中逐滴加入某浓度的KOH溶液,所得溶液中H A、
2 2
HA﹣、A2﹣三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法中不正确的
是( )
A.由图可知,H A的K =10﹣1.2
2 a1
B.曲线3代表A2﹣物质的量分数
C.向H A溶液中滴加氢氧化钾溶液至pH为4.2时:c(K+)+c(H+)=3c(A2﹣)+c(OH﹣)
2
D.pH=4时,溶液中存在下列关系:c(K+)>c(A2﹣)>c(HA﹣)>c(H+)>c(OH﹣)
3.下列方法中,不能使醋酸溶液中CH
3
COOH⇌CH
3
COO﹣+H+电离程度增大的是( )
A.升高温度 B.加水稀释C.加入少量醋酸钠固体 D.加入少量氢氧化钠固体
4.室温时,H S的K =1.0×10﹣7,K =1.0×10﹣15下列说法正确的是( )
2 a1 a2
A.0.1mol•L﹣1的NaHS溶液中:c(S2﹣)>c(H S)
2
B.反应S2﹣+H
2
O⇌HS﹣+OH﹣的平衡常数K=1×10﹣7
C.NaHS与Na S以任意比混合的溶液中:c(Na+)+c(H+)=c(HS﹣)+c(S2﹣)+c(OH﹣)
2
D.0.1mol•L﹣1的Na S溶液中:c(OH﹣)=c(H+)+c(HS﹣)+2c(H S)
2 2
5.某二元弱酸(简写为H B)溶液,按下式发生一级和二级电离:下列说法错误的是( )
2
H
2
B⇌H++HB﹣
HB﹣ ⇌H++B2﹣
已知相同浓度时的电离度a(H B)>a(HB﹣),现有下列四种溶液:
2
①0.01mol•L﹣1的H
2
B溶液
②0.01mol•L﹣1的NaHB溶液
③0.02mol•L﹣1的HCl溶液与0.04mol•L﹣1的NaHB溶液等体积混合后的溶液
④0.02mol•L﹣1的NaOH溶液与0.02mol•L﹣1的NaHB溶液等体积混合后的溶液
A.溶液④一定显碱性 B.c(H B)最大的是③
2
C.c(B2﹣)最小的是① D.c(H+)最大的是③
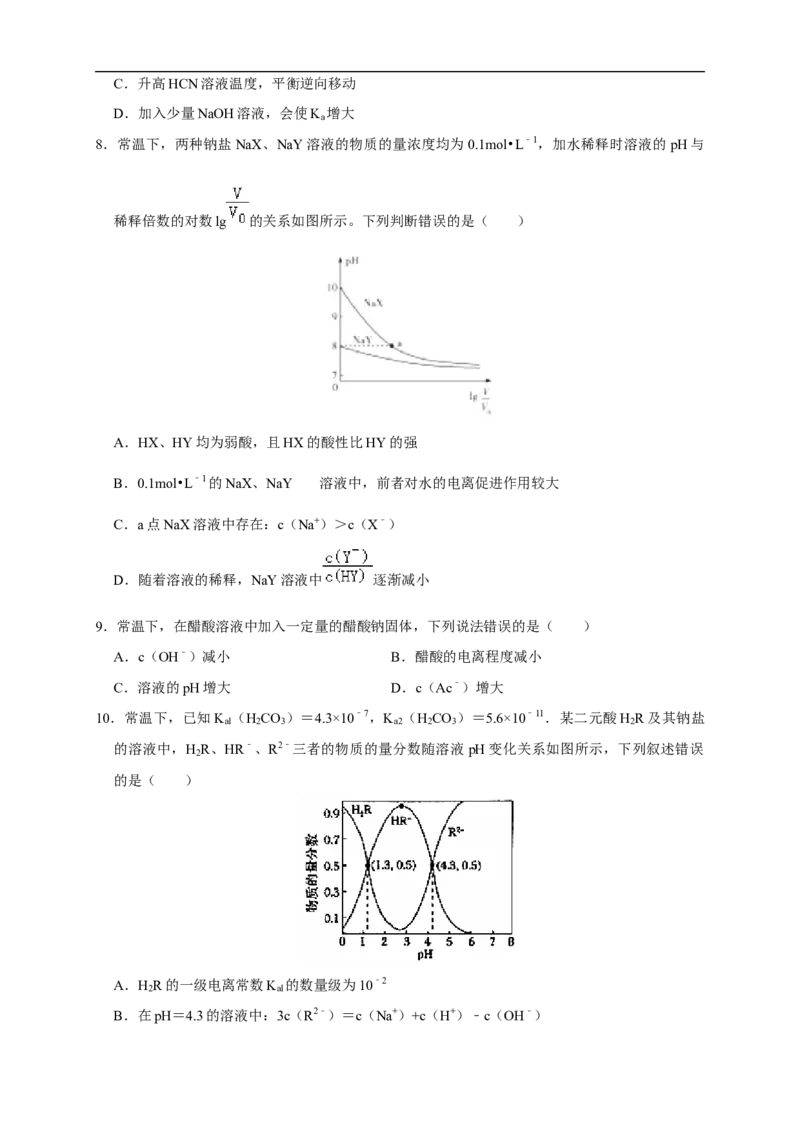
6.298K时,使用NaOH调节溶液pH过程中,二元弱酸H X溶液中含X微粒的分布分数如图所示
2
下列叙述中正确的是( )
A.溶液pH由1升至2.6时主要存在的反应是H X+OH﹣═HX﹣+H O
2 2
B.NaHX溶液中c(H+)=c(OH﹣)
C.K (H X)=10﹣7
a2 2
D.溶液呈中性时,c(Na+)=2c(X2﹣)
7.氢氰酸(HCN)是一种弱酸,在水溶液中存在电离平衡:HCN⇌H++CN﹣,常温下电离常数为
K .下列说法正确的是( )
a
A.0.1mol•L﹣1HCN溶液的pH<1
B.增大HCN溶液浓度,其电离程度减小C.升高HCN溶液温度,平衡逆向移动
D.加入少量NaOH溶液,会使K 增大
a
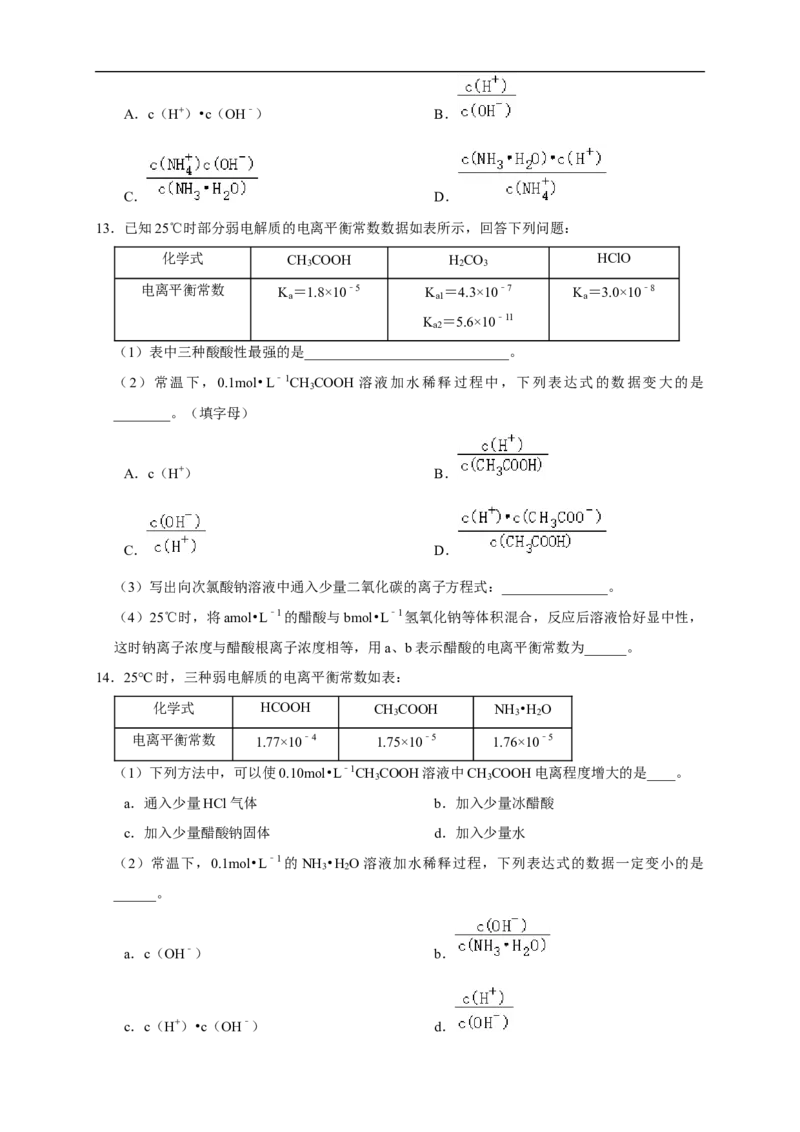
8.常温下,两种钠盐NaX、NaY溶液的物质的量浓度均为0.1mol•L﹣1,加水稀释时溶液的pH与
稀释倍数的对数lg 的关系如图所示。下列判断错误的是( )
A.HX、HY均为弱酸,且HX的酸性比HY的强
B.0.1mol•L﹣1的NaX、NaY 溶液中,前者对水的电离促进作用较大
C.a点NaX溶液中存在:c(Na+)>c(X﹣)
D.随着溶液的稀释,NaY溶液中 逐渐减小
9.常温下,在醋酸溶液中加入一定量的醋酸钠固体,下列说法错误的是( )
A.c(OH﹣)减小 B.醋酸的电离程度减小
C.溶液的pH增大 D.c(Ac﹣)增大
10.常温下,已知K (H CO )=4.3×10﹣7,K (H CO )=5.6×10﹣11.某二元酸H R及其钠盐
al 2 3 a2 2 3 2
的溶液中,H R、HR﹣、R2﹣三者的物质的量分数随溶液pH变化关系如图所示,下列叙述错误
2
的是( )
A.H R的一级电离常数K 的数量级为10﹣2
2 al
B.在pH=4.3的溶液中:3c(R2﹣)=c(Na+)+c(H+)﹣c(OH﹣)C.等体积、等浓度的NaOH溶液与H R溶液混合后,溶液中:c(R2﹣)>c(H R)
2 2
D.向Na CO 溶液中加入少量H R溶液,发生的反应是:CO 2﹣+H R═HCO ﹣+HR﹣
2 3 2 3 2 3
11.在一定温度下,有a、盐酸b、硫酸c、醋酸三种酸(用a、b、c填空):
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是_______________。
(2)若三者pH相同时,中和等体积的该三种溶液所需NaOH的物质的量由大到小的顺序是
________________。
(3)将 c(H+)相同的三种酸均加水稀释至原来的 100 倍后,pH 由大到小的顺序是
_______________。
(4)在25℃下,将amol/L的醋酸与0.01mol/L的NaOH溶液等体积混合后溶液的pH=7,用含
a的代数式表示25℃时CH COOH的电离常数K =__________
3 a
(5)设计一个实验证明醋酸是弱电解质:
操作:_______________________________________________
现象:______________
结论:醋酸是弱电解质。
12.弱电解质有许多如:醋酸、碳酸、氢氰酸、一水合氨等,已知25℃时,醋酸、碳酸、氢氰酸
的电离平衡常数如表:
氢氰酸 碳酸 醋酸
K =6.2×10﹣10 K =4.2×10﹣7Ka =5.6×10﹣11 K =1.7×10﹣5
a a1 2 a
(1)25℃时,pH相等的三种溶液①CH COONa溶液、②Na CO 溶液、③NaCN溶液,浓度由
3 2 3
大到小的顺序为________________。(填序号)
( 2 ) 25℃ 时 , 向 NaCN 溶 液 中 通 入 少 量 CO , 反 应 的 离 子 方 程 式 为
2
__________________________。
(3)将浓度为0.02mol/L的HCN与0.01mol/L NaOH溶液等体积混合,则混合溶液中c(H+)
____c(OH﹣)。(用“<”或“>”或“=”填空)
(4)常温下,向浓度为0.1mol•L﹣1、体积为VL的氨水中逐滴加入一定浓度的盐酸,用pH计
测溶液的pH随盐酸的加入量而降低的滴定曲线,d点两种溶液恰好完全反应。根据图中信息回
答下列问题:
①该温度时NH •H O的电离常数K=________。
3 2
②比较b、c、d三点时的溶液中,由水电离出的c(H+)由大到小顺序为______。(填字母,下
同)
③滴定时,由b点到c点的过程中,下列各选项中数值保持不变的______。A.c(H+)•c(OH﹣) B.
C. D.
13.已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
化学式 CH COOH H CO HClO
3 2 3
电离平衡常数 K =1.8×10﹣5 K =4.3×10﹣7 K =3.0×10﹣8
a a1 a
K =5.6×10﹣11
a2
(1)表中三种酸酸性最强的是_____________________________。
(2)常温下,0.1mol•L﹣1CH COOH 溶液加水稀释过程中,下列表达式的数据变大的是
3
________。(填字母)
A.c(H+) B.
C. D.
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:_______________。
(4)25℃时,将amol•L﹣1的醋酸与bmol•L﹣1氢氧化钠等体积混合,反应后溶液恰好显中性,
这时钠离子浓度与醋酸根离子浓度相等,用a、b表示醋酸的电离平衡常数为______。
14.25°C时,三种弱电解质的电离平衡常数如表:
化学式 HCOOH CH COOH NH •H O
3 3 2
电离平衡常数 1.77×10﹣4 1.75×10﹣5 1.76×10﹣5
(1)下列方法中,可以使0.10mol•L﹣1CH COOH溶液中CH COOH电离程度增大的是____。
3 3
a.通入少量HCl气体 b.加入少量冰醋酸
c.加入少量醋酸钠固体 d.加入少量水
(2)常温下,0.1mol•L﹣1的NH •H O溶液加水稀释过程,下列表达式的数据一定变小的是
3 2
______。
a.c(OH﹣) b.
c.c(H+)•c(OH﹣) d.