文档内容
★秘密·2024年3月12日18:00前
重庆市 2023-2024 学年(下)3 月月度质量检测
高三化学答案及评分标准
【命题单位:重庆缙云教育联盟】
一、选择题(共14小题,每题3分,共42分)
题号 1 2 3 4 5 6
答案 C D D D B B
题号 7 8 9 10 11 12
答案 D B D C A C
题号 13 14
答案 D D
1.A.铜和硫粉共热时直接化合生成Cu S,A项不符合题意;B.氯气和铁加热时直接化合生成FeCl ,B
2 3
项不符合题意;C.N 和O 高温或放电条件下直接化合生成NO,不能生成NO ,NO和O 化合生成
2 2 2 2
NO ,C项符合题意;D.N 和H 在高温、高压、催化剂的作用下直接化合生成FeCl ,D项不符合题意;
2 2 2 3
答案选C。
2.A. 过程中Cl元素的化合价发生改变,故有电子的转移,A不合题意; B. 过
程中Cu元素的化合价发生改变,故有电子的转移,B不合题意; C. 过程中Fe元素的化合
价发生改变,故有电子的转移,C不合题意;D. 过程中S、O元素的化合价都没有发生改变,
故无电子的转移,D符合题意;故答案为:D。
3.A.通过取代反应转化,故A错误;B.通过氧化反应转化,故B错误;C.通过取代反应转化,故C错误;
D.有双键可通过加成反应转化,故D正确。故答案为D。
4.A.清除河底污泥以提高水的质量,有利于水域的保护,A正确;B. 禁止生活污水、小企业废水和其它
未经处理的水排入河中,有利于水体的保护,B正确;C. 鼓励市民和企业采用低碳经济方式进行活动和
生产,减少水体污染,C正确;D. 护城河边的居民可以适当地将生活垃圾和废水倒入河中,增加水体污
染,D错误;答案选D。
5.A.该物质中含有苯环,属于芳香族化合物,A正确;B.该物质含有酚羟基、氯原子、酰胺键、硝基
共四种官能团,B错误;C.该物质不含羧基,所以不能和碳酸氢钠溶液反应,C正确;D.该物质含有苯
环,可以发生加成反应,酚羟基的邻位有空位,可以和溴发生取代反应,D正确;综上所述答案为B。
高三化学答案 第 1 页 共 4 页
学科网(北京)股份有限公司6. 属于易溶强碱弱酸盐,为强电解质,在水中完全电离出 、 , 会发
生微弱水解: ,溶液呈碱性,因此溶液中微粒浓度关系为:
,故答案为B。
7.A.由分析可知,甲池中的石墨电极是电池的正极,故A错误;B.原电池工作时,阳离子向正极移动,
H+通过全氟磺酸膜从乙池进入甲池,故B错误;C.甲池中石墨电极上发生的电极反应为AQ+2H++2e-
=H AQ,故C错误;D.通入硫化氢和氧气,分别生成硫、过氧化氢,则总反应为HS+O HO+S↓,
2 2 2 2 2
故D正确;故答案选D。
8.A.反应前后气体分子数相等,随着反应的进行体系压强不变,容器内压强保持不变,不一定达平衡
状态,故A错误;B.该反应生成固体,则混合气体的质量变化,当其不变时,说明反应达到化学平衡状
态,故B正确;C.反应前后气体分子数相等,则物质的量不变,在恒容密闭容器中体积不变,则混合气
体的总物质的量浓度一直不变,不能说明到达化学平衡状态,故C错误;D.反应前后气体分子数相等,
反应体系中气体的总物质的量是一定值,不能说明到达化学平衡状态,故D错误;故选:B。
9.A.铝粉投入到NaOH溶液中,反应生成偏铝酸钠和氢气,反应的离子方程式为:2Al+2H O+2OH-
2
=2AlO -+3H ↑,A正确;B.Al(OH) 是两性氢氧化物,可溶于NaOH溶液中,反应生成偏铝酸钠和水,反
2 2 3
应的离子方程式为:Al(OH) +OH-=AlO -+2H O,B正确;C.FeCl 溶液跟Cl 反应生成氯化铁,反应的离子
3 2 2 2 2
方程式为:2Fe2++Cl=2Fe3++2Cl-,C正确;D.AlCl 溶液中加入足量的氨水,反应生成氯化铵和氢氧化铝沉
2 3
淀,正确的离子方程式为:Al3++3NH•H O= Al(OH) ↓+3NH+,D错误;故合理选项是D。
3 2 3 4
10.A.玻璃以纯碱、石灰石和石英为原料,水泥以黏土和石灰石为主要原料,陶瓷以黏土为原料,故A
错误;B.聚丙烯中无碳碳双键,不能使溴水褪色,故B错误;C.银催化作用下,乙烯和氧气反应只生
成环氧乙烷,原子利用率为100%,符合“原子经济”,故C正确;D.能消杀病毒的过氧乙酸,具有强
氧化性、弱酸性等性质,是弱电解质,故D错误;故选:C。
11.A.HO 结构式为H-O-O-H,含有极性共价键H-O和非极性共价键O-O,极性不能抵消,是含有非极
2 2
性键的极性分子,A说法正确;B.激发态的钾原子回到基态,释放能量,会形成发射光谱,B说法错误;
C.向草酸亚铁溶液中滴加酸性KMnO 溶液,草酸根离子与亚铁离子均有还原性,则紫色褪去不能证明溶
4
液中含有Fe2+,C说法错误;D.酸的强弱与其电离出的H+个数无关,D说法错误;答案为A。
高三化学答案 第 2 页 共 4 页
学科网(北京)股份有限公司12.A.AlCl 溶液与烧碱溶液反应,当n(OH-):n(Al3+)=7:2时,铝离子部分转化为氢氧化铝和偏
3
铝酸盐,则反应的离子方程式为2Al3++ 7OH-=Al(OH) ↓+ AlO -+ 2H O,A正确;B.CuCl 溶液与NaHS溶
3 2 2 2
液反应,当n(CuCl ):n(NaHS)=1:2时反应的离子方程式为Cu2++2HS-=CuS↓+HS↑,B正确;
2 2
C.Cl 与FeBr 溶液反应,当n(Cl):n(FeBr )=1:1时溴部分被氧化,亚铁离子全部被氧化,则反
2 2 2 2
应的离子方程式为2Fe2++2Br-+2Cl=2Fe3++Br +4Cl-,C错误;D.Fe与稀硝酸反应,当n(Fe):n
2 2
(HNO)=1:2时铁过量,反应的离子方程式为3Fe +2NO -+8H+=3Fe2++2NO↑+4HO,D正确。答案选
3 3 2
C。
13.A.根据图示可知,1-溴-2-丁烯的能量低,更稳定,因此反应时间越长,得到1-溴-2丁烯的比例越大,
A错误;B.根据图示可知,生成3-溴-1-丁烯的第二步反应的活化能低,因此短时间内,生成3-溴-1-丁烯
的比例大,故生成1-溴-2-丁烯的平均速率为 ,B错误;C.根据盖斯定律,生成3-
溴-1-丁烯的反应热为 ,,生成1-溴-2-丁烯的反应热为 ,C错误;D.根据图示可
知,第一步反应的活化能大于第二步反应的活化能,故第一步即 H+与烯烃结合的一步为决速步,第二步
反应中生成3-溴-1-丁烯的活化能小,即 Br-进攻时活化能小的反应得到3-溴-1-丁烯,D正确; 故选D。
14.A. ,由 点可知 ,数量级为 ,故A正确; B.由电
离常数和水解常数知, 溶液显酸性、 溶液显碱性,第一步滴定选择甲基橙作指示剂、第二步
滴定选择酚酞作指示剂,故B正确;C. 点为 溶液, 电离程度大于水解,溶液中
,故C正确;D. 点和 点溶液的 不同,溶液中 不相
等,故D错误;故选D。
15.(1)H
2
(2)促进AlCl 的水解,使晶体析出
3
(3)HCl
(4)bd
(5) bc 硝酸 过滤、洗涤
高三化学答案 第 3 页 共 4 页
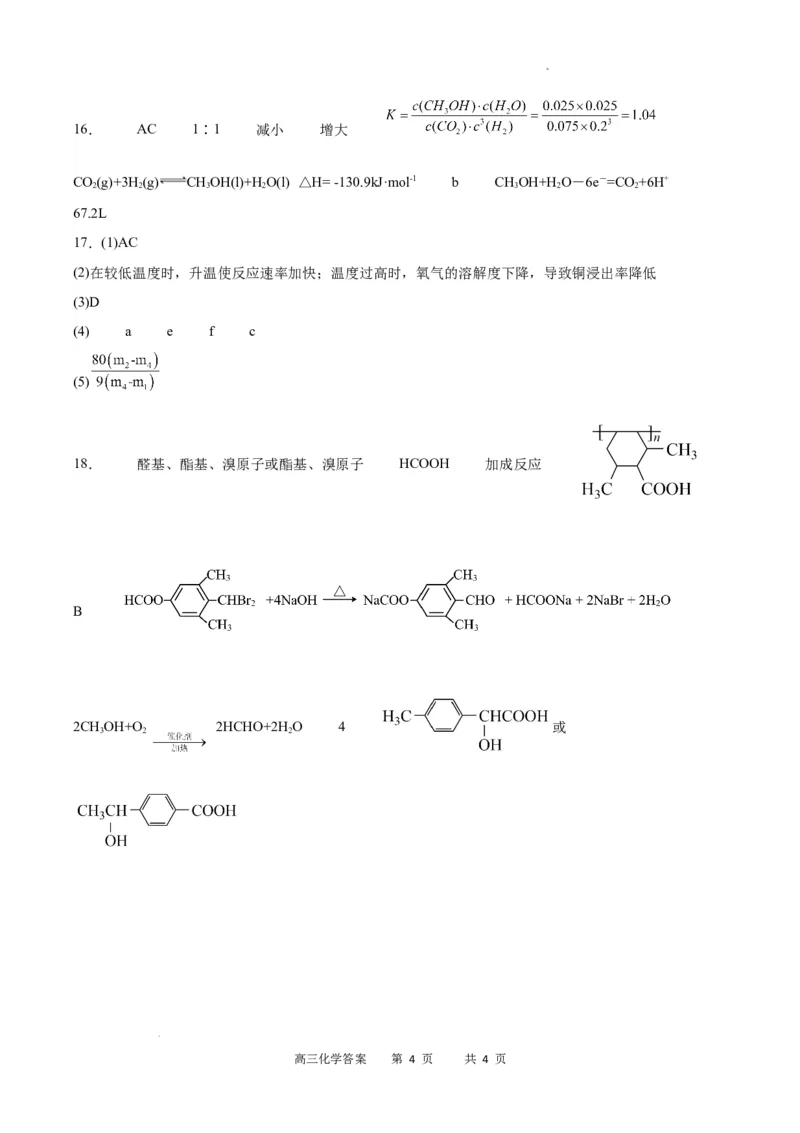
学科网(北京)股份有限公司16. AC 1∶1 减小 增大
CO(g)+3H(g) CHOH(l)+H O(l) △H= -130.9kJ·mol-1 b CHOH+H O-6e-=CO +6H+
2 2 3 2 3 2 2
67.2L
17.(1)AC
(2)在较低温度时,升温使反应速率加快;温度过高时,氧气的溶解度下降,导致铜浸出率降低
(3)D
(4) a e f c
(5)
18. 醛基、酯基、溴原子或酯基、溴原子 HCOOH 加成反应
B
2CHOH+O 2HCHO+2H O 4 或
3 2 2
高三化学答案 第 4 页 共 4 页
学科网(北京)股份有限公司