文档内容
第一章第一节物质的分类及转化小题狂做--人教版(2019)
必修第一册
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列有关物质的分类正确的是
A.氧化物: 、 、
B.碱: 、 、
C.混合物:氢氧化铁胶体、矿泉水、液氯
D.碱性氧化物:过氧化钠、生石灰、铁红
2.下列2022年“全球十大突破性技术”中,发生化学变化的是
A.计算机系统终结密码 B.实用型核聚变反应堆
C.合成抗疟疾和流感的新疫苗 D.AI数据生成
3.下列物质的分类正确的是
A.氧气、水、干冰都属于氧化物 B.NaCl、CuSO 、KMnO 都属于盐
4 4
C.NaHSO、HNO、HPO 都属于酸 D.烧碱、纯碱、熟石灰都属于碱
4 3 3 4
4.下列说法不正确的是
A.咳嗽产生的飞沫分散到空气中易形成气溶胶
B.分散质粒子直径为1-100nm的分散系为胶体
C.可以用丁达尔效应鉴别溶液与胶体
D.明矾溶于水形成胶体用于饮用水的杀菌消毒
5.化学与科技、生产、生活密切相关。下列说法正确的是
A.航母拦阻索的主要材料特种钢属于合金材料
B.硼硅玻璃中含有的NaO•B O•SiO 是一种复杂的氧化物
2 2 3 2
C.用于3D打印的高聚物光敏树脂是纯净物
D.用于净水的纳米铜粉属于胶体
6.Fe(OH) 胶体虽然是由 FeCl 溶液制得,但两者是截然不同的两种物质。FeCl 溶
3 3 3
液、Fe(OH) 胶体共同具有的性质是
3
A.都呈透明的红褐色
B.当有光线透过时,都能产生丁达尔效应
C.稳定,密封保存一段时间都不会产生沉淀
D.都能通过半透膜7.下列关于胶体的叙述正确的是
A.将饱和FeCl 溶液滴入沸腾的NaOH溶液中,可得到氢氧化铁胶体
3
B.制备的Fe(OH) 胶体能长期稳定存在
3
C.胶体与溶液的本质区别:能否产生丁达尔效应
D.新冠病毒奥密克戎变异株可通过气溶胶传播,气溶胶属于胶体
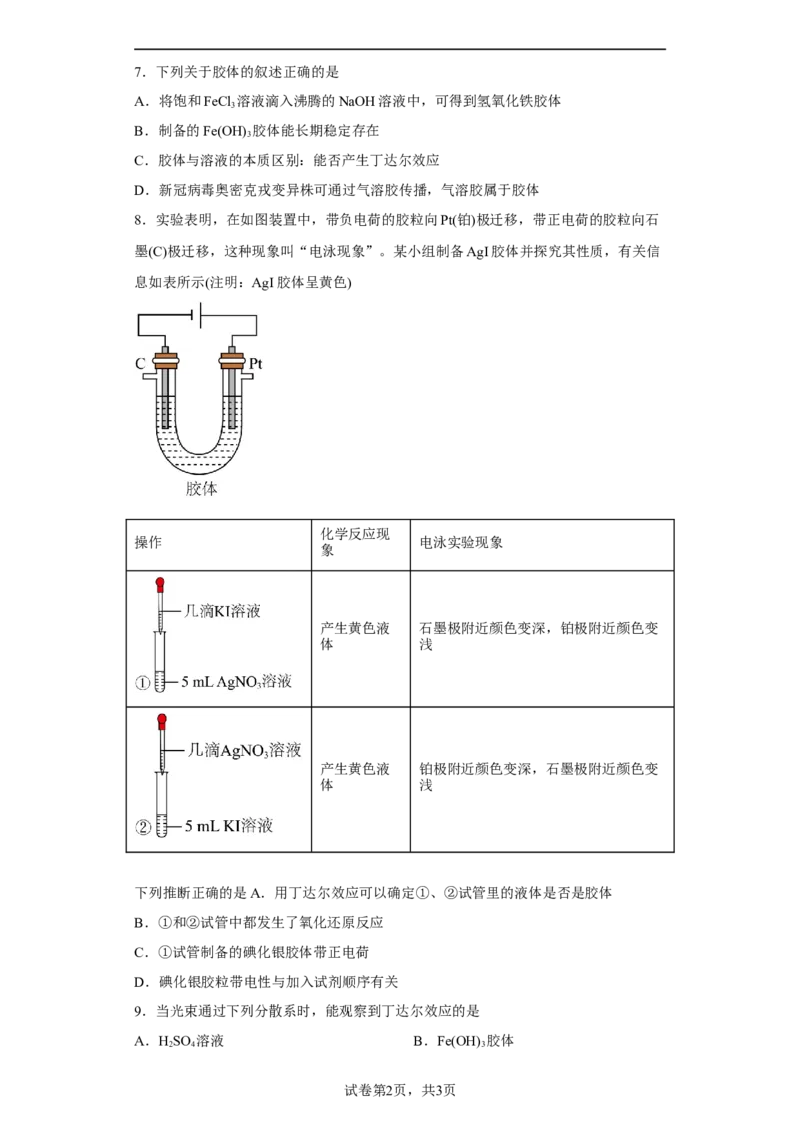
8.实验表明,在如图装置中,带负电荷的胶粒向Pt(铂)极迁移,带正电荷的胶粒向石
墨(C)极迁移,这种现象叫“电泳现象”。某小组制备AgI胶体并探究其性质,有关信
息如表所示(注明:AgI胶体呈黄色)
化学反应现
操作 电泳实验现象
象
产生黄色液 石墨极附近颜色变深,铂极附近颜色变
体 浅
产生黄色液 铂极附近颜色变深,石墨极附近颜色变
体 浅
下列推断正确的是A.用丁达尔效应可以确定①、②试管里的液体是否是胶体
B.①和②试管中都发生了氧化还原反应
C.①试管制备的碘化银胶体带正电荷
D.碘化银胶粒带电性与加入试剂顺序有关
9.当光束通过下列分散系时,能观察到丁达尔效应的是
A.HSO 溶液 B.Fe(OH) 胶体
2 4 3
试卷第2页,共3页C.NaSO 溶液 D.蔗糖溶液
2 4
10.下列有关胶体的叙述不正确的是
A.胶体区别于其他分散系的本质特征是分散质粒子的直径在1nm~100nm之间
B.雾、云都会出现丁达尔现象
C.Fe(OH) 胶体不能透过半透膜和滤纸
3
D.长江三角洲的形成与胶体的聚沉有关
11.化学与生活密切相关,下列关于化学与生活的说法不正确的是
A.“肾功能衰竭”的病人需要做“血液透析”,其原理与胶体的提纯有关
B.雄黄 和雌黄 中, 的化合价不相同
C.碳酸氢钠、氢氧化铝凝胶都可以用作治疗胃酸过多的药物
D.湖水加入明矾可以净水,是由于明矾中铝离子与水反应生成的氢氧化铝胶体可以
吸附细菌和病毒而消毒
12.下列物质中属于碱性氧化物的是
A. B. C. D.
13.当光束通过下列分散系时,能观察到丁达尔效应的是
A.盐酸 B.NaOH溶液 C.Fe(OH) 胶体 D.硫酸铜溶液
3
14.胶体与其它分散系的本质区别是
A.能产生丁达尔效应 B.胶体微粒能通过滤纸
C.分散质直径在 之间 D.胶体有颜色
15.当光束通过下列物质时,出现丁达尔效应的是
A.稀硫酸 B. 溶液 C. 胶体 D.氯水
二、填空题
16.定性和定量是中学化学研究物质性质、组成的常用方法。胶体是一种重要的分散
系(三种分散系分散质粒子大小如图示)。某兴趣小组按如下实验步骤制备Cu(OH) 胶体:用洁净的烧杯取少量蒸馏水,加热至
2
沸腾,向烧杯中慢慢加入数滴浓CuCl 溶液,得到蓝色透明的液体。制备原理用化学
2
方程式表示为:CuCl +2H O(沸水)=Cu(OH) (胶体)+2HCl。
2 2 2
(1)Cu(OH) 胶体中分散质微粒直径范围是_____。
2
A.小于1nm B.1~10nm C.1~100 D.大于100nm
(2)Cu(OH) 浊液与Cu(OH) 胶体性质不同,本质原因是_____。
2 2
A.分散剂的种类不同 B.颜色和透明程度不同
C.分散质粒子的大小不同 D.分散质粒子所带电荷不同
(3)下列哪种用于判断胶体制备成功的方法最简单_____。
A.丁达尔现象 B.半透膜实验 C.聚沉 D.电泳
(4)实验过程中,有一位同学向烧杯中一次性加入大量CuCl 溶液,结果没有制得胶体,
2
反而出现了浑浊,请分析他实验失败的原因_____。
17.由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水
溶性蛋白质混合物,溶于水形成胶体。
(1)已知 中铬元素是 价,则其中铁元素是_______价。 是一种酸根离
子,则 属于_______(填“酸”、“碱”、“盐”或“氧化物”)。
(2)明胶的水溶液和 溶液共同具备的性质是_______(填序号)。
a.都不稳定,密封放置会产生沉淀 b.二者均有丁达尔效应 c.分散质粒子可通过
滤纸
(3)下列各项与胶体性质有关的有_______。(填序号)
a.卤水点豆腐 b.明矾净水 c.油水分离 d.血液透析
e.酸碱中和 f.三角洲形成 g.制备氢氧化铁沉淀 h.臭氧消毒
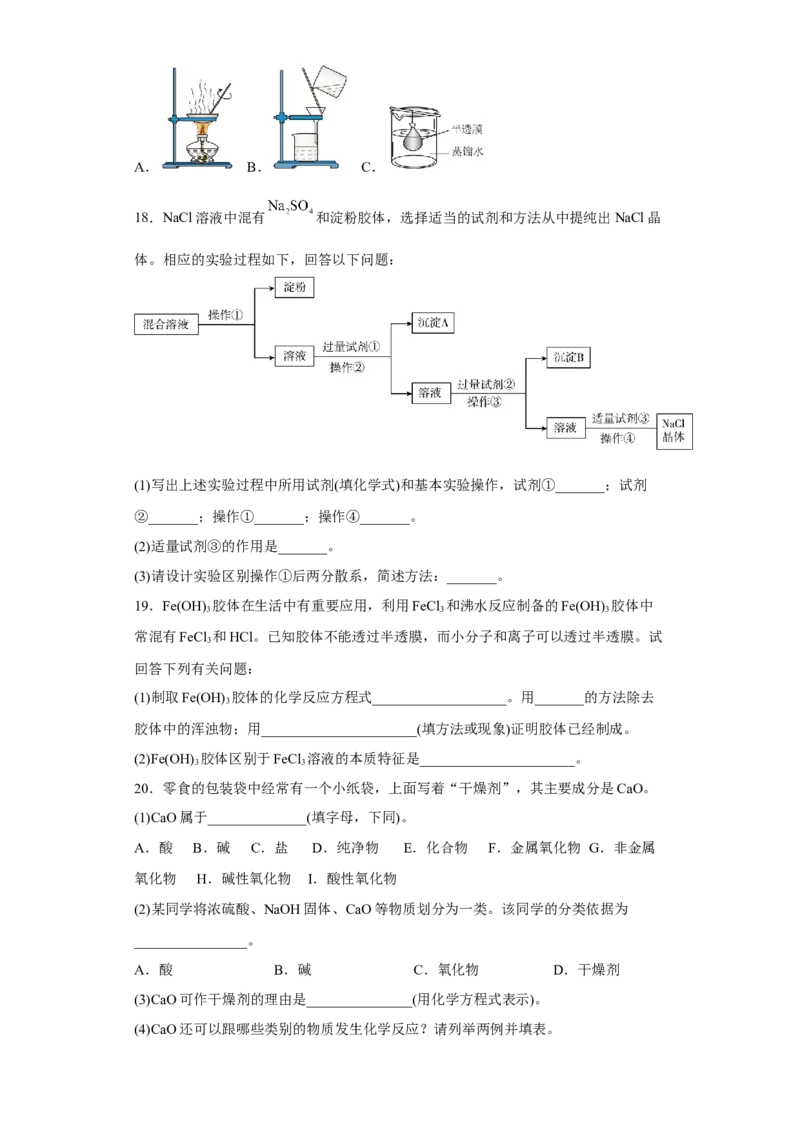
(4)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯
明胶的装置是下列中的_______(填序号)。
试卷第4页,共3页A. B. C.
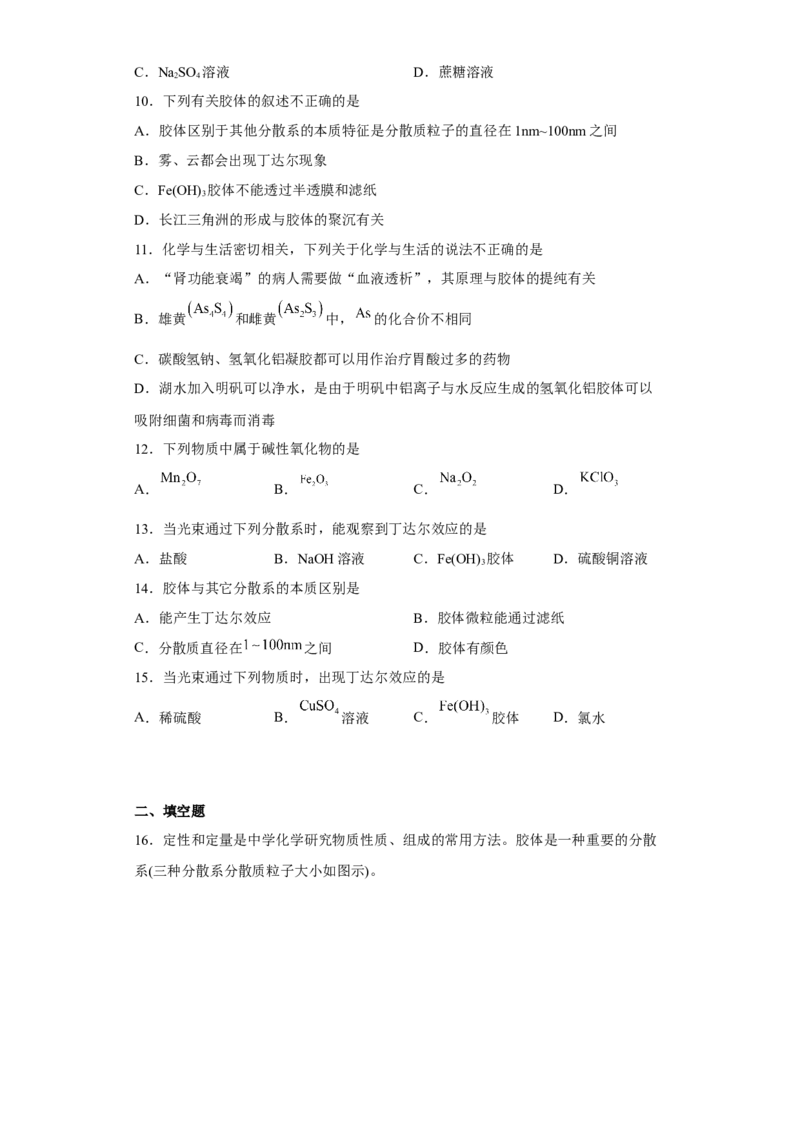
18.NaCl溶液中混有 和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶
体。相应的实验过程如下,回答以下问题:
(1)写出上述实验过程中所用试剂(填化学式)和基本实验操作,试剂①_______;试剂
②_______;操作①_______;操作④_______。
(2)适量试剂③的作用是_______。
(3)请设计实验区别操作①后两分散系,简述方法:_______。
19.Fe(OH) 胶体在生活中有重要应用,利用FeCl 和沸水反应制备的Fe(OH) 胶体中
3 3 3
常混有FeCl 和HCl。已知胶体不能透过半透膜,而小分子和离子可以透过半透膜。试
3
回答下列有关问题:
(1)制取Fe(OH) 胶体的化学反应方程式___________________。用_______的方法除去
3
胶体中的浑浊物;用______________________(填方法或现象)证明胶体已经制成。
(2)Fe(OH) 胶体区别于FeCl 溶液的本质特征是______________________。
3 3
20.零食的包装袋中经常有一个小纸袋,上面写着“干燥剂”,其主要成分是CaO。
(1)CaO属于______________(填字母,下同)。
A.酸 B.碱 C.盐 D.纯净物 E.化合物 F.金属氧化物 G.非金属
氧化物 H.碱性氧化物 I.酸性氧化物
(2)某同学将浓硫酸、NaOH固体、CaO等物质划分为一类。该同学的分类依据为
________________。
A.酸 B.碱 C.氧化物 D.干燥剂
(3)CaO可作干燥剂的理由是_______________(用化学方程式表示)。
(4)CaO还可以跟哪些类别的物质发生化学反应?请列举两例并填表。物质类别 化学方程式
_______________ _______________
_______________ _______________
试卷第6页,共3页参考答案:
1.A
【详解】A.由两种元素构成其中一种元素是氧的化合物叫氧化物,A正确;
B. 是碱式盐,B错误;
C.液氯是单质,是纯净物,C错误;
D.过氧化钠是过氧化物,溶于水生成氢氧化钠和氧气,不是碱性氧化物,D错误;
故选A。
2.C
【分析】有新物质生成的变化是化学变化,据此解答。
【详解】A.计算机系统终结密码过程中没有产生新物质,不是化学变化,A不选;
B.实用型核聚变反应堆过程中没有产生新物质,不是化学变化,B不选;
C.合成抗疟疾和流感的新疫苗过程中产生新物质,属于化学变化,C选;
D.AI数据生成过程中没有产生新物质,不是化学变化,D不选;
答案选C。
3.B
【详解】A.氧气是单质,不属于氧化物,A错误;
B.金属离子或铵根离子与酸根离子或非金属离子结合的化合物叫盐,NaCl、CuSO 、
4
KMnO 都属于盐,B正确;
4
C.硫酸氢钠电离出的阳离子不全部是氢离子,NaHSO 是酸式盐不属于酸,C错误;
4
D.纯碱碳酸钠不是碱而是盐,D错误;
故选B。
4.D
【详解】A.咳嗽产生的飞沫分散到空气中形成气溶胶,故A正确;
B.分散质粒子直径介于1~100nm之间的分散系为胶体,故B正确;
C.胶体能产生丁达尔效应,溶液不能,因此可以用丁达尔效应鉴别溶液与胶体,故C正
确;
D.明矾溶于水Al3+发生水解生成氢氧化铝胶体,胶体吸附水中悬浮杂质一起沉积到水底,
达到净化水的目的,但是不能杀菌消毒,故D错误;
故选D。
5.A
【详解】A.特种钢也叫合金钢,是一种钢材。特种钢是在碳素钢里适量地加入一种或几种合金元素,使钢的组织结构发生变化,从而使钢具有各种不同的特殊性能,故A正确;
B.NaO•B O•SiO 是一种硅酸盐,故B错误;
2 2 3 2
C.高聚物光敏树脂是聚合物,属于混合物,故C错误;
D.纳米材料直接1-100nm,但单纯的纳米铜只是分散质,不能形成分散系,所以不能叫做
胶体,故D错误;
故选A。
6.C
【分析】胶体是分散质粒子大小在 1nm~100nm 的分散系;
【详解】A.FeCl 溶液与Fe(OH) 胶体的颜色分别为棕黄色、红褐色,故A错误;
3 3
B.只有胶体具有丁达尔效应,所以Fe(OH) 胶体具有丁达尔效应,而FeCl 溶液不具备,
3 3
故B错误;
C.胶体具有介稳性,放置不会产生沉淀,溶液是稳定的,故C正确;
D.FeCl 溶液的微粒小于1nm能通过半透膜,Fe(OH) 胶体粒子大小在 1nm~100nm不能通
3 3
过半透膜,故D错误;
故选C。
7.D
【详解】A.制取 红褐色胶体应该向煮沸的蒸馏水中滴加饱和氯化铁溶液至溶液变
红褐色,A错误;
B.胶体具有相对的稳定性,外接条件的改变会破坏其稳定性,故制备的Fe(OH) 胶体不能
3
长期稳定存在,B错误;
C.胶体是分散质粒子大小在 1nm~100nm 的分散系;溶液是分散质粒子大小于1nm的分
散系;胶体与溶液的本质区别:分散质颗粒大小不同;C错误;
D.胶体是分散质粒子大小在 1nm~100nm 的分散系;病毒奥密克戎变异株可通过气溶胶
传播,气溶胶属于胶体,D正确;
故选D。
8.A
【详解】A.胶体能产生丁达尔效应,溶液不能产生,A项正确;
B.硝酸银和碘化钾混合发生复分解反应,B项错误;
C.胶体是分散系,不显电性,胶粒带电荷,C项错误;
D.碘化银胶粒可能带正电荷,也可能带负电荷,与反应物相对量有关。①试管中AgNO
3
答案第2页,共2页过量,胶粒带正电荷;②试管中KI过量,胶粒带负电荷,D项错误。
故选A。
9.B
【分析】胶体的分散质微粒能够使光线发生散射作用而沿直线传播,当用一束光照射胶体
时,在胶体中能够看到有一条光亮的通路,即发生丁达尔效应,而其它分散系不能产生丁
达尔效应,据此分析。
【详解】A..HSO 溶液属于溶液,不属于胶体,因此用光线照射时不能观察到丁达尔效
2 4
应,A不符合题意;
B.Fe(OH) 胶体属于胶体,用光线照射时能观察到丁达尔效应,B符合题意;
2
C.NaSO 溶液属于溶液,不属于胶体,因此用光线照射时不能观察到丁达尔效应,C不
2 4
符合题意;
D.蔗糖溶液属于溶液,不属于胶体,因此用光线照射时不能观察到丁达尔效应,D不符
合题意;
故合理选项是B。
10.C
【详解】A.胶体区别于其他分散系的本质特征是分散质粒子的直径在1nm~100nm之间,
故A正确;
B.雾、云都属于胶体,都会出现丁达尔现象,故B正确;
C.Fe(OH) 胶体能透过滤纸,不能透过半透膜,故C错误;
3
D.长江三角洲的形成是河水遇到海水中的电解质溶液发生的胶体聚沉,故D正确;
故选C。
11.D
【详解】A.“血液透析”利用血液中蛋白质、血细胞等不能透过半透膜而各种有毒物质
可以透过半透膜,即“渗析”,A项正确;
B.雄黄中砷为+2价,雌黄中砷为+3价, 的化合价不相同,B项正确;
C.碳酸氢钠、氢氧化铝凝胶都可以与胃酸中盐酸反应,可以用作治疗胃酸过多的药物,C
项正确;
D.明矾中的铝离子与水反应生成的氢氧化铝胶体只能吸附悬浮物,不能杀菌消毒,D项
错误;
故选D。
12.B【分析】碱性氧化物能与酸生成盐和水,与酸性氧化物生成盐。
【详解】A.MnO 虽然是金属氧化物,但它属于酸性氧化物,A错误;
2 7
B. 能和酸生成盐和水,是碱性氧化物,B正确;
C.NaO 与酸反应除了生成盐和水,还生成氧气,所以不是碱性氧化物,C错误;
2 2
D. 中含有3种元素不是氧化物,D错误;
故选B。
13.C
【详解】A.盐酸是氯化氢的水溶液,分散质粒子直径小于1nm,不能产生丁达尔效应,A
不符合题意;
B.NaOH溶液中,分散质粒子直径小于1nm,不能产生丁达尔效应,B不符合题意;
C.Fe(OH) 胶体中,分散质粒子直径介于1nm~100nm之间,能产生丁达尔效应,C符合题
3
意;
D.硫酸铜溶液中,分散质粒子直径小于1nm,对光不能产生散射作用,不能产生丁达尔
效应,D不符合题意;
故选C。
14.C
【详解】A.能产生丁达尔效应,是胶体的性质,可用于区分溶液和胶体,但不能区分胶
体和浊液,A不符合题意;
B.胶体微粒能通过滤纸,溶液中的微粒也能透过滤纸,不能用于区分胶体和溶液,B不符
合题意;
C.分散质粒子直径在 之间,则有别于溶液(分散质粒子直径小于1nm)、浊液(分
散质粒子直径大于100nm),C符合题意;
D.胶体有颜色,溶液和浊液也可能有颜色,不能用于区分胶体与其它分散质,D不符合
题意;
故选C。
15.C
【详解】A.稀硫酸属于溶液,不是胶体,没有丁达尔效应,故A不选;
B. 溶液,不是胶体,没有丁达尔效应,故B不选;
C. 胶体是液溶胶,具有丁达尔效应,当光束通过 胶体时,出现一条明亮
答案第4页,共2页的通路,故C选;
D.氯水属于溶液,不是胶体,没有丁达尔效应,故D不选;
故选C。
16.(1)C
(2)C
(3)A
(4)胶体发生了聚沉
【详解】(1)分散质微粒直径小于1nm的是溶液,大于100nm的是浊液,Cu(OH) 胶体粒
2
子的微粒直径在1-100nm之间,则选C。
(2)溶液、胶体、浊液的本质区别是分散质粒子的直径,则Cu(OH) 浊液与Cu(OH) 胶体
2 2
性质不同,本质原因是分散质粒子的大小不同,选C。
(3)胶体具有的性质:①能产生丁达尔效应;②胶体粒子能通过滤纸但不能通过半透膜;
③能产生电泳现象;④介稳性;⑤加热、加入电解质等发生聚沉等,其中胶体的丁达尔效
应操作简单现象明显,则用于判断胶体制备成功的方法最简单的方法是丁达尔现象,选
A。
(4)胶体加入电解质等发生聚沉等,故该同学没有制得胶体、反而出现了浑浊的原因是:
由于一次性加入大量CuCl 溶液,使胶体发生了聚沉。
2
17.(1) 盐
(2)c
(3)abdf
(4)C
【详解】(1)已知 中铬元素是 价,氧元素化合价为-2,根据化合价代数和为
零,则其中铁元素是 价。 是一种酸根离子,则 是由金属阳离子和酸根离
子构成的盐;
(2)a.溶液具有稳定性,胶体是介稳体系,a错误;
b.光束通过胶体时,光线能够发生散射作用而产生丁达尔效应,而通入其它分散系时不能
产生丁达尔效应;b错误;c.胶体和溶液的分散质粒子可通过滤纸,c正确;
故选c;
(3)a.卤水点豆腐是胶体的稳定性被破坏;
b.明矾净水是形成了氢氧化铝胶体;
c.油水分离是两者互不溶;
d.血液透析是利用了胶体的透析;
e.酸碱中和是生成盐和水;
f.三角洲形成 是胶体的稳定性被破坏;
g.制备氢氧化铁沉淀是氢氧化钠和铁盐生成沉淀;
h.臭氧消毒是臭氧的氧化性;
故选abdf;
(4)提纯明胶可以利用胶体的透析,故选C。
18.(1) BaCl Na CO 渗析 蒸发
2 2 3
(2)将溶液中过量的NaCO 转化为NaCl
2 3
(3)分别用激光笔照射两个分散系,若出现光亮的通路则为淀粉,若没出现则为溶液。
【分析】混合溶液中利用胶体和溶液粒子直径的不同将其分开,故操作①为渗析,渗析后
的溶液中含有NaCl和NaSO ,加入过量的BaCl ,生成BaSO 沉淀和NaCl,过滤将其分离,
2 4 2 4
故操作②为过滤,过滤后溶液中含有NaCl和BaCl ,加入过量的NaCO,生成BaCO 沉淀
2 2 3 3
和NaCl,过滤将其分离,故操作③为过滤,过滤后溶液中含有NaCl和NaCO,加入适量
2 3
的稀盐酸,生成NaCl、CO 和HO,蒸发得到NaCl晶体,故操作④为蒸发,据此进行分析。
2 2
【详解】(1)由分析可知,试剂①为BaCl ;试剂②为NaCO;操作①为渗析;操作④为
2 2 3
蒸发。
(2)由分析可知,适量试剂③的作用是将溶液中过量的NaCO 转化为NaCl。
2 3
(3)操作①后的分散系分别为溶液和胶体,可利用丁达尔效应进行区别,方法为:分别用
激光笔照射两个分散系,若出现光亮的通路则为淀粉,若没出现则为溶液。
19.(1) 过滤 丁达尔效应
(2)分散质粒子直径在1-100nm
【详解】(1)制取Fe(OH) 胶体的实验操作是在沸水中滴加几滴饱和氯化铁溶液,继续加
3
答案第6页,共2页热,当溶液出现红褐色出现,停止加热,即制得氢氧化铁胶体,化学反应方程式为
。因为胶体可以通过滤纸,而浊液的成分不能通过滤纸,
所以用过滤的方法除去胶体中的浑浊物;因为胶体有丁达尔效应,即一束光照射胶体,出
现光亮的通路,故可以用丁达尔效应证明胶体已经制成。
(2)Fe(OH) 胶体区别于FeCl 溶液的本质特征是分散质粒子直径的大小,胶体的分散质粒
3 3
子直径在1-100nm。
20.(1)DEFH
(2)D
(3)CaO+ H O=Ca(OH)
2 2
(4) 酸 酸性氧化物CO
2
【详解】(1)CaO是由两种元素构成其中一种是氧元素故CaO属于氧化物,且属于金属
氧化物、CaO由同种物质组成属于纯净物、由不同种元素构成的物质属于化合物、CaO能
与酸反应生成盐和水,故属于碱性氧化物,答案为DEFH。
(2)浓硫酸属于酸、NaOH固体属于碱、CaO属于氧化物,但三者都可以吸收水分,都可
以作干燥剂,故答案D。
(3)CaO与水反应生成氢氧化钙,反应的化学方程式为CaO+ H O=Ca(OH) ,可作干燥剂。
2 2
(4)CaO属于碱性氧化物能与水反应生成碱;能与酸反应生成盐和水;能与酸性氧化物反
应生成盐。故答案为:酸 CaO+2 HCl=CaCl2+ H O;酸性氧化物CO ;
2 2答案第8页,共2页