文档内容
人教版(2019)第一章第三节 氧化还原反应 第1课时 氧
化还原反应
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列物质的制备过程涉及氧化还原反应的是( )
A.用四氯化碳萃取溴水中的单质溴 B.压缩空气后分离制备氧气
C.将石油进行常压分馏制备航空柴油 D.加热氧化银制备单质银
2.下列说法正确的是( )
A.不能发生丁达尔效应的分散系有氯化钠溶液、水等
B.实现Fe→Fe O 的变化必须要加入氧化剂
3 4
C.NaSO 溶液在电流作用下电离出Na+与SO 2-而导电
2 4 4
D.离子反应可能是复分解反应,但离子反应一定不是氧化还原反应
3.下列反应属于氧化还原的是
A.氯气与水反应 B.盐酸与氢氧化钠溶液的反应
C.氯化铵固体受热分解 D.氢氧化钡与碳酸钠反应
4.TiCl +4Na 4NaCl+Ti,此反应中金属钠
4
A.只作氧化剂 B.只作还原剂
C.既作氧化剂又作还原剂 D.既不作氧化剂也不作还原剂
5.下列变化需要加入还原剂才能实现的是
A.Fe →FeSO B.Cu(NO ) → Cu .
4 3 2
C.CO→CO D.NaCl →AgCl
2
6.单晶硅是制作电子集成电路的基础材料。用化学方法可制得高纯度硅,其化学方程
式为:①SiO+2C Si+2CO②Si+2Cl SiCl ③SiCl + 2H Si+4HCl,其
2 2 4 4 2
中,反应①和③属于
A.复分解反应 B.分解反应 C.置换反应 D.化合反应
7.下列反应进行分类时,既属于氧化还原反应又属于化合反应的是( )
A.2FeCl +Cl=2FeCl B.Zn+H SO =ZnSO +H ↑
2 2 3 2 4 4 2
C.CO+CaO=CaCO D.CH+2O CO+2H O
2 3 4 2 2 2
8.下列叙述中,正确的是( )A.氧化还原反应的特征是化合价发生变化
B.反应物所含元素的化合价升高的反应为氧化还原反应
C.反应中氧化剂失电子,化合价降低
D.置换反应不一定是氧化还原反应
9.小郡同学在做“典籍里的化学”项目研究时,收集到四个素材,从氧化还原的角度
分析,其中一个与其他三个明显不同。这个素材是
A.煮豆燃豆萁——曹植,《七步诗》
B.爆竹声声一岁除——王安石,《元日》
C.要留清白在人间——于谦,《石灰吟》
D.曾青得铁则化为铜——准南王刘安,《淮南万毕术》
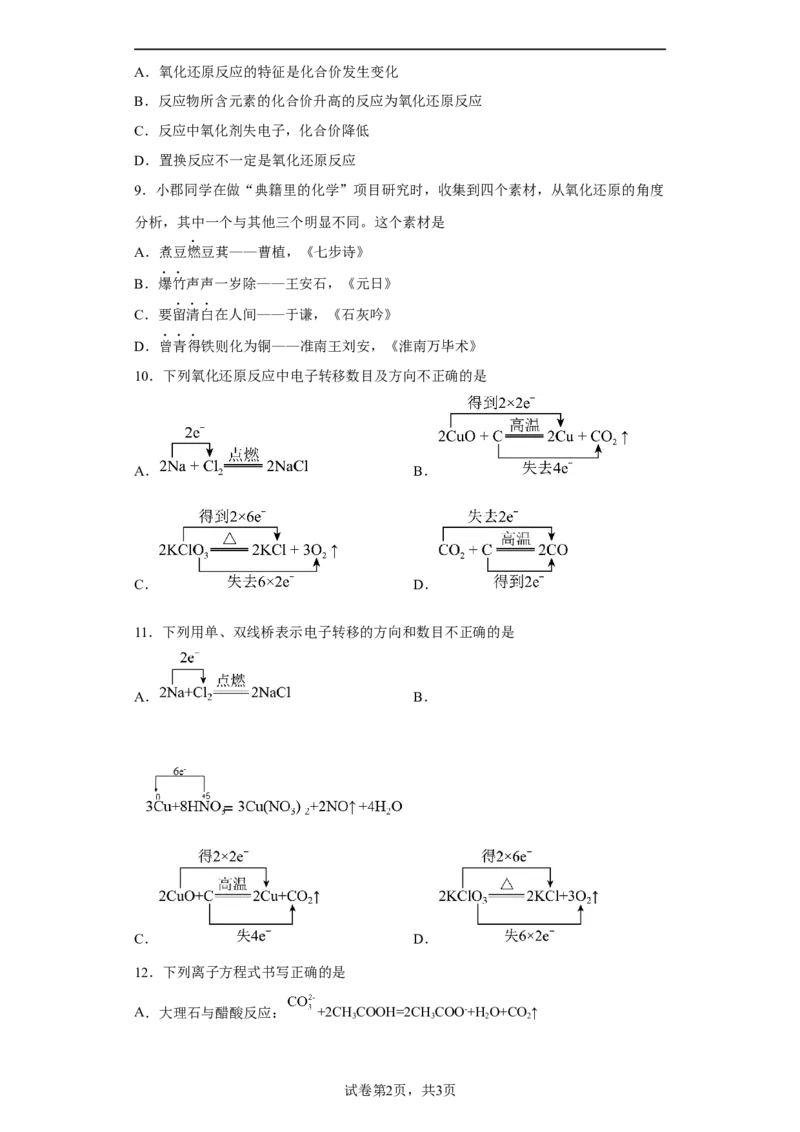
10.下列氧化还原反应中电子转移数目及方向不正确的是
A. B.
C. D.
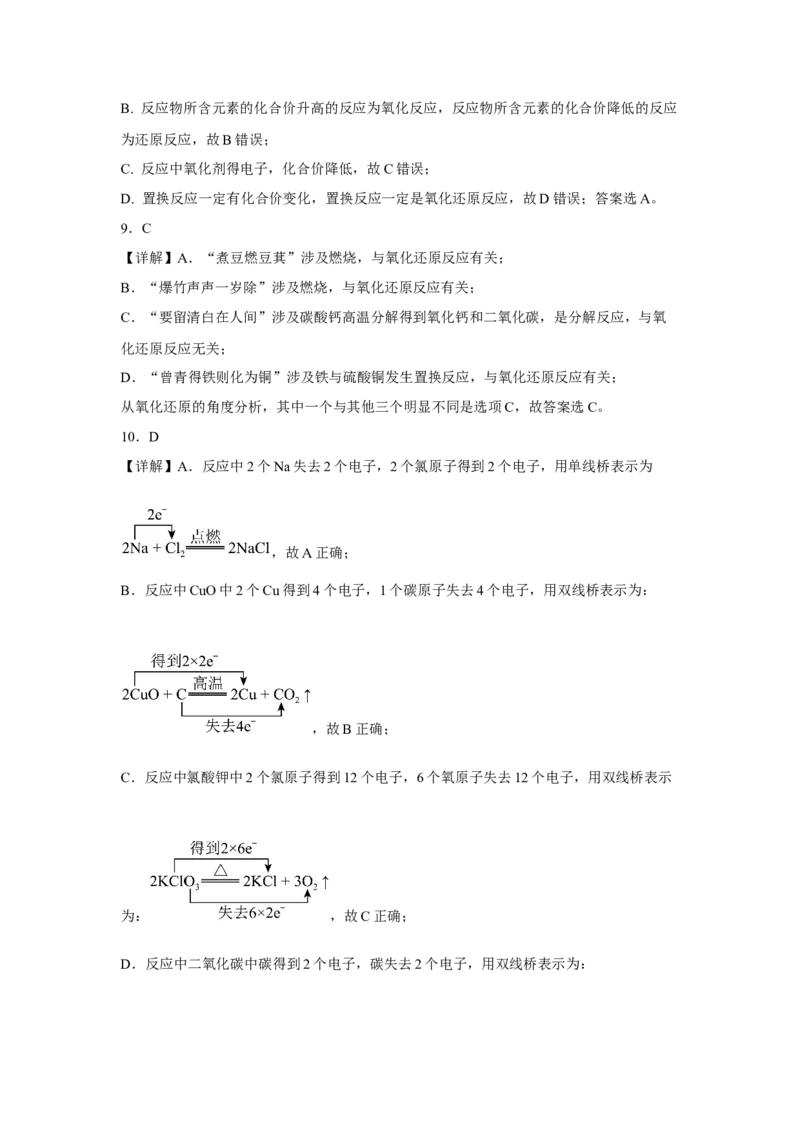
11.下列用单、双线桥表示电子转移的方向和数目不正确的是
A. B.
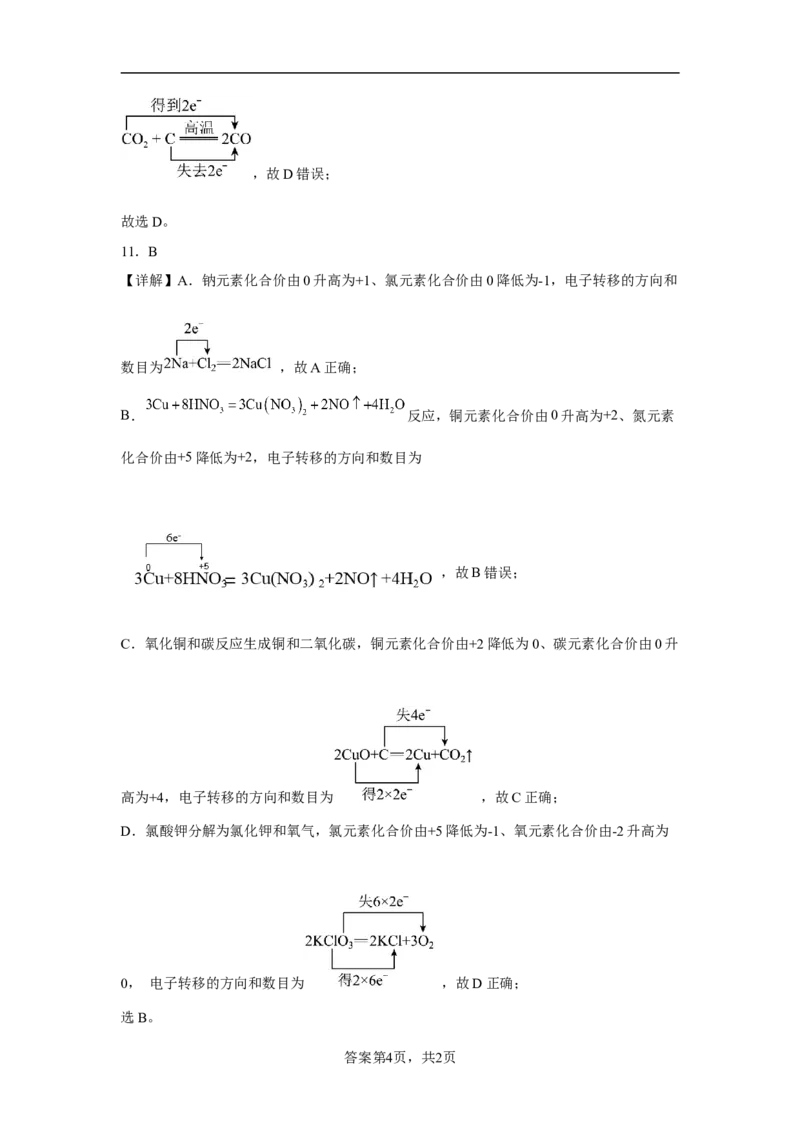
C. D.
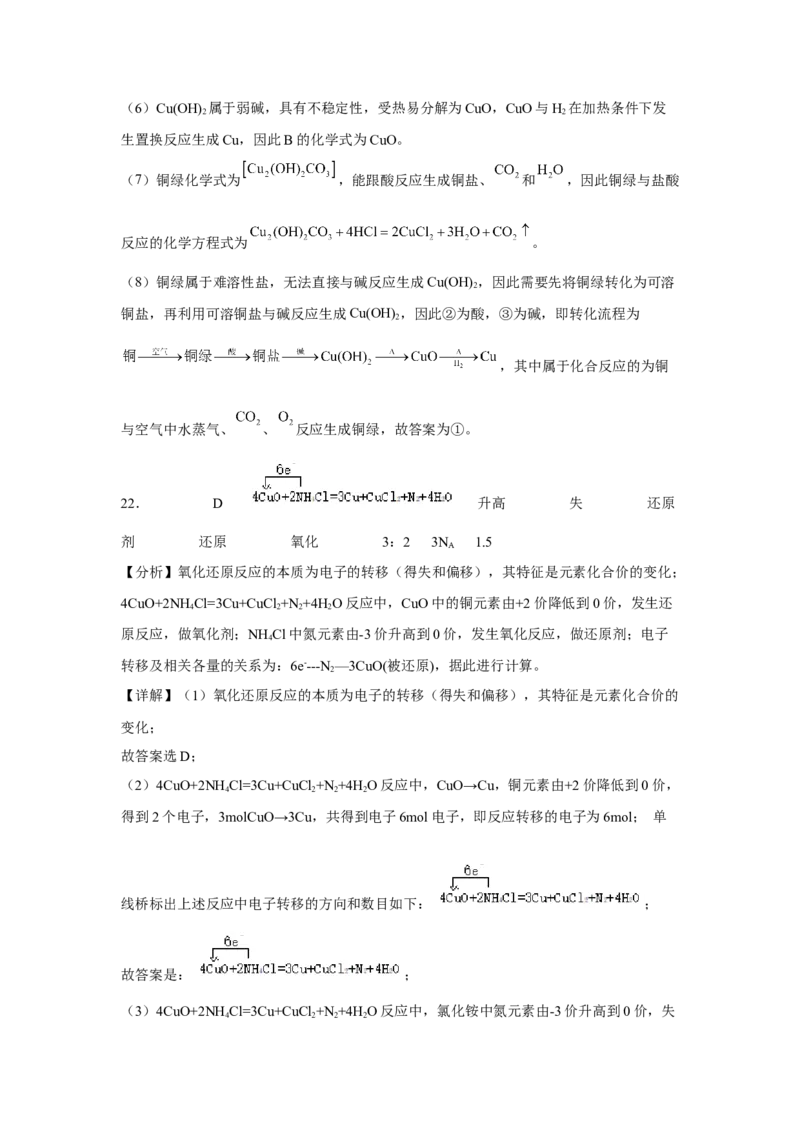
12.下列离子方程式书写正确的是
A.大理石与醋酸反应: +2CH COOH=2CH COO-+H O+CO↑
3 3 2 2
试卷第2页,共3页B.稀硫酸和氢氧化钡溶液反应:H++ +Ba2++OH-=BaSO ↓+H O
4 2
C.澄清石灰水与碳酸钠溶液反应:Ca(OH) + =CaCO ↓+2OH-
2 3
D.Fe2+与HO 在酸性溶液中的反应:2Fe2++H O+2H+=2Fe3++2H O
2 2 2 2 2
13.《中国诗词大会》带动全民重温那些曾经学过的古诗词,分享诗词之美,感受诗
词之趣,从古人的智慧和情怀中汲取营养,涵养心灵。下列诗句涉及氧化还原反应的
是
A.爆竹声中一岁除,春风送暖入屠苏
B.美人首饰侯王印,尽是沙中浪底来
C.南朝四百八十寺,多少楼台烟雨中
D.无边落木萧萧下,不尽长江滚滚来
14.下列反应中,既是化合反应,又是氧化还原反应的是( )
(1)铁和氯气反应 2Fe+3Cl=2FeCl
2 3
(2)氯气通入溴化钠溶液Cl+2NaBr=2NaCl+Br
2 2
(3)氯化钠溶液和浓硫酸混合加热2NaCl+HSO (浓)=Na SO +2HCl↑
2 4 2 4
(4)二氧化锰跟浓盐酸在加热条件下反应 MnO +4HCl(浓) MnCl +Cl↑+2HO
2 2 2 2
(5)氢气在氯气中燃烧 H+Cl=2HCl
2 2
A.(1)(2) B.(1)(3) C.(1)(4) D.(1)(5)
15.下列有关叙述、对应的方程式,所属基本反应类型都正确的是
A.拉瓦锡研究空气成分 分解反应
B.生石灰作干燥剂 化合反应
C.三氧化硫与氢氧化钠溶液反应 复分解反应
D.葡萄糖在人体内氧化 置换反应
16.属于氧化还原反应的离子方程式是
A.CaCO +2H+===Ca2++CO↑+HO
3 2 2
B.2Fe2++Cl===2Fe3++2Cl-
2
C. +H+===CO ↑+HO
2 2D.NaO+HO===2Na++2OH-
2 2
17.下列化学反应中,不属于四种基本反应类型的是
A.CaCO +2HCl=CaCl +HO+CO↑ B.2Na+2HO=2NaOH+H ↑
3 2 2 2 2 2
C.4Fe(OH) +O +2H O= 4Fe(OH) ↓ D.2FeCl +Cu=2FeCl +CuCl
2 2 2 3 3 2 2
18.下列离子方程式不正确的是( )
A.用硝酸银溶液检验自来水中的氯离子:Ag++Cl-=AgCl↓
B.Al O 溶于NaOH 溶液: Al O + 2OH-= 2AlO -+ H O
2 3 2 3 2 2
C.NaOH 溶液不能保存在玻璃塞的试剂瓶中:SiO+ 2OH-= SiO2-+ H O
2 3 2
D.NaHCO 溶液与少量的澄清石灰水反应:HCO -+ Ca2++OH-=CaCO ↓+H O
3 3 3 2
19. 是优良的水处理剂,一种制备方法是将 、 、 混合共熔,
反应的化学方程式为 。下列关于
该反应的说法不正确的是
A.铁元素被氧化,氮元素被还原 B.氧化性:
C.每生成1个 ,转移6个电子 D. 具有氧化杀菌作用
20.下列变化属于化学变化的是
A.滴水成冰 B.蜡烛燃烧 C.汽油挥发 D.铜丝弯折
二、填空题
21.I.对于数以千万计的化学物质和如此丰富的化学变化,分类法的作用几乎是无可替
代的。如:纯净物根据其组成和性质可进行如下分类。
(1)如图所示的分类方法属于_______。
(2)某化学兴趣小组对下列四组物质进行研究:
A.
试卷第4页,共3页B.
C. 溶液、蒸馏水、 悬浊液、 胶体
D.
填写下列空白:
A组 B组 C组 D组
分类标准 含氧酸 _______ 分散系 _______
不属于该类别的物
_______ _______ Fe O
质 2 3
II.现有下列七种物质:① ②铝 ③ ④ ⑤硝酸 ⑥ ⑦氢氧化铁
悬浊液
(3)其中属于混合物的是_______,属于氧化物的是_______,属于单质的是_______(均
填序号)。
(4)上述物质中有两种易溶于水的物质之间可发生酸碱中和反应,该反应对应的化学方
程式为_______。
III.甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有
一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、 、 作用产生
的,化学式为 ,“铜绿”能跟酸反应生成铜盐、 和 。某同学
利用以下反应实现了“铜→铜绿→……→铜”的转化。
(5)从物质分类标准看,“铜绿”属于_______(填字母)。A.酸 B.碱 C.盐
D.氧化物
(6)写出B的化学式:_______。
(7)请写出铜绿与盐酸反应的化学方程式:_______。
(8)上述转化过程中属于化合反应的是_______。
22.进一步认识氧化还原反应。氯化铵可除去铜器表面的氧化铜:(1)氧化还原反应的实质是__________(填写编号)。
A.得氧和失氧 B.化合价的升降 C.有无新物质生成 D.电子的得失和偏移
(2)用单线桥标出上述反应中电子转移的方向和数目________。
(3)上述反应中,氯化铵中N的化合价_______(“升高”或“降低”),_____
(“得”或“失”)电子,作____(“氧化剂”或“还原剂”),表现_____(“氧
化”或“还原”)性,发生____(“氧化”或“还原”)反应。
(4)氧化剂和还原剂物质的量之比是___。
(5)当生成 11.2 L(标准状况)时,转移___个电子,被还原的CuO__mol。
23.回答下列问题:
(1)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成
的,爆炸时的反应为: S+2KNO +3C = K S+N↑+3CO ↑;在该反应中还原剂是(填化学
3 2 2 2
式,下同):___________;氧化剂:___________;还原产物是:_____________;氧
化产物是:____________。
(2)在Fe2+、Fe3+、Al3+、H+、S、C、S2-、Cl- 等离子或原子中,只有还原性的是:
___________;只有氧化性的是:________;既有氧化性又有还原性的是:___________。
试卷第6页,共3页参考答案:
1.D
【详解】A.萃取为物理变化,没有发生氧化还原反应,A不满足题意;
B.压缩空气后分离制备氧气为物理变化,没有发生氧化还原反应,B不满足题意;
C.常压分馏为物理变化,没有发生氧化还原反应,C不满足题意;
D.加热氧化银制备银,银元素由+1价降低为0价,有元素化合价发生变化,发生了氧化
还原反应,D满足题意。
答案选D。
2.B
【详解】A.氯化钠溶液、水不是胶体,不能发生丁达尔效应,但水不是分散系,A错误;
B.Fe→Fe O 的变化中铁元素化合价升高,铁单质作还原剂,0价为铁元素的最低价态,故
3 4
必然另有一种物质作氧化剂,B正确;
C.Na SO 溶液电离出Na+与SO 2-而导电是自发过程,不需要电流的作用,C错误;
2 4 4
D.离子反应可能是复分解反应,也可能是氧化还原反应,例如Cu+2Fe3+=2Fe2++Cu2+既是氧
化还原反应也是离子反应,D错误;
答案选B。
3.A
【详解】A. 氯气与水反应生成盐酸和次氯酸,氯元素化合价发生变化,属于氧化还原反
应,A符合;
B. 盐酸与氢氧化钠溶液反应生成氯化钠和水,属于复分解反应、属于非氧化还原反应,
B不符合;
C. 氯化铵固体受热分解生成氯化氢和氨气,化合价不发生变化,属于非氧化还原反应,
C不符合;
D. 氢氧化钡与碳酸钠反应生成碳酸钡沉淀和氢氧化钠溶液,属于复分解反应、属于非氧
化还原反应,D不符合;
答案选A。
4.B
【详解】Na的化合价由0价升高到+1价,被氧化,Na为还原剂;Ti的化合价由+4价降到
0价,被还原,TiCl 是氧化剂,故金属钠只作还原剂;
4
故选B。
5.B【详解】A.在Fe →FeSO 的过程中,Fe元素化合价升高,发生氧化反应,需要加入氧化
4
剂才能实现,故A错误;
B.在Cu(NO ) → Cu 的过程中,Cu元素化合价降低,发生还原反应,需要加入还原剂才
3 2
能实现,故B正确;
C.在CO→CO 的过程中,C元素化合价升高,发生氧化反应,需要加入氧化剂才能实现,
2
故C错误;
D.在NaCl →AgCl的过程中,不存在元素化合价的变化,未发生氧化还原反应,不需要
加入氧化剂或还原剂,故D错误;
故答案为B。
6.C
【详解】反应①和③都是由一种单质和一种化合物反应生成一种新单质和一种新化合物,
为置换反应,答案选C。
点睛:四大基本反应类型的判断:(1)化合反应的特点是“多变一”,生成物只有一种化
合物;(2)分解反应的特点是“一变多”,反应物只有一种化合物;(3)置换反应的特
点:一种单质+一种化合物→一种新单质+一种新化合物;(4)复分解反应的特点:两种
化合物互相交换成分生成新化合物。
7.A
【分析】属于氧化还原反应,说明该反应中有电子转移,即有元素化合价升降,又属于化
合反应,说明该反应是由两种或多种物质生成一种物质,据此分析解答。
【详解】A. 2FeCl +Cl=2FeCl 反应中,铁元素化合价升高,氯气中氯元素化合价降低,属
2 2 3
于氧化还原反应,且属于化合反应,符合题意,A项正确;
B. Zn+H SO =ZnSO +H ↑反应中,Zn元素化合价升高,H元素化合价降低,属于氧化还原
2 4 4 2
反应,但从基本反应类型上看,属于置换反应,不符合题意,B项错误;
C. CO+CaO=CaCO 从基本反应类型上看,属于化合反应,但反应中无元素化合价的升降,
2 3
不属于氧化还原反应,不符合题意,C项错误;
D. CH +2O CO+2H O反应中,C元素化合价升高,O元素化合价降低,属于氧
4 2 2 2
化还原反应,但从基本反应类型上看,不属于化合反应,不符合题意,D项错误;
答案选A。
8.A
【详解】A. 氧化还原反应的特征是化合价发生变化,故A正确;
答案第2页,共2页B. 反应物所含元素的化合价升高的反应为氧化反应,反应物所含元素的化合价降低的反应
为还原反应,故B错误;
C. 反应中氧化剂得电子,化合价降低,故C错误;
D. 置换反应一定有化合价变化,置换反应一定是氧化还原反应,故D错误;答案选A。
9.C
【详解】A.“煮豆燃豆萁”涉及燃烧,与氧化还原反应有关;
B.“爆竹声声一岁除”涉及燃烧,与氧化还原反应有关;
C.“要留清白在人间”涉及碳酸钙高温分解得到氧化钙和二氧化碳,是分解反应,与氧
化还原反应无关;
D.“曾青得铁则化为铜”涉及铁与硫酸铜发生置换反应,与氧化还原反应有关;
从氧化还原的角度分析,其中一个与其他三个明显不同是选项C,故答案选C。
10.D
【详解】A.反应中2个Na失去2个电子,2个氯原子得到2个电子,用单线桥表示为
,故A正确;
B.反应中CuO中2个Cu得到4个电子,1个碳原子失去4个电子,用双线桥表示为:
,故B正确;
C.反应中氯酸钾中2个氯原子得到12个电子,6个氧原子失去12个电子,用双线桥表示
为: ,故C正确;
D.反应中二氧化碳中碳得到2个电子,碳失去2个电子,用双线桥表示为:,故D错误;
故选D。
11.B
【详解】A.钠元素化合价由0升高为+1、氯元素化合价由0降低为-1,电子转移的方向和
数目为 ,故A正确;
B. 反应,铜元素化合价由0升高为+2、氮元素
化合价由+5降低为+2,电子转移的方向和数目为
,故B错误;
C.氧化铜和碳反应生成铜和二氧化碳,铜元素化合价由+2降低为0、碳元素化合价由0升
高为+4,电子转移的方向和数目为 ,故C正确;
D.氯酸钾分解为氯化钾和氧气,氯元素化合价由+5降低为-1、氧元素化合价由-2升高为
0, 电子转移的方向和数目为 ,故D正确;
选B。
答案第4页,共2页12.D
【详解】A.大理石不溶于水,CaCO 不可拆成离子形式,A错误;
3
B.稀硫酸和氢氧化钡的离子方程式为:2H++ +Ba2++2OH-=BaSO ↓+2H O,不能把
4 2
H+、OH-、HO的系数2删去,B错误;
2
C.澄清石灰水中的Ca(OH) 全部溶解,可以拆写成离子形式,最终所得离子方程式应为:
2
Ca2++ =CaCO ↓,C错误;
3
D.Fe2+与HO 在酸性溶液中的反应方程式为:2Fe2++H O+2H+=2Fe3++2H O,D正确。
2 2 2 2 2
故选D。
13.A
【详解】A.爆竹爆炸过程中发生了氧化还原反应,故A符合题意;
B.描述的是沙里淘金,是物质的分离提纯,没有涉及化学变化,故B不符合题意;
C.诗句描述楼阁矗立在烟雨中未涉及化学变化,故C不符合题意;
D.诗句描述落叶飘落,江水奔腾,未涉及化学变化,故D不符合题意;
故选:A。
14.D
【分析】属于氧化还原反应,说明该反应中有电子转移,其特征是有元素化合价升降,据
此分析解答。
【详解】①该反应中Fe元素化合价由0价变为+3价、Cl元素化合价由0价变为-1价,所
以属于氧化还原反应,且反应物两种,生成物为一种,属于化合反应,所以既属于化合反
应又属于氧化还原反应,故①符合题意;
②氯气通入溴化钠溶液Cl+2NaBr=2NaCl+Br ,该反应中Cl元素化合价由0价变为-1价,
2 2
Br元素化合价由-1价变为0价,属于氧化还原反应,属于置换反应,故②不符合题意;
③氯化钠溶液和浓硫酸混合加热的反应中各元素化合价不变,所以不属于氧化还原反应,
故③不符合题意;
④该反应中Cl元素化合价由-1价变为0价、Mn元素化合价由+4价变为+2价,所以属于
氧化还原反应,但不属于化合反应,故④不符合题意;
⑤氢气在氯气中燃烧属于氧化还原反应,且反应物两种,生成物为一种,属于化合反应,
故⑤符合题意;
故答案选D。15.B
【分析】化合反应:是由两种或两种以上的物质反应生成一种新物质的反应;分解反应:
由一种物质生成两种或两种以上其它的物质的反应叫分解反应;置换反应:一种单质与化
合物反应生成另外一种单质和化合物的化学反应;复分解反应:由两种化合物互相交换成
分,生成另外两种化合物的反应;
【详解】A.该方程式没有配平,方程式为 ,A错误;
B..反应CaO+H O=Ca(OH) 是由两种或两种以上的物质反应生成一种新物质的反应,属
2 2
于化合反应,B正确;
C.SO 与NaOH反应生成NaSO 和HO,方程式为SO +2NaOH=Na SO +H O,C错误;
3 2 4 2 3 2 4 2
D.葡萄糖在人体内氧化的方程式正确,但是氧化反应不属于基本反应类型,D错误;
故选B。
16.B
【详解】A中无化合价的变化,故不属于氧化还原反应;
B中铁元素有化合价的变化,属于氧化还原反应;
C中无化合价的变化,故不属于氧化还原反应;
D中无化合价的变化,故不属于氧化还原反应。
答案选B。
17.D
【分析】化合反应:两种或两种以上物质反应后生成一种物质的反应,其特点可总结为
“多变一”; 分解反应:一种物质反应后生成两种或两种以上的物质,其特点可总结为
“一变多”;置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反
应;复分解反应是两种化合物相互交换成分生成两种新的化合物的反应。
【详解】A、该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解
反应,属于四种基本反应类型之一,选项A错误;B、该反应是一种单质和一种化合物反
应生成另一种单质和另一种化合物的反应,属于置换反应,属于四种基本反应类型之一,
选项B错误;C、该反应符合“多变一”的特征,属于化合反应,属于四种基本反应类型
之一,选项C错误;D、该反应反应物和生成物均为两种,不属于化合反应、分解反应;
生成物均为化合物,不属于置换反应;反应物中铜是单质,不属于复分解反应;选项D正
确;答案选D。
答案第6页,共2页【点睛】本题难度不大,掌握四种基本反应类型的特征并能灵活运用是正确解答本题的关
键。
18.D
【详解】A. 用硝酸银溶液检验自来水中的氯离子反应生辰氯化银沉淀:Ag++Cl-=AgCl↓,
故A正确;
B. AlO 溶于NaOH 溶液反应生成偏铝酸钠和水:Al O + 2OH-= 2AlO -+ H O,故B正确;
2 3 2 3 2 2
C. NaOH 溶液不能保存在玻璃塞的试剂瓶中,主要是氢氧化钠和磨口玻璃成分中的二氧化
硅反应生成硅酸钠:SiO+ 2OH-= SiO2-+ H O,故C正确;
2 3 2
D. NaHCO 溶液与少量的澄清石灰水反应:2HCO -+ Ca2+ + 2OH-= CaCO↓+ CO2-+
3 3 3 3
2HO,故D错误。
2
综上所述,答案为D。
19.C
【详解】A.反应中 元素由 价升高至 价,铁元素被氧化,而N元素由 价降低至
价,氮元素被还原,A项正确;
B.结合该反应中化合价变化可知 为氧化剂, 为氧化产物,根据氧化性:氧
化剂>氧化产物,可知氧化性: ,B项正确;
C.根据 元素化合价变化可知每生成1个 ,转移3个电子,C项错误;
D. 中 元素为 价,决定了 具有强氧化性,可起到氧化杀菌作用,D项
正确;
故选C。
20.B
【详解】A、滴水成冰没有新物质生成,故A错误;B、蜡烛燃烧生成CO 和HO,有新物
2 2
质生成,故B正确;C、汽油挥发没有新物质生成,故C错误;D、铜丝弯折没有新物质生
成,故D错误;故选B。
点睛:分析变化过程中是否有新物质生成,若没有新物质生成属于物理变化,若有新物质
生成属于化学变化。
21.(1)树状分类法
(2) HCl 阳离子种类 蒸馏水 碱(3) ⑦ ③④ ①②
(4)2HNO+ =Ba(NO)+2H O
3 3 2 2
(5)C
(6)CuO
(7)
(8)①
【详解】(1)将同类事物按照某种属性进行分类,按照层次,一层一层来分,就像一棵大
树,该分类方法为树状分类法。
(2)A组中 均属于酸,其中除HCl外,其余均为含氧酸;B
组中 均属于盐,除 外,其余盐中阳离子均为
Na+;C组 溶液、蒸馏水、 悬浊液、 胶体中,除纯净物蒸馏水外,其余
均属于分散系;D组 中,除氧化物Fe O 外,其余均属于碱。
2 3
(3)七种物质:① ②铝 ③ ④ ⑤硝酸 ⑥ ⑦氢氧化铁悬浊液中,
属于混合物的有:⑦氢氧化铁悬浊液;属于氧化物的有:③ 、④ ;属于单质的
有:① ②铝。
(4)上述7种物质中易溶于水的酸为硝酸,易溶于水的碱为 ,二者发生酸碱中和
的化学方程式为2HNO+ =Ba(NO)+2H O。
3 3 2 2
(5)铜绿化学式为 ,化学式可改写为Cu(OH) ·CuCO,属于盐类化合物,
2 3
故答案为C。
答案第8页,共2页(6)Cu(OH) 属于弱碱,具有不稳定性,受热易分解为CuO,CuO与H 在加热条件下发
2 2
生置换反应生成Cu,因此B的化学式为CuO。
(7)铜绿化学式为 ,能跟酸反应生成铜盐、 和 ,因此铜绿与盐酸
反应的化学方程式为 。
(8)铜绿属于难溶性盐,无法直接与碱反应生成Cu(OH) ,因此需要先将铜绿转化为可溶
2
铜盐,再利用可溶铜盐与碱反应生成Cu(OH) ,因此②为酸,③为碱,即转化流程为
2
,其中属于化合反应的为铜
与空气中水蒸气、 、 反应生成铜绿,故答案为①。
22. D 升高 失 还原
剂 还原 氧化 3:2 3N 1.5
A
【分析】氧化还原反应的本质为电子的转移(得失和偏移),其特征是元素化合价的变化;
4CuO+2NH Cl=3Cu+CuCl +N +4H O反应中,CuO中的铜元素由+2价降低到0价,发生还
4 2 2 2
原反应,做氧化剂;NH Cl中氮元素由-3价升高到0价,发生氧化反应,做还原剂;电子
4
转移及相关各量的关系为:6e----N —3CuO(被还原),据此进行计算。
2
【详解】(1)氧化还原反应的本质为电子的转移(得失和偏移),其特征是元素化合价的
变化;
故答案选D;
(2)4CuO+2NH Cl=3Cu+CuCl +N +4H O反应中,CuO→Cu,铜元素由+2价降低到0价,
4 2 2 2
得到2个电子,3molCuO→3Cu,共得到电子6mol电子,即反应转移的电子为6mol; 单
线桥标出上述反应中电子转移的方向和数目如下: ;
故答案是: ;
(3)4CuO+2NH Cl=3Cu+CuCl +N +4H O反应中,氯化铵中氮元素由-3价升高到0价,失
4 2 2 2电子,发生氧化反应,做还原剂,表现还原性;
故答案是:升高;失;还原剂;还原;氧化。
(4)4CuO+2NH Cl=3Cu+CuCl +N +4H O反应中,NH Cl做还原剂,全部被氧化,所以还
4 2 2 2 4
原剂有2mol;4molCuO中有3molCuO被还原,做氧化剂;所以氧化剂和还原剂物质的量
之比是3mol:2mol=3:2;
故答案是:3:2;
(5)根据 可知,6e----N —3CuO(被还原),所以当氮气
2
的量为11.2L/22.4L/mol=0.5mol时,转移3mol电子,个数为3N ;被还原的CuO为
A
1.5mol;
故答案是:3N ;1.5。
A
23.(1) C S和KNO KS、N CO
3 2 2 2
(2) S2-、Cl- Fe3+、Al3+、H+ Fe2+、S、C
【详解】(1)在反应S+2KNO +3C = K S+N↑+3CO ↑中,C的化合价升高,失去电子,被
3 2 2 2
氧化,则还原剂是:C;氧化产物是:CO;S、N的化合价降低,得到电子,则氧化剂:S
2
和KNO;还原产物是:KS、N;
3 2 2
(2)在Fe2+、Fe3+、Al3+、H+、S、C、S2-、Cl- 等离子或原子中,
化合价为最高价态时,只有还原性,则只有还原性的是:S2-、Cl-;
化合价为最低价态时,只有氧化性,则只有氧化性的是:Fe3+、Al3+、H+;
化合价为中间价态时,既有氧化性又有还原性,则既有氧化性又有还原性的是:Fe2+、S、
C。
答案第10页,共2页