文档内容
第三章 第二节 第2课时 酸碱中和滴定 测试题
榆次一中 李金虎
一、选择题(本题共有15小题,每小题4分,共60分,每小题只有一个正确选项)
1. 下列关于酸碱中和滴定实验的说法正确的是( )
A.用图B可准确量取25.00 mL的KMnO 溶液
4
B.滴定过程中,眼睛要时刻注视滴定管中液面的变化
C.滴定管装入液体前需用待装液润洗
D.滴定前平视,滴定结束后仰视读数,不影响测定结果
2. 下列有关叙述中正确的是( )
A.滴定管下端连有橡皮管的为酸式滴定管
B.在滴定时,左手操作锥形瓶,右手操作滴定管活塞
C.滴定前应首先排出尖嘴部分的气泡
D.滴定过程中两眼应注视滴定管内液面的变化
3. 用标准盐酸溶液滴定未知浓度的NaOH溶液,下列各操作中,会引起实验误差的是( )
A.取干燥洁净的酸式滴定管立即装入标准盐酸
B.用蒸馏水洗净锥形瓶后,立即装入一定体积的NaOH溶液后进行滴定
C.往盛有20.00 mL NaOH溶液的锥形瓶中,滴入几滴酚酞指示剂后进行滴定
D.用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗,然后装入一定体积的NaOH溶液
4. 现用0.1000 mol·L-1NaOH溶液滴定浓度相近的乙酸时,上述指示剂( )
A.都可以用 B.只能用③
C.可以用①或② D.可以用②或③
5. 中和滴定是一种操作简单,准确度高的定量分析方法。实际工作中也可利用物质间的氧化还原
反应、沉淀反应进行类似的滴定分析,下列有关几种具体的滴定分析(待测液置于锥形瓶内)的
说法不正确的是( )
A.用标准酸性KMnO 溶液滴定NaSO 溶液以测量其浓度:滴定终点时,溶液由无色变为紫
4 2 3
红色
B.利用“Ag++SCN-===AgSCN↓”反应,用标准 KSCN溶液测量AgNO 溶液浓度时可用
3
Fe(NO ) 作指示剂
3 3
C.利用“2Fe3++2I-===I +2Fe2+”,用FeCl 溶液测量KI样品中KI的百分含量时,可用淀
2 3
粉作指示剂
D.用标准NaOH溶液测量某盐酸溶液的浓度时,若用酚酞作指示剂,当观察到溶液由无色变
为红色,且半分钟不恢复时达到滴定终点
6. 如图是常温下向20.0 mL的盐酸中,逐滴加入0.10 mol·L-1 NaOH溶液时,溶液的pH随NaOH
溶液的体积V(mL)变化的曲线,根据图像所得的下列结论中正确的是( )
A.原盐酸的浓度为0.10 mol·L-1
1
学科网(北京)股份有限公司B.x的值为2.0
C.pH=12,V值为20.4
D.原盐酸的浓度为1.0 mol/L
7. 某同学想了解食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白
醋,用实验室标准NaOH溶液(浓度有0.100 0 mol·L-1和0.010 0 mol·L-1两种)对其进行滴定。
下列说法正确的是( )
A.该实验应选用甲基橙作指示剂
B.用0.100 0 mol·L-1标准NaOH溶液滴定时误差更小
C.准确量取一定体积的白醋放入洗净的锥形瓶中后,可以再加少量蒸馏水后开始滴定
D.滴定时,眼睛一直注视着刻度线,以防止液面下降到滴定管最大刻度以下
8. 为测定某盐酸的浓度,准确量取20.00 mL该盐酸于锥形瓶中,用0.100 0 mol·L-1 NaOH溶液滴
定,下列说法正确的是( )
A.滴定管用蒸馏水洗涤后,装入NaOH溶液进行滴定
B.用酚酞作指示剂,当锥形瓶中溶液出现浅红色时立即停止滴定,开始读数
C.用25 mL酸式滴定管量取20.00 mL待测溶液于锥形瓶中
D.滴定达终点时,发现滴定管尖嘴部分悬有一滴溶液,则测定结果偏小
9. 酸碱中和滴定是重要的定量实验,准确量取25.00 mL某待测浓度的盐酸于锥形瓶中,用0.100
0 mol/L的氢氧化钠标准溶液滴定。下列说法正确的是( )
A.锥形瓶用蒸馏水洗涤以后,再用待测液进行润洗
B.使用酚酞作指示剂,当锥形瓶中的溶液由红色变为无色时停止滴定
C.滴定达到终点时,俯视刻度线进行读数,则测定结果偏低
D.实验结束,某同学记录的氢氧化钠溶液的体积为21.6 mL
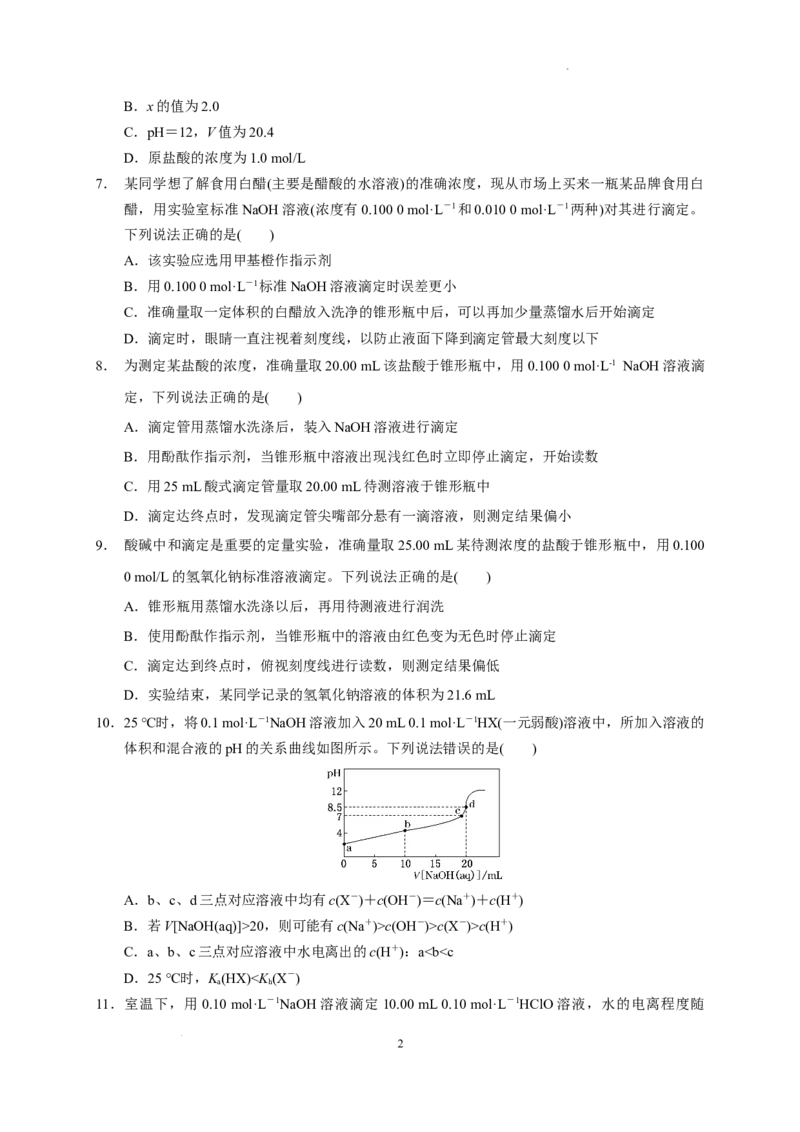
10.25 ℃时,将0.1 mol·L-1NaOH溶液加入20 mL 0.1 mol·L-1HX(一元弱酸)溶液中,所加入溶液的
体积和混合液的pH的关系曲线如图所示。下列说法错误的是( )
A.b、c、d三点对应溶液中均有c(X-)+c(OH-)=c(Na+)+c(H+)
B.若V[NaOH(aq)]>20,则可能有c(Na+)>c(OH-)>c(X-)>c(H+)
C.a、b、c三点对应溶液中水电离出的c(H+):ac(OH-)>c(ClO-)>c(H+)
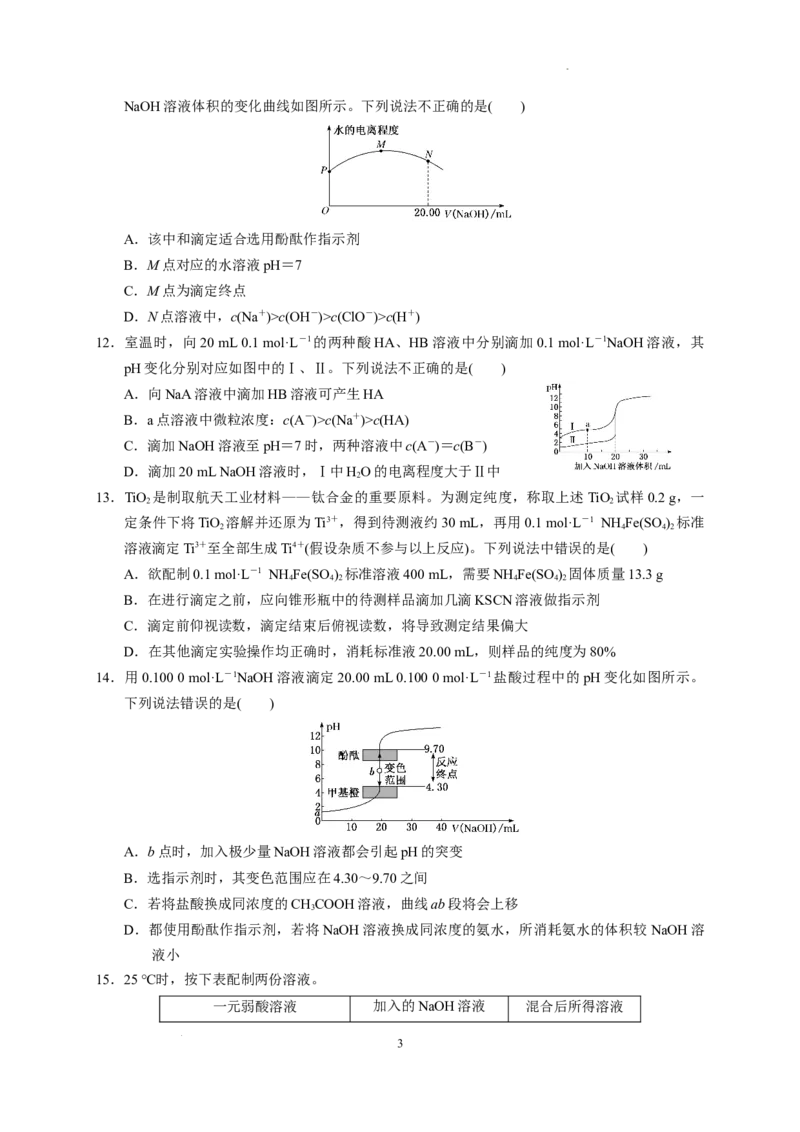
12.室温时,向20 mL 0.1 mol·L-1的两种酸HA、HB溶液中分别滴加0.1 mol·L-1NaOH溶液,其
pH变化分别对应如图中的Ⅰ、Ⅱ。下列说法不正确的是( )
A.向NaA溶液中滴加HB溶液可产生HA
B.a点溶液中微粒浓度:c(A-)>c(Na+)>c(HA)
C.滴加NaOH溶液至pH=7时,两种溶液中c(A-)=c(B-)
D.滴加20 mL NaOH溶液时,Ⅰ中HO的电离程度大于Ⅱ中
2
13.TiO 是制取航天工业材料——钛合金的重要原料。为测定纯度,称取上述TiO 试样0.2 g,一
2 2
定条件下将TiO 溶解并还原为Ti3+,得到待测液约30 mL,再用0.1 mol·L-1 NH Fe(SO ) 标准
2 4 4 2
溶液滴定Ti3+至全部生成Ti4+(假设杂质不参与以上反应)。下列说法中错误的是( )
A.欲配制0.1 mol·L-1 NH Fe(SO ) 标准溶液400 mL,需要NH Fe(SO ) 固体质量13.3 g
4 4 2 4 4 2
B.在进行滴定之前,应向锥形瓶中的待测样品滴加几滴KSCN溶液做指示剂
C.滴定前仰视读数,滴定结束后俯视读数,将导致测定结果偏大
D.在其他滴定实验操作均正确时,消耗标准液20.00 mL,则样品的纯度为80%
14.用0.100 0 mol·L-1NaOH溶液滴定20.00 mL 0.100 0 mol·L-1盐酸过程中的pH变化如图所示。
下列说法错误的是( )
A.b点时,加入极少量NaOH溶液都会引起pH的突变
B.选指示剂时,其变色范围应在4.30~9.70之间
C.若将盐酸换成同浓度的CHCOOH溶液,曲线ab段将会上移
3
D.都使用酚酞作指示剂,若将NaOH溶液换成同浓度的氨水,所消耗氨水的体积较NaOH溶
液小
15.25 ℃时,按下表配制两份溶液。
一元弱酸溶液 加入的NaOH溶液 混合后所得溶液
3
学科网(北京)股份有限公司HA 10.0 mL 5.0 mL
溶液Ⅰ pH=5.0
0.20 mol·L-1 0.20 mol·L-1
HB 10.0 mL 5.0 mL
溶液Ⅱ pH=4.0
0.20 mol·L-1 0.20 mol·L-1
下列说法错误的是( )
A.溶液Ⅰ中,c(A-)>c(Na+)>c(H+)>c(OH-)
B.Ⅰ和Ⅱ的pH相差1.0,说明=10
C.混合Ⅰ和Ⅱ:c(Na+)+c(H+)=c(A-)+c(B-)+c(OH-)
D.混合Ⅰ和Ⅱ:c(HA)>c(HB)
二、填空题(本题包括4个小题,共40分)
16.(8分)某学生用0.2000 mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00 mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数
请回答:
(1)以上步骤有错误的是(填编号)________,该错误操作会导致测定结果(填“偏大”、“偏
小”或“无影响”)___________。
(2)步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,测定结果(填“偏大”、“偏
小”或“无影响”)________。
(3)判断滴定终点的现象是:
_____________________________________。
17.(12分)现用中和滴定测定某盐酸的浓度,有关数据记录如表。
滴定 待测液 所消耗烧碱标准液的体积/mL
序号 体积/mL 滴定前 滴定后 消耗的体积
1 25.00 0.50 25.12 24.62
2 25.00
3 25.00 5.00 29.58 24.58
(1)实验中有石蕊和酚酞两种指示剂,该实验应选用_______作指示剂。用________式滴定管盛
装0.250 0 mol·L-1烧碱标准液,锥形瓶中装有25.00 mL待测盐酸溶液。
(2)如图表示第二次滴定时50 mL滴定管中滴定前后液面的位置。该次滴定所用标准烧碱溶液
体积为________mL。
(3)根据所给数据,计算出该盐酸的物质的量浓度(注意保留合适的有效数字),
c(HCl)=________。
(4)下列操作引起什么误差(填“偏大”“偏小”或“不影响”)。
4
学科网(北京)股份有限公司①摇动锥形瓶时溶液溅出________。
②滴定前滴定管中有气泡,滴定后气泡消失________。
③锥形瓶未干燥有水________。
④滴定终点俯视________。
18.(10分)乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H C O·xHO)进行的探究性学
2 2 4 2
习的过程,请你参与并协助他们完成相关学习任务。
该组同学的研究课题是:探究测定草酸晶体(H C O·xHO)中的x值。通过查阅资料和网络查寻
2 2 4 2
得,草酸易溶于水,水溶液可以用酸性KMnO 溶液进行滴定:2MnO+5HC O+6H+===2Mn2
4 2 2 4
++10CO↑+8HO,学习小组的同学设计了滴定的方法测定x值。
2 2
①称取1.260 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀HSO 。
2 4
③用浓度为0.1000 mol·L-1的酸性KMnO 标准溶液进行滴定,达到终点时消耗10.00 mL。
4
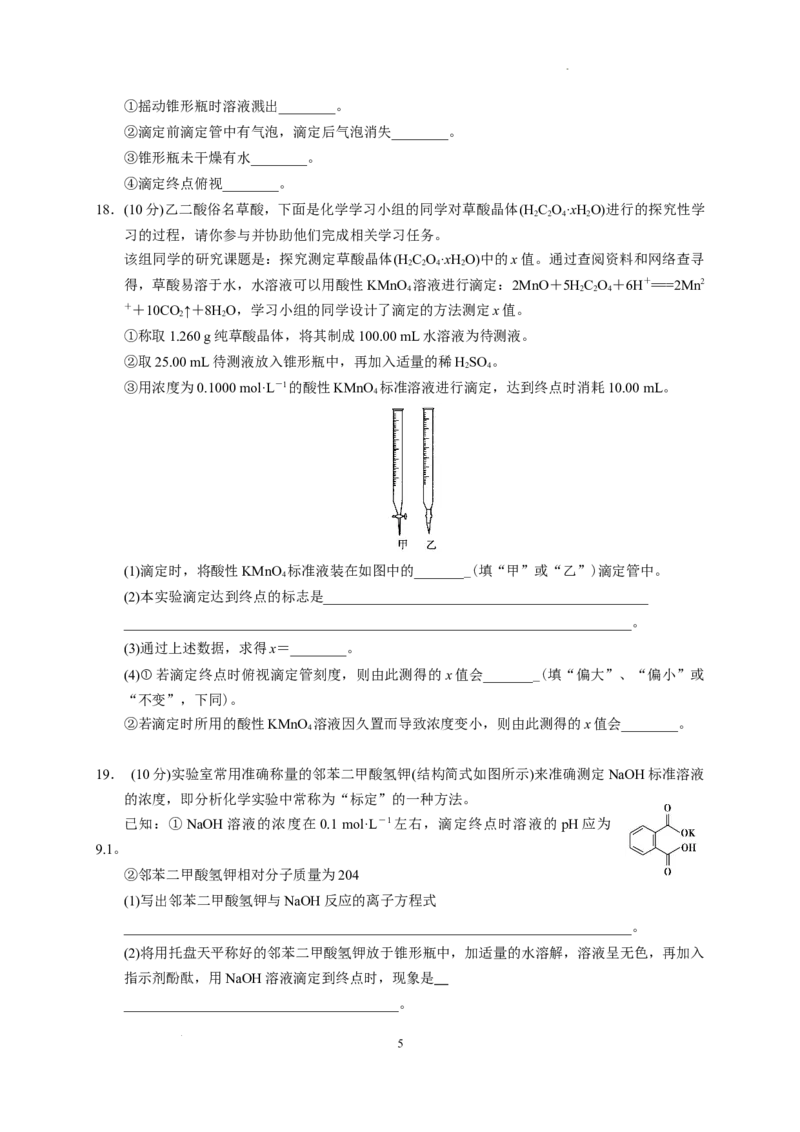
(1)滴定时,将酸性KMnO 标准液装在如图中的________(填“甲”或“乙”)滴定管中。
4
(2)本实验滴定达到终点的标志是______________________________________________
________________________________________________________________________。
(3)通过上述数据,求得x=________。
(4)①若滴定终点时俯视滴定管刻度,则由此测得的x值会________(填“偏大”、“偏小”或
“不变”,下同)。
②若滴定时所用的酸性KMnO 溶液因久置而导致浓度变小,则由此测得的x值会________。
4
19. (10分)实验室常用准确称量的邻苯二甲酸氢钾(结构简式如图所示)来准确测定NaOH标准溶液
的浓度,即分析化学实验中常称为“标定”的一种方法。
已知:①NaOH溶液的浓度在0.1 mol·L-1左右,滴定终点时溶液的pH应为
9.1。
②邻苯二甲酸氢钾相对分子质量为204
(1)写出邻苯二甲酸氢钾与NaOH反应的离子方程式
________________________________________________________________________。
(2)将用托盘天平称好的邻苯二甲酸氢钾放于锥形瓶中,加适量的水溶解,溶液呈无色,再加入
指示剂酚酞,用NaOH溶液滴定到终点时,现象是
_______________________________________。
5
学科网(北京)股份有限公司实验编号 邻苯二甲酸氢钾的质量/g 待测NaOH溶液的体积/mL
1 18.20
2 17.10
0.408 0
3 16.90
4 17.00
(3)滴定中误差较大的是第________次实验,造成这种误差的可能原因是________。
A.碱式滴定管在装液前未用待测NaOH溶液润洗2~3次
B.滴定开始前碱式滴定管尖嘴部分有气泡,在滴定终点读数时未发现气泡
C.盛有邻苯二甲酸氢钾溶液的锥形瓶中有少量水
D.达到滴定终点时,俯视溶液凹液面最低点读数
E.滴定过程中,锥形瓶摇荡得太剧烈,以至有些液滴飞溅出来
(4)该同学所测得的NaOH溶液的物质的量浓度为________mol·L-1(结果保留三位小数)。
1.答案:C
解析:高锰酸钾溶液具有强氧化性,应选用酸式滴定管盛装,图B为碱式滴定管,用于盛装碱性溶
液,A错误;滴定过程中,为了及时判断滴定终点,眼睛要时刻注视锥形瓶中溶液颜色的变化,B
错误;为了避免待装液被稀释,滴定管装入液体前需用待装液润洗,C正确;滴定前平视,滴定结
束后仰视读数,读出的标准液体积偏大,会使测定结果偏大,D错误。
2.答案:C
解析:有橡皮管的为碱式滴定管,A错误;滴定时,左手操作滴定管活塞,右手操作锥形瓶,B错
误;滴定前应排出尖嘴部分的气泡,否则会引起误差,C正确;滴定过程中两眼应注视锥形瓶内液
体的颜色变化,以确定滴定终点,D错误。
3.答案:D
解析:滴定管若干燥洁净,不必用水洗涤,故也不需用标准液润洗,A不会引起误差;锥形瓶内存
有少量蒸馏水,但待测液的物质的量不变,消耗标准液的体积不变,B不会引起误差;锥形瓶不能
用待测液润洗,否则会使测定结果偏高。
4.答案:B
解析:氢氧化钠溶液与乙酸等物质的量反应时,生成的乙酸钠溶液呈碱性,选用在碱性条件下变色
的指示剂酚酞为宜。
5.答案:C
解析:C中只要反应一开始就有I 生成,溶液就呈蓝色。
2
6.答案:A
解析:当V(NaOH)=0 mL时,盐酸溶液的pH=1,因此c(HCl)=0.10 mol·L-1;当反应后溶液pH=
7时,HCl与NaOH恰好完全反应,因此n(HCl)=n(NaOH),故V(NaOH)=20.0 mL;当反应后溶液
6
学科网(北京)股份有限公司pH=12时,=1×10-2 mol·L-1,解得V(NaOH)=24.4 mL。
7.答案:C
解析:该实验滴定终点生成醋酸钠,醋酸钠水解使溶液呈碱性,应选用酚酞作指示剂,故A错误;
由于白醋中醋酸浓度较小,用浓度较小的氢氧化钠溶液滴定误差较小,故 B错误;准确量取一定体
积的白醋放入洗净的锥形瓶中后,可以再加少量蒸馏水,不影响实验结果,故 C正确;滴定时,眼
睛要注视锥形瓶中溶液颜色的变化,故D错误。
8.答案:C
解析:滴定管应用NaOH溶液润洗,否则导致NaOH溶液被稀释,所测盐酸浓度偏大,A错误;当锥
形瓶中溶液由无色变为浅红色且30 s内颜色不再变化时停止滴定,不能出现浅红色立即停止滴定,
B错误;酸性溶液用酸式滴定管量取,C正确;滴定达到终点时发现滴定管尖嘴部分悬有一滴溶液,
导致消耗的NaOH溶液的体积偏大,则所测盐酸浓度偏大,D错误。9.答案:C
解析:锥形瓶用蒸馏水洗涤以后,不能用待测液进行润洗,A错误;使用酚酞作指示剂,滴定前锥
形瓶内溶液为无色,当锥形瓶中的溶液由无色变为浅红色时停止滴定,B错误;滴定达到终点时,
俯视刻度线进行读数,消耗标准液的体积偏小,则测定结果偏低,C正确;滴定管的精确度为0.01
mL,某同学记录的氢氧化钠溶液的体积应为21.60 mL,D错误。
10.答案:C
解析:由溶液呈电中性知,A正确;若V[NaOH(aq)]>20,且HX的体积相对较小时,混合液中可能
存在:c(OH-)>c(X-),溶液中离子浓度关系为:c(Na+)>c(OH-)>c(X-)>c(H+),故B正确;d点时,
酸碱恰好完全反应生成 NaX,溶液中存在平衡:X-+HOHX+OH-,c(X-)≈0.05 mol·L-1,
2
c(HX)≈c(OH-)=1×10-5.5 mol·L-1,K (X-)==2×10-10,又K(HX)×K (X-)=K ,则K(HX)=5×10
h a h W a
-5,D错误;随着碱溶液的不断加入,酸逐渐减少,生成的盐逐渐增多,水电离受抑制的程度减小,
水电离出的c(H+)增大,C正确。
11.答案:B
解析:恰好完全中和时生成NaClO,由于ClO-水解而使溶液呈碱性,故应选用酚酞作指示剂,A
正确;M点水的电离程度最大,此时恰好完全中和生成 NaClO,ClO-发生水解而使溶液呈碱性,
溶液的pH>7,B错误,C正确;N点加入20.00 mL NaOH溶液,所得溶液是等浓度的NaClO和
NaOH的混合液,ClO-会发生水解,则N点溶液中:c(Na+)>c(OH-)>c(ClO-)>c(H+),D正确。
12.答案:C
解析:根据题图,可知未加入NaOH溶液时Ⅱ对应的pH=1,则HB为强酸,Ⅰ对应的pH=3,则
HA为弱酸,酸性HB>HA,强酸可以制备弱酸,所以向NaA溶液中滴加HB溶液可以生成HA,A
选项正确;a点对应溶液中溶质为NaA、HA,二者物质的量相同,a点溶液pH<7,说明HA的电离
程度大于NaA的水解程度,所以c(A-)>c(Na+)>c(HA),B选项正确;滴加NaOH溶液至pH=7时,
根据电荷守恒,c(A-)=c(Na+)、c(B-)=c(Na+),但是两溶液中c(Na+)不相同,所以c(A-)≠c(B-),
C选项错误;滴加20 mL NaOH溶液时,HA、HB恰好被完全中和,但是NaA水解,所以Ⅰ中水的
电离程度大于Ⅱ中,D选项正确。
13.答案:C
7
学科网(北京)股份有限公司解析:实验室没有400 mL的容量瓶,应选用500 mL的容量瓶配制溶液,NH Fe(SO ) 的摩尔质量
4 4 2
为266 g·mol-1,所以需要NH Fe(SO ) 的质量为0.1 mol·L-1×0.5 L×266 g·mol-1=13.3 g,故A不符
4 4 2
合题意;本实验采用KSCN溶液做指示剂,Fe3+与Ti3+反应生成Ti4+与Fe2+,KSCN与Fe2+不发生
显色反应,而与Fe3+生成血红色Fe(SCN) ,因此当Fe3+过量时,溶液呈血红色,故B不符合题意;
3
滴定前仰视读数,滴定后夜视读数,导致读取溶液体积偏小,导致最终结果偏小,故 C符合题意;
Fe3+与Ti3+反应生成Ti4+与Fe2+,根据得失电子守恒可知n(Fe3+)=n(Ti3+)=n(TiO),消耗标准液
2
20.00 mL,则n(Fe3+)=n(TiO)=0.1 mol·L-1×0.02 L=0.002 mol,因此m(TiO)=0.002 mol×80 g·mol
2 2
-1=0.16 g,所以样品的纯度为×100%=80%,故D不符合题意。
14.答案:D
解析:b点在突变范围内,极少量NaOH溶液也会引起pH的突变,A正确;题图中反应终点的pH
在4.30~9.70之间,选择指示剂的变色范围应在反应终点的pH范围内,B正确;醋酸是弱酸,等
浓度时醋酸溶液的pH大于盐酸,滴定终点时醋酸钠溶液水解显碱性,曲线ab段将会上移,C正确;
使用酚酞作指示剂,用同浓度氨水代替NaOH溶液,滴定终点时溶质为NH Cl,溶液显酸性,要使
4
溶液由无色变为浅红色,pH在8.2~10之间,则消耗氨水的体积大于NaOH溶液,D错误。
15.答案:B
解析:由电荷守恒可知溶液Ⅰ中c(Na+)+c(H+)=c(OH-)+c(A-),pH=5.0,则c(H+)>c(OH-),因
此c(A-)>c(Na+)>c(H+)>c(OH-),A正确;溶液Ⅰ的pH=5.0,溶液Ⅱ的pH=4.0,则HB的电离常
数大于HA的电离常数,<1<10,B错误;由电荷守恒可知混合Ⅰ和Ⅱ有c(Na+)+c(H+)=c(A-)+
c(B-)+c(OH-),C 正确;由于 HB 的电离常数大于 HA 的电离常数,则混合Ⅰ和Ⅱ后有:
c(HA)>c(HB),D正确。
16.答案:(1)① 偏大 (2)偏小
(3)滴入最后一滴NaOH溶液,混合液由无色变为红色且半分钟内不变色
解析:(1)碱式滴定管必须用待装液润洗。若不润洗则相当于稀释NaOH溶液,则会使结果偏大。
(3)滴定终点由无色变为红色且半分钟内不变色。
17.答案:(1)酚酞 碱 (2)24.60 (3)0.246 0 mol·L-1 (4)①偏小 ②偏大 ③不影响 ④偏小
解析:(1)石蕊变色范围较大,而且颜色变化不易观察,不能作酸碱中和滴定的指示剂,因此该实验
应选用酚酞作指示剂;NaOH溶液是碱性溶液,应盛放在碱式滴定管中。(2)滴定前读数为 0.30
mL,滴定后读数为24.90 mL,消耗烧碱溶液的体积为24.60 mL。(3)消耗烧碱溶液的平均体积为
V(NaOH)= mL=24.60 mL,则c(HCl)===0.246 0 mol·L-1。
18.答案:(1)甲 (2)当滴入最后一滴酸性KMnO 溶液时,溶液由无色变为紫色,且半分钟内不褪
4
色,即达滴定终点
(3)2 (4) ①偏大 ②偏小
解析:(1)因为酸性KMnO 具有强氧化性,会腐蚀橡胶管,故应用酸式滴定管盛装。(2)可利用酸性
4
KMnO 溶液自身的颜色作为指示剂判断滴定终点,当达到滴定终点时,再滴加酸性 KMnO 溶液时,
4 4
溶液将由无色变为紫色。(3)由题给化学方程式及数据可知,1.260 g纯草酸晶体中含HC O 的物质
2 2 4
的量为0.1000 mol·L-1×10.00 mL×10-3 L·mL-1××=0.0100 mol,则1.260 g H C O·xHO中含HO的
2 2 4 2 2
物质的量为=0.0200 mol,则x=2。若滴定终点时俯视滴定管读数,则所得消耗酸性KMnO 溶液的
4
8
学科网(北京)股份有限公司体积偏小,由此所得n(H C O)偏小,则n(H O)偏大,x偏大;同理,若酸性KMnO 溶液变质浓度
2 2 4 2 4
偏小,则消耗其体积偏大,所得x值偏小。
19. HO
2
(2)当滴入最后一滴NaOH溶液后,溶液颜色由无色变为红色,且半分钟内不褪色
(3)1 AB
(4)0.118
解析:(3)A选项使氢氧化钠浓度减小,所用氢氧化钠溶液体积偏大;C选项无影响;D选项使读数
偏低;E选项消耗氢氧化钠溶液体积偏小;(4)舍去误差大的实验1,取平均值得V(NaOH)=17.00
mL,n(NaOH)=n(邻苯二甲酸氢钾)==0.002 mol,则c(NaOH)==0.118 mol·L-1。
9
学科网(北京)股份有限公司10
学科网(北京)股份有限公司