文档内容
必修第二册 第五章 第二节 氮及其化合物 测试题
榆次一中 李金虎
一、选择题(每小题只有一个正确选项,每小题4分,共40分)
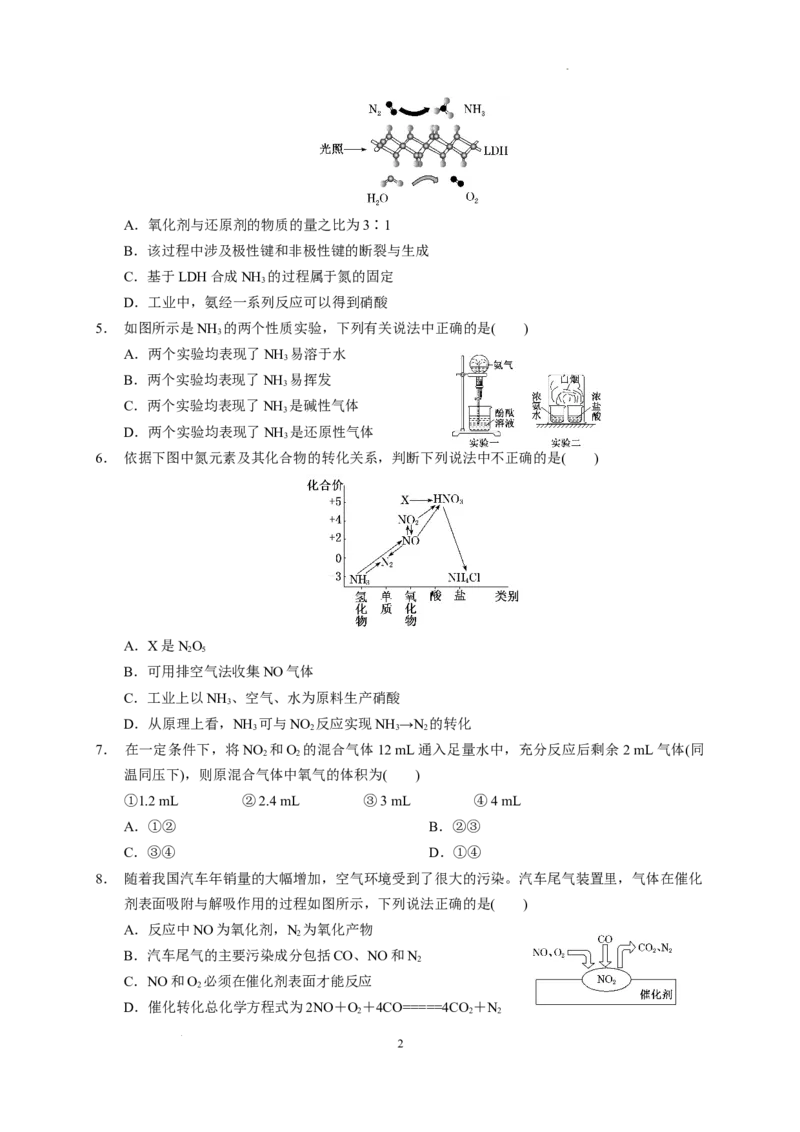
1. 爱吃虾的同学经常遇到这样一个问题,买来的虾,闻起来有刺鼻的氨水味,是虾坏了,还是有不良厂
商进行药物处理了呢。浙江工业大学食品系丁教授研究结论是海虾的消化道里也能分解出氨。
所以吃海鲜要用醋去腥味,其实就是这个道理。
下列关于氨水的说法不正确的是( )
A.氨水和液氨不同,氨水是由多种粒子构成的,液氨的组成中只有氨分子
B.氨水中物质的量浓度最大的粒子是NH ·H O(除水外)
3 2
C.氨水显弱碱性,故通常保存在金属容器中
D.在1 mol·L-1氨水中,NH ·H O、NH +、NH 的物质的量浓度之和为1 mol·L-1
3 2 4 3
2. 氮及其化合物的转化关系如图所示。
则下列说法不正确的是( )
A.路线①②③是工业生产硝酸的主要途径
B.路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径
C.上述所有标号的反应都是氧化还原反应
D.氮气可在足量的氧气中通过一步反应生成NO
2
3. 喷泉实验装置如图所示。应用下列各组气体—溶液,能出现喷泉现象的是( )
选项 气体 溶液
A HS 稀盐酸
2
B HCl 稀氨水
C NO 稀HSO
2 4
D CO 饱和NaHCO 溶液
2 3
4. 中国科学院科研团队研究表明,在常温常压和可见光下,基于 LDH(一种固体催化剂)合成NH
3
的原理示意图如图。下列说法错误的是( )
1
学科网(北京)股份有限公司A.氧化剂与还原剂的物质的量之比为3∶1
B.该过程中涉及极性键和非极性键的断裂与生成
C.基于LDH合成NH 的过程属于氮的固定
3
D.工业中,氨经一系列反应可以得到硝酸
5. 如图所示是NH 的两个性质实验,下列有关说法中正确的是( )
3
A.两个实验均表现了NH 易溶于水
3
B.两个实验均表现了NH 易挥发
3
C.两个实验均表现了NH 是碱性气体
3
D.两个实验均表现了NH 是还原性气体
3
6. 依据下图中氮元素及其化合物的转化关系,判断下列说法中不正确的是( )
A.X是NO
2 5
B.可用排空气法收集NO气体
C.工业上以NH 、空气、水为原料生产硝酸
3
D.从原理上看,NH 可与NO 反应实现NH →N 的转化
3 2 3 2
7. 在一定条件下,将NO 和O 的混合气体12 mL通入足量水中,充分反应后剩余2 mL气体(同
2 2
温同压下),则原混合气体中氧气的体积为( )
①1.2 mL ②2.4 mL ③3 mL ④4 mL
A.①② B.②③
C.③④ D.①④
8. 随着我国汽车年销量的大幅增加,空气环境受到了很大的污染。汽车尾气装置里,气体在催化
剂表面吸附与解吸作用的过程如图所示,下列说法正确的是( )
A.反应中NO为氧化剂,N 为氧化产物
2
B.汽车尾气的主要污染成分包括CO、NO和N
2
C.NO和O 必须在催化剂表面才能反应
2
D.催化转化总化学方程式为2NO+O+4CO=====4CO+N
2 2 2
2
学科网(北京)股份有限公司9.下列制取NH 并验证其还原性、收集并进行尾气处理的装置和原理均正确的是( )
3
10.下列关于自然界中氮循环(如图)的说法错误的是( )
A.①和②均属于氮的固定
B.氢、氧元素也参与了自然界中的氮循环
C.④中每生成1 mol NO,消耗2 mol O
2
D.③和⑤过程中氮元素分别被还原和氧化
二、填空题(本题包括5个小题,共60分)
11.(12分)如图是氮元素的几种价态与物质类别的对应关系,回答下列问题:
(1)写出N 的一种用途:______________________________________________________。
2
(2)从N元素化合价分析,N 具有氧化性和还原性。各举一例说明(用化学方程式表示)
2
氧化性:__________________________________________________________。
还原性:__________________________________________________________。
(3)HNO 与上图中的物质C常用于检验Cl-的存在,则C的化学式为_______________。
3
(4)实验室制取物质B的化学方程式为__________________________________________。
(5)NO 与水反应生成物质A的化学方程式为___________________________________。
2
3
学科网(北京)股份有限公司(6)浓硝酸与木炭在加热条件下反应的化学方程式为______________________________。
12.(12分)氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答
含氮化合物相关的问题:
(1)下列有关NH 的说法中,不正确的是________(填字母)。
3
A.工业合成NH 需要在高温、高压、催化剂下进行
3
B.NH 可用来生产碳铵和尿素等化肥
3
C.NH 可用浓硫酸或无水氯化钙干燥
3
D.NH 受热易分解,须置于冷暗处保存
3
(2)NH 易溶于水,标准状况下,用充满NH 的烧瓶做喷泉实验,水充满整个烧瓶后所形成溶液
3 3
的物质的量浓度为________mol·L-1。
(3)氨气燃烧的化学方程式为_________________________________________________。
(4)HNO 是一种重要的化工原料,工厂生产出的浓硝酸可用铝槽车或铁槽车来运输。在常温下
3
能使铝、铁钝化,说明浓硝酸具有很强的__________性。
(5)“吸收塔” 尾部会有含NO、NO 等氮氧化物的尾气排出,为消除它们对环境的破坏作用,
2
通常用以下两种方法处理:
①纯碱溶液吸收法。纯碱溶液与NO 反应的原理为
2
NaCO+2NO ===NaNO +________+CO(请填写完成化学方程式)。
2 3 2 3 2
②氨转化法。已知7 mol氨恰好能将含NO和NO 共6 mol 的混合气体完全转化为N ,则混合
2 2
气体中NO和NO 的物质的量之比为________,若用通式NO 表示氮氧化物,则每摩尔氨可将
2 x
________mol的NO 转化为N。
x 2
13.(12)某化学自主实验小组通过实验探究NH 、NO 的性质。
3 2
探究Ⅰ:利用如图所示装置探究NO 能否被NH 还原(K 、K 为止水夹,夹持固定装置略去)。
2 3 1 2
(1)A装置中制取NH 的化学方程式是________________________________。
3
(2)甲、乙分别是________(填字母)。
a.浓硫酸、碱石灰 b.碱石灰、碱石灰
c.碱石灰、无水氯化钙 d.五氧化二磷、五氧化二磷
(3)若NO 能够被NH 还原,预期C装置中能观察到的现象是____________________。
2 3
(4)此实验装置存在一个明显的缺陷是_____________________。
探究Ⅱ:探究NO 、O 混合气体的喷泉实验。
2 2
4
学科网(北京)股份有限公司(5)请在G装置中的虚线上描出导管实线图。
(6)G装置中浓硫酸有三种作用:混合NO 、O;干燥NO 、O;_________________。
2 2 2 2
(7)将G装置上面的圆底烧瓶收集满气体进行喷泉实验,若混合气体全部被吸收,则所得溶液
物质的量浓度为________ mol·L-1(保留两位有效数字)。
14.(12分)某化学兴趣小组为了制取并探究氨性质,用下列装置(部分夹持装置已略去)进行
实验[制取氨的反应原理:2NH Cl+Ca(OH) =====CaCl +2NH ↑+2HO]。
4 2 2 3 2
【实验探究】
(1)利用上述原理,实验室制取氨应选用________(填字母)发生装置进行实验。
(2)B装置中的干燥剂可选用________。
(3)气体通过C、D装置时,试纸颜色会发生变化的是________(填“C”或“D”)装置。
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象
是______________________________________。
(5)F装置中倒置漏斗的作用是_________________________。
(6)氨的用途很广,如可用氨处理二氧化氮:8NH +6NO ======7N +12HO,该反应中氨体
3 2 2 2
现________(填“氧化性”或“还原性”)。请你列举出氨的另一种用途: 。
15.(12分)氮的氧化物(NO)是大气污染物之一,工业上在一定温度和催化剂条件下用NH
x 3
将NO 还原生成N。某同学在实验室中对NH 与NO 反应进行了探究。回答下列问题:
x 2 3 2
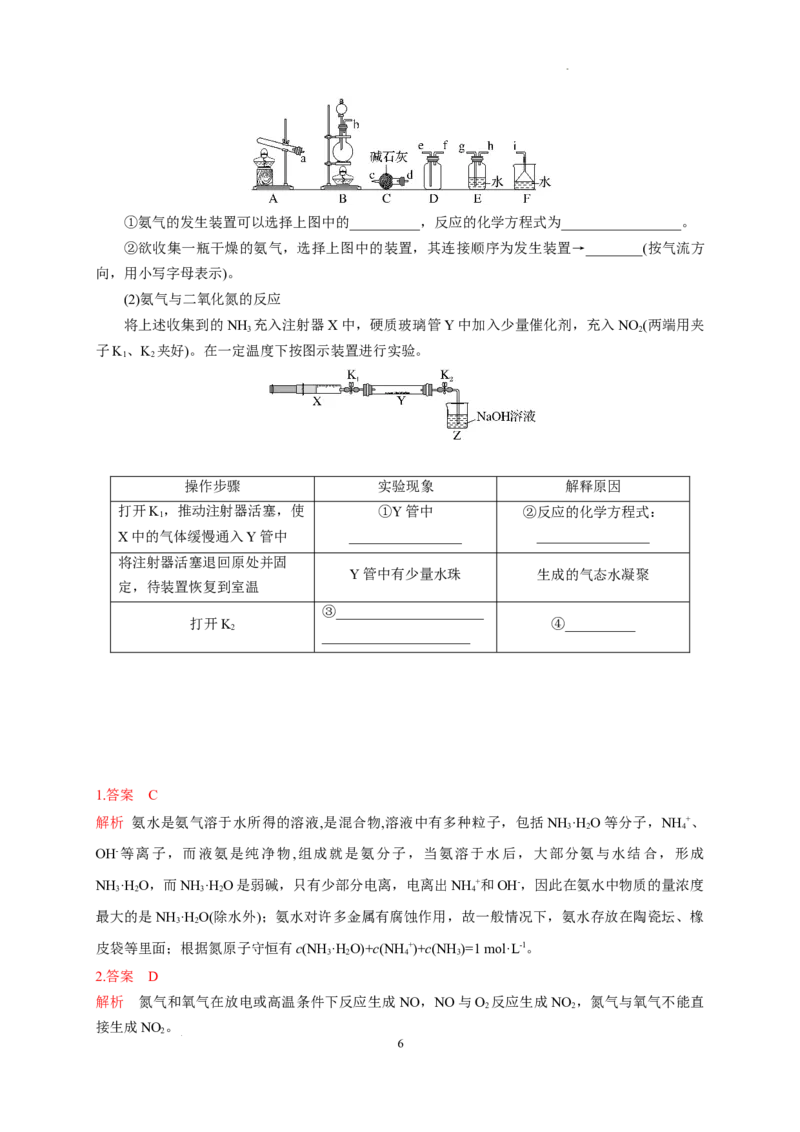
(1)氨气的制备
5
学科网(北京)股份有限公司①氨气的发生装置可以选择上图中的__________,反应的化学方程式为_________________。
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为发生装置→________(按气流方
向,用小写字母表示)。
(2)氨气与二氧化氮的反应
将上述收集到的NH 充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO (两端用夹
3 2
子K、K 夹好)。在一定温度下按图示装置进行实验。
1 2
操作步骤 实验现象 解释原因
打开K,推动注射器活塞,使 ①Y管中 ②反应的化学方程式:
1
X中的气体缓慢通入Y管中 ________________ ________________
将注射器活塞退回原处并固
Y管中有少量水珠 生成的气态水凝聚
定,待装置恢复到室温
③_____________________
打开K ④__________
2
_____________________
1.答案 C
解析 氨水是氨气溶于水所得的溶液,是混合物,溶液中有多种粒子,包括NH ·H O等分子,NH +、
3 2 4
OH-等离子,而液氨是纯净物,组成就是氨分子,当氨溶于水后,大部分氨与水结合,形成
NH ·H O,而NH ·H O是弱碱,只有少部分电离,电离出NH +和OH-,因此在氨水中物质的量浓度
3 2 3 2 4
最大的是NH ·H O(除水外);氨水对许多金属有腐蚀作用,故一般情况下,氨水存放在陶瓷坛、橡
3 2
皮袋等里面;根据氮原子守恒有c(NH ·H O)+c(NH +)+c(NH )=1 mol·L-1。
3 2 4 3
2.答案 D
解析 氮气和氧气在放电或高温条件下反应生成NO,NO与O 反应生成NO ,氮气与氧气不能直
2 2
接生成NO 。
2
6
学科网(北京)股份有限公司3.答案 B
解析 HS与稀盐酸、NO与稀HSO 、CO 与饱和NaHCO 溶液均不反应,不能形成喷泉,A、
2 2 4 2 3
C、D错误。
4.答案 A
解析: 该反应的化学方程式为2N +6HO=====4NH +3O ,氮气是氧化剂、水是还原剂,氧化
2 2 3 2
剂与还原剂的物质的量之比为1∶3,A项错误;该过程中,既有极性键(N—H、O—H)的断裂与生
成,也有非极性键(NN、O===O)的断裂与生成,B项正确;基于LDH合成NH 的过程是将氮气转
3
化为氨气的过程,属于氮的固定,C项正确;工业中,氨可以通过与氧气催化氧化得到NO,NO被
氧化为NO ,NO 再与水反应生成硝酸,D项正确。
2 2
5.答案 C
解析: 实验一是氨气的喷泉实验,喷泉实验证明氨气极易溶于水,溶于水形成一水合氨弱碱溶液,
滴加酚酞溶液变红色,证明氨气是碱性气体;实验二中浓氨水挥发出的氨气分子和浓盐酸挥发出的
氯化氢分子结合生成白烟氯化铵固体小颗粒,证明浓氨水易挥发,氨气遇到氯化氢发生反应生成氯
化铵,证明氨气是碱性气体。
6.答案 B
解析: NO遇空气中的氧气会被氧化为NO ,不可用排空气法收集NO气体,故B错误。
2
7.答案:D
解析:首先分析剩余的2 mL气体有两种可能。如果剩余 2 mL O ,则V(NO )=×(12-2) mL=8
2 2
mL,则混合气中V(O )=12 mL-8 mL=4 mL。若剩余的2 mL气体是NO,则混合气中的V(O )=
2 2
(12 mL-2 mL×3)×=1.2 mL,D项正确。
8.答案:D
解析: 反应过程中NO、O 为氧化剂,N 为还原产物;汽车尾气中的N 不是污染物;NO和O 的
2 2 2 2
反应不需要催化剂;根据题中的图示,可将反应的过程分成如下两步写:2NO+O===2NO 2NO +
2 2, 2
4CO===N +4CO,将两步反应式合并可得总化学方程式为2NO+O+4CO=====4CO+N。
2 2 2 2 2
9.答案 B
.解析:B 氯化铵受热分解生成氨和氯化氢,但在试管口氨和氯化氢又重新化合生成氯化铵,得不
到氨,A项错误;氨具有还原性,氯气具有强氧化性,二者能发生氧化还原反应,又因为氨的密度
小于空气的密度,氯气的密度大于空气的密度,所以长管通入NH ,短管通入Cl ,可以使其充分
3 2
反应,装置和原理均正确,B项正确;氨的密度小于空气的密度,采用向下排空气法收集,即收集
时应该是短管进、长管出,C项错误;氨极易溶于水,倒置的漏斗插入水中,不能防倒吸,D项错
误。
10.答案 D
解析 氮的固定指将N 转化为氮的化合物,反应①将N 转化为NO,属于氮的固定,反应②属于
2 2
植物固氮,A正确;由图示知,氮循环过程中涉及氢、氧元素,B正确;反应④是O 将NH 氧化为
2 3
NO,N元素化合价由-3价升高到+5价,失去8个电子,即1 mol NO生成失去电子8 mol,失去
的电子被O 得到,根据转移电子关系O ~4e-,知得8 mol电子需要2 mol O ,C正确;反应③中
2 2 2
NO被氧化为NO,氮元素被氧化,反应⑤中NO被还原为N,氮元素被还原,D错误。
2
7
学科网(北京)股份有限公司11.答案:(1)作保护气、保存粮食(或合成氨、制硝酸等)
(2)N +3H2NH (或N+3Mg=====MgN) N+O=====2NO
2 2 3 2 3 2 2 2
(3)AgNO
3
(4)Ca(OH) +2NH Cl=====CaCl +2NH ↑+2HO
2 4 2 3 2
(5)3NO +HO===2HNO +NO
2 2 3
(6)4HNO(浓)+C=====CO↑+4NO ↑+2HO
3 2 2 2
12.答案:(1)CD (2)(或0.045)
(3)4NH +3O=====2N+6HO
3 2 2 2
(4)氧化
(5)①NaNO ②1∶3
2
解析:(1)A项,工业合成NH 的反应条件是高温、高压、催化剂,正确;B项,NH 可与碳酸等反
3 3
应生成碳铵等,也可以与二氧化碳反应生成尿素,正确;C项,NH 可与硫酸或氯化钙发生化合反
3
应,不正确;D项,NH 不易分解,不正确。(2)水充满整个烧瓶后所形成溶液的物质的量浓度为
3
mol·L-1≈0.045 mol·L-1。(3)氨气燃烧的化学方程式为4NH +3O=====2N +6HO。(4)在常温下浓
3 2 2 2
硝酸能使铝、铁钝化,说明其具有很强的氧化性。(5)①纯碱溶液与NO 反应的原理为NaCO +
2 2 3
2NO ===NaNO +NaNO +CO 。根据质量守恒定律可知,除 NaNO 和 CO 外,另一种产物为
2 3 2 2 3 2
NaNO 。②7 mol氨失去21 mol电子,根据题意和得失电子守恒可得n(NO)+n(NO )=6 mol,2n(NO)
2 2
+4n(NO )=21 mol,解得n(NO)=1.5 mol,n(NO )=4.5 mol,则混合气体中NO和NO 的物质的量
2 2 2
之比为1∶3,若用通式NO 表示氮氧化物,反应过程中NO 分子得到2xe-,则每摩尔氨可将 mol
x x
的NO 转化为N。
x 2
13.答案:(1)CaO+NH ·H O===NH↑+Ca(OH) (2)c
3 2 3 2
(3)混合气体颜色变浅 (4)缺少尾气处理装置
(5) (进气管短,出气管长)
(6)观察气泡的生成速率,控制混合气体的比例
(7)0.036
解析:(1)将浓氨水滴入生石灰中,发生反应:CaO+NH ·H O===NH↑+Ca(OH) ,放出氨气。
3 2 3 2
(2)干燥氨只能用碱石灰,干燥二氧化氮可用五氧化二磷固体或无水氯化钙。(3)如果能反应,消耗
NO 使装置中混合气体颜色变浅。(4)由于NH 、NO 均能污染空气,所以与它们相关的实验均应有
2 3 2
尾气处理装置。(5)O 、NO 密度比空气大,故应进气管短,出气管长。(6)观察气泡的生成速率,控
2 2
制混合气体的比例。(7)烧瓶中充满溶液,反应4NO +O+2HO===4HNO 恰好发生,HNO 的物质
2 2 2 3 3
的量是恰好完全反应的NO 和O(体积比为4∶1)总物质的量的,溶液体积等于恰好完全反应的NO
2 2 2
和O 的总体积,设烧瓶中恰好完全反应的NO 和O 的总体积为V,则溶液浓度为=× mol·L-1,即
2 2 2
c(HNO)≈0.036 mol·L-1。
3
8
学科网(北京)股份有限公司14.答案 (1)a (2)碱石灰 (3)D (4)产生白烟 (5)防止倒吸
(6)还原性 作制冷剂、制氮肥(或化肥)、制硝酸、作化工原料(任答一点,其他合理答案也可)
15.答案 (1)①A 2NH Cl+Ca(OH) =====CaCl +2HO+2NH ↑(或B NH ·H O=====NH ↑+HO)
4 2 2 2 3 3 2 3 2
②dcfei
(2)①红棕色气体颜色慢慢变浅 ②6NO +8NH =====7N+12HO ③Z中NaOH溶液产
2 3 2 2
生倒吸现象 ④反应后气体分子数减少,Y管中压强小于外压
解析 (1)①在实验室通常是用加热氯化铵和消石灰固体混合物制取氨气,应选用发生装置 A,其
反应的化学方程式为2NH Cl+Ca(OH) =====CaCl +2HO+2NH ↑,或选用发生装置B,直接加热
4 2 2 2 3
浓氨水生成氨气:NH ·H O=====NH ↑+HO。②氨气是碱性气体,可用碱石灰干燥,其密度小于
3 2 3 2
空气,应采用向下排空气法收集,氨气极易溶于水,尾气处理时应防止倒吸,则要收集一瓶干燥的
氨气,仪器的连接顺序为发生装置→dcfei。
(2)打开K ,推动注射器活塞将氨气缓慢通入 Y管中,在一定温度和催化剂的作用下发生反应:
1
6NO +8NH =====7N +12HO,随着反应的发生Y管中红棕色气体颜色变浅;反应生成的水蒸气
2 3 2 2
液化后,NO 和NH 反应后气体的物质的量减小,反应容器中的压强减小,打开K ,Z中的溶液倒
2 3 2
吸入Y管中。
9
学科网(北京)股份有限公司10
学科网(北京)股份有限公司