文档内容
高一化学上学期第一次月考-(拔高 B 卷)
班级___________ 姓名___________ 学号____________ 分数____________
(考试时间:90分钟 试卷满分:100分)
考试范围:第一章 物质及其变化 难度:★★★★☆
注意事项:
1.本试卷分第I卷(选择题)和第II卷(非选择题)两部分。答卷前,考生务必将自己的班级、姓名、
学号填写在试卷上。
2.回答第I卷时,选出每小题答案后,将答案填在选择题上方的答题表中。
3.回答第II卷时,将答案直接写在试卷上。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18
答案
第Ⅰ卷(选择题 54 分)
一、选择题:本题共18个小题,每小题3分,共54分。在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.古诗词是古人为我们留下的宝贵精神财富,下列诗句不涉及氧化还原反应的是 ( )
A.野火烧不尽,春风吹又生
B.春蚕到死丝方尽,蜡炬成灰泪始干
C.粉身碎骨浑不怕,要留青白在人间
D.爆竹声中一岁除,春风送暖入屠苏
【答案】C
【解析】 A.柴草的燃烧是氧化还原反应,A项错误;B.蜡炬的主要成分是烃,烃的燃烧是氧化还原反应,
B项错误;C.碳酸钙的高温煅烧CaCO CaO+ CO ↑,该反应中各元素化合价都没有变化,不涉及氧
3 2
化还原反应,C项正确;D.爆竹中火药的爆炸是氧化还原反应,D项错误;答案选C。
2.下列说法正确的是( )
① 、 、 属于碱性氧化物, 、 、 都能和碱溶液发生反应属于酸性氧化
物②碳酸钠、氢氧化钡、氯化铵、过氧化钠都属于化合物
③混合物:漂白粉、水玻璃、 胶体、冰水混合物
④醋酸、烧碱、纯碱和生石灰分别属于酸、碱、盐和氧化物
⑤硅导电,铝在浓硫酸中钝化均属于物理变化
⑥盐酸属于混合物,而液氯、冰醋酸均属于纯净物
A.①③⑤ B.④⑤⑥ C.②④⑥ D.②③④
【答案】C
【解析】 、 和酸反应生成盐和水属于碱性氧化物, 和酸、碱反应生成盐和水属于两
性氧化物, 、 能和碱溶液发生反应属于酸性氧化物, 和碱反应生成盐和水发生的是氧化还
原反应,不是酸性氧化物,故 错误;
碳酸钠是钠离子和碳酸根离子构成,氢氧化钡是钡离子和氢氧根离子构成,氯化铵是铵根离子和氯离
子构成,过氧化钠是钠离子和过氧根离子构成,都属于化合物,故 正确;
漂白粉是氯化钙和次氯酸钙的混合物、水玻璃是硅酸钠的水溶液、 胶体属于分散系混合物、
冰水混合物是一种物质组成的为纯净物,故 错误;
醋酸属于酸,烧碱是氢氧化钠属于碱,纯碱是碳酸钠属于盐,生石灰为氧化钙属于氧化物,故 正确;
硅导电属于物理变化,铝在浓硫酸中钝化属于化学变化是浓硫酸的强氧化性体现,故 错误;
盐酸是氯化氢的水溶液属于混合物,而液氯、冰醋酸均是一种物质组成属于纯净物,故 正确;
3.初中化学的很多反应可以表示为:甲+乙=丙+丁,其中甲、乙、丙、丁既可能是单质也可能是化合
物。下列说法中,正确的是 ( )
A.若甲、乙、丙、丁均是化合物,则该反应一定是复分解反应
B.若甲、乙、丙分别是酸、碱、盐,则丁一定是水C.若甲是一氧化碳,乙是金属氧化物,则丙一定是二氧化碳
D.若甲是锌,丙是氢气,则乙一定是稀硫酸
【答案】B
【解析】A. 若甲、乙、丙、丁均是化合物,则该反应不一定是复分解反应,例如高温下二氧化硅和碳酸钠反
应生成硅酸钠和二氧化碳。该选项说法不正确;B.酸和碱反应一定生成盐和水,若甲、乙、丙分别是硫酸、
氢氧化钠、硫酸钠,则丁一定是水。该选项说法正确;C. 若甲是一氧化碳,乙是金属氧化物,则丙或丁都
有可能是二氧化碳。该选项说法不正确;D. 若甲是锌,丙是氢气,则乙可能是稀盐酸或稀硫酸。该选项
说法不正确。
4.下列事实与胶体知识有关的是( )
①晨雾中看见叶缝透过光束的通路 ②用明矾净水
③静电选矿 ④在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀
⑤一支钢笔使用不同牌号的蓝黑墨水易出现堵塞
⑥肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
⑦用可见光束可以鉴别红褐色的氢氧化铁胶体和溴水
A.①②⑤⑥⑦ B.①③④⑤⑦ C.①②③⑤⑥⑦ D.全部都有关
【答案】C
【解析】①晨雾中看见叶缝透过光束的通路、⑦用可见光束可以鉴别红褐色的氢氧化铁胶体和溴水为胶体
的丁达尔效应;②用明矾净水利用了胶体的吸附性;③静电选矿利用了胶体粒子带电,能电泳的性质;④
在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀,是发生了复分解反应,与胶体性质无关;⑤
一支钢笔使用不同牌号的蓝黑墨水易出现堵塞,是利用了胶体的聚沉现象;⑥肾功能衰竭等疾病引起的血
液中毒,可利用血液透析进行治疗,是利用渗析提纯血液胶体;①②③⑤⑥⑦与胶体性质有关,故答案为
C。
5.“纳米材料”是粒子直径为1~100nm的材料,纳米碳就是其中一种,若将纳米碳均匀地分散到蒸馏水
中,所形成的物质( )
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后会析出黑色沉淀
A.①④⑤ B.②③④ C.②③⑤ D.①③④⑥
【答案】C
【解析】将纳米碳均匀地分散到蒸馏水中,分散质粒子直径在1~100nm之间,所形成的物质是胶体,不是
溶液;胶体能产生丁达尔效应;胶体粒子直径在1~100nm之间,能透过滤纸,不能透过半透膜;胶体较稳定,静置后不会析出黑色沉淀,故正确的是②③⑤,选C。
6.下列各组关于强电解质、弱电解质、非电解质的归类正确的( )
A B C D
强电解质 Fe NaCl CaCO HNO
3 3
弱电解质 CHCOOH NH HCO Fe(OH)
3 3 2 3 3
非电解质 蔗糖 BaSO C HOH HO
4 2 5 2
【答案】C
【解析】A、Fe是单质,不是化合物,铁既不是电解质也不是非电解质,故A错误;B、NH 是非电解质,
3
本身不能电离出离子,BaSO 是盐属于强电解质,熔融状态完全电离,故B错误;C、碳酸钙是盐属于强
4
电解质,碳酸是弱酸属于弱电解质,乙醇是非电解质,故C正确;D、水能够电离出氢离子和氢氧根离子,
属于弱电解质,故D错误;
7.能正确表示下列化学反应的离子方程式的是( )
A.氢氧化钡溶液与硫酸的反应:OH-+H+=H O
2
B.澄清的石灰水与稀盐酸反应:Ca(OH) +2H+=Ca2++2HO
2 2
C.铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag
D.碳酸钙溶于稀盐酸中:CaCO +2H+=Ca2++HO+CO↑
3 2 2
【答案】D
【解析】A. 氢氧化钡溶液与硫酸的反应: Ba2++2OH-+SO 2-+2H+ =2 H O+BaSO↓,故A错误;B.
4 2 4
澄清的石灰水与稀盐酸反应:OH- + H+= H O,故B错误;C. 铜片插入硝酸银溶液中:Cu+2Ag+=Cu2+
2
+2Ag,故C错误;D. 碳酸钙溶于稀盐酸中:CaCO +2H+=Ca2++HO+CO↑,故D正确。
3 2 2
8.用离子方程式“H++OH−=H O”表示的是( )
2
A.NaHSO 溶液与Ba(OH) 溶液混合 B.NH Cl溶液与Ca(OH) 溶液混合
4 2 4 2
C.HNO 溶液与KOH溶液混合 D.NaHPO 溶液与NaOH溶液混合
3 2 4
【答案】C
【解析】A、NaHSO 溶液与Ba(OH) 溶液混合:H++SO2—+Ba2++OH-=BaSO ↓+H O,A不合题意;B、
4 2 4 4 2
NH Cl溶液与Ca(OH) 溶液混合:NH ++OH-=NH·H O,B不合题意;C、HNO 溶液与KOH溶液混合:
4 2 4 3 2 3
H++OH−=H O,C符合题意;D、NaHPO 溶液与NaOH溶液混合:HPO 2—+OH-=PO3—+H O,D不合题意。
2 2 4 4 4 29.下列碱性透明溶液中,能大量共存的离子组是
A.K+、Na+、MnO -、Cl- B.K+、Ag+、NO -、Cl-
4 3
C.Ba2+、Na+、Cl-、SO 2- D.Na+、Cu2+、NO -、Cl-
4 3
【答案】A
【解析】A、K+、Na+、MnO -、Cl-在碱性透明溶液中不反应,能大量共存,A正确;B、在碱性溶液中
4
Ag+不能大量共存,且与Cl-也不能大量共存,B错误;C、Ba2+与SO 2-在溶液中转化为硫酸钡沉淀,不能
4
大量共存,C错误;D、在碱性溶液中Cu2+不能大量共存,D错误,答案选A。
10.把各组中的气体通入溶液中,溶液的导电能力显著增强的是( )
A.CO(g)通入NaOH溶液 B.CO(g)通入石灰水
2 2
C.NH (g)通入CHCOOH溶液 D.NH (g)通入盐酸中
3 3 3
【答案】C
【解析】
A. 该过程的离子方程式为: ,该过程中,离子浓度与所带电荷的乘积没有变
化,则溶液的导电能力几乎不变,A错误;
B. 该过程的化学方程式为: ,该过程中,离子浓度减小,则溶液的
导电能力减弱,B错误;
C. 该过程发生的离子方程式为: ,则该过程中离子浓度显
著增大,则溶液的导电能力显著增大,C正确;
D. 该过程发生的离子方程式为: ,则该过程中离子浓度几乎不变,则溶液的导电能力
几乎不变,D错误;
11.下列实验过程中产生的现象与如图所示坐标图形相符合的是( )A.稀盐酸滴加到一定量NaHCO ,溶液中(横坐标是稀盐酸的体积,纵坐标为气体体积)
3
B.NaOH溶液滴入Ba(HCO ) 溶液中(横坐标是NaOH溶液的体积,纵坐标为沉淀质量)
3 2
C.稀盐酸滴加到AgNO 溶液中(横坐标是稀盐酸的体积,纵坐标为溶液的导电能力)
3
D.稀硫酸滴加到Ba(OH) 溶液中(横坐标是稀硫酸的体积,纵坐标为溶液的导电能力)
2
【答案】D
【解析】A. 稀盐酸滴加到一定量NaHCO 溶液中生成二氧化碳,气体体积从0逐渐增大到最大值后不变,
3
A不正确;B. NaOH溶液滴入Ba(HCO ) 溶液中生成碳酸钡沉淀,沉淀质量从0逐渐增大到最大值后不变,
3 2
B不正确;C. 稀盐酸滴加到AgNO 溶液中虽然生成氯化银沉淀,但是溶液中的离子浓度不会减少到0后
3
再增大(若两种溶液的浓度相同,则恰好反应时溶液中的离子浓度变为原来的一半),所以溶液的导电能
力也不会减小到0后再增大,C不正确;D. 稀硫酸滴加到Ba(OH) 溶液中发生的离子反应为2H++SO2-
2 4
+Ba2++2OH-=2H O+BaSO↓,溶液中的离子浓度逐渐减小,两者恰好反应时离子浓度达到最小值,继续加
2 4
入氢氧化钡溶液,离子浓度又逐渐增大到最大值(最大值由氢氧化钡溶液中的离子浓度决定)后不变,所
以溶液的导电能力先减小后增大到不变,D正确。本题选D。
12.歌曲《青花瓷》,唱道“帘外芭蕉惹骤雨,门环惹铜绿”,其中的“铜绿”即是铜锈,它的化学成分是
Cu (OH) CO(碱式碳酸铜)。铜在潮湿的空气中生锈的化学反应为2Cu+O +CO +H O=Cu (OH) CO。下列有
2 2 3 2 2 2 2 2 3
关该反应的说法正确的是( )
A.该反应不属于氧化还原反应
B.该反应中氧元素和碳元素化合价发生变化
C.该反应中铜是氧化剂
D.该反应是氧化还原反应,化合价发生改变的只有两种元素
【答案】D
【解析】 A. 在该反应中,铜元素的化合价由0价变成+2价,失去电子,被氧化,氧元素的化合价由0
价变成-2价,得到电子被还原,故该反应属于氧化还原反应,A不正确;B. 该反应中碳元素化合价没有发
生变化,B不正确;C. 该反应中铜失去电子,铜是还原剂,C不正确;D. 该反应是氧化还原反应,化合
价发生改变的只有两种元素,D正确。
13.下列各组微粒中,在一定条件下均可以作氧化剂的是( )
A.Fe、HO、CO B.Fe3+、MnO —、NO —
2 2 4 3
C.Cl、HClO、Mg D.ClO-、Cl-、Ag+
2
【答案】B【解析】A.Fe元素化合价为0,是铁的最低化合价,只有还原性,故A错误;B.Fe、Mn、N元素化合价都
处于最高价态,Fe3+、MnO -、NO -都具有氧化性,在一定条件下可以作为氧化剂,故B正确;C.Mg元
4 3
素化合价为0,是镁的最低化合价,只有还原性,故C错误;D.Cl元素化合价为-1,是氯的最低化合价,
只有还原性,故D错误;
14.随着我国汽车年销量的大幅增加,空气环境受到了很大的污染。汽车尾气装置里,气体在催化剂表面
吸附与解吸作用的过程如图所示,下列说法正确的是( )
A.反应中NO为氧化剂,N 为氧化产物
2
B.汽车尾气的主要污染成分包括CO、NO和N
2
C.NO和O 必须在催化剂表面才能反应
2
D.催化转化总化学方程式为2NO+O+4CO 4CO+N
2 2 2
【答案】D
【解析】反应过程中NO、O 为氧化剂,N 为还原产物;汽车尾气中的N 不是污染物;NO和O 的反应不
2 2 2 2
需要催化剂;根据题中的图示,可将反应的过程分成如下两步写:2NO+O===2NO ,2NO +4CO===N
2 2 2 2
+4CO,将两步反应式合并可得总化学方程式为2NO+O+4CO 4CO+N;
2 2 2 2
15.根据世界环保联盟的要求,广谱消毒剂ClO 将逐渐取代Cl 成为生产自来水的消毒剂。工业上ClO 常
2 2 2
用NaClO 和NaSO 溶液混合并加HSO 酸化后反应制得,则反应后NaSO 转化为
3 2 3 2 4 2 3
A.NaSO B.SO C.S D.NaS
2 4 2 2
【答案】A
【解析】反应物为NaClO 和NaSO ,NaClO 生成ClO 是化合价降低的过程,由此可知在反应中NaClO
3 2 3 3 2 3
为氧化剂,NaSO 为还原剂,NaClO 被NaSO 还原生成ClO ,则NaSO 被氧化生成+6价S,由选项可知,
2 3 3 2 3 2 2 3
只能为NaSO ;
2 4
16.已知有如下反应:①2BrO-+Cl=Br +2ClO -,②ClO -+5Cl-+6H+=3Cl+3H O,
3 2 2 3 3 2 2
③2FeCl +2KI=2FeCl +2KCl+I ,④2FeCl +Cl=2FeCl 。下列各微粒氧化能力由强到弱的顺序正确的是
3 2 2 2 2 3A.ClO ->BrO ->Cl>Fe3+>I B.BrO->Cl>ClO ->I >Fe3+
3 3 2 2 3 2 3 2
C.BrO->ClO ->Cl>Fe3+>I D.BrO->ClO ->Fe3+>Cl>I
3 3 2 2 3 3 2 2
【答案】C
【解析】在氧化还原反应中,氧化剂的氧化性强于氧化产物的氧化性,据此可知:①中是BrO->ClO -;
3 3
②中是ClO ->Cl;③中是Fe3+>I;④中是Cl>Fe3+,则各微粒氧化能力由强到弱的顺序是BrO->ClO -
3 2 2 2 3 3
>Cl>Fe3+>I ;
2 2
17.常温下,发生下列几种反应:①16H++10Z-+2XO —=2X2++5Z+8HO ②2A2++B =2A3++2B-
4 2 2 2
③2B-+Z=B +2Z-根据上述反应,判断下列结论错误的是( )
2 2
A.溶液中可发生:Z+2A2+=2A3++2Z-
2
B.Z 在①③反应中为还原剂
2
C.氧化性强弱的顺序为:XO —>Z>B >A3+
4 2 2
D.X2+是XO —的还原产物
4
【答案】B
【解析】A. 根据分析得出氧化性顺序为XO —>Z>B >A3+,因此溶液中可发生:Z+2A2+=2A3++2Z
4 2 2 2
-,故A正确;B. ①16H++10Z-+2XO —=2X2++5Z+8HO 中Z 是氧化产物,故B错误;C. 根据分析
4 2 2 2
得出氧化性强弱的顺序为:XO —>Z>B >A3+,故C正确;D. ①16H++10Z-+2XO —=2X2++5Z+
4 2 2 4 2
8HO 中XO —中X的化合价降低,因此X2+是XO —的还原产物,故D正确。
2 4 4
18.已知Co O 在酸性溶液中易被还原成Co2+,Co O、Cl、FeCl 、I 的氧化性依次减弱。下列反应在水溶
2 3 2 3 2 3 2
液中不可能发生的是( )
A.3Cl+6FeI =2FeCl +4FeI
2 2 3 3
B.Cl+FeI =FeCl +I
2 2 2 2
C.Co O+6HCl=2CoCl +Cl↑+3H O
2 3 2 2 2
D.2Fe3++2I-=2Fe2++I
2
【答案】A
【解析】A.根据反应:3Cl+6FeI =2FeCl +4FeI ,得出氧化性是:Cl>FeCl ,但是氧化性是FeCl >I,
2 2 3 3 2 3 3 2
还原性是碘离子强于亚铁离子,碘离子会先被氯气氧化,和题意不相符合,不可能发生,故A符合题意;
B.因为氧化性FeCl >I,所以氯气先氧化碘离子后氧化铁离子,故B不符合题意;C.根据反应:
3 2
Co O+6HCl=2CoCl +Cl↑+3H O,得出氧化性是:Co O>Cl,和题意相符合,反应可能发生,故C不符
2 3 2 2 2 2 3 2
合题意;D.因为氧化性FeCl >I,所以2Fe3++2I-=2Fe2++I 能发生,故D不符合题意。
3 2 2第 II 卷(非选择题 46 分)
二、非选择题(46分)
19.(10分)已知NaHSO 溶于水时电离出Na+、H+、SO 2-,某同学欲探究其化学性质,取5份溶液做了
4 4
如下实验,请你用离子方程式解释上述实验现象:
(1)加Zn粒有大量气体生产:____________________
(2)加入Fe O 后溶液变黄色:____________________
2 3
(3)加入Cu(OH) 固体后溶液变蓝色:____________________
2
(4)加入NaHCO 后有大量气泡产生:______________________
3
(5)逐滴滴加Ba(OH) 溶液至SO 2-恰好完全沉淀:__________________
2 4
【答案】(1)Zn+2H+=H ↑+Zn2+
2
(2) Fe O+6H+=2Fe3++3H O
2 3 2
(3) Cu(OH) +2H+=Cu2++2H O
2 2
(4) HCO -+H+=H O+CO↑
3 2 2
(5) Ba2++SO2-+H++OH-=H O+BaSO↓
4 2 4
【解析】(1)锌是活泼的金属,能与酸反应生成氢气,方程式为Zn+2H+=H ↑+Zn2+;
2
(2)氧化铁是碱性氧化物,能与酸反应生成铁离子,方程式为Fe O+6H+=2Fe3++3H O;
2 3 2
(3)氢氧化铜是碱,能与酸反应生成铜离子和水,方程式为Cu(OH) +2H+=Cu2++2H O;
2 2
(4)碳酸氢盐能与酸反应生成CO 和HO,方程式为HCO -+H+=H O+CO↑;
2 2 3 2 2
(5)逐滴滴加Ba(OH) 溶液至SO 2-恰好完全沉淀时生成硫酸钡、氢氧化钠和水,离子方程式为Ba2++SO2-
2 4 4
+ H++OH-=H O+BaSO↓。
2 4
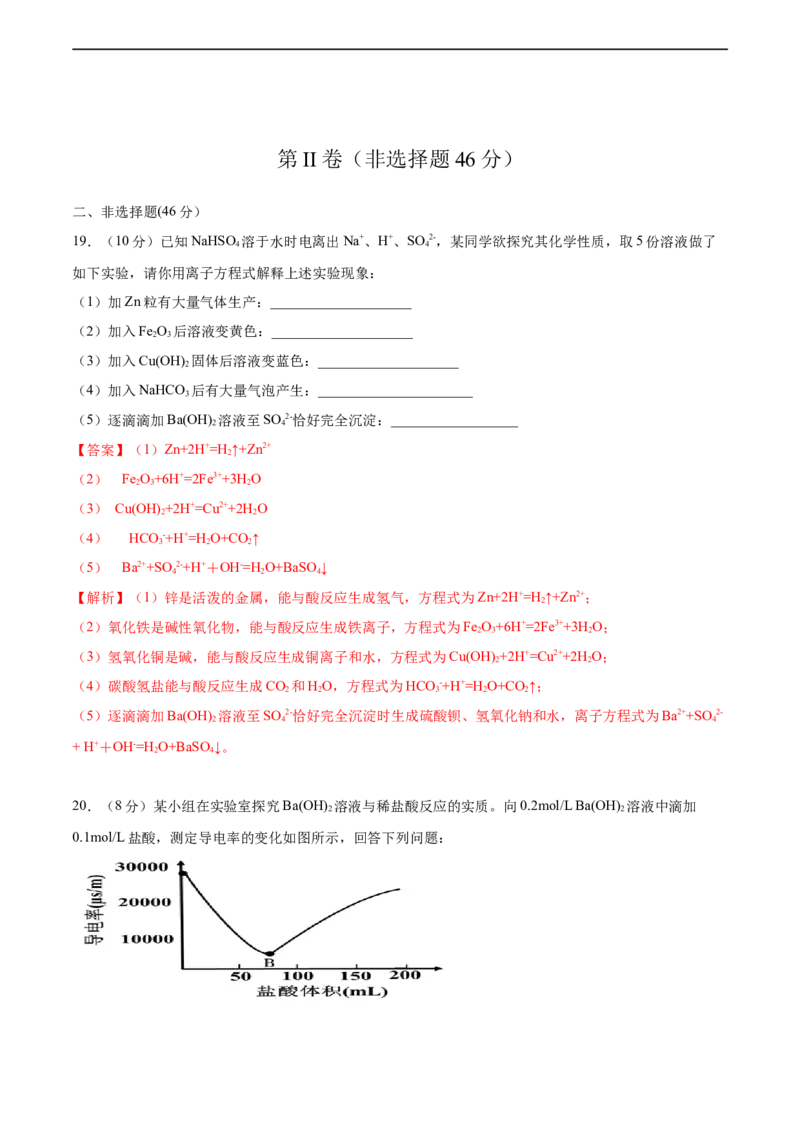
20.(8分)某小组在实验室探究Ba(OH) 溶液与稀盐酸反应的实质。向0.2mol/L Ba(OH) 溶液中滴加
2 2
0.1mol/L盐酸,测定导电率的变化如图所示,回答下列问题:(1)Ba(OH) 在水中以离子形式存在的实验证据是___________。Ba(OH) 的电离方程式为___________。
2 2
(2)A-B段,发生的离子反应是__________。
(3)B点恰好完全反应,此时溶液中存在的微粒有HO、__________。
2
(4)下列化学反应的实质与Ba(OH) 溶液与稀盐酸反应的实质相同的是__________。
2
A.Ba(OH) 和HSO B.NaOH和HSO C.Ba(OH) 与HNO
2 2 4 2 4 2 3
【答案】(1)A点的导电率高 Ba(OH) = Ba2+ + 2OH-
2
(2) H+ + OH-= H O
2
(3) Ba2+、Cl-
(4) BC
【解析】(1)A→B段,A点的溶液导电率高,随着盐酸的量的增多,溶液的导电率减小,是因为发生反
应H++OH-=H O,溶液中离子浓度减小,说明Ba(OH) 在水中以离子形式存在;Ba(OH) 的电离方程式为:
2 2 2
Ba(OH) =Ba2++2OH-;
2
(2)A-B段,Ba(OH) 和HCl发生反应,离子方程式为:H+ +OH-=H O;
2 2
(3)B点,Ba(OH) 和HCl恰好完全反应,此时溶液中存在的微粒有HO、Ba2+、Cl-;
2 2
(4)Ba(OH) 溶液与稀盐酸反应的实质是:H+ +OH-=H O;
2 2
A、Ba(OH) 和HSO 反应的实质是:2H+ +SO2-+Ba2++2OH-=BaSO ↓+2H O;
2 2 4 4 4 2
B、NaOH和HSO 反应的实质是:H+ +OH-=H O;
2 4 2
C、Ba(OH) 与HNO 反应的实质是:H+ +OH-=H O;
2 3 2
21.(12分)某课外活动小组进行Fe(OH) 胶体的制备实验并检验其性质。
3
(1)若将饱和FeCl 溶液分别滴入下列物质中,能形成胶体的是________(填字母)。
3
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
(2)现有甲、乙、丙三名同学进行Fe(OH) 胶体的制备:
3
①甲同学的操作:取一小烧杯,加入25 mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2 mL FeCl 饱和溶液,
3
继续煮沸至混合液呈红褐色,停止加热。请评价该操作是否正确______。
②乙直接加热饱和FeCl 溶液,请评价是否正确______。
3
③丙向沸水中滴加饱和FeCl 溶液,为了使反应进行充分,煮沸10分钟,请评价是否正确________。
3
(3)写出制备Fe(OH) 胶体的化学方程式: ____________________。证明有Fe(OH) 胶体生成的实验操作是
3 3
_____________________。该操作利用胶体的性质是________。
(4)Fe(OH) 胶体稳定存在的主要原因是____________________(填字母,下同)。
3
A.胶体粒子直径小于1nm B.胶体粒子带正电荷C.胶体粒子作布朗运动 D.胶体粒子能透过滤纸
(5)Fe(OH) 胶体区别于FeCl 溶液最本质的特征是________。
3 3
A.Fe(OH) 胶体粒子的直径在1~100 nm之间
3
B.Fe(OH) 胶体具有丁达尔效应
3
C.Fe(OH) 胶体是均一的分散系
3
D.Fe(OH) 胶体的分散质能透过滤纸
3
(6)若取少量制得的胶体加入试管中,加入硫酸铵溶液,现象是_____________,这种现象称为胶体的
________。
【答案】(1)B
(2) 正确 不正确 不正确
(3) FeCl +3H O Fe(OH) (胶体)+3HCl 让一束可见光通过制得的分散系,从侧面观察到一条光
3 2 3
亮的“通路”,说明制得的是胶体 丁达尔效应
(4) B
(5) A
(6) 产生红褐色沉淀 聚沉
【解析】(1)实验室制备氢氧化铁胶体的方法是:在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐
色时立即停止加热,故合理选项是B;
(2)①在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即停止加热,这是制备氢氧化铁胶体
的正确操作,操作合理,①正确;
②直接加热饱和三氯化铁饱和溶液,反应产生的氢氧化铁胶体遇到电解质发生聚沉,不能得到胶体,操作
不合理,②不正确;
③加热到继续沸腾,不能继续加热,否则形成的胶粒会集结在一起,形成沉淀,操作不合理,③不正确;
(3)将3-4滴饱和FeCl 溶液滴入25mL沸腾的蒸馏水中,继续加热煮沸至液体呈红褐色,停止加热,就制取
3
得到氢氧化铁胶体,反应方程式为:FeCl +3H O Fe(OH) (胶体)+3HCl;证明有Fe(OH) 胶体生成的实
3 2 3 3
验操作是:让一束可见光通过制得的分散系,从侧面观察到一条光亮的“通路”,该操作利用胶体的性质
是丁达尔效应;
(4)胶体具有很强的吸附能力,能选择性的吸附溶液中的离子而带电荷,胶粒之间相互排斥,而不易产生较
大微粒而聚沉,故合理选项是B;(5)Fe(OH) 胶体区别于FeCl 溶液最本质的特征是Fe(OH) 胶体的分散质微粒直径大小在1~100nm之间,
3 3 3
故合理选项是A;
(6)向Fe(OH) 胶体中滴入硫酸铵,硫酸铵电离产生的SO 2-的负电荷会中和胶粒上的正电荷,使胶粒之间的
3 4
斥力减小,胶粒聚集形成氢氧化铁沉淀,这种现象叫胶体聚沉,因此看到的现象是产生红褐色沉淀。
22(6分).储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的碳纳米管常伴有大量的杂质
——碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应中的反应物和生成物有C、CO、HSO 、
2 2 4
KCr O、KSO 、Cr (SO ) 和HO七种。
2 2 7 2 4 2 4 3 2
(1)请用上述物质填空(不用配平):C+________+H SO ——________+______+Cr (SO )+H O。
2 4 2 4 3 2
(2)上述反应中氧化剂是(填化学式)________,被氧化的元素是(填元素符号)________。
(3)H SO 在上述反应中表现出来的性质是(填选项序号)________。
2 4
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性
和酸性
【答案】KCr O CO K SO K Cr O C C 4.48 L
2 2 7 2 2 4 2 2 7
【解析】(1)由C→CO、KCr O→Cr (SO ) 可知,碳元素的化合价从0价升高到+4价,失去4个电子。
2 2 2 7 2 4 3
Cr元素的化合价从+6价降低到+3价,得到3个电子,所以根据电子得失守恒可知还原剂与氧化剂的物
质的量之比是3:2。根据原子守恒可知,反应中还有硫酸钾生成,则反应的化学方程式为3C+2KCr O+
2 2 7
8HSO =3CO↑+2KSO +2Cr (SO )+8HO。
2 4 2 2 4 2 4 3 2
(2)根据(1)可知氧化剂为KCr O,还原产物为Cr (SO ),还原剂为C,氧化产物为CO,被氧化的元
2 2 7 2 4 3 2
素是C。
(3)HSO 在反应中各元素的化合价没有发生变化,但反应中有硫酸盐生成,所以硫酸只表现酸性,答案
2 4
选B。
23(10分).KClO 与浓盐酸在一定温度下反应会生成黄绿色的易爆物质二氧化氯,其变化可表述为:
3
KClO+HCl(浓)―KCl+ClO ↑+Cl↑+
3 2 2
(1)请完成该化学方程式
(2)浓盐酸在反应中显示出来的性质是___(填写编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)若产生7.1gCl,则生成ClO 的质量为___g。
2 2
(4)ClO 具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(用单位质量得到的电子数表示)是
2
Cl 的___倍(小数点后保留两位数字)。
2【答案】2KClO+4HCl(浓)=2KCl+2ClO ↑+Cl↑+2H O ② 13.5 2.63
3 2 2 2
【解析】(1)KClO 中氯元素化合价由+5价降低为ClO 中+4价,化合价降低1价;HCl中氯元素化合价
3 2
由-1价升高为Cl 中0价,化合价升高2价,化合价升降最小公倍数为2,故ClO 系数为2,Cl 系数为1;
2 2 2
所以KClO 系数为2,KCl系数为2,HCl系数为4,结合元素守恒,可知未知物是水,水的系数是2;配
3
平完的化学方程式为:2KClO+4HCl(浓)=2KCl+2ClO ↑+Cl↑+2H O;
3 2 2 2
(2)反应2KClO+4HCl(浓)=2KCl+Cl ↑+2ClO ↑+2H O中,HCl中氯元素化合价由-1价升高为Cl 中0
3 2 2 2 2
价可知,HCl中氯元素被氧化,HCl在反应中还原剂与酸的作用,各占一半;故选②;
(3)7.1gCl 的物质的量是0.1mol,根据化学方程式,生成ClO 的物质的量为0.2mol,质量为
2 2
0.2mol×67.5g/mol=13.5g;
(4)设ClO 、Cl 的质量都是71g,氯气是1mol,得到的电子的物质的量是2mol,ClO 得到的电子的物质
2 2 2
的量为 ×5=5.26mol,则ClO 消毒的效率是Cl 的5.26÷2=2.63倍;答案是:2.63。
2 2