文档内容
配套《高中必刷题 化学 必修第一册 LK》使用
第3章 物质的性质与转化
第3节 氮的循环
课时1氮气与氮的氧化物
一、自然界中的氮循环 氮气
1.自然界中的氮循环
(1)氮元素的存在
在自然界中的存在形式有游离态和化合态。
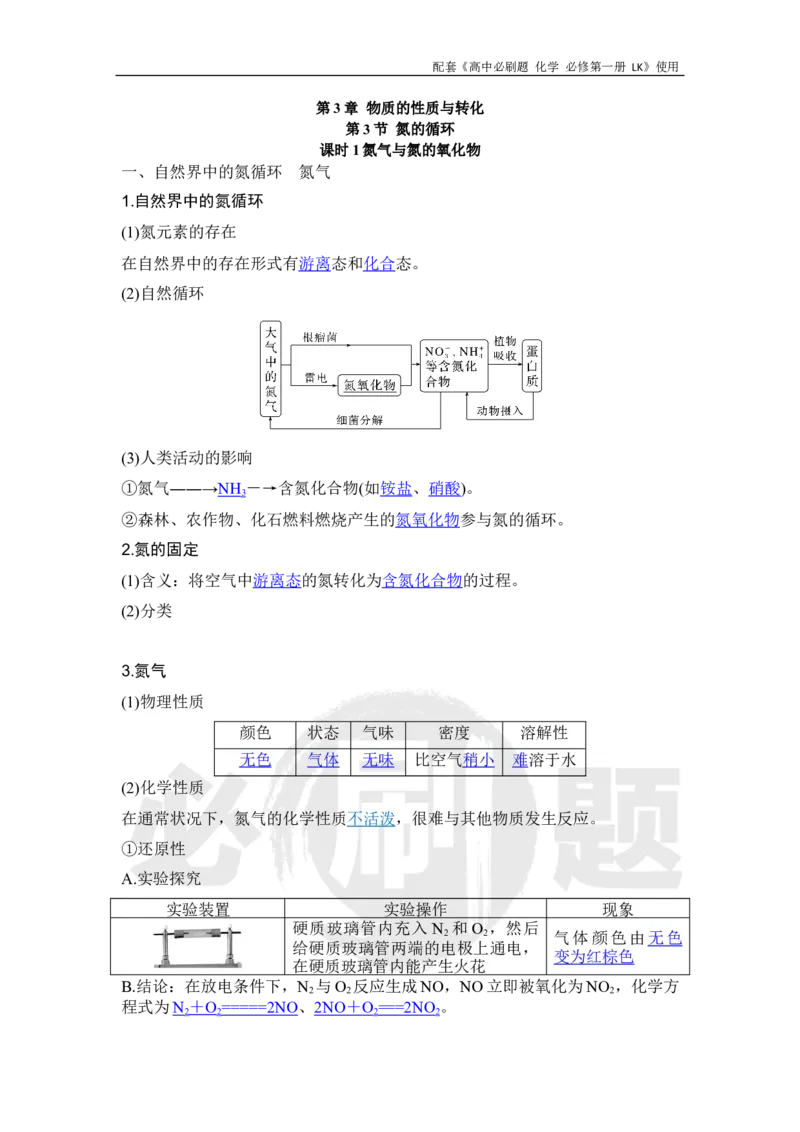
(2)自然循环
(3)人类活动的影响
①氮气――→NH ―→含氮化合物(如铵盐、硝酸)。
3
②森林、农作物、化石燃料燃烧产生的氮氧化物参与氮的循环。
2.氮的固定
(1)含义:将空气中游离态的氮转化为含氮化合物的过程。
(2)分类
3.氮气
(1)物理性质
颜色 状态 气味 密度 溶解性
无色 气体 无味 比空气稍小 难溶于水
(2)化学性质
在通常状况下,氮气的化学性质不活泼,很难与其他物质发生反应。
①还原性
A.实验探究
实验装置 实验操作 现象
硬质玻璃管内充入 N 和 O ,然后
2 2 气体颜色由无色
给硬质玻璃管两端的电极上通电,
变为红棕色
在硬质玻璃管内能产生火花
B.结论:在放电条件下,N 与O 反应生成NO,NO立即被氧化为NO ,化学方
2 2 2
程式为N + O ===== 2NO 、 2NO + O == =2NO 。
2 2 2 2配套《高中必刷题 化学 必修第一册 LK》使用
注意:N 和O 反应的最初产物是NO,而不是NO 。
2 2 2
②氧化性
N 和H 反应生成NH ,化学方程式:N + 3H 2NH 。
2 2 3 2 2 3
Mg在N 中燃烧反应生成Mg N ,化学方程式:N + 3M g ===== M g N 。
2 3 2 2 3 2
(3)主要用途
①氮气常用作保护气,用于焊接金属、填充灯泡、保存食品等。
②氮气是合成氨、制硝酸的主要原料。
③液氮可用作制冷剂,用于医学、科技等领域。
二、一氧化氮、二氧化氮的性质
NO与NO 的比较
2
物质 NO NO
2
红棕色、有刺激性气味、
色、态、味、毒性 无色、无味、有毒气体
有毒气体
水溶性 难溶于水 易溶于水
与氧气反应 2NO+O ===2NO 不反应
2 2
3NO + H O == =2HNO +
与水反应 不反应 2 2 3
NO(自身氧化还原)
4NO+3O + 4NO + O +
与氧气、水同时作用 2 2 2
2H O===4HNO 2H O == =4HNO
2 3 2 3
6NO + 8NH ===7N +
2 3 2
6NO+4NH =====5N + 12H O(NO 能将 I-氧化为
氧化性 3 2 2 2
6H O I ,能使湿润的淀粉KI 试
2 2
纸变蓝)