文档内容
2019年青海省中考化学试卷
一、单项选择题(本题共13小题,1-8题每题1分,9-13题每题2分,共18分.请把正确的选
项序号填入下面相应题号的表格内)
1.(1分)下列属于化学变化的是( )
A.酒精挥发 B.冰雪融化 C.蜡烛燃烧 D.铁水铸锅
2.(1分)下列物质在氧气中剧烈燃烧,火星四射,生成黑色固体的是( )
A.铁丝 B.红磷 C.硫粉 D.镁条
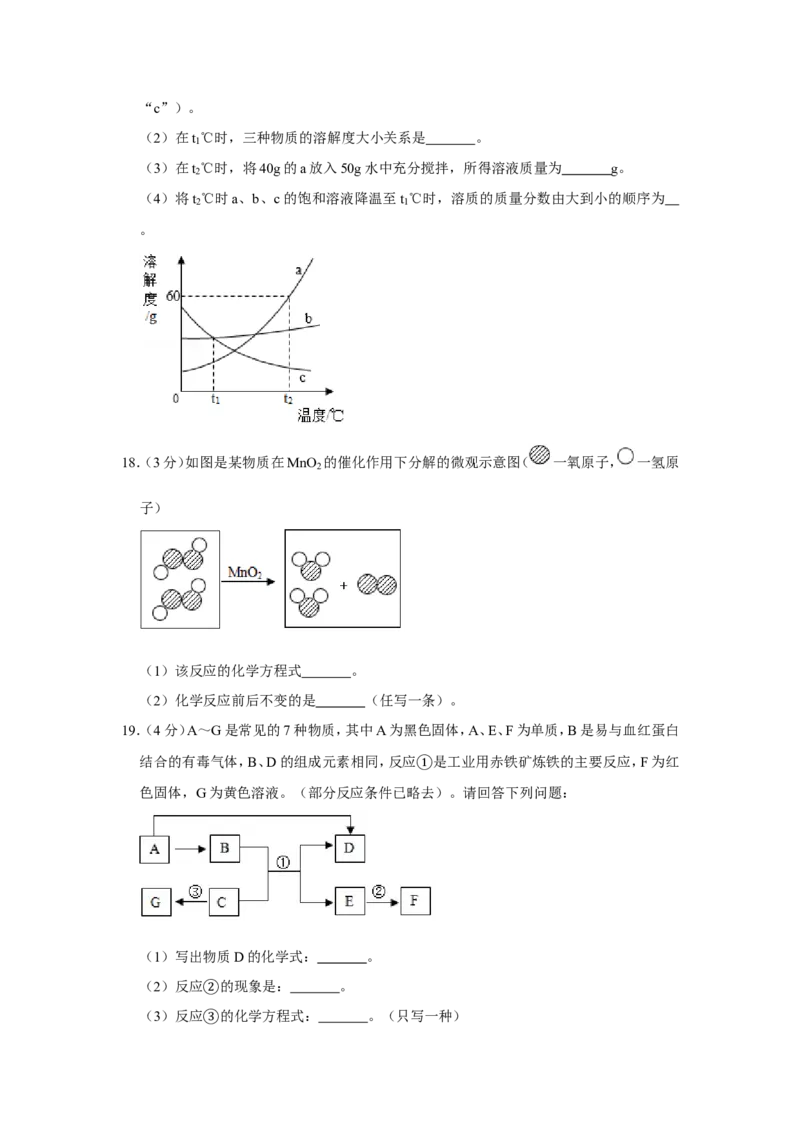
3.(1分)下列实验操作正确的是( )
A B C D
A.倾倒液体 B.滴加液体
C.熄灭酒精灯 D.检查装置气密性
4.(1分)下列物质不属于氧化物的是( )
A.冰水混合物 B.臭氧 C.生石灰 D.干冰
5.(1分)要配制50g质量分数为6%的氯化钠溶液,下列说法错误的是( )
A.需称量的氯化钠固体为3g
B.在烧杯中配制溶液
C.溶解时玻璃棒的作用是引流
D.俯视读数导致溶质质量分数偏大
6.(1分)能保持氢气化学性质的微粒是( )
A.2H B.H C.H+ D.H
2
7.(1分)在化学反应:CH +2O CO +2X中,X的化学式为( )
4 2 2
A.H O B.H C.H O D.CO
2 2 2 2
8.(1分)酸奶中含有的乳酸菌(C H O )能帮助消化。下列说法错误的是( )
3 6 3
A.乳酸菌属于有机物
B.乳酸菌由3个碳原子、6个氢原子、3个氧原子构成C.乳酸菌中氧元素的质量分数最大
D.乳酸菌中碳、氢、氧元素质量比为6:1:8
9.(2分)在一密闭容器中加入下列四种物质充分反应,测得反应前后各物质的质量如表。下
列说法正确的是( )
物质 A B C D
反应前质量/g 20 12 2 6
反应后质量/g 0 2 2 待测
A.该反应是分解反应 B.物质C可能是催化剂
C.物质D的待测值是30g D.反应中B、D的质量比是3:1
10.(2分)下列对所学内容的归纳、总结完全正确的是( )
A.性质与用途 B.元素与健康
金刚石硬度大﹣﹣裁玻璃 缺碘﹣﹣甲状腺肿大
活性炭吸附性﹣﹣去除异味 缺钙﹣﹣贫血
C.化学与生活 D.食品与安全
铁制容器能盛放农药波尔多液 甲醛溶液浸泡的海产品不能食用
油锅着火应立即盖上锅盖 用亚硝酸钠代替氯化钠作调味品
A.A B.B C.C D.D
11.(2分)现有X、Y、Z三种金属,若将X、Y、Z分别放入稀硫酸中,只有X溶解并产生气泡;
若将Y、Z分别放入AgNO 溶液中,Y表面析出银白色固体,而Z表面无变化,则三种金
3
属活动性由强到弱的顺序是( )
A.Z>X>Y B.Y>Z>X C.X>Z>Y D.X>Y>Z
12.(2分)下列图象与变化对应关系错误的是( )
A BC D
A.碱溶液加水稀释 B.通电分解水
C.煅烧石灰石 D.石灰水变质
13.(2分)除去下列物质中的杂质,所选试剂及操作方法错误的是( )
选项 物质(括号内为杂质) 选用试剂及操作方法
A N (水蒸气) 通过浓H SO
2 2 4
B NaOH溶液(Na CO 溶液) 加入过量稀盐酸
2 3
C Cu粉(Fe) 用磁铁吸引
D NaCl(泥沙) 加足量水溶解、过滤、蒸发
A.A B.B C.C D.D
二、填空题(本题包括6小题,化学方程式2分,其余每空1分,共18分)
14.(2分)用化学用语表示:2个镁离子 ;标出Na SO 中硫元素的化合价 。
2 4
15.(3分)锂电池新能源汽车的使用,能有效改善空气质量。如图是锂元素在元素周期表中
的信息:
(1)锂的相对原子质量为 。
(2)与锂元素具有相似化学性质的是 (填“A”或“B”或“C”)。
(3)在A、B、C三种粒子中属于同种元素的是 。
16.(2分)港珠澳大桥是我国自行设计建造的又一项世界级工程。
(1)在建造过程中用到了水泥、砂浆、钢圆筒等物质,其中属于金属材料的是 。
(2)自行车的车架表面刷油漆可防锈,其原理是隔绝了 。
17.(4分)青海省柴达木盆地的察尔汗盐湖是我国最大的天然内陆咸水湖,当地农民通过
“冬天捞碱,夏天晒盐”获得大量湖盐。
(1)“夏天晒盐”中的“盐”其溶解度可用图中 来表示(填“a”、或“b”、或“c”)。
(2)在t ℃时,三种物质的溶解度大小关系是 。
1
(3)在t ℃时,将40g的a放入50g水中充分搅拌,所得溶液质量为 g。
2
(4)将t ℃时a、b、c的饱和溶液降温至t ℃时,溶质的质量分数由大到小的顺序为
2 1
。
18.(3分)如图是某物质在MnO 的催化作用下分解的微观示意图( 一氧原子, 一氢原
2
子)
(1)该反应的化学方程式 。
(2)化学反应前后不变的是 (任写一条)。
19.(4分)A~G是常见的7种物质,其中A为黑色固体,A、E、F为单质,B是易与血红蛋白
结合的有毒气体,B、D的组成元素相同,反应 是工业用赤铁矿炼铁的主要反应,F为红
色固体,G为黄色溶液。(部分反应条件已略①去)。请回答下列问题:
(1)写出物质D的化学式: 。
(2)反应 的现象是: 。
(3)反应②的化学方程式: 。(只写一种)
③三、实验题(本题包括2小题,化学方程式2分,其余每空1分,共20分)
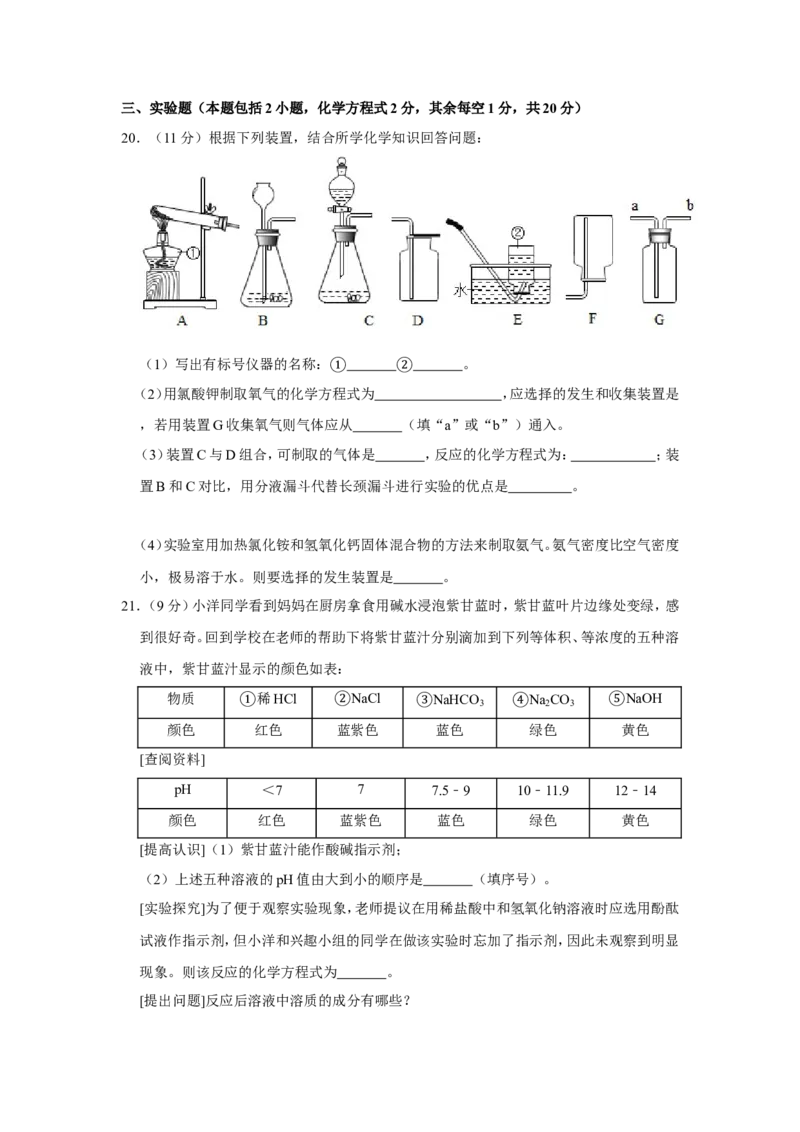
20.(11分)根据下列装置,结合所学化学知识回答问题:
(1)写出有标号仪器的名称: 。
(2)用氯酸钾制取氧气的化学方①程式为 ② ,应选择的发生和收集装置是
,若用装置G收集氧气则气体应从 (填“a”或“b”)通入。
(3)装置C与D组合,可制取的气体是 ,反应的化学方程式为: ;装
置B和C对比,用分液漏斗代替长颈漏斗进行实验的优点是 。
(4)实验室用加热氯化铵和氢氧化钙固体混合物的方法来制取氨气。氨气密度比空气密度
小,极易溶于水。则要选择的发生装置是 。
21.(9分)小洋同学看到妈妈在厨房拿食用碱水浸泡紫甘蓝时,紫甘蓝叶片边缘处变绿,感
到很好奇。回到学校在老师的帮助下将紫甘蓝汁分别滴加到下列等体积、等浓度的五种溶
液中,紫甘蓝汁显示的颜色如表:
物质 稀HCl NaCl NaHCO Na CO NaOH
3 2 3
颜色 ①红色 ②蓝紫色 ③蓝色 ④绿色 ⑤黄色
[查阅资料]
pH <7 7 7.5﹣9 10﹣11.9 12﹣14
颜色 红色 蓝紫色 蓝色 绿色 黄色
[提高认识](1)紫甘蓝汁能作酸碱指示剂;
(2)上述五种溶液的pH值由大到小的顺序是 (填序号)。
[实验探究]为了便于观察实验现象,老师提议在用稀盐酸中和氢氧化钠溶液时应选用酚酞
试液作指示剂,但小洋和兴趣小组的同学在做该实验时忘加了指示剂,因此未观察到明显
现象。则该反应的化学方程式为 。
[提出问题]反应后溶液中溶质的成分有哪些?[问题猜想]猜想一:NaCl 猜想三:NaCl,
猜想二:NaCl,NaOH 猜想四:NaCl,NaOH,HCl
兴趣小组的同学一致认为猜想四不合理,原因是 。
[设计实验]
步骤 现象 结论
方案一 取反应后的溶液于试管中,向其 石蕊溶液变红
中滴加紫色石蕊溶液。
方案二
猜想三成立
(写一种) 。 。
方案三 取反应后的溶液于试管中,向其 产生白色沉淀
中加入适量AgNO 溶液。
3
[讨论交流]上述方案三不可行,原因是 。
[拓展应用]人体胃酸过多时可用 治疗。(化学式)(写一种)
四、计算题(本题共1小题,共4分)
22.(4分)市售的某些银首饰是银、锌合金。小庆同学取该合金样品20g,加入100g稀硫酸恰
好完全反应,产生气体质量与反应时间的关系如图所示,计算:
(1)该合金中锌的质量(精确到0.1g)。
(2)该稀硫酸中溶质的质量分数(精确到0.1%)。