文档内容
2024-2025学年高一下学期4月期中考试化学试题
一、单选题
1.科技发展离不开化学,下列说法错误的是
A.嫦娥五号发射时使用液氢和液氧做推进剂,是利用了燃烧反应提供能量
B.制造5G芯片的材料之一氮化硅属于一种新型陶瓷材料
C.积极推广共享单车以减少雾霾和光化学烟雾
D.“天宫”实验舱太阳能电池采用砷化镓(GaAs)作半导体,砷化镓能将化学能转化为电能
2.下列发明创造不涉及化学反应的是
A.打磨磁石制指南针 B.用胆矾炼铜
C.烧结粘土制陶瓷 D.树皮造纸
3.下列有关化学反应与能量的说法中错误的是
A.“月落乌啼霜满天,江枫渔火对愁眠”,句中涉及的化学变化是放热反应
B.已知石墨转化为金刚石是吸热反应,所以石墨比金刚石稳定
C.化学键断裂和形成时的能量变化是化学反应中能量变化的主要原因
D.化学反应中能量变化的大小与反应物的多少无关
4.下列关于化学物质的用途或性质的叙述正确的是
①氨气极易溶于水,故可用做制冷剂
②单质硫易溶于CS,实验室可用CS 清洗沾有硫单质的试管
2 2
③工业上用氢氟酸溶液腐蚀玻璃生产磨砂玻璃
④常温下浓硝酸可以用铝罐储存,说明铝与浓硝酸不反应
⑤常温下将铜片插入浓硫酸时无明显现象,说明浓硫酸可以使铜钝化
⑥SO 可用做食品添加剂
2
A.①④⑥ B.②③⑥ C.②④⑤ D.①③⑤
5.下列有关化学反应速率的说法正确的是
A.恒温恒容下发生反应2SO (g)+O(g) 2SO (g),充入氦气不改变化学反应速率
2 2 3
B.在金属钠与足量水反应中,增加水的⇌量能加快反应速率
C.用铁片和稀硫酸反应制氢气时,可改用98%的浓硫酸加快生成氢气速率
D.100mL2mol/L的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
6.下列离子方程式正确的是
A.硅酸钠溶液和盐酸反应: +2H+ = H SiO↓
2 3B.硫酸铵溶液和氢氧化钡溶液反应:Ba2++ = BaSO↓
4
C.硝酸与氧化亚铁的反应:FeO+2H+ = Fe2++H O
2
D.向酸性KMnO 溶液中通入SO : =
4 2
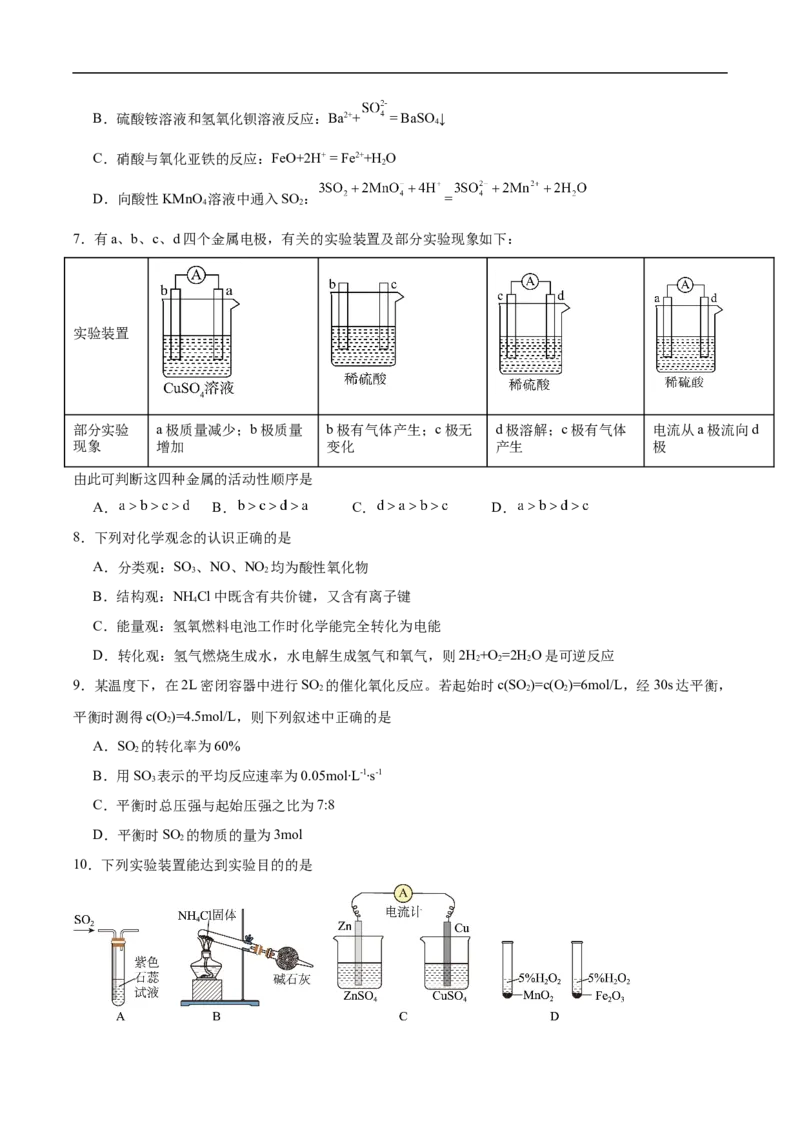
7.有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
实验装置
部分实验 a极质量减少;b极质量 b极有气体产生;c极无 d极溶解;c极有气体 电流从a极流向d
现象 增加 变化 产生 极
由此可判断这四种金属的活动性顺序是
A. B. C. D.
8.下列对化学观念的认识正确的是
A.分类观:SO 、NO、NO 均为酸性氧化物
3 2
B.结构观:NH Cl中既含有共价键,又含有离子键
4
C.能量观:氢氧燃料电池工作时化学能完全转化为电能
D.转化观:氢气燃烧生成水,水电解生成氢气和氧气,则2H+O =2H O是可逆反应
2 2 2
9.某温度下,在2L密闭容器中进行SO 的催化氧化反应。若起始时c(SO )=c(O )=6mol/L,经30s达平衡,
2 2 2
平衡时测得c(O)=4.5mol/L,则下列叙述中正确的是
2
A.SO 的转化率为60%
2
B.用SO 表示的平均反应速率为0.05mol∙L-1∙s-1
3
C.平衡时总压强与起始压强之比为7:8
D.平衡时SO 的物质的量为3mol
2
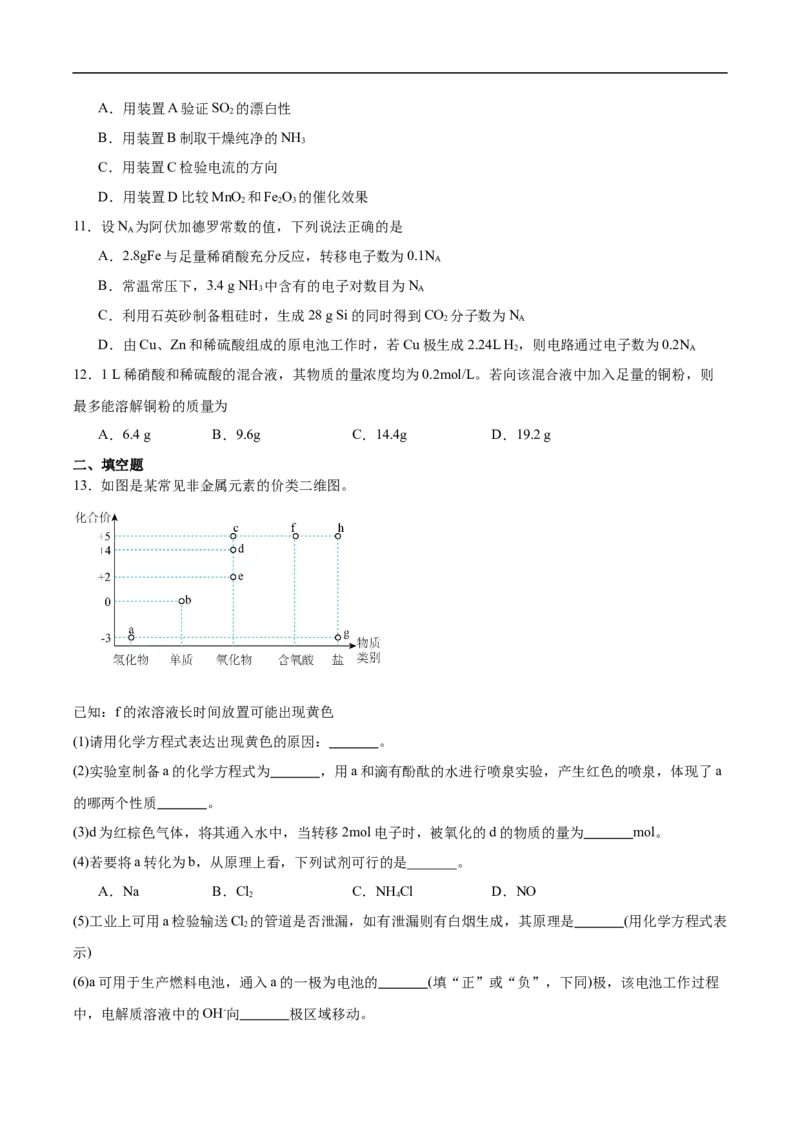
10.下列实验装置能达到实验目的的是A.用装置A验证SO 的漂白性
2
B.用装置B制取干燥纯净的NH
3
C.用装置C检验电流的方向
D.用装置D比较MnO 和Fe O 的催化效果
2 2 3
11.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.2.8gFe与足量稀硝酸充分反应,转移电子数为0.1N
A
B.常温常压下,3.4 g NH 中含有的电子对数目为N
3 A
C.利用石英砂制备粗硅时,生成28 g Si的同时得到CO 分子数为N
2 A
D.由Cu、Zn和稀硫酸组成的原电池工作时,若Cu极生成2.24L H ,则电路通过电子数为0.2N
2 A
12.1 L稀硝酸和稀硫酸的混合液,其物质的量浓度均为0.2mol/L。若向该混合液中加入足量的铜粉,则
最多能溶解铜粉的质量为
A.6.4 g B.9.6g C.14.4g D.19.2 g
二、填空题
13.如图是某常见非金属元素的价类二维图。
已知:f的浓溶液长时间放置可能出现黄色
(1)请用化学方程式表达出现黄色的原因: 。
(2)实验室制备a的化学方程式为 ,用a和滴有酚酞的水进行喷泉实验,产生红色的喷泉,体现了a
的哪两个性质 。
(3)d为红棕色气体,将其通入水中,当转移2mol电子时,被氧化的d的物质的量为 mol。
(4)若要将a转化为b,从原理上看,下列试剂可行的是_______。
A.Na B.Cl C.NH Cl D.NO
2 4
(5)工业上可用a检验输送Cl 的管道是否泄漏,如有泄漏则有白烟生成,其原理是 (用化学方程式表
2
示)
(6)a可用于生产燃料电池,通入a的一极为电池的 (填“正”或“负”,下同)极,该电池工作过程
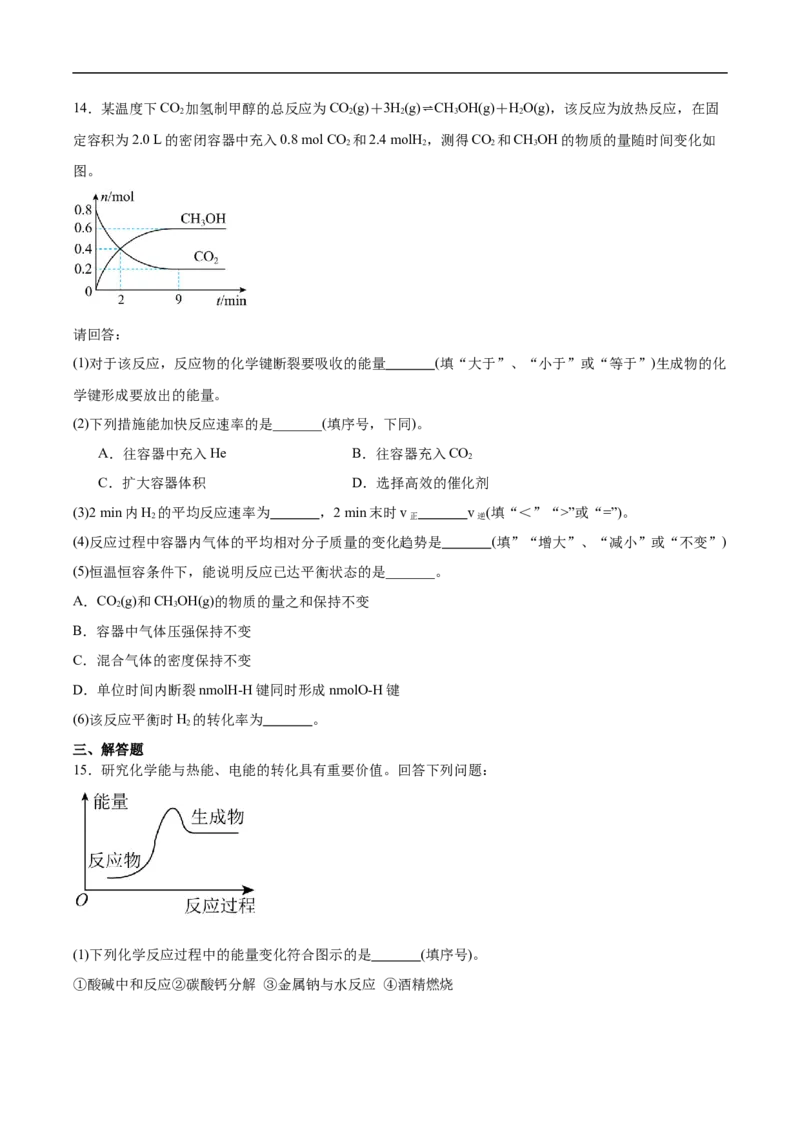
中,电解质溶液中的OH-向 极区域移动。14.某温度下CO
2
加氢制甲醇的总反应为CO
2
(g)+3H
2
(g)⇌CH
3
OH(g)+H
2
O(g),该反应为放热反应,在固
定容积为2.0 L的密闭容器中充入0.8 mol CO 和2.4 molH ,测得CO 和CHOH的物质的量随时间变化如
2 2 2 3
图。
请回答:
(1)对于该反应,反应物的化学键断裂要吸收的能量 (填“大于”、“小于”或“等于”)生成物的化
学键形成要放出的能量。
(2)下列措施能加快反应速率的是_______(填序号,下同)。
A.往容器中充入He B.往容器充入CO
2
C.扩大容器体积 D.选择高效的催化剂
(3)2 min内H 的平均反应速率为 ,2 min末时v v (填“<”“>”或“=”)。
2 正 逆
(4)反应过程中容器内气体的平均相对分子质量的变化趋势是 (填”“增大”、“减小”或“不变”)
(5)恒温恒容条件下,能说明反应已达平衡状态的是_______。
A.CO(g)和CHOH(g)的物质的量之和保持不变
2 3
B.容器中气体压强保持不变
C.混合气体的密度保持不变
D.单位时间内断裂nmolH-H键同时形成nmolO-H键
(6)该反应平衡时H 的转化率为 。
2
三、解答题
15.研究化学能与热能、电能的转化具有重要价值。回答下列问题:
(1)下列化学反应过程中的能量变化符合图示的是 (填序号)。
①酸碱中和反应②碳酸钙分解 ③金属钠与水反应 ④酒精燃烧⑤灼热的碳与二氧化碳反应 ⑥ 与 反应
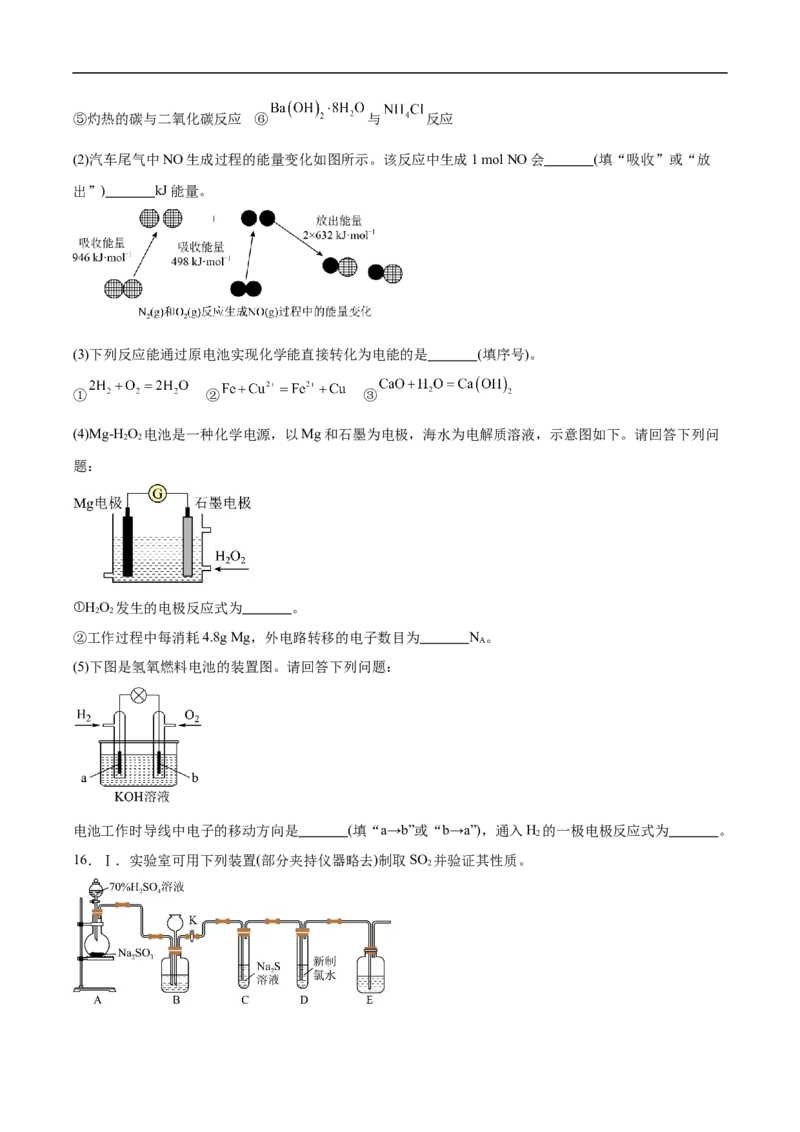
(2)汽车尾气中NO生成过程的能量变化如图所示。该反应中生成1 mol NO会 (填“吸收”或“放
出”) kJ能量。
(3)下列反应能通过原电池实现化学能直接转化为电能的是 (填序号)。
① ② ③
(4)Mg-H O 电池是一种化学电源,以Mg和石墨为电极,海水为电解质溶液,示意图如下。请回答下列问
2 2
题:
①HO 发生的电极反应式为 。
2 2
②工作过程中每消耗4.8g Mg,外电路转移的电子数目为 N 。
A
(5)下图是氢氧燃料电池的装置图。请回答下列问题:
电池工作时导线中电子的移动方向是 (填“a→b”或“b→a”),通入H 的一极电极反应式为 。
2
16.Ⅰ.实验室可用下列装置(部分夹持仪器略去)制取SO 并验证其性质。
2(1)B装置的作用之一是防堵塞,则B中盛放的试剂为 。
(2)实验时,通气一段时间后,C试管中出现大量淡黄色浑浊现象,证明二氧化硫具有 (填“还原
性”、“氧化性”或“漂白性”)。
(3)试管D中反应的离子方程式为 。
Ⅱ.探究外界条件对反应速率的影响
【实验原理】反应:NaSO+H SO =Na SO +SO↑+S↓+H O,反应过程中溶液出现乳白色浑浊和有刺激性
2 2 3 2 4 2 4 2 2
气味的气体。
【实验用品】0.1mol/LNa SO 溶液、0.1mol/LH SO 溶液、蒸馏水。
2 2 3 2 4
试管、烧杯、量筒、胶头滴管等。
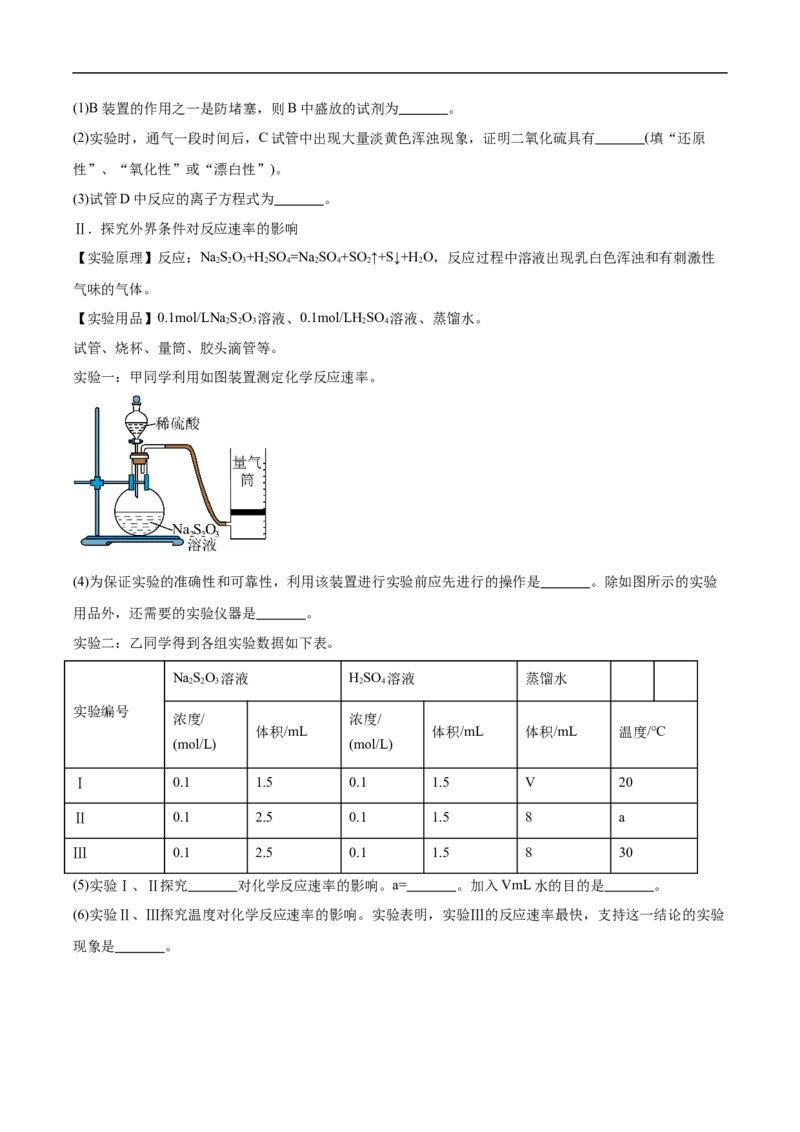
实验一:甲同学利用如图装置测定化学反应速率。
(4)为保证实验的准确性和可靠性,利用该装置进行实验前应先进行的操作是 。除如图所示的实验
用品外,还需要的实验仪器是 。
实验二:乙同学得到各组实验数据如下表。
NaSO 溶液 HSO 溶液 蒸馏水
2 2 3 2 4
实验编号
浓度/ 浓度/
体积/mL 体积/mL 体积/mL 温度/℃
(mol/L) (mol/L)
Ⅰ 0.1 1.5 0.1 1.5 V 20
Ⅱ 0.1 2.5 0.1 1.5 8 a
Ⅲ 0.1 2.5 0.1 1.5 8 30
(5)实验Ⅰ、Ⅱ探究 对化学反应速率的影响。a= 。加入VmL水的目的是 。
(6)实验Ⅱ、Ⅲ探究温度对化学反应速率的影响。实验表明,实验Ⅲ的反应速率最快,支持这一结论的实验
现象是 。题号 1 2 3 4 5 6 7 8 9 10
答案 D A D B A A C B C D
题号 11 12
答案 B C
13.(1)4HNO 4NO ↑+O↑+2HO
3 2 2 2
(2) Ca(OH) + 2NH Cl CaCl + 2NH ↑ + 2H O 极易溶于水,水溶液显碱性
2 4 2 3 2
(3)2
(4)BD
(5)3Cl +8NH=N +6NHCl
2 3 2 4
(6) 负 负
【详解】(1)硝酸分解生成的NO ,溶解在硝酸中使得溶液呈黄色,分解反应为4HNO 4NO ↑+
2 3 2
O↑+2HO;
2 2
(2)实验室利用Ca(OH) 和NH Cl共热制备氨气,反应的方程式为Ca(OH) + 2NH Cl CaCl + 2NH ↑ +
2 4 2 4 2 3
2HO;氨气产生红色喷泉实验,利用了氨气极易溶于水,且水溶液显碱性的性质;
2
(3)NO 溶解在水中的反应为 ,由此可知当转移2mol电子时,被氧化的NO
2 2
的物质的量为2mol;
(4)氨气转化为氮气,需要加入氧化剂,从元素价态分析可知,符合题意的有Cl、NO;
2
(5)氯气与氨气生成NH Cl固体小颗粒,可观察到产生白烟,相关的反应方程式为
4
3Cl+8NH=N +6NHCl;
2 3 2 4
(6)从元素价态分析可知,NH 应通入负极,发生氧化反应;原电池中,阴离子向负极定向移动。
3
14.(1)小于
(2)BD
(3) 0.3 mol/(L·min) >
(4)增大
(5)BD
(6)75%【详解】(1)反应物断键吸收的能量小于生成物形成键放出的能量时反应为放热,答案为小于;
(2)A.容器中充入He不改变反应体系各物质的浓度反应速率不变,A错误;
B.充入CO,反应物浓度增大速率加快,B正确;
2
C.增大容器体积,反应体系各物质浓度减小反应速率减慢,C错误;
D.催化剂能加快反应速率,D正确;
故选BD;
(3)从图看CHOH物质的量由0增加到0.4mol即 ,v(CHOH)=
3 3
;v(H )=3v(CH OH)= 0.3 mol/(L·min);由图可知,2 min末时甲醇在增加,
2 3
二氧化碳在减小,则此时反应正向进行,故v > v ;
正 逆
(4)该反应过程中,气体总质量不变,气体总分子数减小,则反应过程中容器内气体的平均相对分子质
量= ,则其变化趋势是增大;
(5)A.根据碳守恒可知,反应过程中,CO(g)和CHOH(g)的物质的量之和保持不变,则当其不变时,
2 3
不能证明反应达到平衡,A错误;
B.随着反应进行,体系中气体减少,恒容下压强降低,平衡时压强不变可判断平衡,B正确;
C.气体质量守恒,恒容所以反应中密度一直不发变化,密度不变无法判断平衡,C错误;
D.该反应中,氢气是反应物,甲醇和水是产物,则单位时间内断裂nmolH-H键同时形成nmolO-H键,说
明正、逆反应速率相等,反应平衡,D正确;
故选BD;
(6)在反应开始时n(CO)=0.8 mol,反应达到平衡时n(CO)=0.2 mol,则该反应平衡时CO 的转化率
2 2 2
=75%。
15.(1)②⑤⑥
(2) 吸收 90
(3)①②
(4) H O +2e- =2OH- 0.4
2 2
(5) a→b H -2e- +2OH-= 2H O
2 2
【详解】(1)由图可知,反应物的总能量低于生成物的总能量,反应吸热;而②碳酸钙的分解、⑤灼热的碳与二氧化碳反应、⑥ 与 反应都是吸热反应,故选②⑤⑥;
(2)由能量变化可知,1mol N 和1mol O 反应生成2mol NO,断键需要吸收的总能量为
2 2
,成键释放出的总能量为 ,故生成1mol NO
会吸收 的能量;
(3)原电池发生的是氧化还原反应,其中反应①②涉及元素化合价变化,为氧化还原反应;
(4)①依题可知Mg为负极,HO 通入正极发生还原反应,海水呈弱碱性,故电极反应式为HO +2e-
2 2 2 2
=2OH-;
②根据得失电子情况,存在如下计量关系:Mg~2e-,故当消耗4.8g Mg时,转移的电子数为
;
(5)对于氢氧燃料电池,H 通入负极,故a为负极,b为正极;原电池外电路的电子由负极经导线流向正
2
极,即a→b;H 在负极发生氧化反应,电极反应为H -2e- +2OH-= 2H O。
2 2 2
16.(1)饱和亚硫酸氢钠(NaHSO)溶液
3
(2)氧化性
(3)Cl +SO +2HO=4H++2Cl-+
2 2 2
(4) 检查装置的气密性 计时器(或秒表)
(5) Na SO 溶液浓度 20 控制硫酸的起始浓度相同
2 2 3
(6)实验III观察到出现浑浊的时间更短
【详解】(1)由分析可知,装置B可用于储存少量的SO 气体,或作安全瓶即B装置的作用之一是防堵
2
塞,则B中盛放的试剂不能溶解二氧化硫,其中试剂为饱和亚硫酸氢钠(NaHSO)溶液;
3
(2)实验时,通气一段时间后,C中试管中出现大量淡黄色浑浊现象,说明SO 与NaS反应生成S等,
2 2
从而证明二氧化硫具有氧化性;
(3)试管D中二氧化硫和氯气反应生成盐酸和硫酸,离子方程式为:Cl+SO +2HO=4H++2Cl-+
2 2 2
;
(4)气体制备或性质探究实验,本实验是探究化学反应速率的影响因素,需保证气密性良好,否则会影
响实验结果,故实验前需要检验装置的气密性。反应速率的计算公式v= ,测反应速率是在一定时间段内,故还需要秒表,故答案为:检查装置的气密性;计时器(或秒表);
(5)实验Ⅰ、Ⅱ硫酸用量不变,NaSO 溶液用量不同,则实验Ⅰ、Ⅱ探究NaSO 溶液浓度对化学反应
2 2 3 2 2 3
速率的影响;实验I、II硫酸用量不变,所以控制总体积不变,加入VmL水的目的是保证硫酸浓度不变,
另外还需要控制温度不变,则a=20;故答案为:NaSO 溶液的浓度;20;控制硫酸的起始浓度相同;
2 2 3
(6)探究实验II、III改变的是温度条件,其他条件不变时,升高反应温度,化学反应速率增大,因为反
应中有S沉淀生成,故可以测定溶液变浑浊的快慢,故答案为:实验III观察到出现浑浊的时间更短。