文档内容
最新更新~初中高中考试真题/模拟 ~微信: vzan8899
2017 年江苏省南京市中考化学试卷
一、选择题(每小题2分,每小题只有一个选项符合题意)
1.(2分)地壳中含量最多的元素是( )
A.氧 B.硅 C.铝 D.钙
2.(2分)物质的下列性质中,属于化学性质的是( )
A.颜色B.状态 C.熔点D.氧化性
3.(2分)下列图标中表示禁止吸烟的是( )
A. B. C. D.
4.(2分)下列金属中,金属活动性最弱的是( )
A.金 B.银 C.铜 D.铁
5.(2分)能用酒精灯直接加热的仪器是( )
A.漏斗B.量筒 C.试管D.烧杯
6.(2分)我国科技创新成果卓越,下列成果中获得诺贝尔奖的是( )
A.侯德榜发明联合制碱法
B.屠呦呦发现抗疟新药青蒿素
C.闵恩泽研发石油炼制催化剂
D.张青莲主持测定了几种元素相对原子质量的新值
7.(2分)下列物质由分子构成的是( )
A.锌 B.硫酸铜 C.C D.金刚石
60
8.(2分)下列行为会增加空气中PM2.5的是( )
A.治理工地扬尘 B.露天焚烧垃圾
C.使用公共自行车D.禁止焚烧秸杆
9.(2分)下列关于干冰升华过程的说法正确的是( )
A.二氧化碳分子的体积变大B.二氧化碳分子的质量变小
C.二氧化碳分子的种类改变D.二氧化碳分子间的间隔变大
1 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
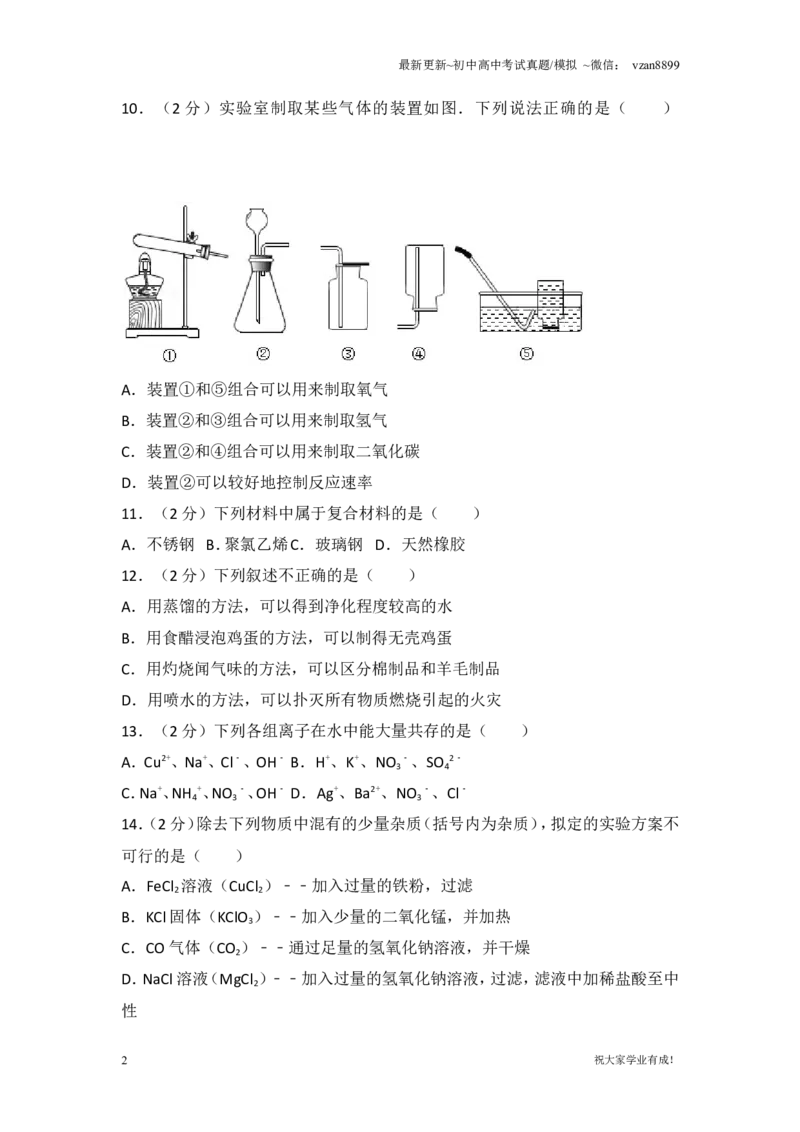
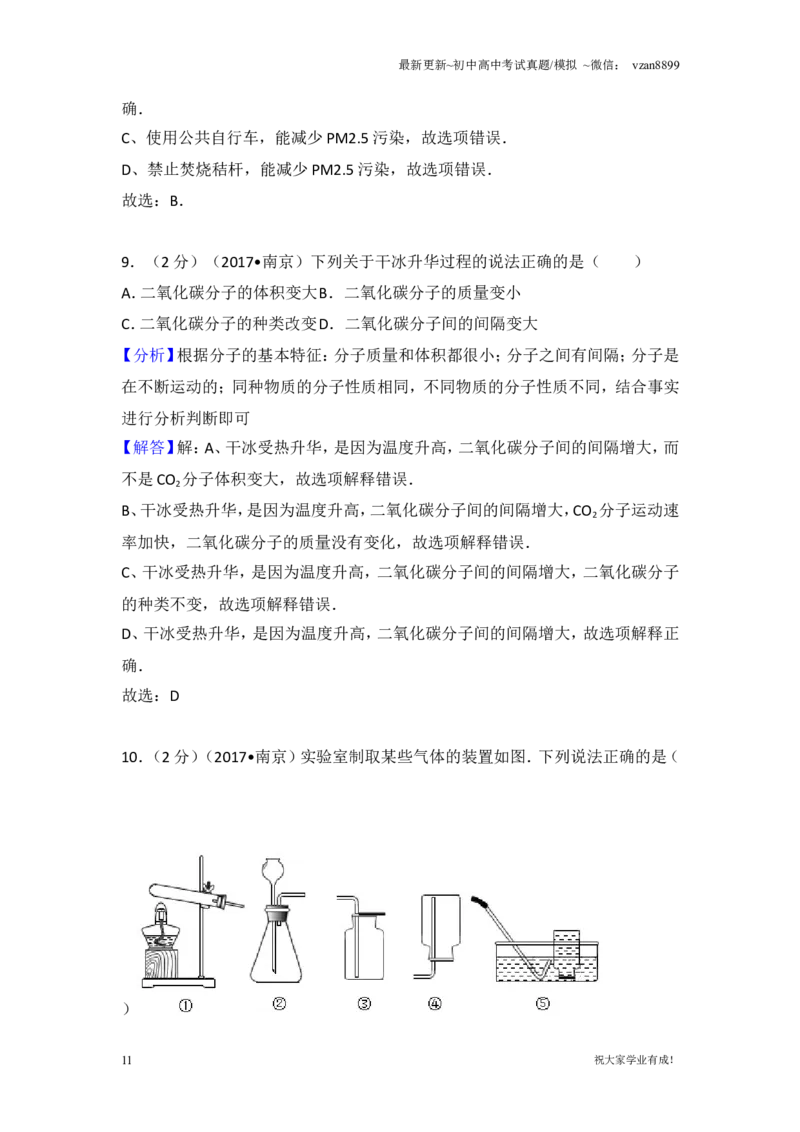
10.(2 分)实验室制取某些气体的装置如图.下列说法正确的是( )
A.装置①和⑤组合可以用来制取氧气
B.装置②和③组合可以用来制取氢气
C.装置②和④组合可以用来制取二氧化碳
D.装置②可以较好地控制反应速率
11.(2分)下列材料中属于复合材料的是( )
A.不锈钢 B.聚氯乙烯C.玻璃钢 D.天然橡胶
12.(2分)下列叙述不正确的是( )
A.用蒸馏的方法,可以得到净化程度较高的水
B.用食醋浸泡鸡蛋的方法,可以制得无壳鸡蛋
C.用灼烧闻气味的方法,可以区分棉制品和羊毛制品
D.用喷水的方法,可以扑灭所有物质燃烧引起的火灾
13.(2分)下列各组离子在水中能大量共存的是( )
A.Cu2+、Na+、Cl﹣、OH﹣ B.H+、K+、NO ﹣、SO 2﹣
3 4
C.Na+、NH +、NO ﹣、OH﹣ D.Ag+、Ba2+、NO ﹣、Cl﹣
4 3 3
14.(2分)除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案不
可行的是( )
A.FeCl 溶液(CuCl )﹣﹣加入过量的铁粉,过滤
2 2
B.KCl固体(KClO )﹣﹣加入少量的二氧化锰,并加热
3
C.CO气体(CO )﹣﹣通过足量的氢氧化钠溶液,并干燥
2
D.NaCl溶液(MgCl )﹣﹣加入过量的氢氧化钠溶液,过滤,滤液中加稀盐酸至中
2
性
2 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
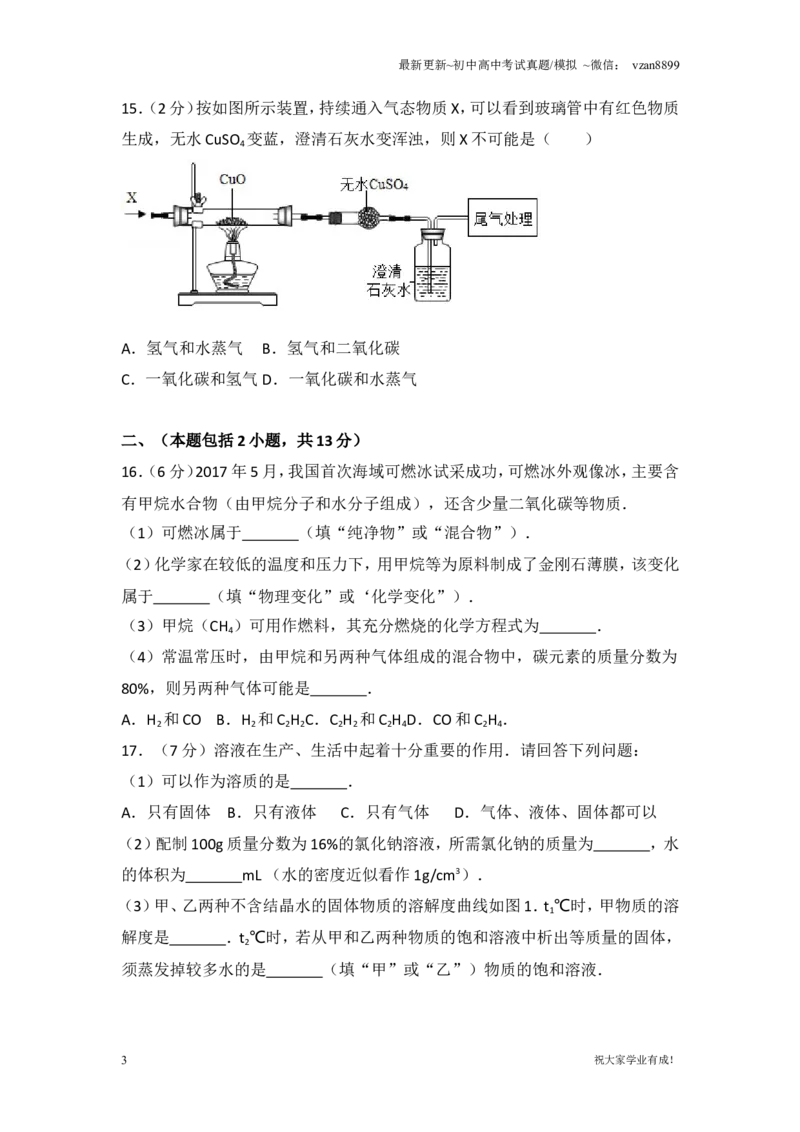
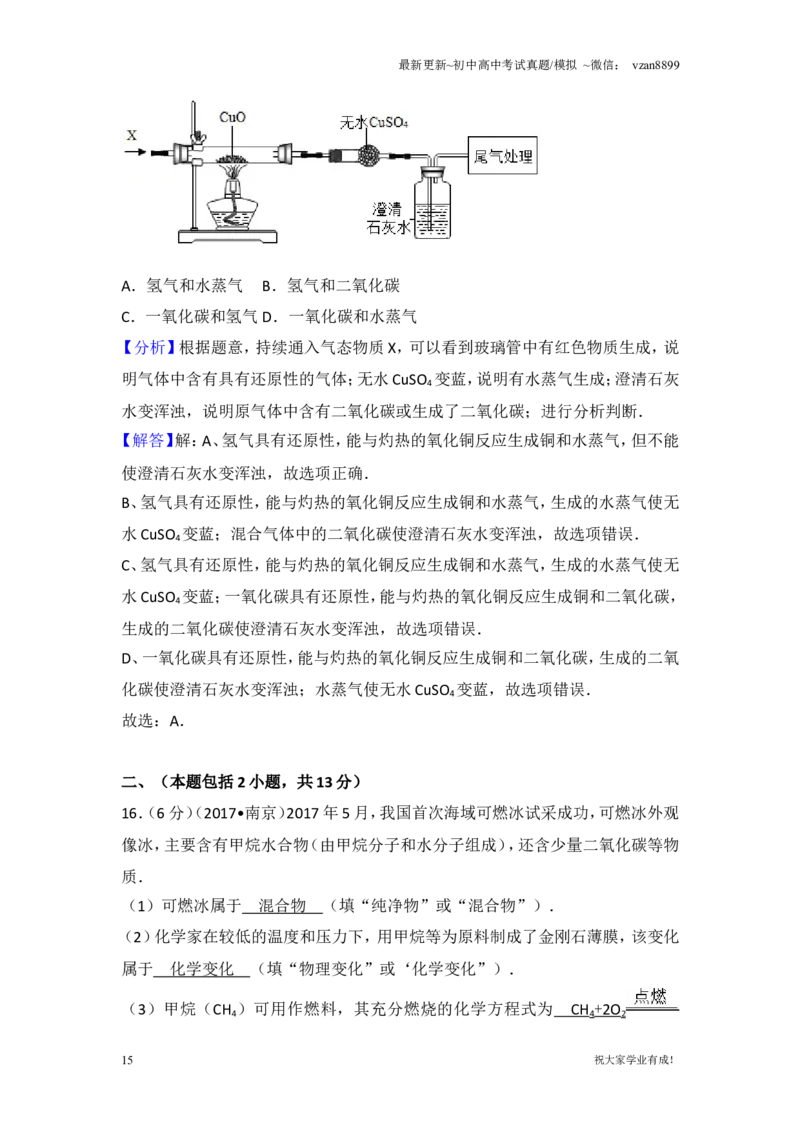
15.(2分)按如图所示装置,持续通入气态物质X,可以看到玻璃管中有红色物质
生成,无水CuSO 变蓝,澄清石灰水变浑浊,则X不可能是( )
4
A.氢气和水蒸气 B.氢气和二氧化碳
C.一氧化碳和氢气D.一氧化碳和水蒸气
二、(本题包括2小题,共13分)
16.(6分)2017年5月,我国首次海域可燃冰试采成功,可燃冰外观像冰,主要含
有甲烷水合物(由甲烷分子和水分子组成),还含少量二氧化碳等物质.
(1)可燃冰属于 (填“纯净物”或“混合物”).
(2)化学家在较低的温度和压力下,用甲烷等为原料制成了金刚石薄膜,该变化
属于 (填“物理变化”或‘化学变化”).
(3)甲烷(CH )可用作燃料,其充分燃烧的化学方程式为 .
4
(4)常温常压时,由甲烷和另两种气体组成的混合物中,碳元素的质量分数为
80%,则另两种气体可能是 .
A.H 和CO B.H 和C H C.C H 和C H D.CO和C H .
2 2 2 2 2 2 2 4 2 4
17.(7分)溶液在生产、生活中起着十分重要的作用.请回答下列问题:
(1)可以作为溶质的是 .
A.只有固体 B.只有液体 C.只有气体 D.气体、液体、固体都可以
(2)配制100g质量分数为16%的氯化钠溶液,所需氯化钠的质量为 ,水
的体积为 mL (水的密度近似看作1g/cm3).
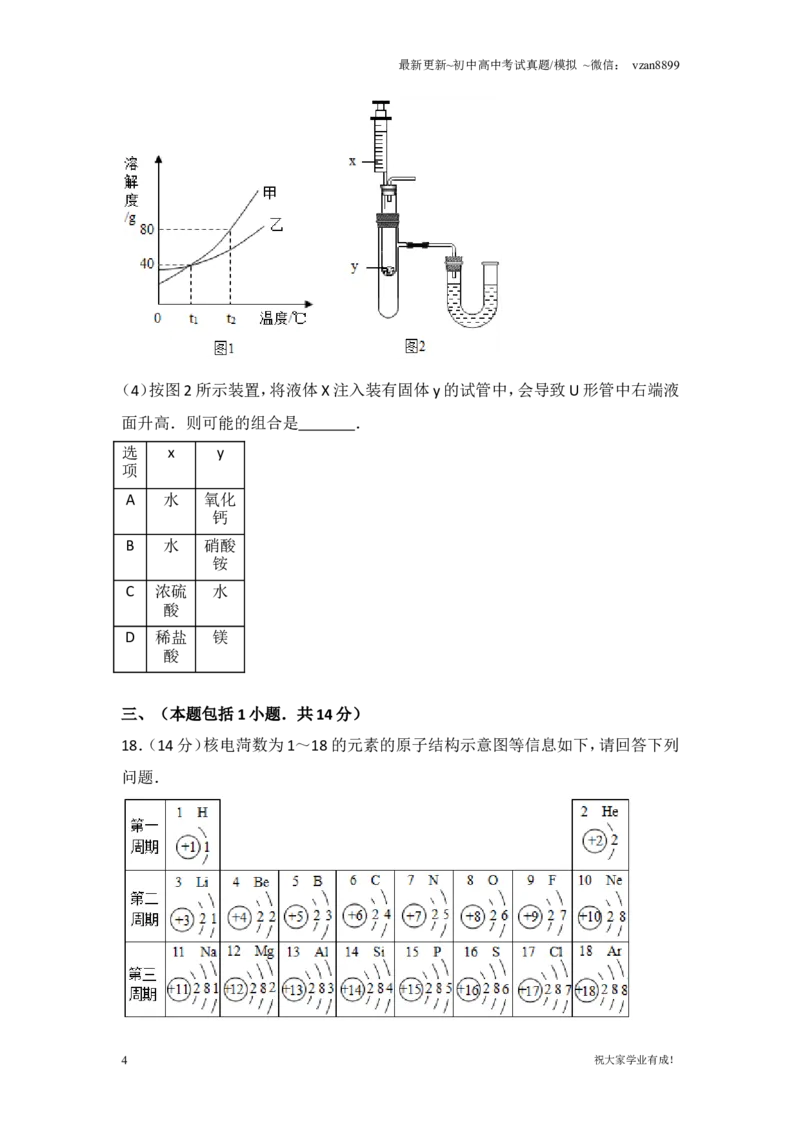
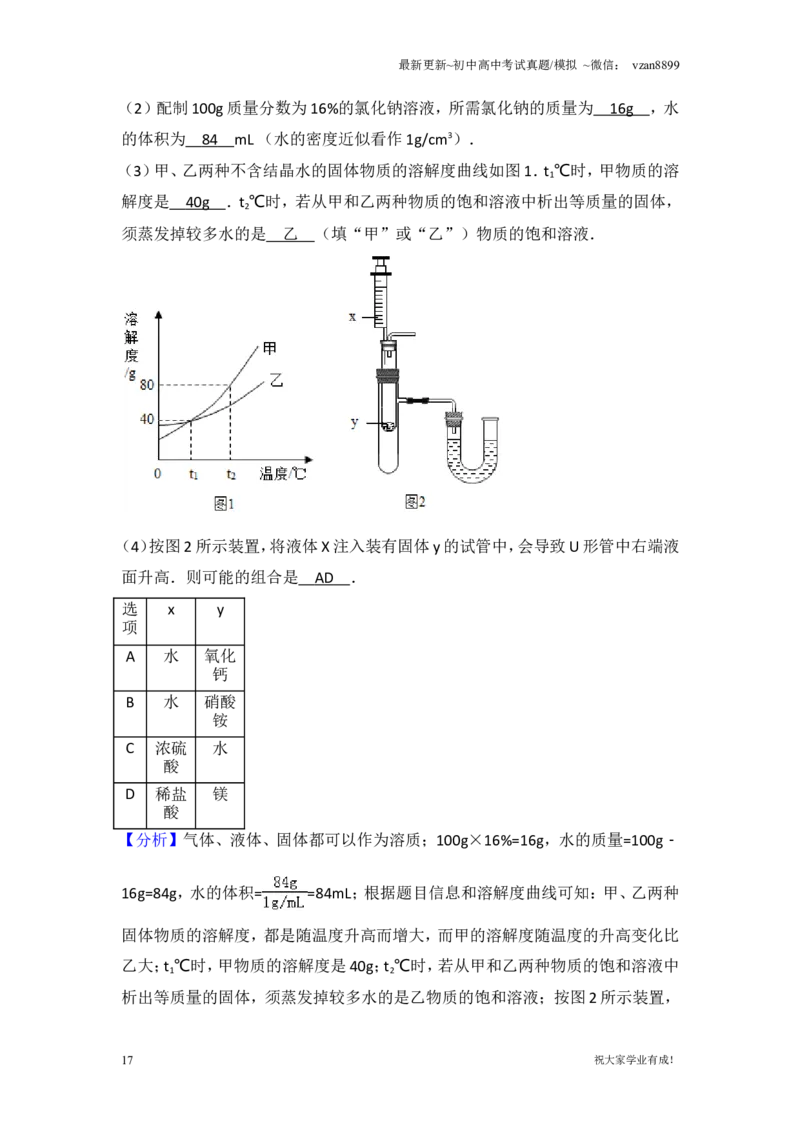
(3)甲、乙两种不含结晶水的固体物质的溶解度曲线如图1.t ℃时,甲物质的溶
1
解度是 .t ℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,
2
须蒸发掉较多水的是 (填“甲”或“乙”)物质的饱和溶液.
3 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
(4)按图2所示装置,将液体X注入装有固体y的试管中,会导致U形管中右端液
面升高.则可能的组合是 .
选 x y
项
A 水 氧化
钙
B 水 硝酸
铵
C 浓硫 水
酸
D 稀盐 镁
酸
三、(本题包括1小题.共14分)
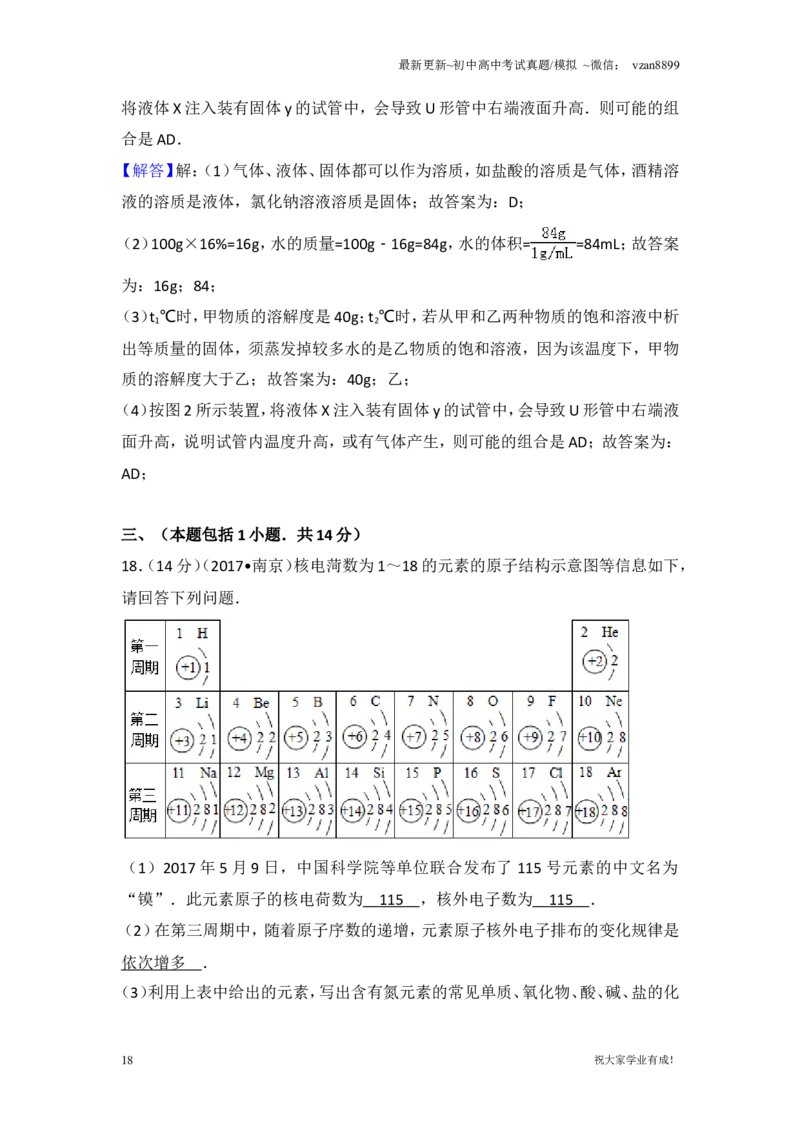
18.(14分)核电菏数为1~18的元素的原子结构示意图等信息如下,请回答下列
问题.
4 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
(1)2017年5月9日,中国科学院等单位联合发布了 115号元素的中文名为
“镆”.此元素原子的核电荷数为 ,核外电子数为 .
(2)在第三周期中,随着原子序数的递增,元素原子核外电子排布的变化规律是
.
(3)利用上表中给出的元素,写出含有氮元素的常见单质、氧化物、酸、碱、盐的化
学式各一个,并标出所写化学式中氮元素的化合价:单质 、氧化物
、酸 、碱 、盐 .
(4)以钠和氯为例,简述结构与性质的关系. .
(5)国产C919大型客机上使用了大量的铝合金.工业上用电解氧化铝(Al O )得
2 3
到铝和氧气、试计算电解102t氧化铝最多能生成铝的质量是多少?(写出计算过
程)
四、(本题包括2小题,共12分)
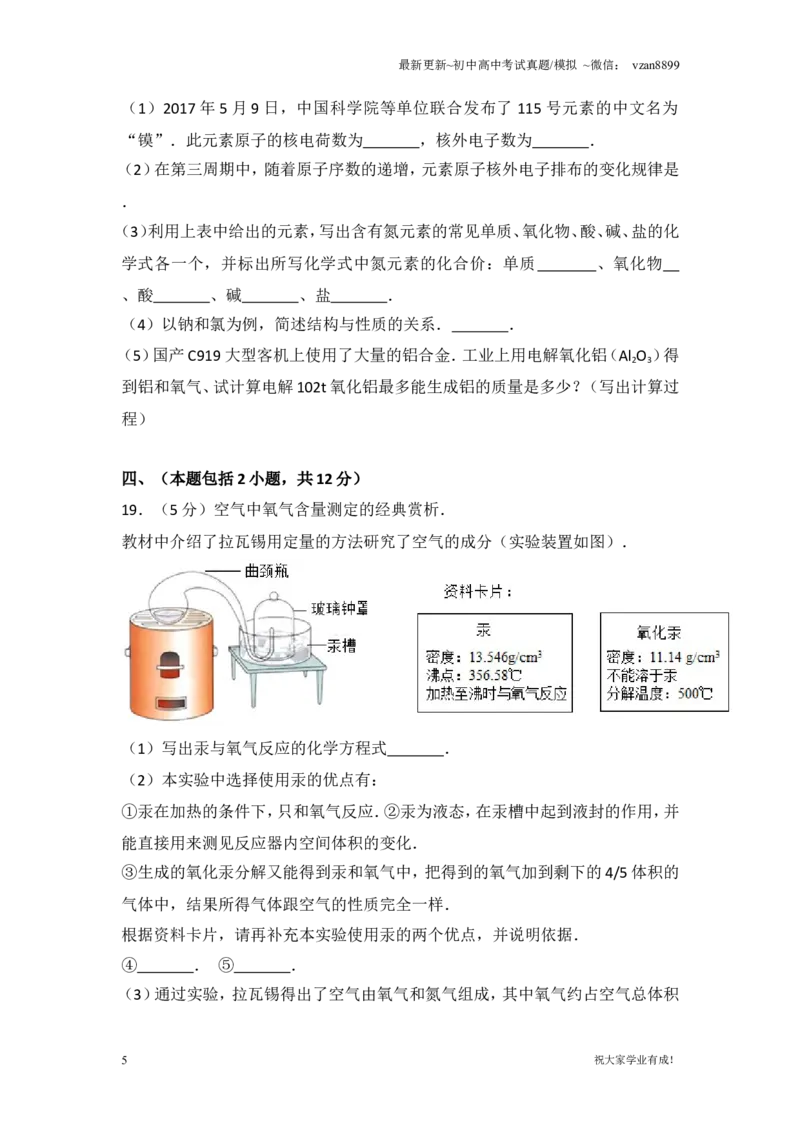
19.(5分)空气中氧气含量测定的经典赏析.
教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图).
(1)写出汞与氧气反应的化学方程式 .
(2)本实验中选择使用汞的优点有:
①汞在加热的条件下,只和氧气反应.②汞为液态,在汞槽中起到液封的作用,并
能直接用来测见反应器内空间体积的变化.
③生成的氧化汞分解又能得到汞和氧气中,把得到的氧气加到剩下的4/5体积的
气体中,结果所得气体跟空气的性质完全一样.
根据资料卡片,请再补充本实验使用汞的两个优点,并说明依据.
④ . ⑤ .
(3)通过实验,拉瓦锡得出了空气由氧气和氮气组成,其中氧气约占空气总体积
5 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
1/5的结论.请根据现在的认识,对此结论予以补充. .
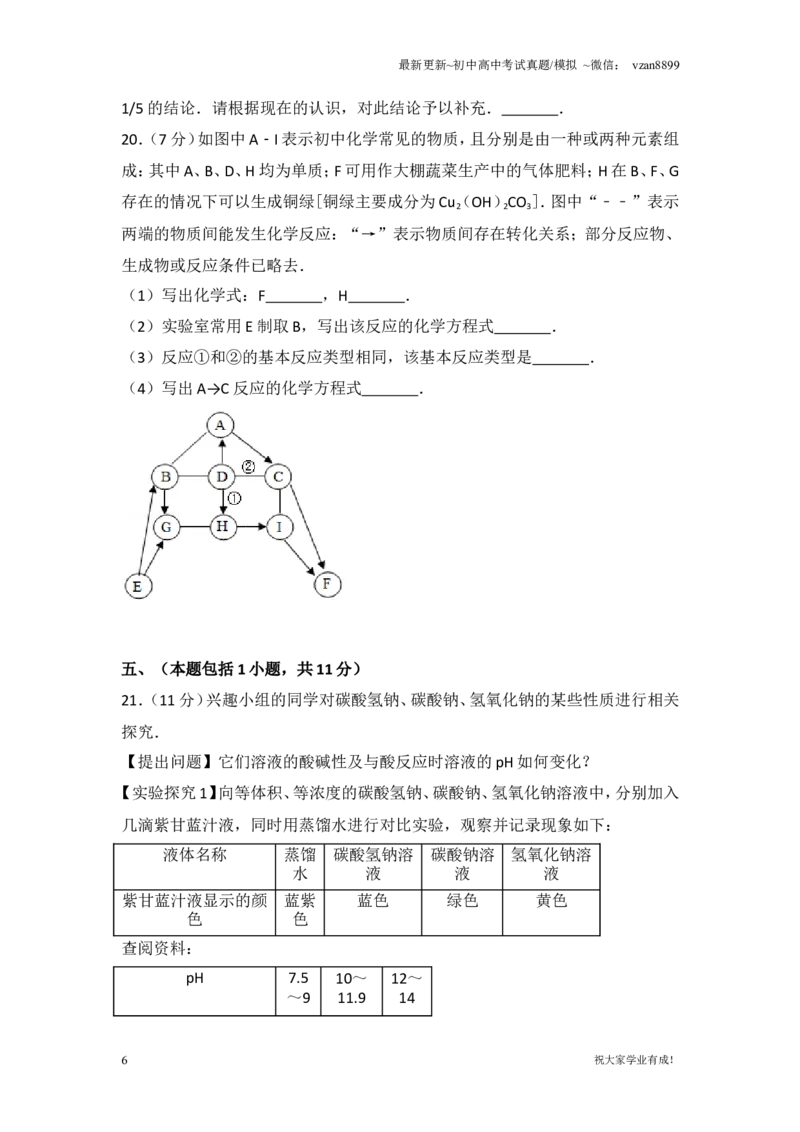
20.(7分)如图中A﹣I表示初中化学常见的物质,且分别是由一种或两种元素组
成:其中A、B、D、H均为单质;F可用作大棚蔬菜生产中的气体肥料;H在B、F、G
存在的情况下可以生成铜绿[铜绿主要成分为Cu(OH)CO ].图中“﹣﹣”表示
2 2 3
两端的物质间能发生化学反应:“→”表示物质间存在转化关系;部分反应物、
生成物或反应条件已略去.
(1)写出化学式:F ,H .
(2)实验室常用E制取B,写出该反应的化学方程式 .
(3)反应①和②的基本反应类型相同,该基本反应类型是 .
(4)写出A→C反应的化学方程式 .
五、(本题包括1小题,共11分)
21.(11分)兴趣小组的同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质进行相关
探究.
【提出问题】它们溶液的酸碱性及与酸反应时溶液的pH如何变化?
【实验探究1】向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入
几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
液体名称 蒸馏 碳酸氢钠溶 碳酸钠溶 氢氧化钠溶
水 液 液 液
紫甘蓝汁液显示的颜 蓝紫 蓝色 绿色 黄色
色 色
查阅资料:
pH 7.5 10~ 12~
~9 11.9 14
6 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
紫甘蓝汁液显示的颜 蓝 绿色 黄色
色 色
【得出结论1】三种溶液的碱性由强到弱的顺序为 .
【实验探究2】甲同学在烧杯溶液中加入约5mL稀氢氧化钠溶液,滴入几滴酚酞溶
液,此时溶液由 色变为 色.向其中加入稀盐酸,该反应的化学方
程式为 .
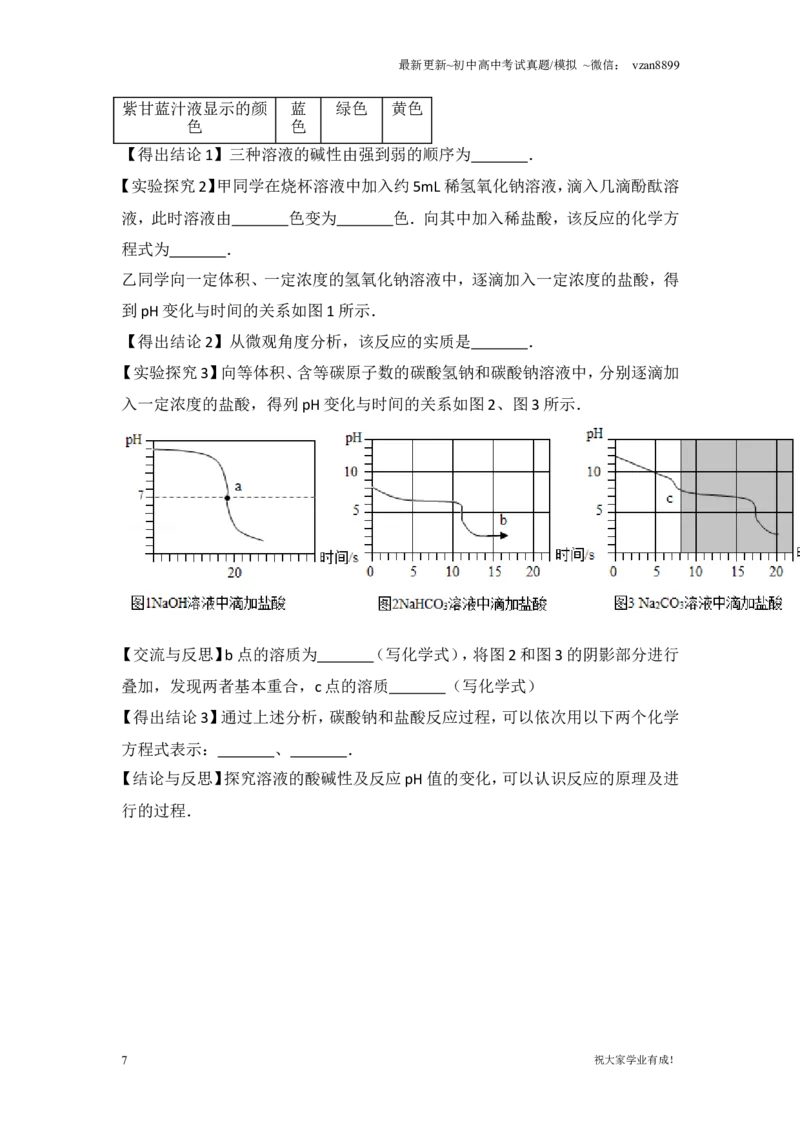
乙同学向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,得
到pH变化与时间的关系如图1所示.
【得出结论2】从微观角度分析,该反应的实质是 .
【实验探究3】向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加
入一定浓度的盐酸,得列pH变化与时间的关系如图2、图3所示.
【交流与反思】b点的溶质为 (写化学式),将图2和图3的阴影部分进行
叠加,发现两者基本重合,c点的溶质 (写化学式)
【得出结论3】通过上述分析,碳酸钠和盐酸反应过程,可以依次用以下两个化学
方程式表示: 、 .
【结论与反思】探究溶液的酸碱性及反应pH值的变化,可以认识反应的原理及进
行的过程.
7 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
2017 年江苏省南京市中考化学试卷
参考答案与试题解析
一、选择题(每小题2分,每小题只有一个选项符合题意)
1.(2分)(2017•南京)地壳中含量最多的元素是( )
A.氧 B.硅 C.铝 D.钙
【分析】利用识记知识,结合地壳中元素的含有情况的比例进行判断解决即可.
【解答】解:根据记忆可知在地壳中元素含量排在前四位的元素是:氧、硅、铝、铁;
故选A.
2.(2分)(2017•南京)物质的下列性质中,属于化学性质的是( )
A.颜色B.状态 C.熔点D.氧化性
【分析】物理性质是指物质不需要发生化学变化就表现出来的性质.包括物质的
颜色、状态、气味、熔点、沸点、硬度、密度等性质;化学性质是指物质在化学变化
中表现出来的性质.化学性质包括可燃性、氧化性、还原性、毒性、稳定性等.
【解答】解:A、颜色不需要发生化学变化就表现出来,属于物理性质,故A错;
B、状态不需要发生化学变化就表现出来,属于物理性质,故B错;
C、熔点不需要发生化学变化就表现出来,属于物理性质,故C错;
D、氧化性需要通过化学变化表现出来,属于化学性质,故D正确.
故选D.
3.(2分)(2017•南京)下列图标中表示禁止吸烟的是( )
A. B. C. D.
【分析】根据已有的图标的意义进行分析解答即可.
【解答】解:A.表示的是禁止烟火;
8 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
B.表示的是禁止携带火种;
C.表示的是禁止燃放鞭炮;
D.表示的是禁止吸烟.
故选D.
4.(2分)(2017•南京)下列金属中,金属活动性最弱的是( )
A.金 B.银 C.铜 D.铁
【分析】根据金属活动性顺序:K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、
Pt、Au,则可知答案.
【解答】解:根据金属活动性顺序:K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、
Ag、Pt、Au,则可知金属活动性大小为:铁>铜>银>金,所以金属活动性最弱的
是金.
故选A.
5.(2分)(2017•南京)能用酒精灯直接加热的仪器是( )
A.漏斗B.量筒 C.试管D.烧杯
【分析】通过我们学过的知识可知,能够直接加热的仪器有:试管、燃烧匙、蒸发皿
和坩埚等;需要垫石棉网的是:烧杯、烧瓶、锥形瓶等;不能加热的仪器有:漏斗、
量筒、集气瓶等.
【解答】解:A、漏斗不能直接在酒精灯火焰上加热,故选项错误.
B、量筒不能用作药品反应,也不能加热,故选项错误.
C、试管能直接在酒精灯火焰上加热,故选项正确.
D、烧杯热需垫石棉网,不能直接在酒精灯火焰上加热,故选项错误.
故选C.
6.(2分)(2017•南京)我国科技创新成果卓越,下列成果中获得诺贝尔奖的是(
)
A.侯德榜发明联合制碱法
B.屠呦呦发现抗疟新药青蒿素
C.闵恩泽研发石油炼制催化剂
9 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
D.张青莲主持测定了几种元素相对原子质量的新值
【分析】根据科学家们各自在科学上做出的贡献,进行分析解答本题.
【解答】解:A、侯德榜发明联合制碱法,没有获得诺贝尔奖,故选项错误.
B、屠呦呦发现抗疟新药青蒿素,获得了2015年度诺贝尔生理学或医学奖,故选
项正确.
C、闵恩泽研发石油炼制催化剂,没有获得诺贝尔奖,故选项错误.
D、张青莲主持测定了几种元素相对原子质量的新值,没有获得诺贝尔奖,故选项
错误.
故选:B.
7.(2分)(2017•南京)下列物质由分子构成的是( )
A.锌 B.硫酸铜 C.C D.金刚石
60
【分析】根据金属、大多数固态非金属单质、稀有气体等由原子构成;有些物质是
由分子构成的,气态的非金属单质和一般由非金属元素组成的化合物,如氢气、
水等;有些物质是由离子构成的,一般是含有金属元素和非金属元素的化合物,
如氯化钠,进行分析判断即可.
【解答】解:A、锌属于金属单质,是由锌原子直接构成的,故选项错误.
B、硫酸铜是含有金属元素和非金属元素的化合物,硫酸铜是由铜离子和硫酸根
离子构成的,故选项错误.
C、C 是由C 分子构成的,故选项正确.
60 60
D、金刚石属于固态非金属单质,是由碳原子直接构成的,故选项错误.
故选:C.
8.(2分)(2017•南京)下列行为会增加空气中PM2.5的是( )
A.治理工地扬尘 B.露天焚烧垃圾
C.使用公共自行车D.禁止焚烧秸杆
【分析】PM2.5是指大气中直径不超过2.5μm的颗粒物,主要来源是化石燃料的燃
烧和扬尘,根据PM2.5的来源进行分析判断所采取的做法是否合理.
【解答】解:A、治理工地扬尘,能减少PM2.5污染,故选项错误.
B、露天焚烧垃圾,燃烧会产生大量的微小颗粒物,会增加PM2.5污染,故选项正
10 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
确.
C、使用公共自行车,能减少PM2.5污染,故选项错误.
D、禁止焚烧秸杆,能减少PM2.5污染,故选项错误.
故选:B.
9.(2分)(2017•南京)下列关于干冰升华过程的说法正确的是( )
A.二氧化碳分子的体积变大B.二氧化碳分子的质量变小
C.二氧化碳分子的种类改变D.二氧化碳分子间的间隔变大
【分析】根据分子的基本特征:分子质量和体积都很小;分子之间有间隔;分子是
在不断运动的;同种物质的分子性质相同,不同物质的分子性质不同,结合事实
进行分析判断即可
【解答】解:A、干冰受热升华,是因为温度升高,二氧化碳分子间的间隔增大,而
不是CO 分子体积变大,故选项解释错误.
2
B、干冰受热升华,是因为温度升高,二氧化碳分子间的间隔增大,CO 分子运动速
2
率加快,二氧化碳分子的质量没有变化,故选项解释错误.
C、干冰受热升华,是因为温度升高,二氧化碳分子间的间隔增大,二氧化碳分子
的种类不变,故选项解释错误.
D、干冰受热升华,是因为温度升高,二氧化碳分子间的间隔增大,故选项解释正
确.
故选:D
10.(2分)(2017•南京)实验室制取某些气体的装置如图.下列说法正确的是(
)
11 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
A.装置①和⑤组合可以用来制取氧气
B.装置②和③组合可以用来制取氢气
C.装置②和④组合可以用来制取二氧化碳
D.装置②可以较好地控制反应速率
【分析】A、根据实验室制取氧气的反应原理、氧气的收集方法,进行分析判断.
B、根据实验室制取氢气的反应原理、氢气的收集方法,进行分析判断.
C、根据实验室制取二氧化碳的反应原理、二氧化碳的收集方法,进行分析判断.
D、根据装置②固体与液体接触后不能进行分离,进行分析判断.
【解答】解:A、实验室制取氧气可用加热氯酸钾和二氧化锰混合物的方法,属于固
体加热型,应选用的发生装置是①;氧气不易溶于水,可用排水法收集;故选项说
法正确.
B、实验室制取氢气常采用锌与稀硫酸反应来制取,属于固液常温型,应选用的发
生装置是②;但氢气密度比空气的小,应用向下排空气法收集,故选项说法错误.
C、实验室中制取二氧化碳常用大理石或石灰石和稀盐酸反应来制取,属于固液
常温型,应选用的发生装置是②;但二氧化碳密度比空气的大,应用向上排空气
法收集,故选项说法错误.
D、装置②固体与液体接触后不能进行分离,不能控制反应速率,故选项说法错误
故选:A.
11.(2分)(2017•南京)下列材料中属于复合材料的是( )
A.不锈钢 B.聚氯乙烯C.玻璃钢 D.天然橡胶
【分析】复合材料是由两种或两种以上不同性质的材料,通过物理或化学的方法,
在宏观上组成具有新性能的材料.
【解答】解:A.不锈钢属于合金,属于金属材料,故错误;
B.聚氯乙烯是一种塑料,塑料属于合成材料,故错误;
C.玻璃钢是由玻璃与树脂混合成的,前者是无机非金属材料,后者是有机高分子
合成材料,故玻璃钢是两种材料复合成的,故正确;
D.天然橡胶属于天然材料,故错误.
故选C.
12 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
12.(2分)(2017•南京)下列叙述不正确的是( )
A.用蒸馏的方法,可以得到净化程度较高的水
B.用食醋浸泡鸡蛋的方法,可以制得无壳鸡蛋
C.用灼烧闻气味的方法,可以区分棉制品和羊毛制品
D.用喷水的方法,可以扑灭所有物质燃烧引起的火灾
【分析】A.根据净化水的原理来分析;
B.根据酸的性质来分析;
C.根据棉纤维与羊毛纤维成分的不同来分析;
D.根据灭火的方法来分析.
【解答】解:A.蒸馏可以除去水中的所有杂质,所以蒸馏可以得到净化程度最高的
水,故正确;
B.蛋壳的主要成分是碳酸钙,食醋中含有醋酸,二者反应生成可溶性的醋酸钙、
水和二氧化碳,可以制得无壳鸡蛋,故正确;
C.羊毛的主要成分是蛋白质,燃烧时有烧焦羽毛的气味,棉花没有,可用燃烧闻
气味的方法区别羊毛制品和棉制品,故正确;
D.火灾是否可以用水应根据燃烧的物质确定,电路失火、油类物质失火、活泼金
属的失火等不能用水,故错误.
故选D.
13.(2分)(2017•南京)下列各组离子在水中能大量共存的是( )
A.Cu2+、Na+、Cl﹣、OH﹣ B.H+、K+、NO ﹣、SO 2﹣
3 4
C.Na+、NH +、NO ﹣、OH﹣ D.Ag+、Ba2+、NO ﹣、Cl﹣
4 3 3
【分析】根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子
不能共存,据此进行分析判断即可.
【解答】解:A、Cu2+、OH﹣两种离子能结合成氢氧化铜沉淀,不能大量共存,故选项
错误.
B、四种离子间不能结合成沉淀、气体或水,能大量共存,故选项正确.
C、NH +、OH﹣两种离子能结合成氨气和水,不能大量共存,故选项错误.
4
D、Ag+、Cl﹣能结合成氯化银白色沉淀,不能大量共存,故选项错误.
故选:B.
13 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
14.(2分)(2017•南京)除去下列物质中混有的少量杂质(括号内为杂质),拟定
的实验方案不可行的是( )
A.FeCl 溶液(CuCl )﹣﹣加入过量的铁粉,过滤
2 2
B.KCl固体(KClO )﹣﹣加入少量的二氧化锰,并加热
3
C.CO气体(CO )﹣﹣通过足量的氢氧化钠溶液,并干燥
2
D.NaCl溶液(MgCl )﹣﹣加入过量的氢氧化钠溶液,过滤,滤液中加稀盐酸至中
2
性
【分析】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提
纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:
①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质
【解答】解:A、过量的铁粉能与CuCl 溶液反应生成氯化亚铁溶液和铜,再过滤,能
2
除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
B、KClO 在二氧化锰的催化作用下生成氯化钾和氧气,二氧化锰作催化剂,反应前
3
后质量不变,能除去杂质但引入了新的杂质二氧化锰,不符合除杂原则,故选项
所采取的方法错误.
C、CO 能与氢氧化钠溶液反应生成碳酸钠和水,CO不与氢氧化钠溶液反应,再干
2
燥,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、MgCl 能与过量的氢氧化钠溶液反应生成氢氧化镁沉淀和氯化钠,过滤,滤液
2
中加稀盐酸至中性,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所
采取的方法正确.
故选:B.
15.(2分)(2017•南京)按如图所示装置,持续通入气态物质X,可以看到玻璃管
中有红色物质生成,无水CuSO 变蓝,澄清石灰水变浑浊,则X不可能是( )
4
14 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
A.氢气和水蒸气 B.氢气和二氧化碳
C.一氧化碳和氢气D.一氧化碳和水蒸气
【分析】根据题意,持续通入气态物质X,可以看到玻璃管中有红色物质生成,说
明气体中含有具有还原性的气体;无水CuSO 变蓝,说明有水蒸气生成;澄清石灰
4
水变浑浊,说明原气体中含有二氧化碳或生成了二氧化碳;进行分析判断.
【解答】解:A、氢气具有还原性,能与灼热的氧化铜反应生成铜和水蒸气,但不能
使澄清石灰水变浑浊,故选项正确.
B、氢气具有还原性,能与灼热的氧化铜反应生成铜和水蒸气,生成的水蒸气使无
水CuSO 变蓝;混合气体中的二氧化碳使澄清石灰水变浑浊,故选项错误.
4
C、氢气具有还原性,能与灼热的氧化铜反应生成铜和水蒸气,生成的水蒸气使无
水CuSO 变蓝;一氧化碳具有还原性,能与灼热的氧化铜反应生成铜和二氧化碳,
4
生成的二氧化碳使澄清石灰水变浑浊,故选项错误.
D、一氧化碳具有还原性,能与灼热的氧化铜反应生成铜和二氧化碳,生成的二氧
化碳使澄清石灰水变浑浊;水蒸气使无水CuSO 变蓝,故选项错误.
4
故选:A.
二、(本题包括2小题,共13分)
16.(6分)(2017•南京)2017年5月,我国首次海域可燃冰试采成功,可燃冰外观
像冰,主要含有甲烷水合物(由甲烷分子和水分子组成),还含少量二氧化碳等物
质.
(1)可燃冰属于 混合物 (填“纯净物”或“混合物”).
(2)化学家在较低的温度和压力下,用甲烷等为原料制成了金刚石薄膜,该变化
属于 化学变化 (填“物理变化”或‘化学变化”).
(3)甲烷(CH )可用作燃料,其充分燃烧的化学方程式为 CH + 2O
4 4 2
15 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
CO + 2H O .
2 2
(4)常温常压时,由甲烷和另两种气体组成的混合物中,碳元素的质量分数为
80%,则另两种气体可能是 BCD .
A.H 和CO B.H 和C H C.C H 和C H D.CO和C H .
2 2 2 2 2 2 2 4 2 4
【分析】(1)根据可燃冰的组成分析回答;
(2)根据化学变化与物理变化的本质区别进行解答;
(3)根据甲烷燃烧生成二氧化碳和水分析解答;
(4)根据物质中某元素的质量分数计算方法进行解答.
【解答】解:(1)“可燃冰”是甲烷和水在低温、高压条件下形成的一种比较复杂
的固体混合物,能够燃烧,外形和冰相似,又称为可燃冰;
(2)用甲烷等为原料制成金刚石薄膜的过程中有新物质生成,属于化学变化;
(3)甲烷充分燃烧生成二氧化碳和水,反应的化学方程式为:CH +2O
4 2
CO +2H O;
2 2
(4)甲烷中,碳元素的质量百分比= ×100%=75%,
CO中碳元素的质量百分比= ×100%=42.9%;
C H 中碳元素的质量百分比= ×100%=92.3%
2 2
C H 中碳元素的质量百分比= ×100%=85.7%
2 4
因为混合气体的碳元素质量分数为80%,而甲烷<80%,所以,另两种气体的含碳
量一定要>80% 才能使混合气体中碳元素质量分数达到80%,A中H 和CO达不
2
到要求,B中H 和C H ,C中C H 和C H ,D中CO和C H ;都可以达到要求;
2 2 2 2 2 2 4 2 4
故答案为:(1)混合物;(2)化学变化;(3)CH +2O CO +2H O; (4)BCD.
4 2 2 2
17.(7分)(2017•南京)溶液在生产、生活中起着十分重要的作用.请回答下列问
题:
(1)可以作为溶质的是 D .
A.只有固体 B.只有液体 C.只有气体 D.气体、液体、固体都可以
16 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
(2)配制100g质量分数为16%的氯化钠溶液,所需氯化钠的质量为 16 g ,水
的体积为 8 4 mL (水的密度近似看作1g/cm3).
(3)甲、乙两种不含结晶水的固体物质的溶解度曲线如图1.t ℃时,甲物质的溶
1
解度是 40 g .t ℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,
2
须蒸发掉较多水的是 乙 (填“甲”或“乙”)物质的饱和溶液.
(4)按图2所示装置,将液体X注入装有固体y的试管中,会导致U形管中右端液
面升高.则可能的组合是 AD .
选 x y
项
A 水 氧化
钙
B 水 硝酸
铵
C 浓硫 水
酸
D 稀盐 镁
酸
【分析】气体、液体、固体都可以作为溶质;100g×16%=16g,水的质量=100g﹣
16g=84g,水的体积= =84mL;根据题目信息和溶解度曲线可知:甲、乙两种
固体物质的溶解度,都是随温度升高而增大,而甲的溶解度随温度的升高变化比
乙大;t ℃时,甲物质的溶解度是40g;t ℃时,若从甲和乙两种物质的饱和溶液中
1 2
析出等质量的固体,须蒸发掉较多水的是乙物质的饱和溶液;按图2所示装置,
17 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
将液体X注入装有固体y的试管中,会导致U形管中右端液面升高.则可能的组
合是AD.
【解答】解:(1)气体、液体、固体都可以作为溶质,如盐酸的溶质是气体,酒精溶
液的溶质是液体,氯化钠溶液溶质是固体;故答案为:D;
(2)100g×16%=16g,水的质量=100g﹣16g=84g,水的体积= =84mL;故答案
为:16g;84;
(3)t ℃时,甲物质的溶解度是40g;t ℃时,若从甲和乙两种物质的饱和溶液中析
1 2
出等质量的固体,须蒸发掉较多水的是乙物质的饱和溶液,因为该温度下,甲物
质的溶解度大于乙;故答案为:40g;乙;
(4)按图2所示装置,将液体X注入装有固体y的试管中,会导致U形管中右端液
面升高,说明试管内温度升高,或有气体产生,则可能的组合是AD;故答案为:
AD;
三、(本题包括1小题.共14分)
18.(14分)(2017•南京)核电菏数为1~18的元素的原子结构示意图等信息如下,
请回答下列问题.
(1)2017年5月9日,中国科学院等单位联合发布了 115号元素的中文名为
“镆”.此元素原子的核电荷数为 11 5 ,核外电子数为 11 5 .
(2)在第三周期中,随着原子序数的递增,元素原子核外电子排布的变化规律是
依次增多 .
(3)利用上表中给出的元素,写出含有氮元素的常见单质、氧化物、酸、碱、盐的化
18 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
学式各一个,并标出所写化学式中氮元素的化合价:单质 、氧化物 O
2
、酸 H O 或者 H O 、碱 H •H O 或者 H OH 、盐 H HCO .
2 3 3 2 4 4 3
(4)以钠和氯为例,简述结构与性质的关系. 钠原子最外层一个电子,容易失去
一个电子.而氯原子最外层 7 个电子,容易得到一个电子.结构决定性质. .
(5)国产C919大型客机上使用了大量的铝合金.工业上用电解氧化铝(Al O )得
2 3
到铝和氧气、试计算电解102t氧化铝最多能生成铝的质量是多少?(写出计算过
程)
【分析】(1)在元素的相关数据中,元素序数=原子的核电荷数=原子的核外电子
数.
(2)周期表中,同一周期,随着原子序数的递增,元素原子核外电子排布的变化规
律是 依次增多.
(3)注意化合价与化学式的一一对应和答案的不唯一.
(4)以钠和氯为例,简述结构与性质的关系. 钠原子最外层一个电子,容易失去
一个电子.而氯原子最外层7个电子,容易得到一个电子.结构决定性质..
(5)根据反应物的质量和对应的化学方程式求算生成物铝的质量.
【解答】解:
(1)“镆”为115号元素,根据元素序数=原子的核电荷数=原子的核外电子数,
可知此元素原子的核电荷数为 115,核外电子数为 115.
(2)在第三周期中,随着原子序数的递增,元素原子核外电子排布的变化规律是
依次增多.
(3)注意物质的分类,同时要注意根据化合价书写对应化学式,本题答案有的不
是唯一的.单质 、氧化物 O(不唯一)、酸 H O 或者H O 、碱 H •H O或
2 2 3 3 2
者 H OH、盐 H HCO (不唯一).
4 4 3
(4)以钠和氯为例,简述结构与性质的关系. 钠原子最外层一个电子,容易失去
一个电子.而氯原子最外层7个电子,容易得到一个电子.结构决定性质..
(5)设电解102t氧化铝最多能生成铝的质量为x
19 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
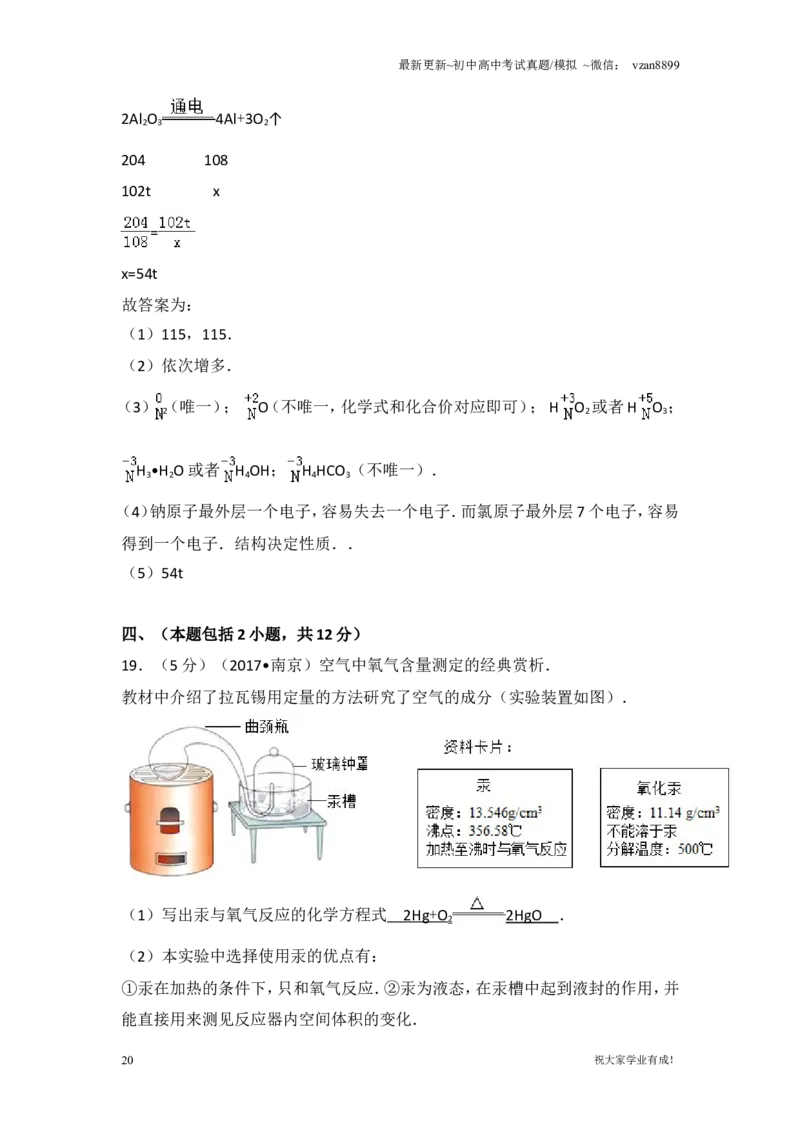
2Al O 4Al+3O ↑
2 3 2
204 108
102t x
=
x=54t
故答案为:
(1)115,115.
(2)依次增多.
(3) (唯一); O(不唯一,化学式和化合价对应即可); H O 或者H O ;
2 2 3
H •H O或者 H OH; H HCO (不唯一).
3 2 4 4 3
(4)钠原子最外层一个电子,容易失去一个电子.而氯原子最外层7个电子,容易
得到一个电子.结构决定性质..
(5)54t
四、(本题包括2小题,共12分)
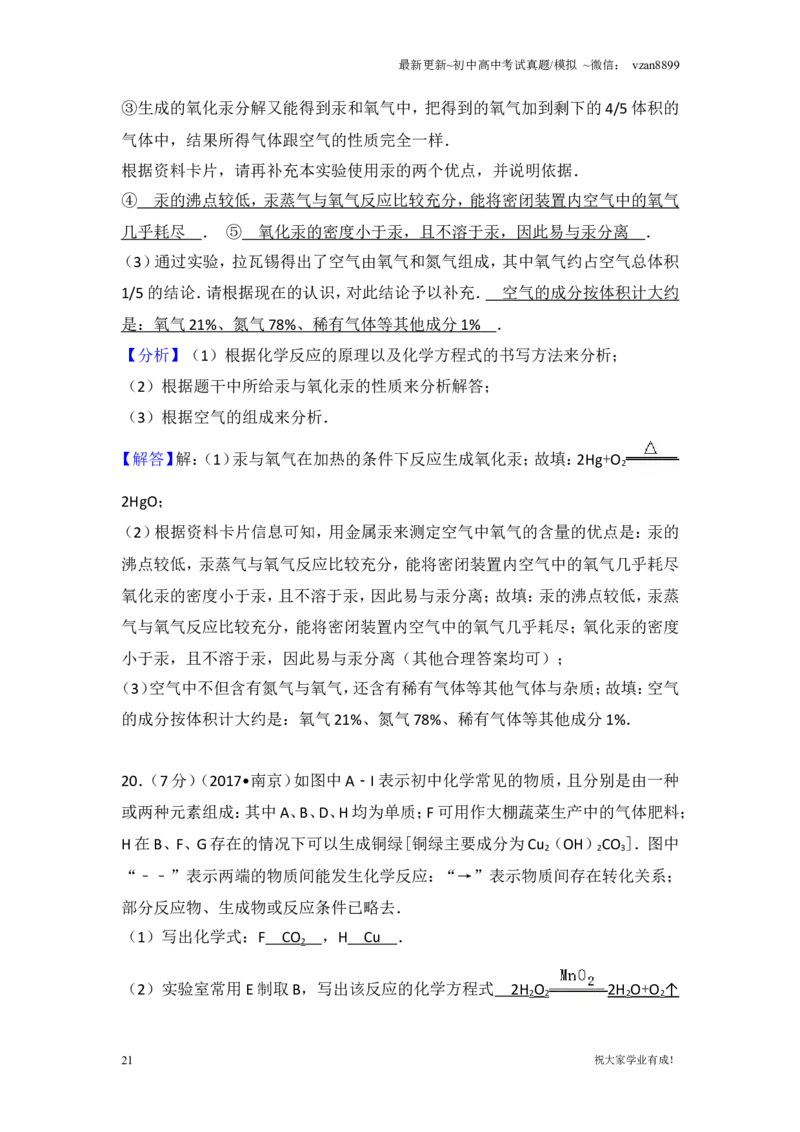
19.(5分)(2017•南京)空气中氧气含量测定的经典赏析.
教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图).
(1)写出汞与氧气反应的化学方程式 2H g + O 2HgO .
2
(2)本实验中选择使用汞的优点有:
①汞在加热的条件下,只和氧气反应.②汞为液态,在汞槽中起到液封的作用,并
能直接用来测见反应器内空间体积的变化.
20 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
③生成的氧化汞分解又能得到汞和氧气中,把得到的氧气加到剩下的4/5体积的
气体中,结果所得气体跟空气的性质完全一样.
根据资料卡片,请再补充本实验使用汞的两个优点,并说明依据.
④ 汞的沸点较低,汞蒸气与氧气反应比较充分,能将密闭装置内空气中的氧气
几乎耗尽 . ⑤ 氧化汞的密度小于汞,且不溶于汞,因此易与汞分离 .
(3)通过实验,拉瓦锡得出了空气由氧气和氮气组成,其中氧气约占空气总体积
1/5的结论.请根据现在的认识,对此结论予以补充. 空气的成分按体积计大约
是:氧气 21% 、氮气 78% 、稀有气体等其他成分 1% .
【分析】(1)根据化学反应的原理以及化学方程式的书写方法来分析;
(2)根据题干中所给汞与氧化汞的性质来分析解答;
(3)根据空气的组成来分析.
【解答】解:(1)汞与氧气在加热的条件下反应生成氧化汞;故填:2Hg+O
2
2HgO;
(2)根据资料卡片信息可知,用金属汞来测定空气中氧气的含量的优点是:汞的
沸点较低,汞蒸气与氧气反应比较充分,能将密闭装置内空气中的氧气几乎耗尽
氧化汞的密度小于汞,且不溶于汞,因此易与汞分离;故填:汞的沸点较低,汞蒸
气与氧气反应比较充分,能将密闭装置内空气中的氧气几乎耗尽;氧化汞的密度
小于汞,且不溶于汞,因此易与汞分离(其他合理答案均可);
(3)空气中不但含有氮气与氧气,还含有稀有气体等其他气体与杂质;故填:空气
的成分按体积计大约是:氧气21%、氮气78%、稀有气体等其他成分1%.
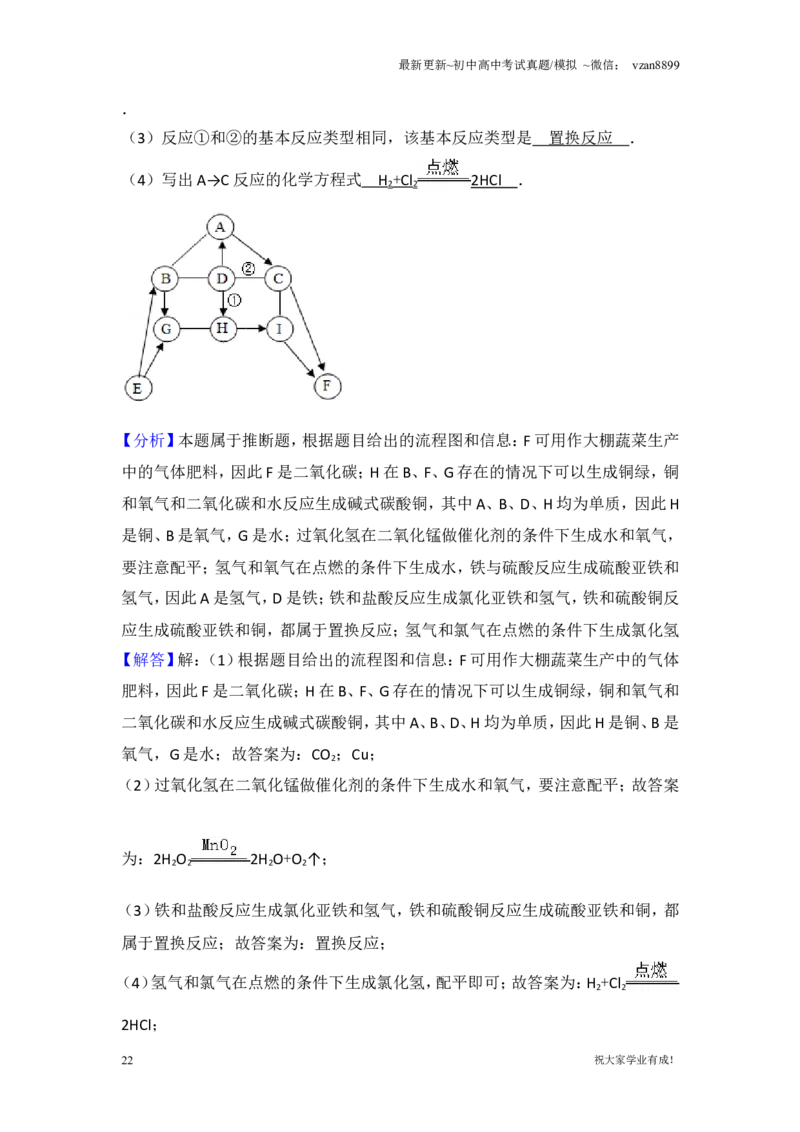
20.(7分)(2017•南京)如图中A﹣I表示初中化学常见的物质,且分别是由一种
或两种元素组成:其中A、B、D、H均为单质;F可用作大棚蔬菜生产中的气体肥料;
H在B、F、G存在的情况下可以生成铜绿[铜绿主要成分为Cu(OH)CO ].图中
2 2 3
“﹣﹣”表示两端的物质间能发生化学反应:“→”表示物质间存在转化关系;
部分反应物、生成物或反应条件已略去.
(1)写出化学式:F CO ,H Cu .
2
(2)实验室常用E制取B,写出该反应的化学方程式 2H O 2H O + O ↑
2 2 2 2
21 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
.
(3)反应①和②的基本反应类型相同,该基本反应类型是 置换反应 .
(4)写出A→C反应的化学方程式 H + C l 2HC l .
2 2
【分析】本题属于推断题,根据题目给出的流程图和信息:F可用作大棚蔬菜生产
中的气体肥料,因此F是二氧化碳;H在B、F、G存在的情况下可以生成铜绿,铜
和氧气和二氧化碳和水反应生成碱式碳酸铜,其中A、B、D、H均为单质,因此H
是铜、B是氧气,G是水;过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,
要注意配平;氢气和氧气在点燃的条件下生成水,铁与硫酸反应生成硫酸亚铁和
氢气,因此A是氢气,D是铁;铁和盐酸反应生成氯化亚铁和氢气,铁和硫酸铜反
应生成硫酸亚铁和铜,都属于置换反应;氢气和氯气在点燃的条件下生成氯化氢
【解答】解:(1)根据题目给出的流程图和信息:F可用作大棚蔬菜生产中的气体
肥料,因此F是二氧化碳;H在B、F、G存在的情况下可以生成铜绿,铜和氧气和
二氧化碳和水反应生成碱式碳酸铜,其中A、B、D、H均为单质,因此H是铜、B是
氧气,G是水;故答案为:CO ;Cu;
2
(2)过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;故答案
为:2H O 2H O+O ↑;
2 2 2 2
(3)铁和盐酸反应生成氯化亚铁和氢气,铁和硫酸铜反应生成硫酸亚铁和铜,都
属于置换反应;故答案为:置换反应;
(4)氢气和氯气在点燃的条件下生成氯化氢,配平即可;故答案为:H +Cl
2 2
2HCl;
22 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
五、(本题包括1小题,共11分)
21.(11分)(2017•南京)兴趣小组的同学对碳酸氢钠、碳酸钠、氢氧化钠的某些
性质进行相关探究.
【提出问题】它们溶液的酸碱性及与酸反应时溶液的pH如何变化?
【实验探究1】向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入
几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
液体名称 蒸馏 碳酸氢钠溶 碳酸钠溶 氢氧化钠溶
水 液 液 液
紫甘蓝汁液显示的颜 蓝紫 蓝色 绿色 黄色
色 色
查阅资料:
pH 7.5 10~ 12~
~9 11.9 14
紫甘蓝汁液显示的颜 蓝 绿色 黄色
色 色
【得出结论1】三种溶液的碱性由强到弱的顺序为 氢氧化钠溶液 > 碳酸钠溶液
> 碳酸氢钠溶液 .
【实验探究2】甲同学在烧杯溶液中加入约5mL稀氢氧化钠溶液,滴入几滴酚酞溶
液,此时溶液由 无 色变为 红 色.向其中加入稀盐酸,该反应的化学方程
式为 NaOH + HCl=NaC l + H O .
2
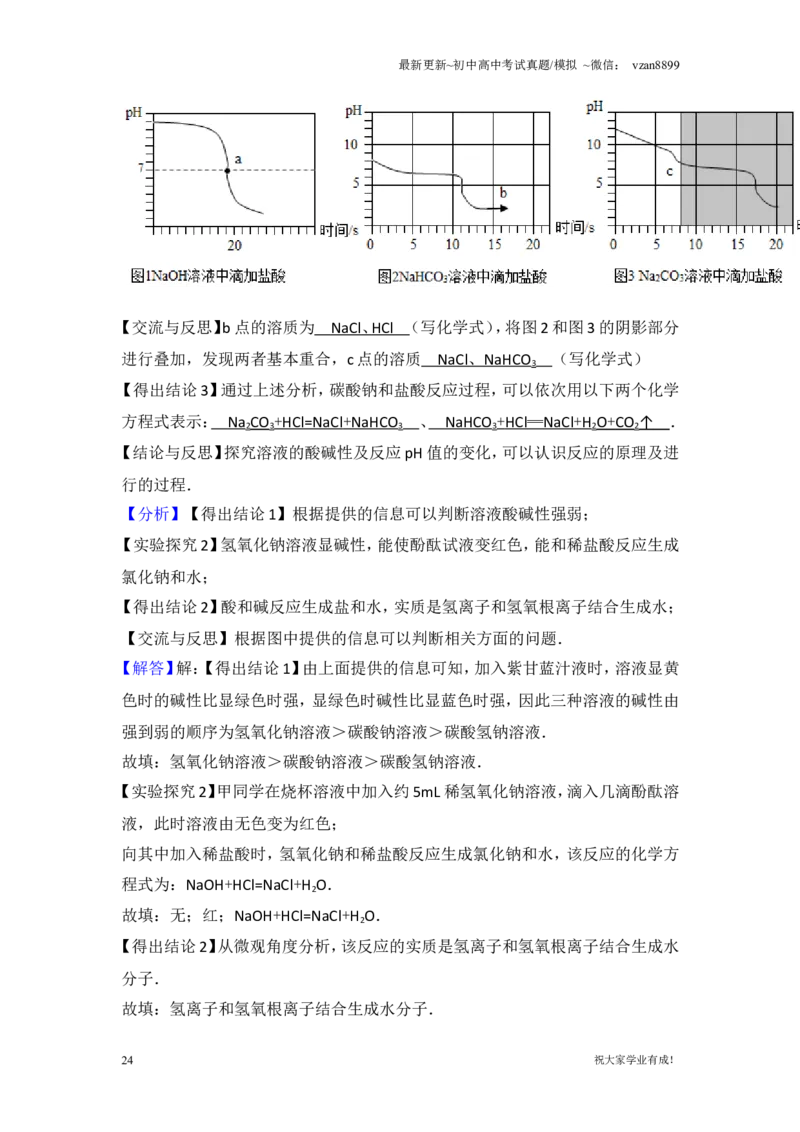
乙同学向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,得
到pH变化与时间的关系如图1所示.
【得出结论2】从微观角度分析,该反应的实质是 氢离子和氢氧根离子结合生成
水分子 .
【实验探究3】向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加
入一定浓度的盐酸,得列pH变化与时间的关系如图2、图3所示.
23 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
【交流与反思】b点的溶质为 NaC l 、 HC l (写化学式),将图2和图3的阴影部分
进行叠加,发现两者基本重合,c点的溶质 NaC l 、 NaHCO (写化学式)
3
【得出结论3】通过上述分析,碳酸钠和盐酸反应过程,可以依次用以下两个化学
方程式表示: N a CO + HCl=NaC l + NaHCO 、 NaHCO + HC l ═ NaC l + H O + CO ↑ .
2 3 3 3 2 2
【结论与反思】探究溶液的酸碱性及反应pH值的变化,可以认识反应的原理及进
行的过程.
【分析】【得出结论1】根据提供的信息可以判断溶液酸碱性强弱;
【实验探究2】氢氧化钠溶液显碱性,能使酚酞试液变红色,能和稀盐酸反应生成
氯化钠和水;
【得出结论2】酸和碱反应生成盐和水,实质是氢离子和氢氧根离子结合生成水;
【交流与反思】根据图中提供的信息可以判断相关方面的问题.
【解答】解:【得出结论1】由上面提供的信息可知,加入紫甘蓝汁液时,溶液显黄
色时的碱性比显绿色时强,显绿色时碱性比显蓝色时强,因此三种溶液的碱性由
强到弱的顺序为氢氧化钠溶液>碳酸钠溶液>碳酸氢钠溶液.
故填:氢氧化钠溶液>碳酸钠溶液>碳酸氢钠溶液.
【实验探究2】甲同学在烧杯溶液中加入约5mL稀氢氧化钠溶液,滴入几滴酚酞溶
液,此时溶液由无色变为红色;
向其中加入稀盐酸时,氢氧化钠和稀盐酸反应生成氯化钠和水,该反应的化学方
程式为:NaOH+HCl=NaCl+H O.
2
故填:无;红;NaOH+HCl=NaCl+H O.
2
【得出结论2】从微观角度分析,该反应的实质是氢离子和氢氧根离子结合生成水
分子.
故填:氢离子和氢氧根离子结合生成水分子.
24 祝大家学业有成!最新更新~初中高中考试真题/模拟 ~微信: vzan8899
【交流与反思】碳酸氢钠和稀盐酸反应生成氯化钠、水和二氧化碳,b点时稀盐酸
过量,因此溶质是反应生成的NaCl和过量的HCl;
将图2和图3的阴影部分进行叠加,发现两者基本重合,说明向碳酸钠溶液中加
入稀盐酸时,碳酸钠先和稀盐酸反应生成碳酸氢钠和氯化钠,然后碳酸氢钠再和
稀盐酸反应生成氯化钠、水和二氧化碳,因此 c点的溶质是反应生成的NaCl和
NaHCO .
3
故填:NaCl、HCl;NaCl、NaHCO .
3
【得出结论3】通过上述分析,碳酸钠和盐酸反应的过程是:碳酸钠先和稀盐酸反
应生成碳酸氢钠和氯化钠,然后碳酸氢钠再和稀盐酸反应生成氯化钠、水和二氧
化 碳 , 反 应 的 化 学 方 程 式 为 : Na CO +HCl=NaCl+NaHCO ,
2 3 3
NaHCO +HCl═NaCl+H O+CO ↑.
3 2 2
故填:Na CO +HCl=NaCl+NaHCO ;NaHCO +HCl═NaCl+H O+CO ↑.
2 3 3 3 2 2
25 祝大家学业有成!