文档内容
2010 年北京市高考化学试卷 B.“NO 2 球”浸泡在冷水中,颜色变浅:2NO 2 (g)(红棕色)⇌N 2 O 4 (g)(无色)△H<0
C.铁溶于稀硝酸,溶液变黄:3Fe+8H++2NO ﹣⇌3Fe2++2NO +4H O
一、选择题(共 7小题,每小题 6分,满分 42分) 3 2 2
D.向Na CO 溶液中滴入酚酞,溶液变红:CO 2﹣+H O⇌HCO ﹣+OH﹣
1.(6分)下列有关钢铁腐蚀与防护的说法正确的是( ) 2 3 3 2 3
6.(6分)自然界地表层原生铜的硫化物经氧化、淋滤作用后变成 CuSO 溶液,向地下深层渗
A.钢管与电源正极连接,钢管可被保护 4
透,遇到难溶的ZnS或 PbS,慢慢转变为铜蓝(CuS).下列分析正确的是( )
B.铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀
A.CuS 的溶解度大于PbS 的溶解度
C.钢管与铜管露天堆放在一起时,钢管不易被腐蚀
B.原生铜的硫化物具有还原性,而铜蓝没有还原性
D.钢铁发生析氢腐蚀时,负极反应是Fe﹣3e﹣═Fe3+
C.CuSO 与ZnS反应的离子方程式是 Cu2++S2﹣═CuS↓
2.(6分)下列物质与常用危险化学品的类别不对应的是( ) 4
D.整个过程涉及的反应类型有氧化还原反应和复分解反应,然后硫酸铜与ZnS、PbS 发生复
A.H SO 、NaOH﹣﹣腐蚀品 B.CH 、C H ﹣﹣易燃液体
2 4 4 2 4
分解反应生成更难溶的 CuS
C.CaC 、Na﹣﹣遇湿易燃物品 D.KMnO 、K CrO ﹣﹣氧化剂
2 4 2 7
7.(6 分)某温度下,H (g)+CO (g)⇌H O(g)+CO(g)的平衡常数 K= ,该温度下在
3.(6分)下列说法正确的是( ) 2 2 2
甲、乙、丙三个恒容密闭容器中,投入 H (g)和 CO (g),其起始浓度如表所示,下列判
2 2
A. 的结构中含有酯基
断不正确的是( )
B.顺﹣2﹣丁烯和反﹣2﹣丁烯的加氢产物不同
起始浓度 甲 乙 丙
C.1mol葡萄糖可水解生成2mol乳酸(C H O )
3 6 3
D.脂肪和蛋白质都是能发生水解反应的高分子化合物 c(H 2 )/mol•L﹣1 0.010 0.020 0.020
4.(6分)用如图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应.下列实验不 c(CO )/mol•L﹣1 0.010 0.010 0.020
2
合理的是( ) A.平衡时,乙中CO 的转化率大于60%
2
B.平衡时,甲中和丙中H 的转化率均是60%
2
C.平衡时,丙中c(CO )是甲中的2倍,是0.008 mol•L﹣1
2
D.反应开始时,乙中的反应速率最快,甲中的反应速率最慢
二、非选择题(共 58分)
A.上下移动①中铜丝可控制SO 的量
2
8.(14分)由短周期元素组成的化合物X 是某抗酸药的有效成分.甲同学欲探究X 的组成.
B.②中选用品红溶液验证SO 的生成
2
查阅资料:
C.③中选用NaOH 溶液吸收多余的SO
2
①由短周期元素组成的抗酸药的有效成分有碳酸氢钠、碳酸镁、氢氧化铝、硅酸镁铝、磷酸铝、
D.为确认CuSO 生成,向①中加水,观察颜色
4
碱式碳酸镁铝.
5.(6分)下列解释实验事实的方程式不正确的是( )
②Al3+在pH=5.0 时沉淀完全;Mg2+在pH=8.8 时开始沉淀,在pH=11.4 时沉淀完全.
A.0.1mol/LCH COOH 溶液的 pH>1:CH COOH⇌CH COO﹣+H+
3 3 3
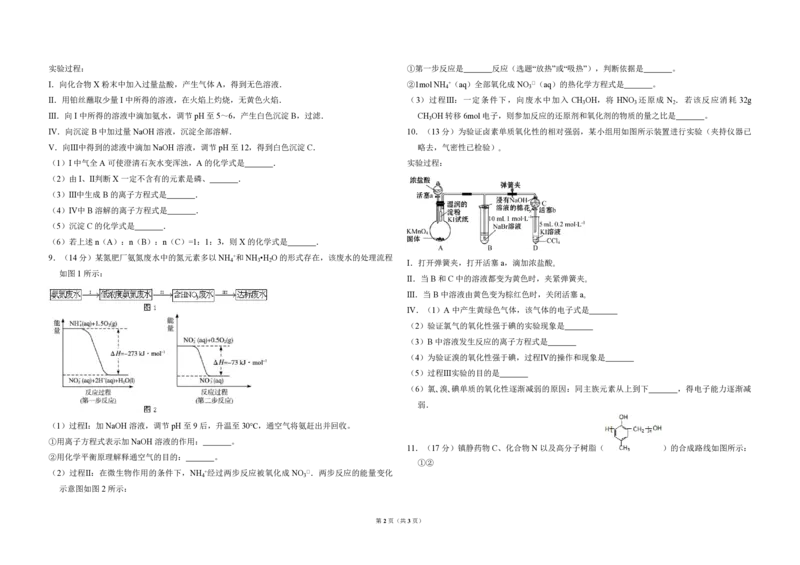
第1页(共3页)实验过程: ①第一步反应是 反应(选题“放热”或“吸热”),判断依据是 。
I.向化合物 X 粉末中加入过量盐酸,产生气体A,得到无色溶液. ②1mol NH +(aq)全部氧化成 NO ﹣(aq)的热化学方程式是 。
4 3
Ⅱ.用铂丝蘸取少量 I中所得的溶液,在火焰上灼烧,无黄色火焰. (3)过程Ⅲ:一定条件下,向废水中加入 CH OH,将 HNO 还原成 N .若该反应消耗 32g
3 3 2
Ⅲ.向I中所得的溶液中滴加氨水,调节pH 至5~6,产生白色沉淀B,过滤. CH OH 转移6mol电子,则参加反应的还原剂和氧化剂的物质的量之比是 。
3
Ⅳ.向沉淀 B 中加过量NaOH 溶液,沉淀全部溶解. 10.(13分)为验证卤素单质氧化性的相对强弱,某小组用如图所示装置进行实验(夹持仪器已
Ⅴ.向Ⅲ中得到的滤液中滴加NaOH 溶液,调节pH 至12,得到白色沉淀C. 略去,气密性已检验)。
(1)I中气全 A 可使澄清石灰水变浑浊,A 的化学式是 . 实验过程:
(2)由I、Ⅱ判断X 一定不含有的元素是磷、 .
(3)Ⅲ中生成 B的离子方程式是 .
(4)Ⅳ中B 溶解的离子方程式是 .
(5)沉淀C的化学式是 .
(6)若上述n(A):n(B):n(C)=1:1:3,则X 的化学式是 .
9.(14 分)某氮肥厂氨氮废水中的氮元素多以 NH +和 NH •H O 的形式存在,该废水的处理流程
4 3 2 Ⅰ.打开弹簧夹,打开活塞 a,滴加浓盐酸。
如图1所示:
Ⅱ.当B 和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B 中溶液由黄色变为棕红色时,关闭活塞 a。
Ⅳ.(1)A 中产生黄绿色气体,该气体的电子式是
(2)验证氯气的氧化性强于碘的实验现象是
(3)B 中溶液发生反应的离子方程式是
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是
(5)过程Ⅲ实验的目的是
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下 ,得电子能力逐渐减
弱.
(1)过程Ⅰ:加 NaOH 溶液,调节 pH 至9后,升温至30℃,通空气将氨赶出并回收。
①用离子方程式表示加NaOH 溶液的作用: 。
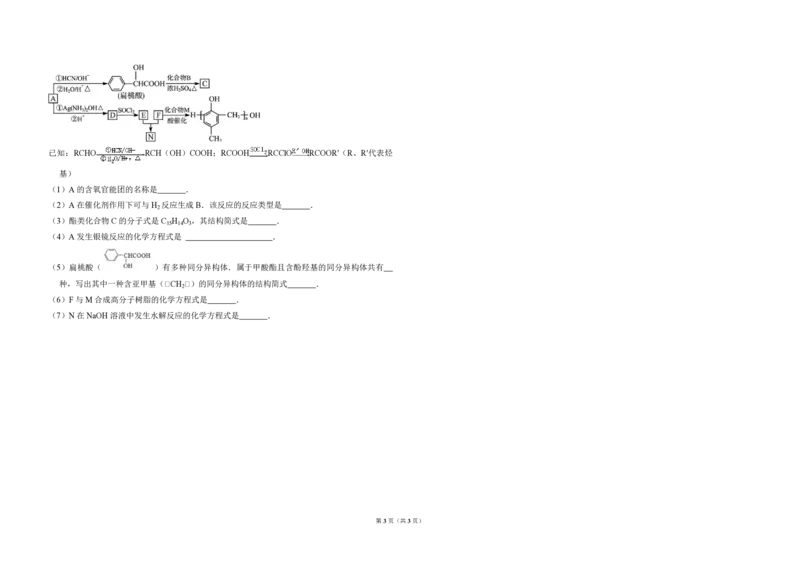
11.(17分)镇静药物 C、化合物 N 以及高分子树脂( )的合成路线如图所示:
②用化学平衡原理解释通空气的目的: 。
①②
(2)过程Ⅱ:在微生物作用的条件下,NH +经过两步反应被氧化成 NO ﹣.两步反应的能量变化
4 3
示意图如图2所示:
第2页(共3页)已知:RCHO RCH(OH)COOH;RCOOH RCClO RCOOR′(R、R′代表烃
基)
(1)A 的含氧官能团的名称是 .
(2)A 在催化剂作用下可与H 反应生成B.该反应的反应类型是 .
2
(3)酯类化合物C的分子式是 C H O ,其结构简式是 .
15 14 3
(4)A 发生银镜反应的化学方程式是 .
(5)扁桃酸( )有多种同分异构体.属于甲酸酯且含酚羟基的同分异构体共有
种,写出其中一种含亚甲基(﹣CH ﹣)的同分异构体的结构简式 .
2
(6)F 与M 合成高分子树脂的化学方程式是 .
(7)N 在NaOH 溶液中发生水解反应的化学方程式是 .
第3页(共3页)