文档内容
2016年山西省中考化学试卷
一、选择题(共10小题,每小题2分,满分20分)
1.(2分)我们每时每刻都离不开空气.空气中含量最多的气体是( )
A.N B.CO C.H D.O
2 2 2 2
2.(2 分)我们每天要保证各种营养素的均衡摄入.以下食物主要提供蛋白质的是
( )
A.鸡蛋 B.大米 C.香蕉 D.黄瓜
3.(2分)在牙膏中添加NaF等氟化物,具有防止龋齿的作用.则NaF中氟元素的化合价
为( )
A.+2 B.0 C.﹣1 D.﹣2
4.(2分)化肥的使用大大提高了粮食的产量.下列化肥属于磷肥的是( )
A.KNO B.NH Cl C.KCl D.Ca (PO )
3 4 3 4 2
5.(2分)你遇到过很多酸性或碱性物质.一些食物的近似pH如下,其中显碱性的物质
是( )
A.食醋,pH为2~3 B.厕所清洁剂,pH为1~2
C.橘子,pH为3~4 D.炉具清洁剂,pH为12~13
6.(2分)世界上的物质多种多样,下列物质属于氧化物的是( )
A.葡萄糖 B.液氨 C.氯酸钾 D.一氧化碳
7.(2分)我国许多地方的家用燃料是天然气。天然气的主要成分是甲烷,下列说法正确
的是( )
A.甲烷的相对分子质量为16g
B.32g甲烷含有24g碳元素
C.甲烷中碳、氢元素的质量比为1:4
D.甲烷由1个碳原子和4个氢原子构成
8.(2分)在学习金属的化学性质时,老师给大家演示了如图所示的实验,下列说法正确
的是( )A.铜片表面始终没有明显变化
B.一段时间后溶液由无色变为浅绿色
C.反应后溶液中一定有硝酸铜,可能有硝酸银
D.通过实验现象推测银和硫酸铜溶液也可以反应
9.(2分)化学对环境的保护和改善起着重要作用,下列做法错误的是( )
A.工业废水经处理达标后再排放
B.化石燃料燃烧会造成空气污染,所以禁止使用
C.使用可降解的塑料可以有效缓解“白色污染”
D.使用汽油和柴油的汽车为其应采用催化净化装置,将有害气体转化为无害物质
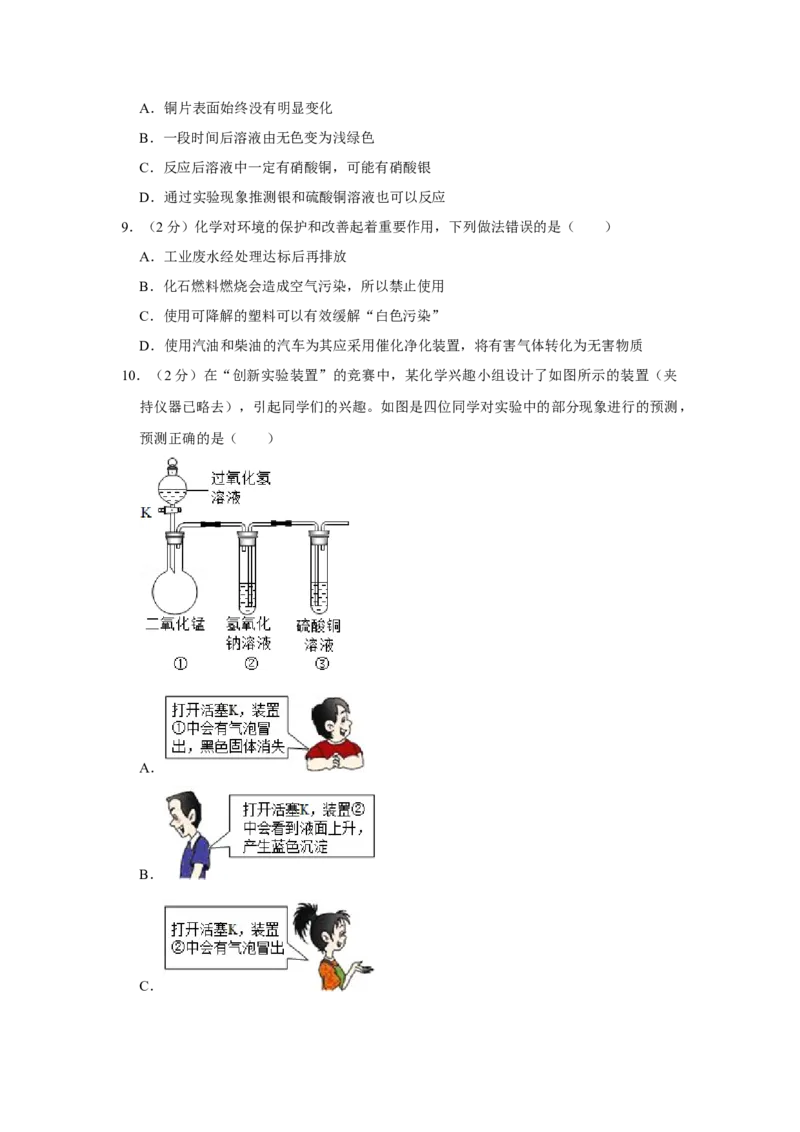
10.(2分)在“创新实验装置”的竞赛中,某化学兴趣小组设计了如图所示的装置(夹
持仪器已略去),引起同学们的兴趣。如图是四位同学对实验中的部分现象进行的预测,
预测正确的是( )
A.
B.
C.D.
二、解答题(共2小题,满分0分)
11.如图为生活中常见“暖贴”的部分标签。暖贴可以贴于身体的某个部位呢,自行发热,
用于取暖或热敷。
(1)任意写出暖贴中两种主要成分的化学式 、 。
(2)暖贴中活性炭具有 作用,使用时空气进入暖贴,空气中的氧气与暖贴中的
发生反应而使暖贴放热。
(3)使用后,发现暖贴内有的物质变为红色,该红色固体主要成分的化学式为 。
12.乐乐查阅资料发现CaCl 可用作干燥剂.他设计了下面的转化方法,用 CaCO 制得
2 3
CaCl .图中“→”表示物之间的转化关系,“→”上方为反应条件或参与反应的另一
2
种物质.
请回答下列问题:
(1)A的化学式为 ;反应①②③都不涉及的基本反应类型是 反应.
(2)牛牛认为CaCO 经一步反应就可以转化为CaCl ,反应的化学方程式为 .
3 2
(3)对比两同学的转化关系,我们发现熟练掌握物质的化学性质可以优化物质的转化
途径.写出物质B经一步转化为CaCO 的化学方程式 .
3
三、解答题(共2小题,满分0分)
13.学习化学使我们从五彩缤纷的宏观世界步入了充满神奇色彩的微观世界.
(1)我们身边有各种各样的物质,例如铜、氧气、熟石灰、金刚石、乙醇等,它们都
是由不同微粒构成的.请选择上述物质填空(每空只填一种物质):
分子构成的物质 ;原子构成的物质 .
(2)学习完“原子的构成”之后,小英幻想自己变成一个进入原子内部的微粒,写了
如下短文.
我想象中的原子结构进入镁原子,我发现①原子是由原子核与核外电子构成的,②原子核相比较原子的
体积竟然那么小.③核外的12个电子围绕原子核作高速运动,④我试着去搬动它们,
发现电子的质量与原子核的质量差不多…
我走出幻境,画出了镁原子结构示意图 .
小英对原子结构的认识有些是错误的,指出文中有错误的一句话 (填句子前的
序号).文中提到的原子在化学变化中易 电子(填“得到”或“失去”).
(3)同学们已经学会从微观角度认识物质的变化,下列变化中微粒种类发生了改变的
是 (填字母,符合题意的选项都选).
a.食物腐烂 b.冰雪融化 c.酒精挥发 d.红磷燃烧
(4)我们接触过很多化学变化,如“氢气燃烧”、“铁和硝酸银溶液反应”、“稀盐
酸与澄清石灰水反应”等,这些变化的微观本质各不相同.
①写出上述三个反应中任意两个反应的化学方程式: .
②从上述三个反应中任取一个写出其微观本质: .
14.阅读下列科普短文.
根据短文回答以下问题:
提到炸药,同学们可能会想到战争和暴力,但炸药的发明却促进了工业和经济的进
步.我国是最早发明火药的国家,黑火药是我国古代的四大发明之一,主要分为硝酸钾、
硫、木炭等.黑火药经点燃,发生剧烈燃烧,反应原理为:
一定条件
2KNO +S+3C K S+N ↑+3CO ↑
3 2 2 2
¯
❑
黑火药经阿拉伯传到欧洲,随后各国化学家陆续研制出各种炸药,如意大利化学家
索布雷罗发明的硝化甘油,爆炸时威力很大,但安全性很低.瑞典化学家诺贝尔在前人
研究的基础上,经过反复实验,研制出安全性很高的硝化甘油炸药,提高了它的利用价
值.炸药的研发还在继续,安全烈性炸药不断问世,如TNT、黑索金等.
黑火药推动了炸药的快速发展,它虽然已退出军事领域,但依然发挥着重要的民用
价值,如制造焰火、定向爆破等.我国近年来研制的纳米级黑索金,在理论和实验制备
等方面获得了突破,将会继续在工业和军事领域做出贡献.
(1)黑火药不需外界提供氧气也可以发生爆炸,这是因为其成分中的 生成氧气的结果.
(2)通过阅读,下列说法正确的是 (填字母,符合题意的选项都选).
a.黑火药作为一种古老的炸药,现在已停止使用
b.黑火药能发生爆炸与它燃烧后生成气体并放出热量有关
c.使用危险物质时,我们应采取一些措施提高其安全性,更好地发挥其作用
(3)炸药属于易爆物,生活中我们有时会接触一些易爆物,下列建议正确的是 .
a.在加油加气站禁止打电话 b.夜晚发现家中燃气泄漏需要开灯检查.
四、解答题(共3小题,满分0分)
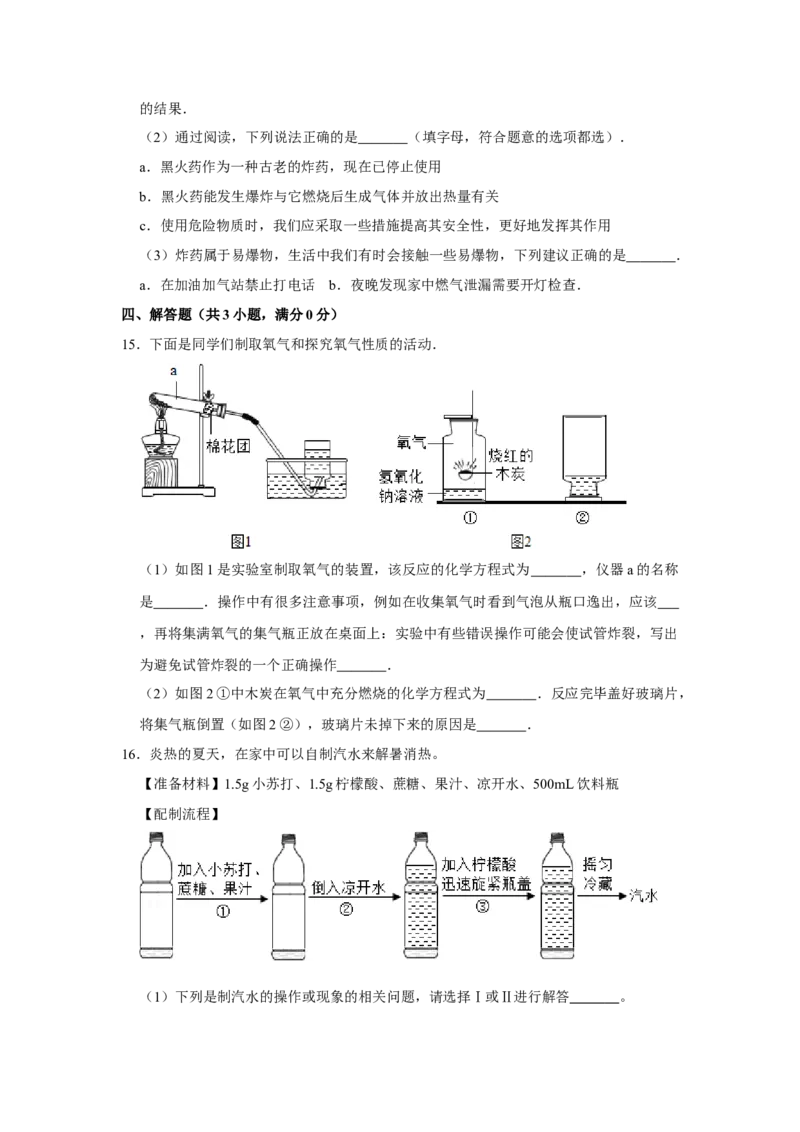
15.下面是同学们制取氧气和探究氧气性质的活动.
(1)如图1是实验室制取氧气的装置,该反应的化学方程式为 ,仪器a的名称
是 .操作中有很多注意事项,例如在收集氧气时看到气泡从瓶口逸出,应该
,再将集满氧气的集气瓶正放在桌面上:实验中有些错误操作可能会使试管炸裂,写出
为避免试管炸裂的一个正确操作 .
(2)如图2①中木炭在氧气中充分燃烧的化学方程式为 .反应完毕盖好玻璃片,
将集气瓶倒置(如图2②),玻璃片未掉下来的原因是 .
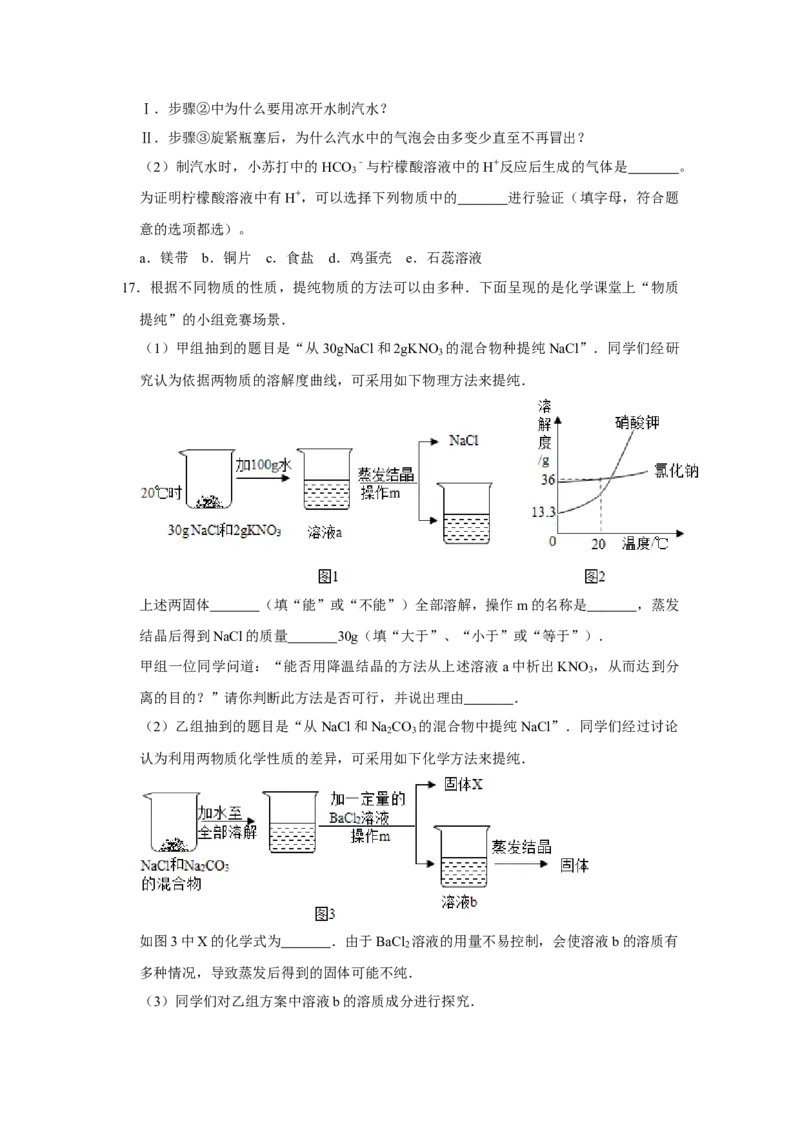
16.炎热的夏天,在家中可以自制汽水来解暑消热。
【准备材料】1.5g小苏打、1.5g柠檬酸、蔗糖、果汁、凉开水、500mL饮料瓶
【配制流程】
(1)下列是制汽水的操作或现象的相关问题,请选择Ⅰ或Ⅱ进行解答 。Ⅰ.步骤②中为什么要用凉开水制汽水?
Ⅱ.步骤③旋紧瓶塞后,为什么汽水中的气泡会由多变少直至不再冒出?
(2)制汽水时,小苏打中的HCO ﹣与柠檬酸溶液中的H+反应后生成的气体是 。
3
为证明柠檬酸溶液中有H+,可以选择下列物质中的 进行验证(填字母,符合题
意的选项都选)。
a.镁带 b.铜片 c.食盐 d.鸡蛋壳 e.石蕊溶液
17.根据不同物质的性质,提纯物质的方法可以由多种.下面呈现的是化学课堂上“物质
提纯”的小组竞赛场景.
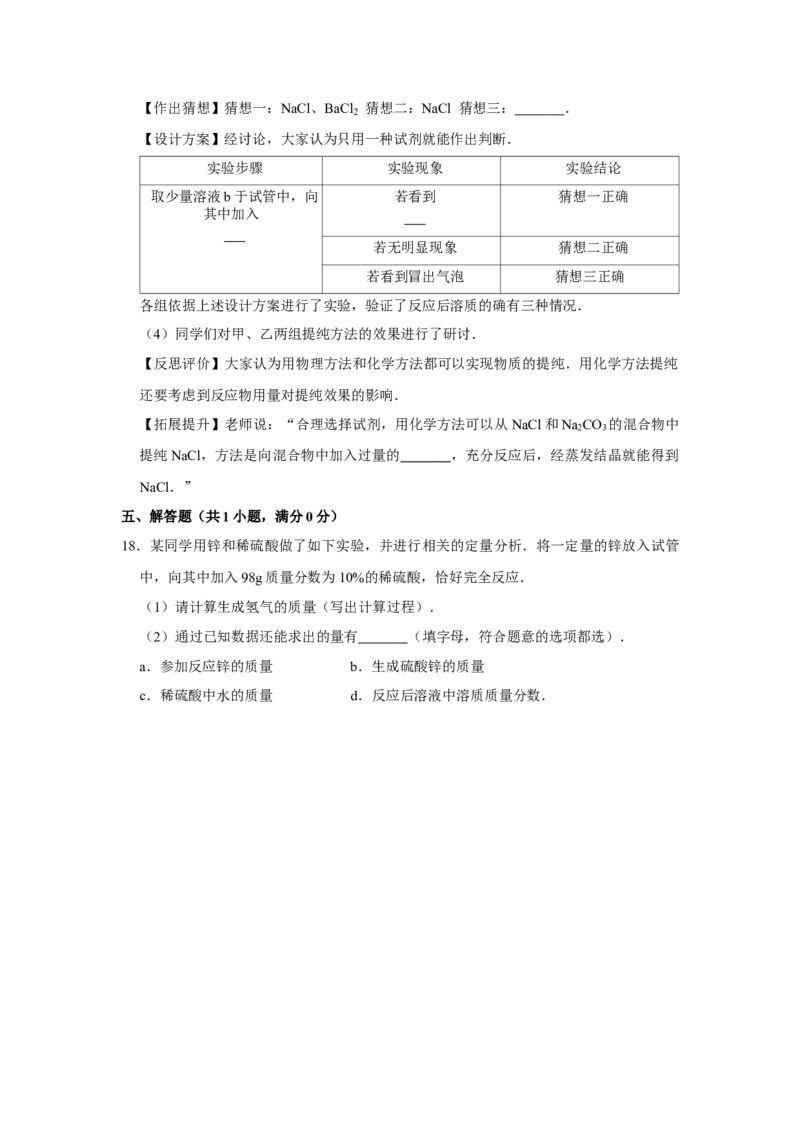
(1)甲组抽到的题目是“从30gNaCl和2gKNO 的混合物种提纯NaCl”.同学们经研
3
究认为依据两物质的溶解度曲线,可采用如下物理方法来提纯.
上述两固体 (填“能”或“不能”)全部溶解,操作m的名称是 ,蒸发
结晶后得到NaCl的质量 30g(填“大于”、“小于”或“等于”).
甲组一位同学问道:“能否用降温结晶的方法从上述溶液a中析出KNO ,从而达到分
3
离的目的?”请你判断此方法是否可行,并说出理由 .
(2)乙组抽到的题目是“从NaCl和Na CO 的混合物中提纯NaCl”.同学们经过讨论
2 3
认为利用两物质化学性质的差异,可采用如下化学方法来提纯.
如图3中X的化学式为 .由于BaCl 溶液的用量不易控制,会使溶液b的溶质有
2
多种情况,导致蒸发后得到的固体可能不纯.
(3)同学们对乙组方案中溶液b的溶质成分进行探究.【作出猜想】猜想一:NaCl、BaCl 猜想二:NaCl 猜想三: .
2
【设计方案】经讨论,大家认为只用一种试剂就能作出判断.
实验步骤 实验现象 实验结论
取少量溶液b于试管中,向 若看到 猜想一正确
其中加入
若无明显现象 猜想二正确
若看到冒出气泡 猜想三正确
各组依据上述设计方案进行了实验,验证了反应后溶质的确有三种情况.
(4)同学们对甲、乙两组提纯方法的效果进行了研讨.
【反思评价】大家认为用物理方法和化学方法都可以实现物质的提纯.用化学方法提纯
还要考虑到反应物用量对提纯效果的影响.
【拓展提升】老师说:“合理选择试剂,用化学方法可以从NaCl和Na CO 的混合物中
2 3
提纯NaCl,方法是向混合物中加入过量的 ,充分反应后,经蒸发结晶就能得到
NaCl.”
五、解答题(共1小题,满分0分)
18.某同学用锌和稀硫酸做了如下实验,并进行相关的定量分析.将一定量的锌放入试管
中,向其中加入98g质量分数为10%的稀硫酸,恰好完全反应.
(1)请计算生成氢气的质量(写出计算过程).
(2)通过已知数据还能求出的量有 (填字母,符合题意的选项都选).
a.参加反应锌的质量 b.生成硫酸锌的质量
c.稀硫酸中水的质量 d.反应后溶液中溶质质量分数.