文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题六 科普阅读题
(试题分值:80分 测试时间:45分钟)
一、选择题(本题包括6小题,每小题2分,共12分.每小题只有一个正确答案)
【新考法】结合重要火箭发射阅读下列材料,完成下面小题。
2024年11月30日,我国新型运载火箭长征十二号运载火箭在海南商业航天发射场成功发射。长征十二号
运载火箭是我国首型4米级直径运载火箭,也是目前我国运载能力最大的单芯级运载火箭,一级采用4台
推力1250千牛的泵后摆液氧煤油发动机,该运载火箭实现我国在运载火箭领域的多个“首次应用”,突破
了牵制释放、铝锂合金贮箱、全三平无人值守等二系列新技术,提高了全箭的可靠性、安全性、经济性。
1.如图为锂和铝两种元素在元素周期表中的相关信息及离子结构示意图。下列有关说法正确的是
A. ,
B.氧化锂的化学式为
C.图中两种元素的本质区别是核内质子数不同
D.铝元素的相对原子质量为26.982g
2.下列说法不正确的是
A.煤油燃烧会放出热量
B.氧气变为液氧时,分子间的间隔减小
C.火箭发射时,液氧可以使煤油充分燃烧
D.铝的抗腐蚀性比较强,在自然界中以单质形式存在
【答案】1.C 2.D
【解析】1.A、元素周期表单元格中,左上角的数字表示原子序数,原子序数=原子的质子数,则m=2,
又由于原子的质子数=核外电子数,则铝原子核外电子排布为2、8、3,在化学变化中易失去3个电子形成
带铝离子,则n=8,该选项说法不正确;
B、锂原子核外电子排布为2、1,在化学变化中易失去1个电子形成带1个单位正电荷的锂离子,则在化
合物中,锂元素化合价为+1价,而氧元素化合价为-2价,则氧化锂的化学式为LiO,该选项说法不正确;
2
C、决定元素种类的为质子数,则两种元素的本质区别是核内质子数不同,该选项说法正确;
D、相对原子质量的单位为“1”,而不是“g”,该选项说法不正确。
故选C。
2.A、燃烧为发光、放热的反应,该选项说法正确;
B、氧气变为液氧时,温度降低,分子间的间隔减小,该选项说法正确;
C、液氧具有助燃性,且氧气越充分,燃烧越剧烈,则液氧可以使煤油充分燃烧,该选项说法正确;
D、铝的抗腐蚀性很强,是因为铝在空气中能和氧气反应生成一层致密的氧化铝薄膜,则铝在自然界中以
化合物存在,该选项说法不正确。
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
故选D。
【新情境】结合氮的固定(2025·江苏扬州·一模)阅读下列材料,完成下列各题
在自然界里,氮元素主要以氮分子的形式存在于空气中,部分氮元素存在于动植物体内的蛋白质中,还有
部分氮元素存在于土壤、海洋里的硝酸盐和铵盐中。
将大气中的氮气转化为氮的化合物的过程叫作氮的固定。自然界多种形态的氮及其化合物间的相互转化,
形成了自然界的“氮循环”(如图)。
3.自然界中氮元素主要以单质形式存在的是
A.人体 B.大气 C.土壤 D.海洋
4.下列叙述正确的是
A.空气中N 的含量相对稳定,利用分离液态空气法获得氮气是利用氮气和氧气的密度不同
2
B.水体中过量的 、 转化为N 的过程属于氮的固定
2
C.科研人员将N 与HO在一定条件下转化为NH 和O 可实现人工固氮
2 2 3 2
D.将N 转化为NH 的过程中氮元素化合价升高
2 3
【答案】3.B 4.C
【解析】3.根据短文可知,氮元素主要以氮分子(即氮气)的形式存在于空气中,部分氮元素存在于动
植物体内的蛋白质中,还有部分氮元素存在于土壤、海洋里的硝酸盐和铵盐中,其中蛋白质、硝酸盐和铵
盐均属于化合物,而氮气属于单质,故选B。
4.A、空气中利用氮气和氧气的沸点不同,可将它们进行分离,该选项叙述不正确;
B、将大气中的氮气转化为氮的化合物的过程叫作氮的固定,则将铵根、硝酸根转化为氮气的过程不属于
氮的固定,该选项叙述不正确;
C、将N 与HO在一定条件下转化为NH 和O 属于人工固氮,该选项叙述正确;
2 2 3 2
D、氮气中氮元素化合价为0,而氮气中氢元素化合价为+1价,设氮元素化合价为x,根据“化合物中各元
素化合价代数和为零,则x+(+1)×3=0,解得x=-3,过程中氮元素化合价降低,该选项叙述不正确。
故选C。
阅读下列材料,完成下面小题。
通常的酸奶是将牛奶发酵而制成的。酸奶中含有大量乳酸菌,乳酸菌把乳糖(C H O )转化成乳酸
12 22 11
(C HO),使得牛奶的酸度升高。科研人员研究了保存时间、温度对活性乳酸菌含量的影响,研究结果见
3 6 3
下表1.酸奶的酸度会影响口感,一般人可接受的酸奶酸度为70.00~100.00°T (数值越大,酸奶酸度越高)。
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
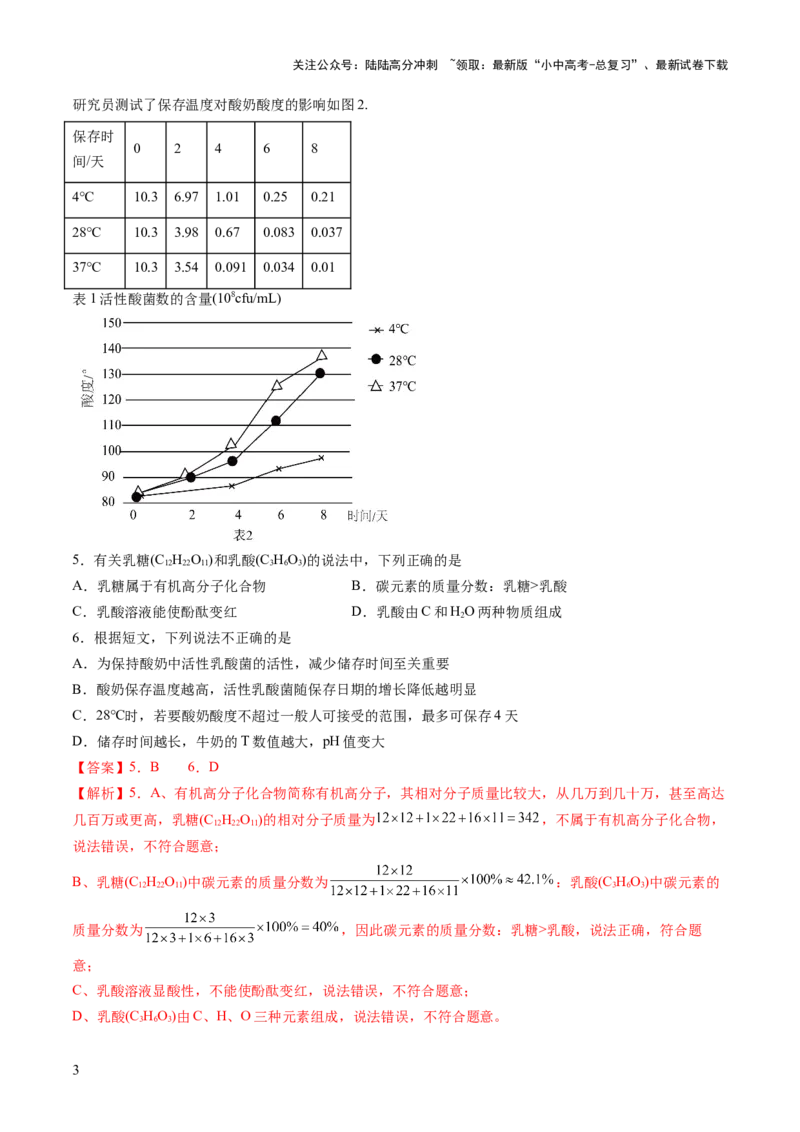
研究员测试了保存温度对酸奶酸度的影响如图2.
保存时
0 2 4 6 8
间/天
4℃ 10.3 6.97 1.01 0.25 0.21
28℃ 10.3 3.98 0.67 0.083 0.037
37℃ 10.3 3.54 0.091 0.034 0.01
表1活性酸菌数的含量(108cfu/mL)
5.有关乳糖(C H O )和乳酸(C HO)的说法中,下列正确的是
12 22 11 3 6 3
A.乳糖属于有机高分子化合物 B.碳元素的质量分数:乳糖>乳酸
C.乳酸溶液能使酚酞变红 D.乳酸由C和HO两种物质组成
2
6.根据短文,下列说法不正确的是
A.为保持酸奶中活性乳酸菌的活性,减少储存时间至关重要
B.酸奶保存温度越高,活性乳酸菌随保存日期的增长降低越明显
C.28℃时,若要酸奶酸度不超过一般人可接受的范围,最多可保存4天
D.储存时间越长,牛奶的T数值越大,pH值变大
【答案】5.B 6.D
【解析】5.A、有机高分子化合物简称有机高分子,其相对分子质量比较大,从几万到几十万,甚至高达
几百万或更高,乳糖(C H O )的相对分子质量为 ,不属于有机高分子化合物,
12 22 11
说法错误,不符合题意;
B、乳糖(C H O )中碳元素的质量分数为 :乳酸(C HO)中碳元素的
12 22 11 3 6 3
质量分数为 ,因此碳元素的质量分数:乳糖>乳酸,说法正确,符合题
意;
C、乳酸溶液显酸性,不能使酚酞变红,说法错误,不符合题意;
D、乳酸(C HO)由C、H、O三种元素组成,说法错误,不符合题意。
3 6 3
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
故选:B;
6.A、由表1数据可知,为保持酸奶中活性乳酸菌的活性,减少储存时间至关重要,说法正确,不符合题
意;
B、由表1数据可知,酸奶保存温度越高,活性乳酸菌随保存日期的增长降低越明显,说法正确,不符合
题意;
C、一般人可接受的酸奶酸度为70.00~100.00°T(数值越大,酸奶酸度越高),由图2可知,28℃时保存4
天,酸奶酸度约为100°T ,且保存天数越多酸奶酸度越高,所以28℃时,若要酸奶酸度不超过一般人可接
受的范围,最多可保存4天,说法正确,不符合题意;
D、由图2可知,储存时间越长,酸奶的T数值越大,则酸奶酸度越高,则pH值越小,说法错误,符合题
意。
故选:D。
二、填空题(本题10小题,化学方程式每空2分,其余除标注外每空1分,共68分)
7.(5分)【新情境】阅读下列短文,并回答相关问题。
【材料一】芯片的主要材料由高纯度单晶硅(化学式为 )制作,工业上用粗硅经两步反应制得单品硅。
第一步:粗硅和氯化氢在 发生反应,生成三氯硅烷(化学式为 )和氢气。第二步:三氯硅烷
和氢气在 时发生反应,生成单晶硅和氯化氢。
【材料二】石墨烯最有潜力成为硅的替代品,它是目前已知材料中电子传导速率最快的,石墨烯是将石墨
逐层剥离,直到最后形成一个单层,厚度只有一个碳原子的单层石墨。
(1)制取单晶硅第二步反应的化学方程式是 ,该化学反应的基本类型是 。
(2)石墨烯属于 (填“单质”或“化合物”);石墨烯和石墨分别在空气中完全燃烧,产物
(填“相同”或“不同”)。
【答案】(1) 置换反应
(2) 单质 相同
【详解】(1)三氯硅烷和氢气在1000°C时发生反应,生成单品硅和氯化氢,化学方程式为:
,该反应是由一种单质与一种化合物反应生成另一种单质与另一种化合物的反
应,属于置换反应;
(2)石墨烯是由碳元素组成的纯净物,属于单质,石墨烯和石墨都是由碳元素组成的单质,由质量守恒
定律可知,它们在空气中完全燃烧,产物都是二氧化碳。
8.(7分)阅读下面科普短文,回答问题。
“84消毒液”于1984年由北京第一传染病医院研制成功,故称之为“84消毒液”,其有效成分是次氯酸
钠。制作方法之一是将氯气(Cl )通入氢氧化钠(NaOH)溶液,反应生成氯化钠、水和次氯酸钠(NaClO)。次
2
氯酸钠具有强氧化性,能和棉纤维上的天然色素之间发生复杂反应,使其褪色。不同温度下,通过实验测
得“84消毒液”的ORP值(ORP可衡量“84消毒液”的漂白能力,数值越大,“84消毒液”的漂白能力越
强),记录如下表所示:
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
“84消毒液”与水的体积 温
ORP值
比 度/℃
1:25 3 608
1:25 16 592
1:25 52 558
“84消毒液”为无色或淡黄色液体,具有刺激性气味,见光或受热就迅速分解。“84消毒液”常用于医疗
器械、餐具、地面等处的消毒。
依据上文,回答下列问题:
(1)制作“84消毒液”时发生反应的化学方程式为 ,该反应中涉及到物质类别有 种。
(2)下列物质不能用“84消毒液”进行消毒的是________(填字母)。
A.塑料玩具 B.教室桌椅 C.红色纯棉短袖
(3)“84消毒液”的物理性质是 (写一条)。
(4)分析表格可知使用“84消毒液”漂白时温度不宜过高的原因是 。(2分)
【答案】(1) 4/四
(2)C
(3)无色或淡黄色液体,具有刺激性气味(合理即可)
(4)温度越高,其漂白能力越弱(ORP值越小)
【详解】(1)根据题给信息可知,将氯气(Cl )通入氢氧化钠(NaOH)溶液中,反应生成氯化钠、水和次氯
2
酸钠(NaClO),反应的化学方程式为 ;
NaCl和NaClO均是由金属离子和酸根离子构成的化合物,属于盐;HO是由两种元素组成,其中一种是
2
氧元素的化合物,属于氧化物;Cl 是由一种元素组成的纯净物,属于单质;NaOH是由钠离子和氢氧根离
2
子构成的化合物,属于碱;故该反应中涉及到的物质类别有4种;
(2)次氯酸钠具有强氧化性,能和棉纤维上的天然色素之间发生复杂反应,使其褪色,因此不能用“84
消毒液”对红色纯棉短袖进行消毒,故选C;
(3)“84消毒液”为无色或淡黄色液体,具有刺激性气味,这些性质都不需发生化学变化就能表现出
来,属于其物理性质,见光或受热就迅速分解需发生化学变化才能表现出来,属于其属于其化学性质;
(4)分析表格中的信息可知使用“84消毒液”漂白时,温度越高,其漂白能力越弱,因此漂白时温度不
宜过高。
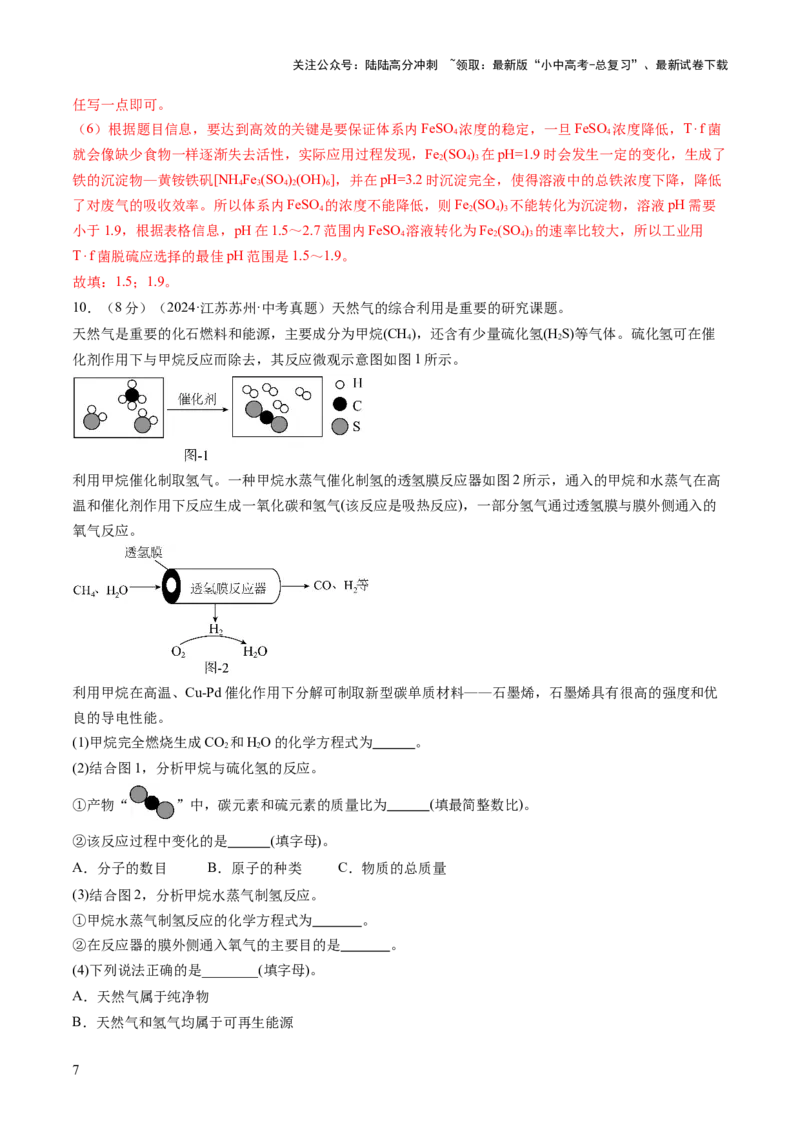
9.(7分)(2024·广西柳州·模拟预测)阅读下列科技短文并回答问题。
T⋅f菌(见图1)是一种细菌,用T⋅f菌脱除工业废气中的一种有毒、有腐蚀性的气体—硫化氢(H S)。其作用
2
原理如图2所示。用这种方法处理废气大大降低了治污的成本,脱除率达到99.97%,且无废物排出。但要
达到高效的关键是要保证体系内FeSO 浓度的稳定,一旦FeSO 浓度降低,T⋅f菌就会像缺少食物一样逐
4 4
渐失去活性。实际应用过程发现,Fe (SO ) 在pH=1.9时会发生一定的变化,生成了铁的沉淀物—黄铵铁矾
2 4 3
[NH Fe (SO )(OH) ],并在pH=3.2时沉淀完全,使得溶液中的总铁浓度下降,降低了对废气的吸收效率。
4 3 4 2 6
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
实验测得30℃时,不同pH环境下T⋅f菌的活性也不同。表现为FeSO 溶液转化为Fe (SO ) 溶液的速率不
4 2 4 3
同,如下表:
pH 0.9 1.2 1.5 1.9 2.1 2.4 2.7 3.0
FeSO 溶液转化为Fe (SO ) 速率/
4 2 4 3
4.5 5.3 6.2 6.8 7.0 6.6 6.2 5.6
(g⋅L-1⋅h-1)
回答下列问题:
(1)请根据文中信息写出硫化氢的化学性质: (写其中一点即可)。
(2)在环节①中化合价升高的元素是 。
(3)净化过程中,只需要不断补充 (填物质名称)使反应持续进行,同时释放的能量还能供给
菌生长。
(4)黄铵铁矾[NH Fe (SO )(OH) ]的化学式中“3”表示___________的个数。
4 3 4 2 6
A.铁元素 B.铁原子 C.铁分子
(5)用T⋅f菌脱除废气中的HS气体的价值是 (写出1点即可)。
2
(6)请结合文中信息,判断工业用T⋅f菌脱硫应选择的最佳pH范围是 He>N ,相对分子质量分别为2、4、28,因此:分子运动
2 2
平均速率与相对分子质量有关;
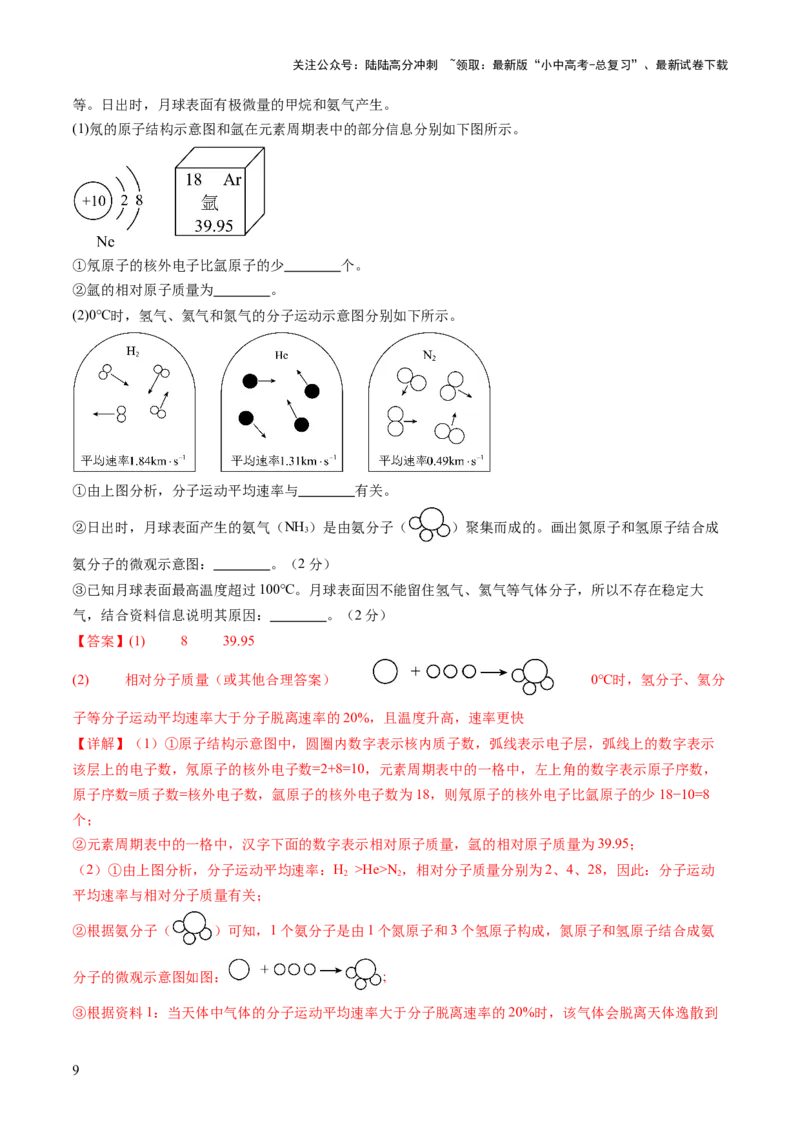
②根据氨分子( )可知,1个氨分子是由1个氮原子和3个氢原子构成,氮原子和氢原子结合成氨
分子的微观示意图如图: ;
③根据资料1:当天体中气体的分子运动平均速率大于分子脱离速率的20%时,该气体会脱离天体逸散到
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
宇宙中。月球表面气体分子的脱离速率均为 , 可知,当分子运动平均速
率大于0.48kms-1时,会脱离天体逸散到宇宙中,H 的平均速率为1.84 kms-1,He的平均速率为1.31 kms-1,
2
因此H、He会脱离天体逸散到宇宙中;已知月球表面最高温度超过100℃。月球表面因不能留住氢气、氦
2
气等气体分子,所以不存在稳定大气,结合资料信息说明其原因:0℃时,氢分子、氦分子等分子运动平
均速率大于分子脱离速率的20%,且温度升高,速率更快。
12.(5分)阅读短文,回答问题。
在日常生活中,人们打开直饮水机就可以获取安全的饮用水。某品牌的直饮水机处理水的过程如下图所
示:
超滤膜的孔径为0.002~0.1μm(微米),能有效地去除(截留)水体中的悬浮物以及细菌、病毒等微生物,也能
有效去除(截留)相对分子质量大于68000的大分子有机物。
KDF是一种铜锌合金,通过化学反应将水体中的余氯(包括Cl、HClO等)转化为对人体无害的Cl-,Zn转
2
化成Zn2+进入水体,Cu不发生反应。KDF还能去除水体中的Pb2+、Cd2+(镉离子)等对人体有害重金属离
子。
(1)超滤膜能去除细菌、病毒等微生物的原因是 。
(2)若自来水中含有下列物质,超滤膜能有效去除的是 (填选项)。
选项 A B C D
物质名称 γ-球蛋白 细胞色素 维生素B 葡萄糖
12
相对分子质量 156000 13000 1355 180
(3)活性炭的作用是 。
(4)若水体中Pb2+以氯化物形式存在,KDF去除Pb2+的化学方程式是 。
【答案】(1)细菌、病毒等微生物的直径大于超滤膜的孔径
(2)A
(3)吸附水中的色素及异味
(4)
【详解】(1)由题干信息可知,超滤膜能去除细菌、病毒等微生物的原因是:细菌、病毒等微生物的直
径大于超滤膜的孔径;
(2)由题干信息可知,超滤膜能有效去除(截留)相对分子质量大于68000的大分子有机物;
A、γ-球蛋白的相对分子质量为156000>68000,能被超滤膜有效去除,符合题意;
B、细胞色素的相对分子质量为13000<68000,不能被超滤膜有效去除,不符合题意;
C、维生素B 的相对分子质量为1355<68000,不能被超滤膜有效去除,不符合题意;
12
D、葡萄糖的相对分子质量为180<68000,不能被超滤膜有效去除,不符合题意。
故选:A;
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(3)活性炭具有吸附性,其作用是吸附水中的色素及异味;
(4)由题干信息可知,KDF是一种铜锌合金,若水体中Pb2+以氯化物形式存在,则KDF去除Pb2+的反应
是锌与氯化铅反应生成铅和氯化锌,化学方程式为 。
13.(10分)(2024·山西太原·二模)我国推行支柱产业“立柱”,新兴产业“架梁”,一大批战略性新
兴产业集群正加速核心技术攻关,无人体系的蝶变正是其中亮眼的一笔,无人机、无人船、无人车…过去
神秘的“硬科技”近年来已逐渐揭开面纱,迈步进入经济社会主战场。分析图文信息,解答21~24题的相
关问题。
(1)图I:中国无人机性能在不断提升,应用场景越来越多。消防无人机在森林火灾监测及救援指挥等方面
具有其独特的优势。人工降雨是扑灭森林火灾的一种方法,其灭火原理是 。可用于人工降雨的一种
物质是 。
(2)图Ⅱ:无人船艇可以适应特殊、极端的各类环境,在海洋保护开发、海上维权执法中具有巨大的优势。
传统的无人船壳用铝合金制造,铝合金属于 材料。现代无人船壳用碳纤维复合材料制造,它更轻
便,并且延长了无人船壳的使用寿命,这是因为碳纤维复合材料具有的优良性质是 (写一条)。
(3)图Ⅲ:无人配送车是物流领域的研发成果之一,大大解决了物流配送最后一公里的配送难题。作为硬件
的“灵魂”,A芯片的制作材料主要包括硅、铜等,采用湿法炼铜(铁与硫酸铜溶液反应)的化学方程式为
,其基本反应类型属于 。
(4)无人机、无人船、无人车等无人体系的动力来自电池,其中之一是氢氧燃料电池,该电池的优点是
。未来能够为无人体系提供电力的可再生能源是 (写一种)。无人体系在现代生活中的应用越来越多,
请再举出一例 。
【答案】(1) 降温到可燃物的着火点以下 干冰
(2) 金属 耐腐蚀
(3) 置换反应
(4) 生成物无污染 风能 无人售货机
【详解】(1)灭火的原理:移除可燃物、降低温度到可燃物的着火点以下、隔绝氧气或空气,人工降雨
是扑灭森林火灾的一种方法,其灭火原理是降低温度到可燃物的着火点以下。固体二氧化碳俗称干冰,干
冰易升华吸热,可用于人工降雨。
(2)金属材料包括合金和纯金属,铝合金属于金属材料。无人船壳用碳纤维复合材料制造,它更轻便,
并且延长了无人船壳的使用寿命,这是因为碳纤维复合材料具有的优良性质是耐腐蚀。
(3)采用湿法炼铜(铁与硫酸铜溶液反应)生成铜和硫酸亚铁,该反应化学方程式:
,一种单质和一种化合物反应生成另一种单质和另一种化合物的反应叫做置换反应,其基本反应类型属于
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
置换反应。
(4)氢氧燃料电池产物是水,该电池的优点是产物无污染。未来能够为无人体系提供电力的可再生能源
是风能等。无人体系在现代生活中的应用越来越多,如无人售票、无人驾驶等。
14.(8分)(2024·江苏连云港·模拟预测)认真阅读下列材料,请回答下列有关问题。
材料一:乘联会发布今年1~4月份我国新能源电动汽车的销量数据,比亚迪排名第一、大部分新能源电动
汽车使用锂电池驱动,比亚迪公司生产的锂电池——“刀片电池”中的正极材料之一为 。
可用 、LiOH和 为原料反应制得。
材料二:金属锂(Li)的熔点低、密度小、质地软,能与水反应生成LiOH。
(1)锂的物理性质有 (写一点即可)。金属锂与水反应生成LiOH的同时还生成氢气,请写出反应的化学
方程式 。
(2)LiOH中锂元素的化合价为 。LiOH的化学性质与NaOH相似,适用于某些场合吸收二氧化碳,请
写出反应的化学方程式 。
(3)用磷酸铁、氢氧化锂和草酸为原料合成 ,请补充完整下列化学方程式:
。
(4)相对于传统燃油车,新能源电动汽车所具有的优点是 (写一点即可)。
【答案】(1) 熔点低、密度小、质地软
(2) +1
(3)H O
2
(4)无污染
【详解】(1)物质的物理性质是物质不需要发生物理变化就能表现出来的性质,包括颜色、状态、气
味、熔点、沸点、硬度、密度、溶解性、导电性、导热性、溶解性等,锂的物理性质有熔点低、密度小、
质地软;锂与水反应生成LiOH和氢气,反应的化学方程式为 ;
(2) LiOH中氢氧根的化合价为-1,根据化合物中各元素化合价的代数和为零,锂元素的化合价为+1;
LiOH的化学性质与NaOH相似,氢氧化钠与二氧化碳反应生成碳酸钠和水,则氢氧化锂与二氧化碳反应
生成碳酸锂和水,反应的化学方程式为 ;
(3)反应前有2Fe、2P、34O、14H、12C、2Li,反应后待确定物质除去,有2Fe、2P、27O、12C、2Li,
根据化学反应前后各种原子个数相等,待补充化学方程式中的化学式为:HO;
2
(4)相对于传统燃油车,新能源电动汽车所具有的优点是无污染。
15.(7分)(2024·江苏无锡·三模)阅读下列科普短文,回答问题。
神器的石墨烯
科学家成功地从石墨中分离出单层的石墨片(称为石墨烯),在电子、复合材料、医疗健康等多领域具有
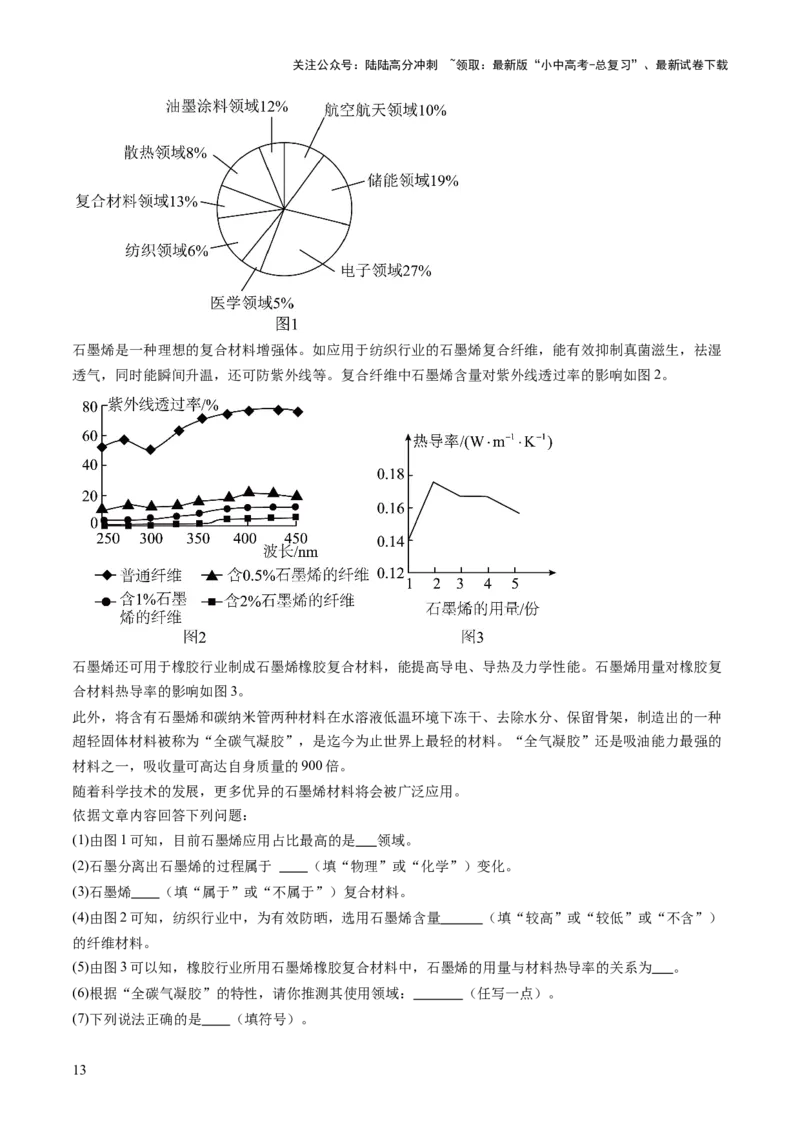
广泛应用,不同领域的应用分布如图1所示。
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
石墨烯是一种理想的复合材料增强体。如应用于纺织行业的石墨烯复合纤维,能有效抑制真菌滋生,祛湿
透气,同时能瞬间升温,还可防紫外线等。复合纤维中石墨烯含量对紫外线透过率的影响如图2。
石墨烯还可用于橡胶行业制成石墨烯橡胶复合材料,能提高导电、导热及力学性能。石墨烯用量对橡胶复
合材料热导率的影响如图3。
此外,将含有石墨烯和碳纳米管两种材料在水溶液低温环境下冻干、去除水分、保留骨架,制造出的一种
超轻固体材料被称为“全碳气凝胶”,是迄今为止世界上最轻的材料。“全气凝胶”还是吸油能力最强的
材料之一,吸收量可高达自身质量的900倍。
随着科学技术的发展,更多优异的石墨烯材料将会被广泛应用。
依据文章内容回答下列问题:
(1)由图1可知,目前石墨烯应用占比最高的是 领域。
(2)石墨分离出石墨烯的过程属于 (填“物理”或“化学”)变化。
(3)石墨烯 (填“属于”或“不属于”)复合材料。
(4)由图2可知,纺织行业中,为有效防晒,选用石墨烯含量 (填“较高”或“较低”或“不含”)
的纤维材料。
(5)由图3可以知,橡胶行业所用石墨烯橡胶复合材料中,石墨烯的用量与材料热导率的关系为 。
(6)根据“全碳气凝胶”的特性,请你推测其使用领域: (任写一点)。
(7)下列说法正确的是 (填符号)。
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
a.石墨、石墨烯、纳米碳管均为碳单质
b.石墨烯化学性质非常活泼,使用领域有限
c.通过短文,印证了结构决定性质,性质决定用途。
【答案】(1)电子
(2)化学
(3)不属于
(4)较高
(5)一定范围内,随着石墨烯用量增加,导热率先增加后降低,当石墨烯的用量为2份时,热导率最高
(6)污水处理(合理即可)
(7)ac
【详解】(1)由图1可知,目前石墨烯应用占比最高的是电子领域;
(2)石墨与石墨烯是两种不同的物质,故石墨分离出石墨烯的过程属于化学变化;
(3)石墨烯是碳的单质,不属于复合材料;
(4)由图2可知,石墨烯含量越高的纤维,紫外线透过率越低,故纺织行业中,为有效防晒,选用石墨烯
含量较高的纤维材料;
(5)由图3可以知,橡胶行业所用石墨烯橡胶复合材料中,石墨烯的用量与材料热导率的关系为:一定范
围内,随着石墨烯用量增加,热导率先增加后降低,当石墨烯的用量为2份时,热导率最高;
(6)“全气凝胶”还是吸油能力最强的材料之一,故可用于污水处理、清理海洋石油泄漏等(合理即
可);
(7)a、石墨、石墨烯、纳米碳管均为碳单质,该选项说法正确;
b、石墨烯为碳的单质,常温下化学性质稳定,该选项说法错误;
c、通过短文,印证了结构决定性质,性质决定用途,该选项说法正确;
故选ac。
16.(5分)(2025·江苏无锡·一模)阅读下列短文,回答相关问题。
酸碱度与人体健康
我们知道许多物质具有酸性或碱性。其实,人体的体液也有一定的酸碱性,且其酸碱度保持在一个相对稳
定的范围内,才能维持人体正常的生命活动。人体血液的量较多,分布广,正常人体血浆pH为
7.35~7.45。氧气充足时,人体摄取的糖类、脂肪、蛋白质会被彻底氧化分解,最终生成CO 和HO,在组
2 2
织细胞与血液之间进行气体交换时,CO 扩散到血液中,会引起血浆的pH略有改变。
2
人体胃液担负着食物的消化,pH为0.9~1.5。20世纪初科学家在人体胃内发现了幽门螺旋杆菌,幽门螺旋
杆菌能引起慢性胃炎,它主要是通过其产生的脲酶分解尿素产生氨而中和人体胃酸,导致人体胃内酸碱失
衡,胃液分泌异常。
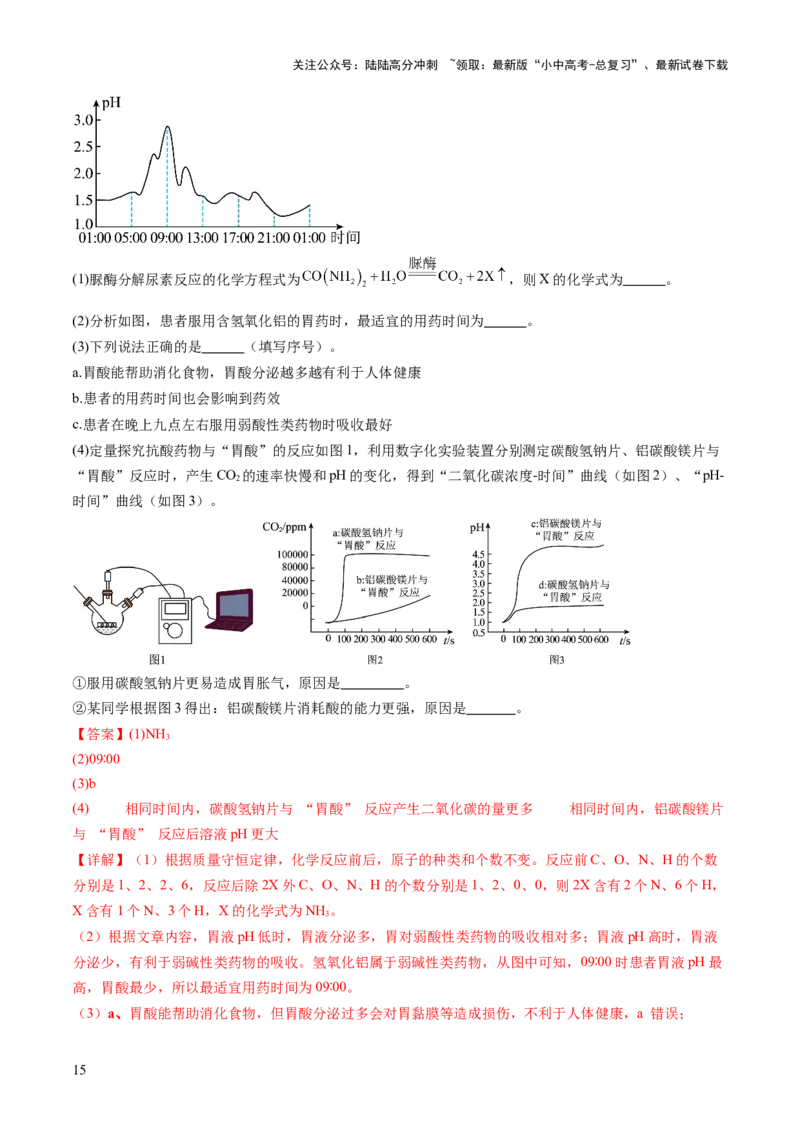
如图是一组胃病患者在空腹状态下24小时胃液pH的变化曲线。科学家发现人体胃液的pH影响人体对药
物的吸收,胃液pH低时,胃液分泌多,胃对弱酸性类药物的吸收相对多;胃液pH高时,胃液分泌少,有
利于弱碱性类药物的吸收。
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)脲酶分解尿素反应的化学方程式为 ,则X的化学式为 。
(2)分析如图,患者服用含氢氧化铝的胃药时,最适宜的用药时间为 。
(3)下列说法正确的是 (填写序号)。
a.胃酸能帮助消化食物,胃酸分泌越多越有利于人体健康
b.患者的用药时间也会影响到药效
c.患者在晚上九点左右服用弱酸性类药物时吸收最好
(4)定量探究抗酸药物与“胃酸”的反应如图1,利用数字化实验装置分别测定碳酸氢钠片、铝碳酸镁片与
“胃酸”反应时,产生CO 的速率快慢和pH的变化,得到“二氧化碳浓度-时间”曲线(如图2)、“pH-
2
时间”曲线(如图3)。
①服用碳酸氢钠片更易造成胃胀气,原因是 。
②某同学根据图3得出:铝碳酸镁片消耗酸的能力更强,原因是 。
【答案】(1)NH
3
(2)09∶00
(3)b
(4) 相同时间内,碳酸氢钠片与 “胃酸” 反应产生二氧化碳的量更多 相同时间内,铝碳酸镁片
与 “胃酸” 反应后溶液pH更大
【详解】(1)根据质量守恒定律,化学反应前后,原子的种类和个数不变。反应前C、O、N、H的个数
分别是1、2、2、6,反应后除2X外C、O、N、H的个数分别是1、2、0、0,则2X含有2个N、6个H,
X含有1个N、3个H,X的化学式为NH 。
3
(2)根据文章内容,胃液pH低时,胃液分泌多,胃对弱酸性类药物的吸收相对多;胃液pH高时,胃液
分泌少,有利于弱碱性类药物的吸收。氢氧化铝属于弱碱性类药物,从图中可知,09∶00时患者胃液pH最
高,胃酸最少,所以最适宜用药时间为09∶00。
(3)a、胃酸能帮助消化食物,但胃酸分泌过多会对胃黏膜等造成损伤,不利于人体健康,a 错误;
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
b、由文中可知人体胃液的pH影响人体对药物的吸收,不同时间胃液pH不同,可知患者的用药时间会影
响药效,b 正确;
c、胃液pH低时,胃对弱酸性类药物的吸收相对多,晚上九点左右胃液pH不是最低,此时服用弱酸性类
药物吸收不是最好,c 错误。
故选b。
(4)①从 “二氧化碳浓度 - 时间” 曲线(图 2)可知,相同时间内,碳酸氢钠片与 “胃酸” 反应产
生二氧化碳的浓度更高,即产生二氧化碳的量更多,所以服用碳酸氢钠片更易造成胃胀气。
②从 “ pH- 时间” 曲线(图 3)可知,相同时间内,铝碳酸镁片与 “胃酸” 反应后溶液的pH比碳酸
氢钠片与 “胃酸” 反应后溶液的pH更大,说明铝碳酸镁片消耗酸的能力更强。
16